

2023年第4期,总第139期
1月23日,Nature杂志发表了题为“SEVEN TECHNOLOGIES TO WATCH IN 2023”的文章,阐述了七项对2023年科学创新具有重大影响的新技术。其中包括五项生物医药领域技术和两项显示相关技术。它们是:单分子蛋白质测序、詹姆斯·韦伯太空望远镜、立体电子显微术、基因编辑CRISPR、高精度放射性碳测、单细胞代谢组学、体外胚胎模型。
从蛋白质测序到电子显微镜,从考古学到天文学,这七项技术可能会在未来一年撼动科学界。
 图片来自Nature
图片来自Nature
01
单分子蛋白质测序
(Single-molecule protein sequencing)
蛋白质组代表了由细胞或生物体产生的完整蛋白质组,可以提供关于健康和疾病的深刻信息,但对其进行表征仍具有挑战性。
曾经大多数蛋白质组学分析使用质谱学,一种根据蛋白质混合物的质量和电荷来分析蛋白质的技术,该技术可以同时量化蛋白质的数量,但不能明确识别每个分子,而且混合物中的低丰度蛋白质易被忽视。
现在,可以对样本中的许多单个蛋白分子进行测序。奥斯汀德克萨斯大学的生物化学家Edward Marcotte正在研究一种叫做荧光测序的方法。用荧光标记的“结合”蛋白质来识别蛋白质末端的特定氨基酸(或多肽)序列,其他研究人员正在开发模仿基于纳米孔的DNA测序的技术,根据多肽通过微小通道时在电流中诱导的变化来分析多肽。
目前,单分子蛋白质测序技术已经成功应用于蛋白质结构和功能研究、蛋白质质量控制和疾病诊断等领域。另外,单分子蛋白测序还可应用于癌症诊断和治疗监测,可以更准确地评估癌症患者的疾病进展情况。
02
詹姆斯·韦伯太空望远镜
(James Webb Space Telescope)
韦伯太空望远镜被设计用来接替哈勃太空望远镜的工作。哈勃拍摄了令人惊叹的宇宙景象,但也有盲点:它基本上看不到具有红外波段光信号的古老恒星和星系。要纠正这一点,需要一种仪器,能够灵敏地探测到源自数十亿光年之外的极其微弱的红外信号。
韦伯太空望远镜的最终设计包含了18个非常光滑的铍镜阵列,当完全展开时,直径为6.5米。
该设计填补了哈勃的空白。英国卡迪夫大学的天体物理学家Mikako Matsuura正在借助韦伯太空望远镜观察恒星和行星形成的宇宙尘埃的产生和毁灭。她说,与她的团队过去使用的望远镜相比,“这是完全不同的灵敏度和锐度”。“我们已经看到这些物体内部正在发生完全不同的现象——这太神奇了。”

03
立体电子显微术
(Volume electron microscopy)
之前的电子显微镜(EM)只能观测到样品的表面。深入研究需要将标本切成非常薄的薄片,这对生物学家来说通常是不够的。现在,研究人员正在将立体电子显微技术应用于包含数立方毫米的3D组织样本。
相较于传统的光学显微镜,体积电子显微镜具有更高的分辨率和更大的成像深度,能够清晰地显示出细胞内结构和器官间关系。此外,体积电子显微镜还具有较高的灵敏度和动态范围,能够对动态过程进行成像。
伦敦弗朗西斯·克里克研究所的电子显微镜专家Lucy Collinson已经在传染病研究和癌症生物学中看到了价值。她正在探索以高分辨率重建整个小鼠大脑的可行性——这项工作将需要进行十多年,耗资数十亿美元,并产生5亿千兆字节的数据。“这可能与绘制第一个人类基因组的努力处于同一数量级。”她说。
04
CRISPR无处不在
(CRISPR anywhere)
CRISPR 是一种基因编辑技术,能够精确地修改基因组中的特定位置,具有高效率、简便、灵敏等特点,而CRISPR-Cas9是精确整个基因组目标位置的首选方法,推动了基因治疗、疾病建模和其他研究领域的突破。
CRISPR编辑由一个短引导RNA协调,利用RNA分子将特定的酶,如CRISPR-associated 9(Cas9)酶,导向特定的基因位置,并进行基因修饰,但这种酶还需要一个邻近的序列,称为原氨基酸邻接基序(PAM);如果缺失,编辑很可能会失败。随着技术的进步,基因组工程师Benjamin Kleinstiver使用蛋白质工程技术,从化脓性链球菌中创造出了常用的Cas9酶的Cas变体,这种酶几乎没有PAM。此外,Kleinstiver的团队正在设计和测试大量的Cas9变体,每个变体都对不同的PAM序列表现出高度的特异性。
还有许多自然产生的Cas变体仍有待发现。在自然界中,CRISPR-Cas9系统是一种细菌防御病毒感染的机制,不同的微生物进化出具有不同PAM偏好的各种酶,理论上来说,它允许研究人员编辑任何想要的碱基。
05
高精度放射性碳测
(High-precision radiocarbon dating)
自20世纪40年代以来,科学家们一直在使用放射性碳测定有机人工制品的年代,以缩小历史事件的日期。他们通过测量同位素碳14的痕迹来做到这一点,碳14是宇宙射线与地球大气相互作用的结果,并在数千年内缓慢衰变。但是这项技术通常只能精确到几十年以内。
2012年,由日本名古屋大学的物理学家Fusa Miyake领导的研究人员发现他们可以将日本雪松年轮中的碳14水平的一个特殊峰值确定为公元774年至公元775年。后续研究不仅证实了这种钉子存在于这一时期世界各地的木材样本中,而且还确定了至少五种其他类似的钉子,可追溯到公元前7176年。
考古学家现在将这种方法应用于新石器时代的定居点和火山爆发的遗址,并且希望用它来研究中美洲的玛雅帝国。

06
单细胞代谢组学
(Single-cell metabolomics)
代谢组学是研究驱动细胞的脂质、碳水化合物和其他小分子细胞组织代谢物的方法,目前正转向单细胞水平。单细胞代谢组学是一种对单个细胞的代谢过程进行研究的技术,它的基本原理是利用高通量测序技术,如RNA测序和质谱分析等,对单个细胞的代谢物进行测定。
许多代谢组学实验室研究解离的细胞,它们在毛细管中被捕获,并使用质谱进行单独分析。相比之下,“成像质谱”方法捕捉的是关于细胞代谢产物在样本中不同位置如何变化的空间信息。
现在,研究人员正在使这项技术大众化。2021年,德国海德堡欧洲分子生物学实验室的代谢组学研究员Alexandrov的小组制造了SpaceM,这是一种开源软件工具,它使用光学显微镜成像数据,通过标准的商业质谱仪实现培养细胞的空间代谢组学分析。
07
体外胚胎模型
(In vitro embryo models)
“类胚胎”模型中的一系列活动有助于胚胎早期阶段的分子机制研究,让研究人员更清楚地了解决定胎儿发育成败的关键早期事件。而体外胚胎模型正是一种在实验室中通过人工手段培养胚胎的方法。这种技术可以用来研究胚胎发育的初期阶段,也可以用来进行遗传学研究和药物筛选。
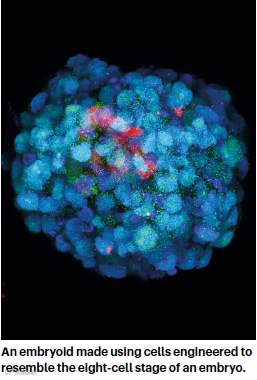
一种由类似胚胎八细胞阶段的细胞构成的胚状体
图片来自Nature
八细胞阶段的细胞,像所有多能干细胞一样,可以形成任何细胞或组织类型。它们可以与两种类型的胚胎外细胞密切相互作用,从而完成正常的胚胎发育。帕萨迪纳加州理工学院和英国剑桥大学的发育生物学家Magdalena Zernicka-Goetz和她的团队诱导胚胎干细胞成功形成了这些胚胎外细胞,并且可以在试管内生长。
在中国科学院广州生物医学与健康研究所,干细胞生物学家Miguel Esteban和他的同事们正在研究新的胚胎模型:对人类干细胞进行重新编程,以模拟早期发育阶段。他们的模型展示了天然八细胞胚胎中细胞的关键特征,并突显了人类和小鼠胚胎启动向八细胞阶段过渡的重要差异,这些模型可以帮助研究人员绘制出仅仅几个细胞是如何导致脊椎动物身体惊人的复杂性的。
请在后台回复“Nature”获取文章原文
科技不凡
致敬未来
出品:中技所研究发展部
参考:Nature、腾讯新闻、Hanson临床科研、细胞plus、Small Small bird
封面图片来自Nature

科技头条| 国新办2022年知识产权工作新闻发布会:知识产权高质量发展态势更显著

科技头条 | CES2023开幕,这些技术值得关注

科技头条 | 科技部部长王志刚:2023年科技工作这么干!




