哈佛大学医学院陶伟教授团队的研究方向主要包括生物材料、纳米技术和药物递送系统,以及它们在转化医学中的各种应用。在2023年伊始,我们持续关注并回顾了陶老师团队在2022年发表的研究成果供大家交流学习。
在2022年这一年中,陶老师团队取得了一系列高质量原创性的成果,其中13篇文章发表在PNAS / Nature子刊(包括Nature Medicine, Nature Nanotechnology, Nature Reviews Cardiology,Nature Protocols等)/ Cell姊妹刊上,另有10篇发表在Chemical Reviews / Chemical Society Reviews / Advanced Materials / Angewandte Chemie /Advanced Drug Delivery Reviews等领域内权威期刊上。去年,陶老师课题组的工作主要集中在先进mRNA药物递送系统、靶向心血管疾病的siRNA纳米药物、药物递送和组织再生水凝胶、智能口服给药系统、诊疗纳米药物等的开发。

陶伟教授是哈佛大学附属布莱根妇女医院Farokhzad Family创新杰出讲席教授(Endowed Chair)、哈佛大学医学院助理教授,也是所在单位历史上第一个以助理教授身份获得冠名杰出讲席教授头衔(Farokhzad Family Distinguished Chair for Innovation)的华人学者。陶教授致力于药物载体和生物材料的研发及其广泛的生物医学应用(尤其是mRNA/siRNA等核酸药物的递送)。陶教授目前以最后通讯或独立通讯作者身份在《Nature Medicine》、《Nature Nanotechnology》、《PNAS》、《Nature Reviews Materials》、《Nature Reviews Cardiology》、《Nature Protocols》、《Nature Communications》等国际顶级期刊发表论文70余篇。陶教授所带领团队所研发的多种mRNA药物递送核心技术已获系统性的专利、具有良好的产业化背景,鉴于他在药物递送研究领域的影响力和积极贡献,他团队研发的药物递送技术(尤其mRNA递送技术)受到顶级医学期刊《Nature Medicine》的大篇幅亮点报道(Nature Medicine 2022, 28(6):1100-1102),与陶教授共同接受专访的专家还包括Moderna公司共同创始人/麻省理工学院Robert Langer院士、辉瑞制药(Pfizer)研发副总裁Nicholas Warne博士、BioNTech药物递送技术副总裁Steffen Panzner博士、哈佛大学Samir Mitragotri院士等全球行业领袖或顶级学者。
陶教授是科睿唯安“全球高被引学者”(2021年起连续入选榜单)、全球前2%顶尖科学家(2019年起连续入选斯坦福大学发布的年度影响力榜单),《麻省理工科技评论》曾将他选为科技创新35人之一(TR35),微软学术曾将他选为纳米技术的全球前5位趋势作者以及纳米医学的顶级作者。此外,化学领域期刊《Chemical Society Reviews》曾将陶教授选为全球范围内的Emerging Investigator,材料领域期刊《Advanced Materials》和《Materials Today》也都曾共同将陶教授评为全球范围内Rising Star。陶教授还曾作为PI获得了美国METAvivor青年研究员奖、美国心脏协会合作科学奖、哈佛大学医学院/布莱根妇女医院启动基金、纳米医学研究中心基金、系基础科学基金、Khoury科技创新奖、Gillian Reny Stepping Strong研究中心突破创新者奖、纳米技术基金等项目资助。
陶教授还受邀担任了爱思唯尔和中国科学出版社旗下期刊《Biomedical Technology》的创刊主编、约翰威立出版社旗下期刊《Exploration》副主编、施普林格·自然集团和BMC旗下期刊《Journal of Nanobiotechnology》期刊副主编,细胞出版社旗下期刊《Matter》的顾问编委(Advisory Board Member),以及《eLife》期刊客座编辑(Guest Editor)等。
课题组网站主页: https://www.weitaolab.com/
陶伟教授课题组2022年成果集锦:
1. PNAS (IF 12.779) 封面论文“首个粘膜黏附mRNA纳米粒子”:膀胱内灌注粘膜黏附纳米粒子递送KDM6A-mRNA抑制膀胱癌的转移

转移是膀胱癌等恶性肿瘤治疗失败的重要原因,间质微环境的表观遗传调控是影响肿瘤转移的重要因素。赖氨酸特异性去甲基化酶6A(KDM6A),在膀胱癌中频繁突变。虽然被认为是一种肿瘤抑制因子,但KDM6A在膀胱癌转移中的治疗潜力仍然难以捉摸。在膀胱肿瘤组织中有效上调KDM6A水平,以验证其治疗膀胱癌转移的潜力,也仍有困难。
基于此,哈佛大学医学院陶伟教授团队报道了一种粘膜黏附mRNA纳米颗粒策略,用于KDM6A-mRNA在原位Kdm6a基因缺失的膀胱癌小鼠模型的膀胱内膀胱灌注给药,并显示了KDM6A抑癌因子的表达在抑制膀胱癌转移方面的治疗潜力。通过这种粘膜黏附mRNA纳米颗粒策略,可以大大延长KDM6A-mRNA在原位膀胱癌区域的暴露时间,使其有效表达KDM6A抑癌因子,与此同时也可以通过膀胱黏附性能增强其穿透力,使其持续递送。这种mRNA纳米颗粒策略也被证明是有效的联合癌症治疗与其他临床批准的药物,这可以进一步提高治疗效果。本研究不仅实现了通过粘膜黏附mRNA纳米颗粒策略在膀胱内灌注给药递送mRNA,而且还为这些mRNA纳米颗粒作为有效工具在膀胱相关疾病的机制理解和转化研究中的实用性提供了概念证明。
【论文信息】Kong N, …, Tao W*. Intravesical delivery of KDM6A-mRNA via mucoadhesive nanoparticles inhibits the metastasis of bladder cancer. PNAS2022, 119(7): e2112696119.
https://www.pnas.org/doi/10.1073/pnas.2112696119
2. Nature Medicine (IF 87.241): mRNA纳米药物全景解读
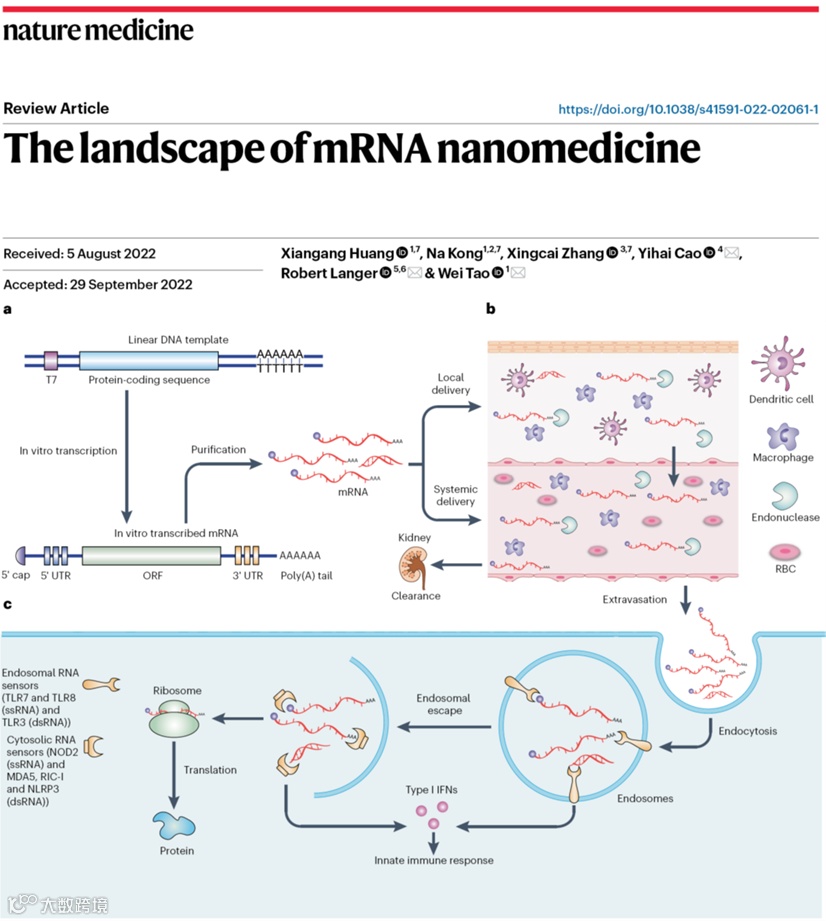
mRNA是一类新兴的治疗性药物,可用于预防和治疗多种疾病。Moderna和辉瑞-BioNTech生产的两种高效mRNA疫苗在预防新冠肺炎方面大获成功,突显了mRNA技术在改变生命科学和医学研究方面的巨大潜力。mRNA在稳定性、免疫原性、体内递送和跨越多种生物屏障的能力等方面面临的挑战,近年来,已经在很大程度上通过mRNA工程和递送的进展得到了解决。
基于此,哈佛大学医学院陶伟教授团队联合麻省理工学院Robert Langer教授、卡罗林斯卡学院曹义海教授合作,撰文概述了mRNA纳米药物,讨论了基于mRNA的治疗面临的技术挑战,并将其与生物学机制和临床结果联系起来。并详细介绍了在不断发展的mRNA纳米医学领域的最新进展和创新,以及正在进行的临床转化和未来提高临床疗效的方向。
【论文信息】Huang X, …, Tao W*. The landscape of mRNA nanomedicine. Nature Medicine 2022, 28(11):2273–2287.
https://www.nature.com/articles/s41591-022-02061-1
3. Nature Reviews Cardiology (IF 49.421): 巨噬细胞靶向纳米医学在动脉粥样硬化诊断和治疗中的应用

动脉粥样硬化(Atherosclerosis)所引发的心肌梗塞和中风等心血管疾病是全球常见的疾病及致死原因,而巨噬细胞对于此疾病的发展与病理成因扮演了重要且关键的角色。因此,和巨噬细胞相关的病理过程也被视为极其重要的动脉粥样硬化诊断与治疗的靶点。然而现有的临床方法对于动脉粥样硬化的诊疗仍然存在相当多的瓶颈与挑战。基于纳米颗粒的纳米医药,因其可有效地负载并提升药物的稳定性以及精准地递送药物至病灶部位,已被视为能有效地提升动脉粥样硬化的诊断与治疗的新兴技术。
哈佛大学医学院陶伟教授团队联合哥伦比亚大学医学院Ira Tabas教授团队、哈佛大学医学院施进军教授合作,共同撰文系统全面地介绍了过去二十年中关于靶向巨噬细胞的纳米医药在动脉粥样硬化的诊断与治疗的应用,并对目前该领域仍存在的挑战提出相应的解决方案及展望。
【论文信息】Chen W, …, Tao W*. Macrophage-targeted nanomedicine for diagnosis and treatment of atherosclerosis. Nature Reviews Cardiology 2022, 19(4):228–249.
https://www.nature.com/articles/s41569-021-00629-x
4. Nature Nanotechnology(IF 40.523): 基于纳米技术的策略对抗SARS-CoV-2变异株
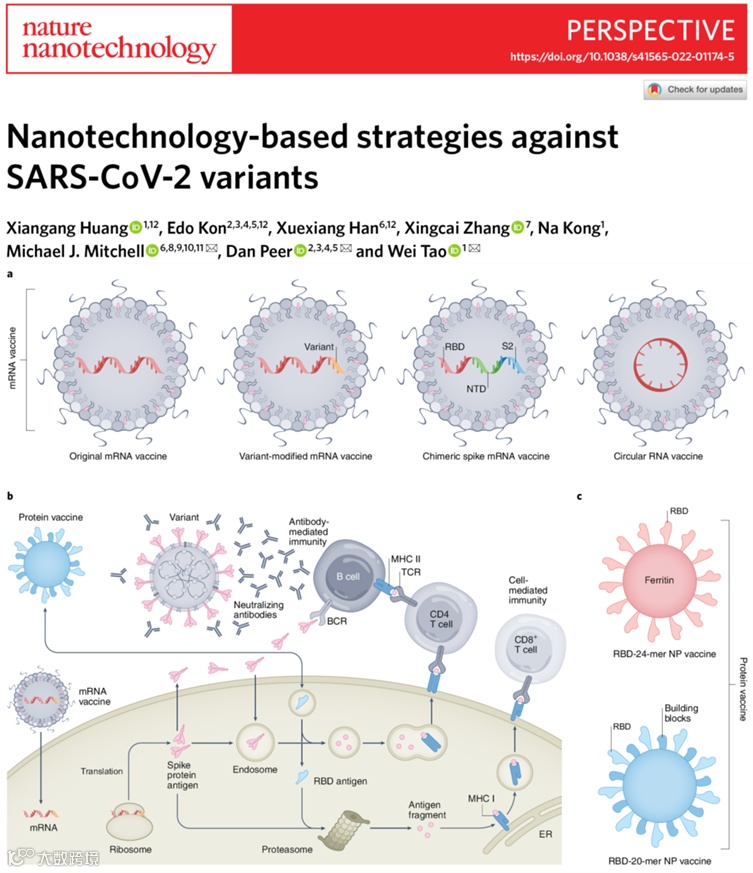
新型冠状病毒(SARS-CoV-2)引发目前的新冠肺炎大流行并在全球范围导致超过5亿人感染。纳米技术在对抗新冠病毒的各个方面都发挥着重要的作用,尤其是在发展高效的基于纳米技术的新冠mRNA疫苗方面。尽管目前的mRNA疫苗能有效预防原始的新冠毒株,但是利用该疫苗快速结束新冠肺炎大流行的期望被不断涌现的新冠病毒变种浇灭。
哈佛大学医学院陶伟教授团队、以色列特拉维夫大学Dan Peer教授团队以及宾夕法尼亚大学Michael J. Mitchell教授团队合作,联合撰写了基于纳米技术的策略在对抗新冠病毒变种领域的重要应用,并展望了各项新型抗病毒纳米疗法临床转化的进展和挑战,对后续开发更有效的对抗新冠病毒变种的疫苗和疗法具有重要意义。
【论文信息】Huang X, …, Tao W*. Nanotechnology-based strategies against SARS-CoV-2 variants. Nature Nanotechnology 2022, 17(10):1027–1037.
https://www.nature.com/articles/s41565-022-01174-5
5. Nature Protocols (IF 17.021): 合成siRNA纳米颗粒以沉默动脉粥样硬化病变巨噬细胞中斑块不稳定基因

动脉粥样硬化病变中的巨噬细胞促进斑块进展,是心血管研究中一个有吸引力的治疗靶点。在人类和小鼠动脉粥样硬化斑块的晚期巨噬细胞中,Ca2+/钙调蛋白依赖性蛋白激酶γ(CaMKIIγ)活性通过下调胞浆化受体MerTK的表达来驱动坏死。因此,选择性抑制病变巨噬细胞中的CaMKIIγ为晚期动脉粥样硬化的治疗带来了巨大希望。
基于此,哈佛大学医学院陶伟教授课题组提出了一种小干扰RNA(siRNA)纳米颗粒的合成方案,靶向病变巨噬细胞作为动脉粥样硬化的潜在治疗。提供了一套详细的方案,包括纳米粒组分的合成,siRNA纳米粒的制备和表征(物理化学和体外),以及siRNA纳米粒的体内治疗效果及其在动脉粥样硬化小鼠中的生物相容性评估。并通过改变纳米颗粒中装载的RNA分子,考察其靶向病变巨噬细胞,探索和验证了动脉粥样硬化的新靶点/通路。
【论文信息】Huang X, …, Tao W*. Synthesis of siRNA nanoparticles to silence plaque-destabilizing gene in atherosclerotic lesional macrophages. Nature Protocols 2022, 17(3):748–780.
https://www.nature.com/articles/s41596-021-00665-4
6. Nature Communications (IF 17.694): 基于微藻的口服微载体用于肠道肿瘤放疗中的菌群稳态维护和肠道保护
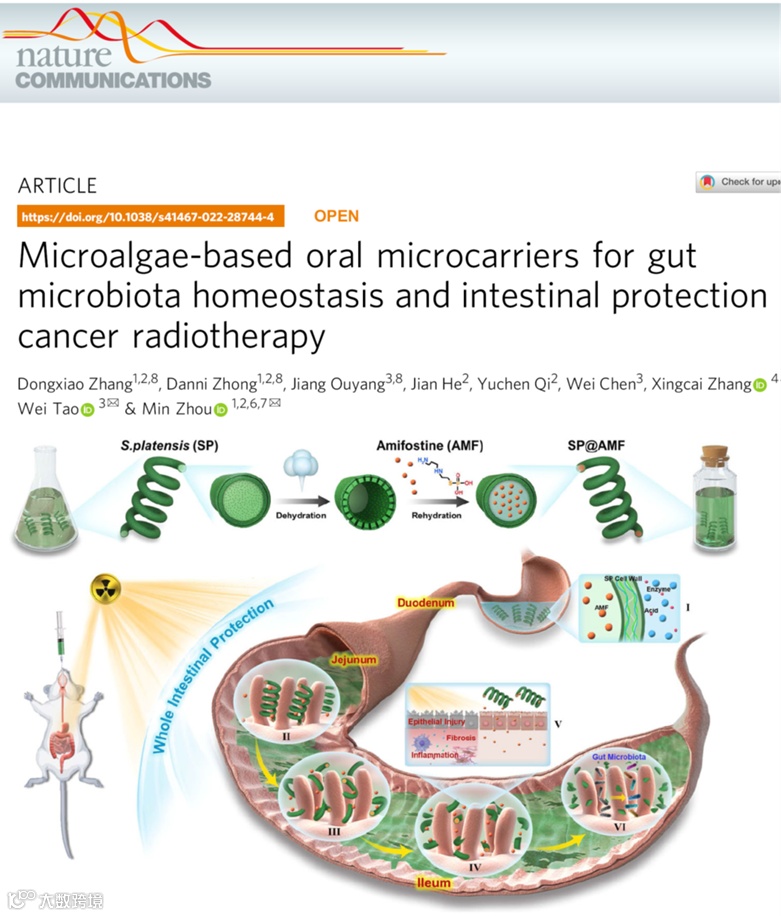
放疗是一种在临床治疗中被广泛使用的癌症治疗方法,然而,放疗中的辐照除了杀伤癌细胞,同样也会损害健康组织,从而导致多种副作用。在腹部/盆腔实体瘤(例如胰腺癌、前列腺癌、结直肠癌等)的放疗中,由于小肠对辐射敏感、器官体积大,因此成为放疗的常见损伤部位。强放疗引起的肠道损伤可导致胃肠功能障碍甚至死亡。因此,在放疗中需要预防辐射引起的肠道损伤。但在实际治疗中,放疗的辐照部位因人而异,导致小肠的受损部位难以预测。这使得对整个小肠进行全面辐射防护成为一个亟待解决的重要问题。
在腹盆腔实体肿瘤放疗过程中,如何保护全小肠免受放射性肠损伤仍是临床亟待解决的问题。阿米福汀是一种有前景的正常组织选择性辐射防护剂,但其口服应用于肠道辐射防护仍具有挑战。因此,开发出合适的口服给药策略,将有助于使用阿米福汀保护肠道组织免受放疗过程中的辐射损伤。基于此,哈佛大学医学院陶伟教授团队联合浙江大学周民教授团队,以钝顶螺旋藻作为阿米福汀的微载体,构建阿米福汀口服给药系统。该系统在全小肠内表现出全面的药物蓄积和有效的辐射防护,明显优于游离药物及其肠胶囊,在不影响肿瘤消退的情况下预防了放射性肠损伤,延长了生存期,可实现对全小肠的有效辐射防护,为临床转化提供了一种具有竞争力的策略。
【论文信息】Zhong D, …, Tao W*, Zhou M*. Microalgae-based oral microcarriers for gut microbiota homeostasis and intestinal protection in cancer radiotherapy. Nature Communications 2022, 13:1413.
https://www.nature.com/articles/s41467-022-28744-4
7. 细胞出版社Trends in Chemistry (IF 22.448): 新兴仿生纳米技术在骨科疾病中的应用:进展、挑战与机遇
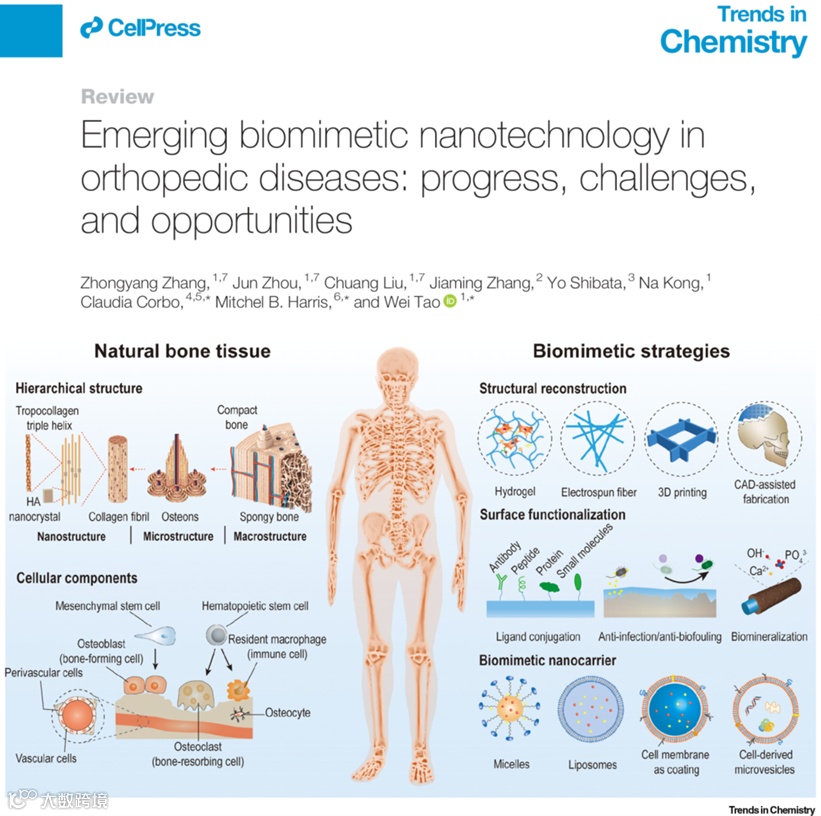
骨科疾病(如骨折、骨肿瘤、骨关节炎、骨质疏松、慢性炎症和感染)可导致运动障碍、对其他软组织/器官的保护丧失、造血功能障碍、矿物质稳态和其他功能障碍。仿生纳米技术的发展促进了修复天然骨组织结构、成分和生物生理功能的骨科治疗创新。明确发病机制和了解疾病进展对设计和优化疾病特异性治疗具有重要意义。
哈佛大学医学院陶伟教授课题组就仿生纳米技术如何更有效地应用于各种骨科疾病的治疗进行综述,并讨论了未满足的需求和当前可能阻碍基于仿生纳米技术的骨科治疗临床实施的挑战及展望。
【论文信息】Zhang Z, …, Tao W*. Emerging biomimetic nanotechnology in orthopedic diseases: progress, challenges, and opportunities.Trends in Chemistry 2022, 4(5):420-436.
https://www.cell.com/trends/chemistry/fulltext/S2589-5974(22)00048-X
8. 细胞出版社Matter (IF 19.967): 通过肿瘤微环境响应性siRNA微束将“冷”肿瘤转化为“热”肿瘤用于增强免疫治疗
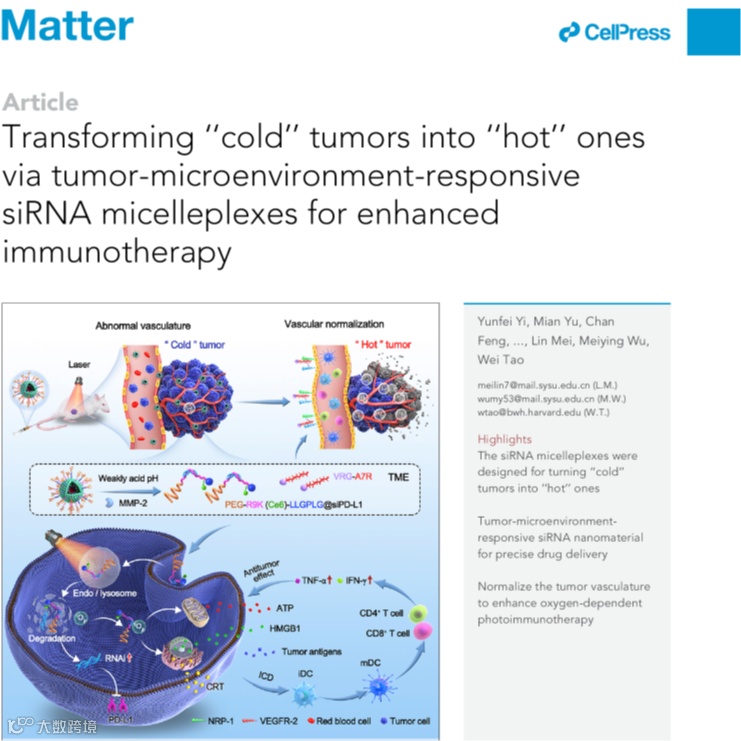
将“冷”肿瘤转变为“热”肿瘤以提高抗肿瘤免疫治疗的疗效在临床医学上是非常有前景的。鉴于此,哈佛大学医学院陶伟教授团队联合中山大学梅林、吴玫颖教授团队开发了基于肽的小干扰RNA胶束复合物(PA7R@siPD-L1),用于使血管免疫串扰正常化,从而在增强抗肿瘤免疫治疗中建立正反馈回路,增强抗肿瘤作用免疫疗法。这些微束具有肿瘤微环境响应特性,可实现精确的药物递送和释放。所制备的PA7R@siPD-L1介导的光动力治疗可清除实体瘤并激发免疫原性细胞以产生系统的免疫反应。与此同时,抗血管生成肽A7R使肿瘤血管正常化将混乱的血管系统转化为成熟和有组织的从而减轻肿瘤乏氧,促进瘤内生长免疫细胞的浸润。抗肿瘤免疫原性在siPD-L1的辅助下,通过减弱肿瘤细胞对免疫效应细胞的耐药性进一步增强。这项研究提供了一种独特的治疗策略,将“冷”肿瘤转化为siRNA纳米材料致“热”肿瘤。
【论文信息】Yi Y, …, Tao W*. Transforming “cold” tumors into “hot” ones via tumor-microenvironment-responsive siRNA micelleplexes for enhanced immunotherapy. Matter 2022, 5(7):2285-2305.
https://www.cell.com/matter/fulltext/S2590-2385(22)00210-7
9. 细胞出版社Med:癌症纳米医学走向临床转化:障碍、机遇和未来展望

随着纳米技术在医学领域的广泛应用,纳米药物在治疗包括癌症在内的各种疾病方面取得了长足的进步。癌症纳米药物在临床前研究中不仅改善了治疗效果,还延长了生存期,减少了副作用。然而,从实验室到临床的转化仍然具有挑战性。虽然一些纳米药物已经进入临床试验,但只有少数被批准用于临床应用。
近期,哈佛大学药学院陶伟教授团队接受细胞出版社Cell姊妹刊(医学方向)Med邀请,撰写介绍了肿瘤纳米医学的最新进展,讨论了当前肿瘤纳米医学的临床进展和转化面临的挑战,并提出了加速肿瘤纳米医学临床转化的观点和展望。
【论文信息】Zhang P, …, Tao W*. Cancer nanomedicine toward clinical translation: Obstacles, opportunities, and future prospects. Med 2022, doi:10.1016/j.medj.2022.12.001.
https://www.cell.com/med/fulltext/S2666-6340(22)00517-7
10. 细胞出版社Matter (IF 19.967): 精确控制合成水凝胶网络的结构用于精准医学应用

水凝胶是在水或生物流体中膨胀的三维聚合物网络。值得注意的是,水凝胶设计和合成的快速进展已迅速应用于生物医学应用,如抗癌和抗菌治疗以及生物传感。由于精准医学是一种快速发展和流行的全球疾病治疗趋势,考虑到个体差异以解决未满足的医疗需求的方案尤其有潜力。因此,人们对定制材料(如水凝胶)的需求很高,它可以靶向患者的特定组织和细胞,并以可控的方式释放负载的药物。为此,精确控制具有独特刚度、结构、溶质扩散和理化性质的人工合成水凝胶网络结构,对生物医学应用尤为有利。近期,哈佛大学医学院陶伟教授团队接受细胞出版社Cell姊妹刊(材料科学方向)Matter邀请,撰写前瞻论文讨论了人工合成水凝胶网络结构的精确控制在药物递送和生物医学领域发挥着重要作用。
【论文信息】Chen W, …, Tao W*. Precise control of the structure of synthetic hydrogel networks for precision medicine applications. Matter 2022, 5(1):18-19.
https://www.cell.com/matter/fulltext/S2590-2385(21)00632-9
11. 细胞出版社Matter (IF 19.967): 用于胃肠道靶向mRNA口服给药的机器人药丸
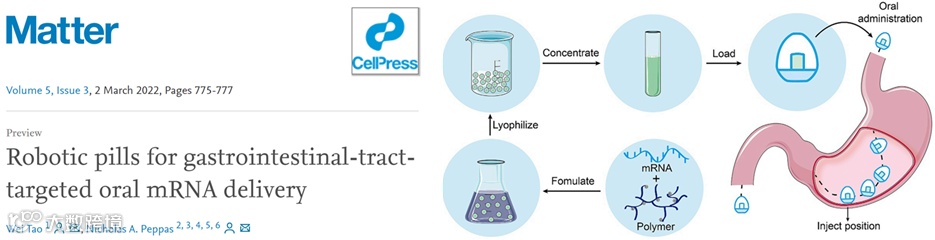
以核酸为基础的药物,尤其是以mRNA为基础的药物和疫苗,已被证明在治疗和预防多种疾病方面表现出较高的疗效。mRNA疫苗在控制COVID-19大流行方面的关键作用凸显了基于mRNA的药物的巨大潜力,促进了各种基于mRNA的生物医学应用的快速发展,包括疫苗、免疫治疗、基因编辑和功能蛋白修复等,以应对不同的疾病。与传统疫苗相比,mRNA疫苗具有极高的效力和短得多的开发周期,这对于快速减缓SARS-CoV-2等传染性强的病毒的传播至关重要。
近期,哈佛大学医学院陶伟教授和德克萨斯大学奥斯汀分校Nicholas A. Peppas教授共同接受细胞出版社Cell姊妹刊(材料科学方向)Matter邀请,撰写前瞻论文讨论了口服mRNA药物的可能性和未来发展。该论文也同时评论了麻省理工学院Robert Langer教授和Giovanni Traverso教授团队报道的机器人药丸用于胃肠道靶向口服mRNA递送的设计和使用,为口服mRNA药物开辟了新途径。
【论文信息】Tao W*, Peppas NA*. Robotic pills for gastrointestinal-tract-targeted oral mRNA delivery. Matter 2022, 5(3): 775-777.
https://www.cell.com/matter/fulltext/S2590-2385(22)00059-5
12. 细胞出版社Matter (IF 19.967): 基于膨胀聚合物网络模型的应用优化水凝胶设计

水凝胶是具有三维网络的聚合物,在水或生物流体中膨胀。水凝胶设计和合成的快速进展使其在生物医学领域得到了广泛的应用。例如,水凝胶可作为不同生物活性分子包括小干扰RNA (siRNA)、细胞因子和抗体的新型递送载体,或作为模拟细胞外基质的细胞培养支架。由于水凝胶的聚合物网络结构在货物运输效率方面发挥着重要作用,因此提高对水凝胶物理性质(如橡胶弹性、平衡膨胀和网格运输)的理解具有重要意义,尤其是对于实现精准医疗。这为建立稳健的数学模型提供了强有力的理论基础,该模型可以将水凝胶的物理性质与其合成条件关联起来,因此当定制的水凝胶可用时,可以很好地控制货物的释放和扩散行为。近期,哈佛大学医学院陶伟教授团队接受细胞出版社Cell姊妹刊(材料科学方向)Matter邀请,撰写前瞻论文讨论了应用优化水凝胶的设计在扩大其生物医学应用方面的前景。
【论文信息】Ouyang J, Chen W, Tao W*. Design of application-optimized hydrogels based on a swollen polymer network model. Matter 2022, 5(8): 2471-2473.
https://www.cell.com/matter/fulltext/S2590-2385(22)00315-0
13. 细胞出版社The Innovation: 二维单元素纳米片(Xenes)和水凝胶的结合:基础、应用和展望
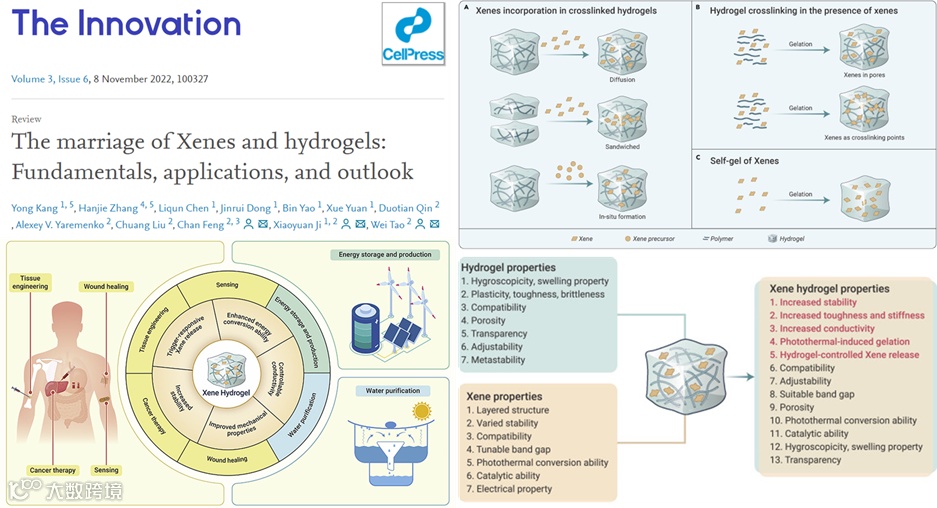
水凝胶通常是由亲水性聚合物和水组成的三维网络,具有膨胀性、透光性、柔软性、生物相容性和易改性等特点。水凝胶在日常生活和生物医学领域中具有极大的实用价值。然而,水凝胶聚合物之间的相互作用较弱,无法保持延展性和稳定性。水凝胶可以为其他材料提供附着点,作为很好的载体。为了进一步提升水凝胶性能,通常将不同的材料加入到水凝胶基质中。由于二维平面内载流子的受限迁移和热扩散,二维材料的介入是改善水凝胶性能和扩大其应用范围的有效方法。一方面,由于Xenes具有的原子级厚度,显示出优异的物理和化学反应活性,如电学、光学、磁学和催化性质;另一方面,从其单元素组成来看,Xenes与其他二维材料相比具有优异的性能和广泛的应用前景。
Xenes中X原子的杂化形式是sp2或sp3,使Xenes结构简单,可预测、可控制和可感知。 Xenes还可以通过改变其结构来调整其性质。Xenes组分简单,降解只产生有限或无害的产物,有助于保护环境和实现高生物兼容性。但Xenes在反应中受限、在嵌入3D基质中缺乏稳定性等问题限制了其应用范围,因此,学界尝试将新兴的Xenes引入水凝胶网络中,即利用三维水凝胶作为二维Xenes的支架,提高水凝胶的性能,拓展其应用空间。
近期,哈佛大学医学院陶伟教授团队接受细胞出版社The Innovation邀请,联合天津大学姬晓元教授团队发表了综述论文,对Xenes水凝胶的合成方法、性能及应用进行详细的综述。介绍了各种合成方法的一般特点和优缺点,供研究人员根据不同的需要进行选择。详细介绍新兴Xenes水凝胶的一般和特殊性质,并与传统水凝胶进行比较,总结了它们的优势和未来面临的挑战。
【论文信息】Kong Y, …, Tao W*. The marriage of Xenes and hydrogels: Fundamentals, applications, and outlook. The Innovation 2022, 3(6): 100327.
https://www.cell.com/the-innovation/fulltext/S2666-6758(22)00123-0
14. Chemical Reviews (IF 72.087): NIR-II诊疗纳米药物: 分类、制备和其生物医学应用

近二十年来,近红外II(NIR-II)窗口(1000 ~ 1700 nm)的多功能无机/有机荧光团或生物材料的快速发展,促进了诊疗纳米医学的快速发展。高分辨率的深部组织NIR-IIa/IIb成像具有无放射性、灵敏度高、反馈快的特点。近期,哈佛大学医学院陶伟教授联合Omid C. Farokhzad教授,共同接受ACS出版社Chemical Reviews邀请,综述了NIR-II诊疗纳米药物在成像引导的联合治疗、药物释放监测、治疗反应监测等方面的生物医学应用。NIR-II诊疗纳米药物能够将成像/诊断功能与治疗功能整合在一起,实现成像引导的高治疗效果。基于无机/有机荧光团或生物材料的诊疗纳米药物的进展能够实现无创的NIR-IIa/IIb成像,推动了诊疗纳米医学从“近红外I窗口”时代进入“近红外II窗口”时代。该论文也前瞻性地讨论了NIR-II诊疗纳米药物各类生物医学应用和未来发展趋势。
【论文信息】Tao W*, Farokhzad OC*. Theranostic Nanomedicine in the NIR-II Window: Classification, Fabrication, and Biomedical Applications. Chemical Reviews 2022, 122(6):5405-5407.
https://pubs.acs.org/doi/10.1021/acs.chemrev.2c00089
15. Chemical Society Reviews (IF 60.615): 微创纳米医学:光/超声/辐射/磁介导的纳米技术在治疗和成像中的应用
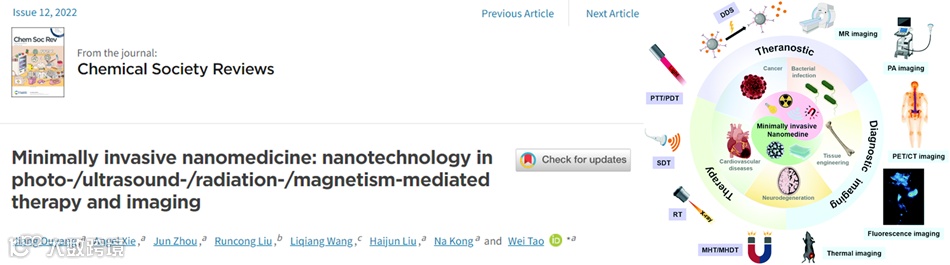
传统的治疗方法如化疗和手术通常会引起严重的副作用和难以忍受的疼痛。纳米医学和微创疗法的出现为恶性疾病患者带来了希望。特别是微创纳米药物,将纳米药物和微创疗法的优势结合起来,可有效靶向病理细胞/组织/器官,提高药物的生物利用度,减少副作用,实现小切口或无切口的无痛治疗,从而获得良好的治疗效果。
近期,哈佛大学医学院陶伟教授作为Chemical Society Reviews期刊Emerging Investigator Lectureship的获得者受邀发表综述论文,就纳米技术在光/超声/辐射/磁介导的治疗和成像方面的医学应用现状、面临的挑战等进行了全面总结,并就其内在机制进行了探讨。此外,本论文还讨论了微创纳米药物在各种生物医学领域的应用,包括癌症、心血管疾病、组织工程、神经功能疾病、细菌感染及其与其他治疗模式的结合等。本论文最后还有建设性地展望了该领域所面临的挑战的解决办法、及微创纳米药物的未来发展和临床转化。
【论文信息】Ouyang J, …, Tao W*. Minimally invasive nanomedicine: nanotechnology in photo-/ultrasound-/radiation-/magnetism-mediated therapy and imaging. Chemical Society Reviews 2022, 51(12): 4996–5041.
https://pubs.rsc.org/en/content/articlelanding/2022/cs/d1cs01148k
16. Chemical Society Reviews (IF 60.615) 封面论文:新兴mRNA技术:递送策略和生物医学应用

信使RNA(mRNA)在1960年代初首次被发现,并在1970年代被递送到细胞内并成功表达蛋白质。与基于DNA的蛋白质表达技术不同,mRNA不需要进入细胞核来实现其功能,因此不会插入原始基因组,引起基因变异。在过去的几十年中,利用mRNA表达多种蛋白质来治疗不同疾病的概念引起了科学界的关注。对mRNA的修饰和递送平台设计的研究高效、快速地推动了mRNA技术的发展,但早期主要停留在学术界。直到COVID-19的全球爆发,Pfizer/ BioNTech和Moderna的mRNA疫苗的成功上市及其在预防病毒传播方面的有效性让mRNA技术从学术界进入公众视野(也铸就了历史上最赚钱疫苗的传奇:已在全世界接种数亿剂;仅2021年一年,其全球销量就能达到500亿美元),对mRNA技术的研究也蓬勃发展。
mRNA属于单链长多核苷酸,极易被核糖核酸酶快速降解。此外,细胞膜通过静电排斥作用进一步阻碍了mRNA进入细胞执行蛋白转染功能。因此,需要载体保护mRNA免被降解、高效运输mRNA至目标细胞内才能实现其功能。目前研究中已经开发了各类非病毒载体来实现mRNA的高效递送,主要包括:蛋白质-mRNA复合物、脂质载体(Lipid Nanoparticles)、聚合物载体、混合载体等。通过对载体的化学设计,可以实现mRNA在不同器官内的递送;通过对载体内各组分的比例优化,可以实现mRNA的高效递送。
基于此,哈佛大学医学院陶伟教授团队联合浙江大学孔娜教授团队发表综述论文,对新兴mRNA技术的重要进展,以及潜在的化学设计和原理进行了总结和讨论。重点介绍了用于各种生物医学应用(例如功能性蛋白表达、疫苗、癌症免疫治疗和基因组编辑)的典型mRNA递送平台,并展望了mRNA技术临床转化的进展和挑战,为mRNA技术今后进一步的发展指出了可能的方向。
【论文信息】Xiao Y, …, Tao W*. Emerging mRNA technologies: Delivery strategies and biomedical applications. Chemical Society Reviews 2022, 51(10): 3828-3845.
https://pubs.rsc.org/en/content/articlelanding/2022/cs/d1cs00617g
17. Advanced Materials (IF 32.086): 基于白细胞的药物递送系统

白细胞在免疫应答中发挥重要作用,包括防御入侵病原体、重建受损组织和维持免疫稳态。当体内免疫系统被激活时,白细胞完成了一系列有序而复杂的调节过程,对疾病的发生和控制至关重要。白细胞已被证明会大量聚集在病灶部位,并显著促进炎症和癌症进展。近年来,以白细胞为基础的给药系统因其固有和特异性靶向作用、低免疫原性、疗效提高和低逆转作用而受到广泛关注。
基于此,哈佛大学医学院陶伟教授团队联合清华大学张灿阳研究员团队发表了综述论文,聚焦白细胞给药体系(巨噬细胞、中性粒细胞和淋巴细胞等)在治疗癌症和炎症相关疾病的最新进展,讨论基于白细胞的药物递送系统的优势、目前面临的挑战和局限性,并对未来精准靶向治疗在临床的发展进行了展望。
【论文信息】Chen Y, …, Tao W*. Living Leukocyte-Based Drug Delivery Systems. Advanced Materials2022, doi:10.1002/adma.202207787.
https://onlinelibrary.wiley.com/doi/10.1002/adma.202207787
18. Advanced Materials (IF 32.086): 纳米异质结介导的热电策略用于癌症手术辅助治疗和β-榄香烯联合治疗

手术作为肿瘤治疗不可或缺的策略,具有肿瘤复发和伤口感染的缺点。本文提供了一种热电治疗策略,可作为独立的癌症治疗或手术辅助治疗。通过两步水热法制备了由z型热电异质结(BST/BTS)组成的Bi0.5Sb1.5Te3(BST)和Bi2Te2.8Se0.2(BTS)纳米片。BST和BTS之间的接触由于费米能级重排而形成界面电场,引导BTS的导电带(CB)中的电子与BST的价带(VB)中的空穴结合,使BST的CB和BTS的VB中的电子和空穴具有更强的还原/氧化电位。此外,在温和的温度梯度下,形成了另一个自内置电场,促进电子和空穴向其表面迁移。
基于此,哈佛大学医学院陶伟教授团队联合杭州师范大学药学院谢恬教授团队、天津大学姬晓元教授团队合作发表论文,构建了聚乙二醇化BST/BTS异质结,通过静脉注射BST/BTS和肿瘤外部冷却,开发了一种新型的热电治疗平台。这种热电策略也被证明是有效的联合β-榄香烯治疗癌症。此外,将异质结与水凝胶结合应用于术后创面,可实现有效的残余肿瘤治疗和抗菌作用。
【论文信息】Ji X*, …, Tao W*, Xie T*. Nanoheterojunction-mediated thermoelectric strategy for cancer surgical adjuvant treatment and β-elemene combination therapy. Advanced Materials 2022, doi: 10.1002/adma.202207391.
https://onlinelibrary.wiley.com/doi/10.1002/adma.202207391
19. Advanced Materials (IF 32.086): 调整光敏剂的聚集程度来增强光疗效力以激发全身抗肿瘤免疫
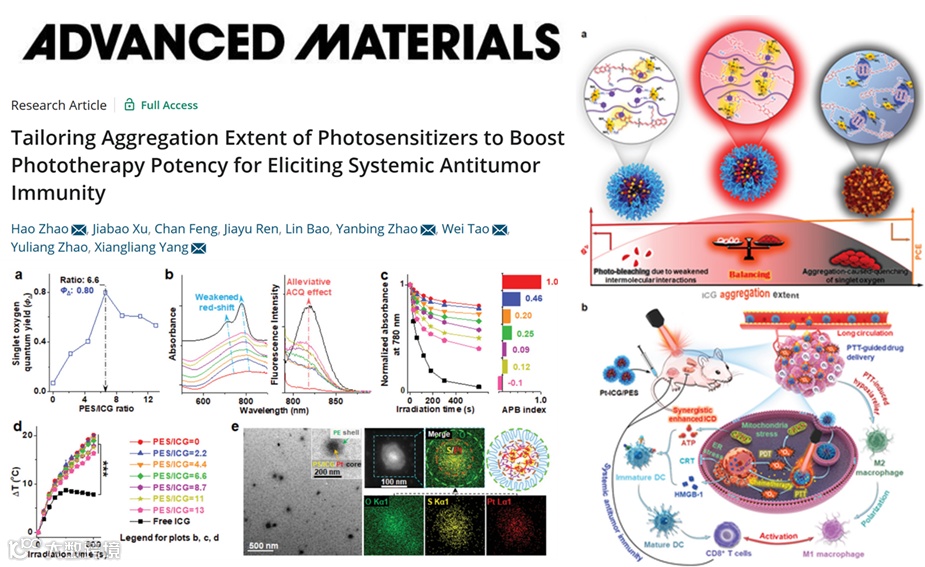
肿瘤的复发与转移是导致癌症患者死亡的主要原因,而免疫治疗对转移性肿瘤具有优异的抑制作用。采用多种物理化学方法(如近红外光、药物、放射线等)触发肿瘤细胞的免疫原性死亡(ICD),释放肿瘤相关抗原,增强杀伤性T细胞的肿瘤浸润是提高肿瘤免疫治疗效果的常用手段。如光热/光动疗法(PDT/PTT)是触发ICD效应、增强抗肿瘤免疫响应最为有效的疗法之一。然而,大部分光敏剂都面临聚集诱导猝灭(ACQ)和光漂白效应这两个不可调和的矛盾,光物理性能大大降低。这极大地限制了PDT/PTT激活抗肿瘤免疫响应以及肿瘤复发转移抑制的能力。当前主要采用复杂的化学接枝/偶联反应路线,引入大位阻基团或装载到纳米笼内等增加分子间距离的方法来克服ACQ效应。但这些策略往往忽视了分子间距离增大导致光敏剂耐光漂白性能降低问题。
基于此,华中科技大学生命学院/国家纳米药物工程技术中心赵彦兵/杨祥良团队与国家纳米中心赵宇亮院士团队、哈佛大学医学院陶伟教授团队合作,提出了离散纳米组装策略以调控光敏剂分子间距离。首先,利用温敏大分子间隔剂PES的分子组成和用量调控化疗药物顺铂金属离子与光敏剂吲哚菁绿(ICG)的配位共组装,所构建的离散纳米组装体Pt-ICG/PES在ICG与PES摩尔比(PES/ICG)为6.6时,表现出优异的PDT/PTT效应(单线态氧量子产率Φ∆ ≈ 0.8,比文献报道最大值高7~8倍),并与顺铂协同激发强烈的ICD效应,激活DC细胞和杀伤性T淋巴细胞,表现出了强大的肿瘤转移抑制能力。而且,利用PES的温敏性亲水-疏水转变特性,Pt-ICG/PES在静脉注射后,还实现了高效的光热靶向递送,增强其激光引导下的肿瘤定位蓄积。此外,Pt-ICG/PES还改善了肿瘤乏氧微环境,促进M2向M1型巨噬细胞逆极化,与杀伤性T淋巴细胞协同发挥全身肿瘤抑制效应。在荷瘤小鼠模型中,Pt-ICG/PES诱导了危险相关分子模式的有效释放、树突状细胞成熟、细胞毒性T淋巴细胞活化、细胞因子分泌、M2型巨噬细胞复极和远端肿瘤抑制,证实了良好的原位肿瘤ICD效应和强大的系统性抗肿瘤免疫。本工作首次表明离散纳米组装策略能成功地增强光敏剂全身静脉给药后肿瘤组织内的特异性ICD效应,改善PDT/PTT抑制肿瘤复发转移的作用。
【论文信息】Zhao H*, …, Tao W*, Zhao Y, Yang X*. Tailoring Aggregation Extent of Photosensitizer to Boost Phototherapy Potency for Eliciting Systemic Antitumor Immunity. Advanced Materials 2022, 34(8):e2106390.
https://onlinelibrary.wiley.com/doi/10.1002/adma.202106390
20. Angewandte Chemie International Edition (IF=16.823)封面论文: 靶向DNA损伤应答的线粒体激活前药策略用于自我防御肿瘤治疗

化学治疗是目前临床治疗癌症最有效的手段之一。铂衍生物、拓扑异构酶抑制剂、DNA烷化剂和氟嘧啶类似物等化疗药物均是通过造成DNA损伤来诱导肿瘤细胞凋亡,进而发挥治疗作用。然而,癌细胞对常规化学疗法存在多重耐药机制,如抑制细胞凋亡、DNA损伤修复和细胞周期停滞等。5-氟脱氧尿苷(FUDR)是一种氟嘧啶类抗代谢药,于1970年被美国FDA批准用于治疗各种类型的实体瘤。其在体内的代谢物5-氟尿嘧啶(5-FU)为活性形式,可以干扰RNA和DNA合成。PP2A是一种丝氨酸/苏氨酸蛋白磷酸酶,位于线粒体和细胞核等细胞器中,并调节许多细胞生理过程,如细胞周期进程、基因转录、DNA复制和细胞分化。当细胞DNA损伤特别是化疗或放疗诱导的DNA损伤时,PP2A会参与DNA损伤修复,进而阻碍细胞凋亡。因此,PP2A是逆转肿瘤化疗耐受的潜在靶点。
基于此,哈佛大学医学院陶伟教授团队联合韩国高丽大学Jong Seung Kim团队、浙江大学孔娜教授团队发表论文,报道了一种新型靶向线粒体的多功能前药M1,成功实现了药物的精准递送和可控释放,前药M1释放出的PP2A抑制剂(DMC)与化疗药物FUDR以协同作用机制发挥抗肿瘤作用。相比于传统的化疗药物,前药M1策略在肿瘤治疗方面具有更广阔的应用前景。这项工作为解决传统化疗药物出现的耐药性问题提供了新思路,对靶向线粒体药物的设计具有重要参考的价值。
【论文信息】JangiliP, …, Tao W*, Kim JS*. DNA-Damage-Response-Targeting Mitochondria-Activated Multifunctional Prodrug Strategy for Self-defensive Tumor Therapy. Angewandte Chemie International Edition 2022, 61(16):e202117075.
https://onlinelibrary.wiley.com/doi/10.1002/anie.202117075
21. Advanced Drug Delivery Reviews (IF=17.873): 基于二维材料的纳米药物:从发现到应用

二维材料因其独特的理化特性在生物医学领域受到越来越多的关注。目前,基于二维材料的纳米药物已广泛应用于癌症、细菌感染、组织工程、生物防护、神经退行性疾病和心血管疾病等多种疾病。这些二维纳米药物根据其不同的特性,以不同的方式发挥治疗作用,显示出巨大的临床应用前景。
近期,哈佛大学医学院陶伟教授团队联合浙江大学孔娜教授团队,共同接受药剂学综述期刊Advanced Drug Delivery Reviews邀请,发表特邀论文重点讨论了基于二维材料的纳米医学的各种生物医学应用。介绍了几种典型的不同构型的二维纳米材料的结构、特点及其相应的生物医学应用,讨论了二维纳米药物在治疗和成像方面的潜力以及它们的生物功能化,对二维纳米药物在各种疾病中的治疗潜力进行了全面总结,并对2D纳米药物临床转化面临的挑战和发展前景进行了展望。
【论文信息】Ouyang J, …, Tao W*, Kong N*. 2D materials-based nanomedicine: From discovery to applications. Advanced Drug Delivery Reviews 2022, 185:114268.
https://www.sciencedirect.com/science/article/abs/pii/S0169409X22001582?via%3Dihub
22. Nano Today (IF 18.962): 用于增强免疫治疗的治疗性水凝胶:MnO2纳米片和血管破坏强效组合策略

血管破坏的肿瘤饥饿疗法的疗效受到潜在的缺氧诱导的免疫抑制的负面影响,选择具有类Fenton催化活性和免疫原性细胞死亡诱导活性的MnO2纳米片作为补充成分,可以克服上述血管破裂治疗的瓶颈。基于此,哈佛大学医学院陶伟教授团队联合暨南大学罗良平/肖泽宇教授团队、北京协和药物研究所胡宽研究员团队合作,采用肿瘤微环境响应性水凝胶,负载强效血管破坏剂和高分散性MnO2纳米片。血管破坏剂的强效血管破坏作用阻断肿瘤营养供应,并通过水凝胶长效药物释放以及MnO2纳米片抵抗血管破坏剂的免疫负性,逆转肿瘤免疫抑制微环境;同时采用多模态磁共振成像和小动物荧光成像进行疗效精准评估,为临床工作提供新的思路和可行性。我们开发了一种治疗性水凝胶(CM@Gel),它共封装了MnO2纳米片和血管破坏剂CA4P,以加剧肿瘤饥饿和增强免疫治疗。此外,水凝胶通过局部给药的形式有助于持久的药物释放,同时避免了全身给药时潜在的血管破坏不良事件。在乳腺癌动物模型中,制备的CM@Gel不仅选择性阻断肿瘤营养来源后缓解缺氧,还将免疫抑制的肿瘤环境转化为免疫活性表型。CM@Gel还可以在肿瘤饥饿的情况下显著增强免疫检查点治疗(ICB)的疗效,进一步验证了其作为抗肿瘤免疫增强剂的潜力。这项研究利用MnO2纳米片和血管破坏的强大结合,提供了一种独特的肿瘤饥饿治疗和免疫治疗的协同策略。
【论文信息】Wang D, …, Tao W*. Therapeutic hydrogel for enhanced immunotherapy: A powerful combination of MnO2 nanosheets and vascular disruption. Nano Today 2022, 47:101673.
https://www.sciencedirect.com/science/article/abs/pii/S1748013222003012?via%3Dihub
23. Nano Today (IF 18.962): 用于检测、恢复、分析和消除癌症中的液体活检成分的纳米技术

液体活检可以快速、无创地检测肿瘤相关成分。可以分析各种液体活检成分,包括循环肿瘤细胞、肿瘤来源的细胞外囊泡、循环肿瘤核酸和肿瘤相关血小板。这些成分在跟踪肿瘤的进化动力学和检测治疗抵抗和肿瘤复发的早期出现方面具有巨大的潜力。近几十年来,纳米技术的显著进步促进了基于血液的液体活检的发展,使其具有更高的敏感性和特异性。
近期,哈佛大学医学院陶伟教授团队和成都中医药大学石三军教授团队联合发表综述,讨论了可用于检测、分离和回收肿瘤相关成分的关键纳米技术,简要概述了这些成分的下游分析,然后重点介绍了可用于治疗循环肿瘤细胞以预防转移的不同类型纳米材料。这些非侵入性纳米技术介导的诊断方法可以帮助精确的癌症评估,并指导当前治疗策略的改进。
【论文信息】Zhao M, …, Tao W*. State-of-the-art nanotechnologies for the detection, recovery, analysis and elimination of liquid biopsy components in cancer. Nano Today 2022, 42:101361.
https://www.sciencedirect.com/science/article/abs/pii/S1748013221002863?via%3Dihub
































