防疫物资出口指南:免洗洗手液、消毒液及新冠检测试剂通关与准入全解析
涵盖主要国家准入要求、HS Code归类及出口合规要点
随着全球疫情防控常态化,免洗洗手液、酒精消毒液及新冠病毒检测试剂的出口需求持续增长。为助力外贸企业高效合规出海,本文整合最新政策与国际准入要求,提供权威出口指南,并附世界海关组织(WCO)防疫物资归类及HS Code查询信息。
一、免洗洗手液与酒精消毒液出口指南
相关产品属危险化学品或消毒类物资,出口需关注监管条件、申报资料及目的国准入标准。企业应确保产品符合输入国质量与标签规范,提前准备技术文件、检测报告及合规认证。












二、新冠病毒检测试剂出口指南
出口通关要求
商品归类:新冠病毒检测试剂归入海关编码38220090。
出口退税:退税率为13%。
检验检疫:
1. 新冠病毒检测试剂属出入境特殊物品,出口前须申请《入/出境特殊物品卫生检疫审批单》。疫情防控用途的试剂可凭省级药监部门特别批准文件免办审批。
2. 属出口法检货物,发货人需通过单一窗口申报,提交审批单,经检验合格后取得电子底账。
3. 报关时填写电子底账号,申报要求与口罩、防护服一致。
出口前准备
新冠病毒检测试剂属于体外诊断产品(IVD),主要分为核酸检测试剂和抗体检测试剂,各国通常按医疗器械管理。


主要国家准入条件
美国:由FDA监管,属Ⅱ类医疗器械,需提交510(k)上市前通知。企业须完成FDA企业注册(Form 2891)和产品登记(Form 2892),并在上市前至少90天提交申请。紧急使用授权(EUA)下,企业可申请EUA审查,获批受理后即可出口。
欧盟:依据IVDD指令,新冠病毒检测试剂属附录Ⅰ-A类高风险产品,需取得CE认证。企业须建立符合ISO 9000和EN 46000的质量体系,通过公告机构审核,并在欧盟指定代表处注册。
日本:归为医药品,由厚生劳动省监管。需提供“医药品生产销售许可证”及“生产销售批准书”复印件。产品按检测项目分为第1类(新产品)和第2类(已有项目),其中传染性疾病检测类属重点管理范围。
韩国:由MFDS管理,试剂统一归为体外诊断产品(IVD)。Ⅱ~Ⅳ类医疗器械需通过KGMP认证,提交技术文件并接受现场审核。审核基于ISO 13485标准,通常需30天资料评审及3~5天现场检查。
澳大利亚:通过TGA注册管理,产品分为注册类(高风险)和备案类(低风险)。HIV、丙肝等高风险试剂需上市前审批,完成审查约需3个月;其他产品备案约1个月。鼓励使用DEAL电子系统提交申请。
提示:所有CE等认证须由进口国认可机构颁发,第三方认证无效。
主要国家检测试剂生产技术标准
国别 |
标准号 |
中文名称 |
标准状态 |
发布时间 |
中国 |
YY/T 1579—2018 |
《体外诊断医疗器械体外诊断试剂稳定性评价》 |
现行 |
2008年第27号 |
YY/T 1441—2016 |
《体外诊断医疗器械性能评估通用要求》 |
现行 |
2016年第25号 |
|
YY/T 1443—2016 |
《甲型流感病毒抗原检测试剂盒(免疫层析法)》 |
现行 |
2016年第25号 |
|
YY/T 1462—2016 |
《甲型H1N1流感病毒RNA检测试剂盒(荧光PCR法)》 |
现行 |
2016年第25号 |
|
YY/T 1596—2017 |
《甲型流感病毒核酸检测试剂盒(荧光PCR法)》 |
现行 |
2017年第151号 |
|
YY/T 1513—2017 |
《C反应蛋白测定试剂盒》 |
现行 |
2017年第38号 |
|
YY/T 1518—2017 |
《C-肽(C-P)定量标记免疫分析试剂盒》 |
现行 |
2017年第38号 |
|
GB/T 26124-2011 |
《临床化学体外诊断试剂(盒)》 |
现行 |
2011年5月12日 |
|
GB/T 29791-2013 |
《体外诊断医疗器械制造商提供的信息(标示)》 |
现行 |
2013年10月10日 |
|
国外 |
ISO 23640-2015 |
《体外诊断医疗器械--体外诊断试剂的稳定性评定》 |
现行 |
2015年6月1日 |
EN 13532:2002 |
自检用体外诊断医疗设备的一般要求 |
现行 |
2002年12月17日 |
|
EN 13612:2002 |
体外诊断医疗设备的性能评估 |
现行 |
2002年12月17日 |
|
EN 14254:2004 |
体外诊断医疗装置.收集来自于人体的试样(血液除外)用一次性容器 |
现行 |
2005年4月28日 |
|
EN ISO 15193:2009 |
体外诊断医疗设备.生物源样品中数量的测量.参考测量程序的内容和表示要求 |
现行 |
2010年7月7日 |
|
EN ISO 15194:2009 |
医用体外诊断装置.生物原始试样中数量值的测量.合格参考材料的要求和支持文件的内容 |
现行 |
2010年7月7日 |
|
EN ISO 17511:2003 |
体外诊断医疗设备.生物试样中的数量测量.校准器和控制材料赋予值的测量可追踪性 |
现行 |
2005年4月28日 |
|
EN ISO 18113-1:2011 |
体外诊断医疗器械.制造商提供的信息(标签).术语、定义和一般要求 |
现行 |
2012年4月27日 |
|
EN ISO 18113-2:2011 |
体外诊断医疗器械.制造商提供的信息(标签).第2部分:体外诊断试剂供专业使用 |
现行 |
2012年4月27日 |
|
EN ISO 18113-3:2011 |
体外诊断医疗器械.制造商提供的信息(标签).第3部分:专业用体外诊断仪器 |
现行 |
2012年4月27日 |
|
EN ISO 18113-4:2011 |
体外诊断医疗器械.制造商提供的信息(标签).第4部分:体外诊断试剂进行自我测试 |
现行 |
2012年4月27日 |
|
EN ISO 18113-5:2011 |
体外诊断医疗器械.制造商提供的信息(标签).第5部分:体外诊断仪器自检 |
现行 |
2012年4月27日 |
|
EN ISO 18153:2003 |
体外诊断医疗设备.生物试样中的数量测量.校准器和控制材料规定的酶催化剂浓度值的测量可追踪性 |
现行 |
2003年11月21日 |
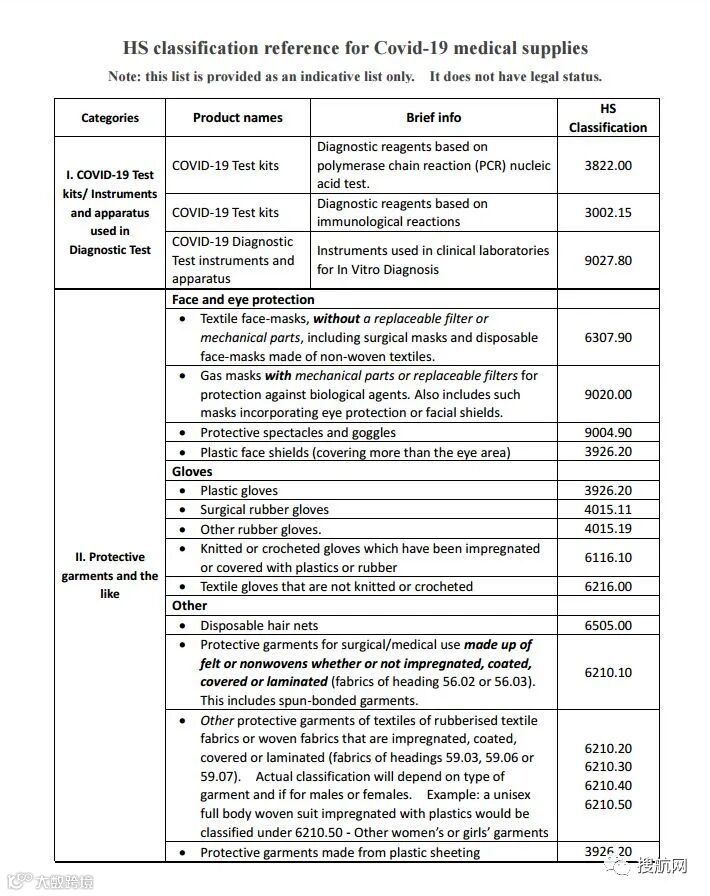
三、WCO最新防疫物资归类指南及HS Code查询
世界海关组织(WCO)已发布防疫物资归类指南,便于全球通关协作。出口企业可据此明确口罩、洗手液、消毒液、检测试剂等物资的HS编码,提升申报效率。


注:本文所列准入条件、技术标准等信息来源于国内外政府机构及公开资料,仅供参考。具体执行以相关主管机构最新规定为准。


