
第一作者:王君妍、张好雨、年瑶
通讯作者:于涛
通讯单位:天津大学
论文DOI:10.1002/adfm.202406549
C=O键断裂、*COOH形成能垒的降低与有效抑制光生载流子复合,都是光催化CO2还原反应和质子-电子参与表面催化反应过程的关键。通过S空位和Al掺杂破坏Cu/TiO2的对称结构(最佳样品表示为Al-CuS/TiO2),显著扩大了电子的局域范围,促进了Cu 3d轨道的顺式配位分裂。实验结果表明,Al-CuS/TiO2的CO选择性约为90.68%,产率约为335.68 μmol·g−1·h−1。Cu电子态在特定d/s/p轨道上的重新分布增加了对CO2的吸附,降低了*COOH的反应能垒,同时有效地断裂了C=O键。掺杂的Al作为H2O分子的吸附位点,有效地避免了光催化CO2还原在Cu位点上的竞争。本研究通过破坏局部对称性来调节晶体结构,为降低*COOH形成的能量势垒和加速光载流子迁移提供了新的途径,这对进一步提高光催化CO2还原反应的活性和选择性具有重要意义。
太阳能驱动的光催化二氧化碳还原因具有原料丰富、环境友好、成本低等优点而受到广泛的关注。然而,光催化CO2还原过程的转化率和产物选择性受到光生载流子迁移效率低和反应中间体能量势垒高的限制,其应用水平较低。硫化铜是一种重要的p型半导体,由于Cu-S键合后形成五元环结构,性能稳定,对近红外光吸收强,因此常被用作光电材料。TiO2作为一种n型半导体,因其合适的能带势和较高的化学稳定性而受到广泛关注,但其对可见光的响应较低,制约了其在半导体光催化材料中的实际应用。半导体异质结可以结合两者的优点,促进电荷的快速分离,从而成为高效太阳能转换的重要策略。最近的研究表明,对称的稳定结构实际上限制了金属位点的暴露,又影响了反应位点的活性。为了更好地利用活性位点的活性,解决这一限制,需要通过缺陷工程、元素掺杂、异质结构构建等方法对活性位点的电子结构进行有效调控。然而,相关研究都是在有机计量学框架下进行的,如何将上述理论推广到无机催化剂和一般掺杂领域是值得探讨的。
1. 通过负载TiO2、引入S空位和Al掺杂来破坏CuS的对称结构,从而调节活性位点的电子结构。
2. 在热力学上Al-CuS/TiO2大大降低了*COOH生成的能垒,提高了光催化CO2还原速率;在动力学上,异质结界面之间的相互作用加速了光电子-空穴对的分离,有利于CO2的还原。
3. 兼具热力学和动力学的优势,CO的选择性达90.68%,产率达335.68 μmol·g−1·h−1,优于目前报道的大部分CuS基光催化剂。
为了探究光催化CO2还原反应过程中,光催化剂在破坏C=O键和降低*COOH形成能垒的关键作用,将TiO2与含S空位的CuS复合,以促进电荷转移和分离,并掺杂Al以促进更多H质子参与反应,将该光催化剂命名为Al-CuS/TiO2。首先采用高分辨率透射电镜对光催化剂的形貌和微观结构进行了表征。观察到Al-CuS/TiO2晶格条纹的分化(图1a),证明了两种不同相结构的存在,其中CuS粒子的晶格条纹距离约为0.30 nm(图1b),对应于六边形CuS的(102)晶面。在TiO2颗粒中,0.24 nm的面间距离指向(004)晶面。两相界面清晰,表明CuS纳米颗粒与TiO2形成复合材料。EDX光谱显示Cu、Ti、Al、O和S在空间上分布均匀(图1c),证明材料合成成功。
电子顺磁共振证实了S空位的存在,并且由于Al-CuS/TiO2掺杂的Al原子要共用硫原子,使得Al-CuS/TiO2表面出现了更多的S空位(图1d)。适当浓度的S空位可以通过增加CO2的吸附和活化以及构建特定的反应构型来促进光生载流子转移,如打破局部对称性,从而加速光催化CO2还原反应进行。测试X射线光电子能谱,以验证光催化剂价态的变化。在Al-CuS/TiO2表面检测到73.6和75.9 eV的新峰对,归属于Al 2p谱(图1e),分别对应Al 2p3/2和Al 2p1/2的结合能,在Al的XPS中未出现Al-O峰,证实了Al掺杂在CuS而不是TiO2。Cu 2p光谱中位于931.1 eV和950.9 eV处的两个峰(图1f)显示了Cu(I)和Cu(II)离子的存在。Cu (I)的结合能从931.6 eV (CuS)转变为931.1 eV (Al-CuS/TiO2),证实了掺杂Al后铜原子价态的降低,这是电子迁移到Cu离子上所致。复合材料CuS/TiO2的结合能与CuS相比没有明显的位移,但Al-CuS/TiO2的结合能向较低结合能偏移,这表明Al的掺杂为反应中的进一步电子富集带来了动力学优势。
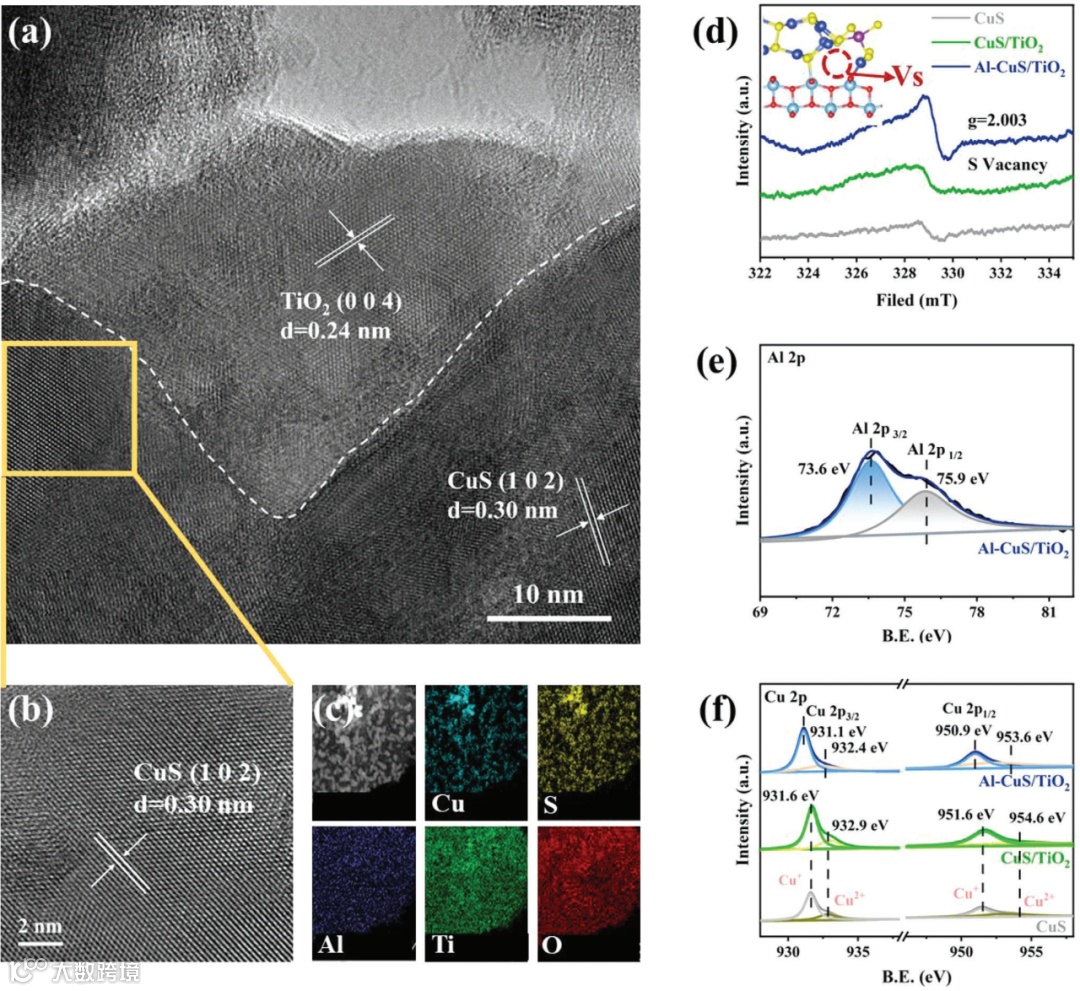
图1:结构表征。a) Al-CuS/TiO2的HRTEM图像和b) 相应的CuS的HRTEM放大图像;c) Al-CuS/TiO2的元素分布图;d) ESR光谱(插图:Al-CuS/TiO2上S空位的球棒模型);e) Al 2p和f) Cu 2p在不同样品上的高分辨率XPS光谱。
在300 W氙灯(λ≥420 nm)照射下,对不同样品的光催化CO2还原性能进行了研究。为了改善CuS中电子空穴复合严重的问题,通过负载一定量的TiO2来提高催化性能。以CuS与TiO2的最佳组成比(0.1CuS/TiO2)为基础,探讨Al掺杂对提高反应活性的影响。Al是H2O的吸附位点,促使更多的H+参与光催化CO2反应。随着Al掺杂量的增加,Al-0.1CuS/TiO2(Al-CuS/TiO2)的CO产率提高到355.68 μmol·g−1·h−1,选择性提高到90.68%(图2a, b)。为了确定光催化反应过程的驱动力,测量了Al-CuS/TiO2的表观量子效率。Al-CuS/TiO2分别在400 nm(1.35%)、420 nm(0.86%)、450 nm(0.66%)和470nm(0.47%)的单色光下测得量子产率(图2c),与紫外-可见吸收光谱吻合良好,为典型的光驱动反应。排除对照实验分别在黑暗和无光催化剂条件下进行(图2d),没有检测到CO和碳氢化合物产物,证明在Al-CuS/TiO2光催化剂中,CO2的还原反应是由光驱动的。在没有CO2的情况下,没有CH4和CO的出现,证明碳源完全来自输入的CO2。在没有H2O的情况下,没有检测到产物,证明氢源完全来自添加的H2O。进行同位素标记13CO2的实验也添加TEOA作为孔洞清除剂,并采用GC-MS对产物进行测定。CO、CO2的GC-MS峰序列及各峰的离子片段分析结果如图2e所示,说明Al-CuS/TiO2上生成的CO和碳氢化合物来源于CO2的还原,而不是其他来源。最佳的Al-CuS/TiO2样品在可见光照射下的5个循环中表现出了显著的性能稳定性,总测试时间为25 h。循环实验表明,即使在5个光反应循环中(图2f),每个CO2还原产物的产率仍保持在第一个循环的90%左右,表明Al-CuS/TiO2样品具有显著的结构稳定性。
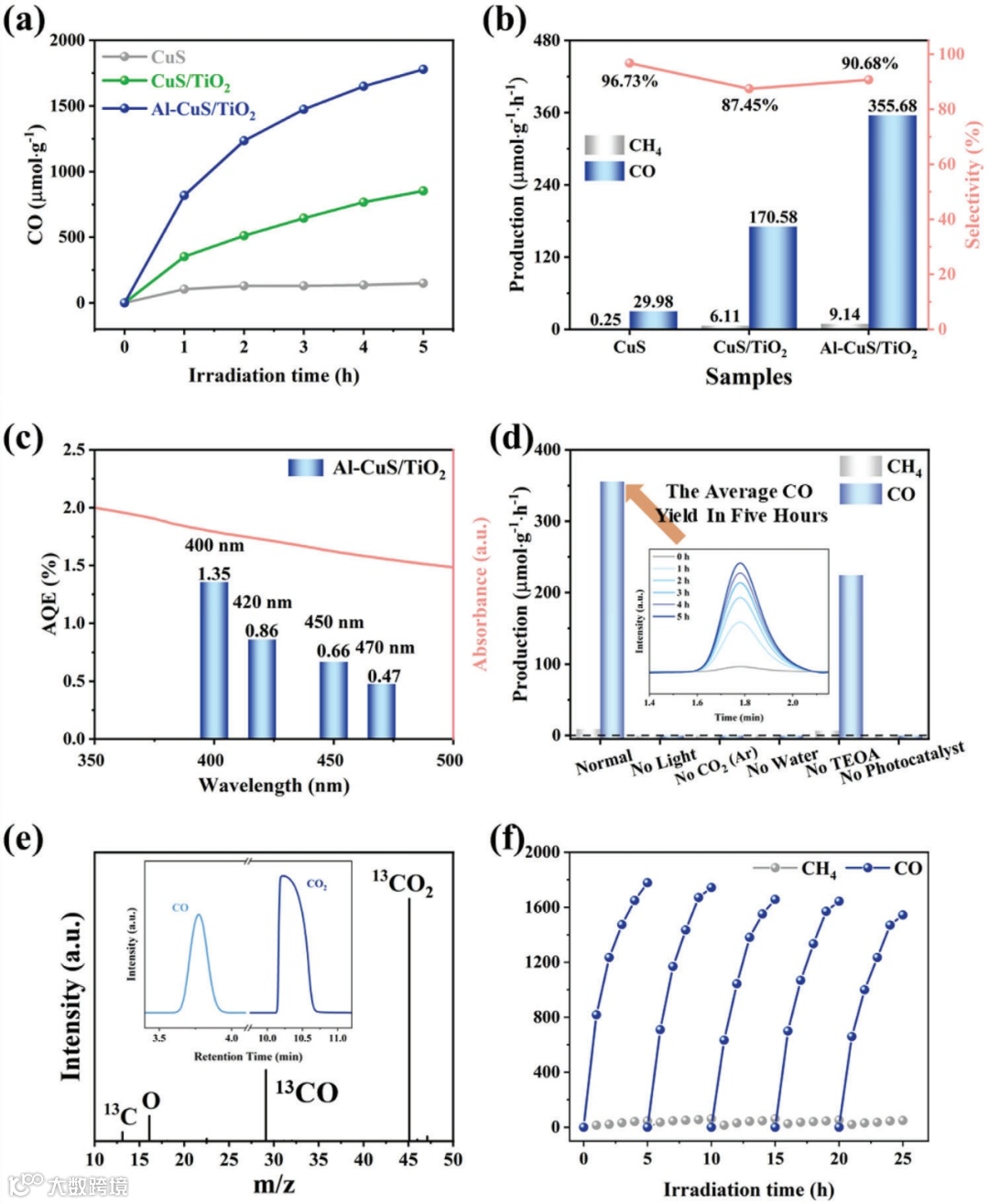
图2:光催化CO2还原性能。a) 随时间变化的CO2转化为CO的量;b) 不同样品对CO2的选择性和平均产率;c) AQE和紫外可见光谱;d) 不同条件下光催化CO2还原性能(插图:原始GC数据);e) 13CO2气氛下同位素实验的GC-MS结果(插图:保留时间);f) Al-CuS/TiO2光催化CO2还原循环稳定性。
电子传递性能对提高光催化性能起着重要的作用。在扫描探针显微镜系统中,暗光和可见光照射条件下,采用开尔文探针力显微镜探究了界面处的电荷转移机理。在Al-CuS/TiO2的KPFM图像中(图3a),TiO2(位置A)分布在CuS(位置B)的边缘,光照射后,A位置的电位升高~80.8 mV,B位置的电位降低~112.5 mV,说明电子从TiO2转移到CuS,为CO2生成CO提供了更多的电子。CuS/TiO2的表面电位降低了82.7 mV(图3b),小于Al-CuS/TiO2,说明掺杂Al和负载的TiO2可以提供更多的光生电子,可以促进CO2在光催化剂表面的吸附和活化。
计算出的电子定位函数图(图3c, e)显示,S空位扩大了周围原子的电子定位范围,使价壳层电子更加活跃。由于反应物中C的部分正电荷,电子定位范围的扩大有利于反应物的吸附。同时,通过掺杂Al和引入S空位打破CuS的结构对称性,电子可以在金属Cu位点的特定d/s/p轨道上重新分布,调整杂化相互作用的能量尺度,从而最大限度地调节Cu的杂化相互作用。这种局部对称调节可以促进CO2分子的吸附和活化,优化光催化CO2还原反应的反应途径,从而实现高活性和选择性的CO2还原。此外,复合结构和Al掺杂后CuS中Cu1、S1和S2的电荷变化由Bader电荷测定(图3d、f)。发现异质结的形成使电子从TiO2向CuS迁移,表明异质结界面与Al掺杂的相互作用使S原子的电荷增加,表明Al掺杂促进了原子间电荷转移。

图3:光物理和电化学性质。a) Al-CuS/TiO2和b) CuS/TiO2在暗光和可见光照射下的表面光电压,其中,Δ是用可见光照射下的电势减去样品在暗光条件下的电势(插图:暗光和可见光照射下的表面光电压分布);c, d) Al-CuS/TiO2和e, f) CuS/TiO2的ELF和Bader电荷。
采用理论计算和相应的检测技术分析CO2光催化还原反应的反应途径和能垒。通过原位傅立叶变换红外光谱测量,实时检测了CuS、CuS/TiO2和Al-CuS/TiO2表面光催化CO2还原(图4a、b)。光谱中位于1500-1797 cm−1的峰属于*COOH中O-H键的伸缩振动,位于2278 cm−1的峰属于化学吸附CO,即*CO。与CuS和CuS/TiO2相比,Al-CuS/TiO2的峰强度最高,这表明Al-CuS/TiO2捕获了更多的光生电子,更容易破坏C=O键,从而有效地提高了光催化CO2还原为CO的效率。
为了进一步探索Al-CuS/TiO2光催化的高选择性机理,通过DFT模拟系统地计算了反应物和中间体的吸附自由能。d带中心是光催化CO2还原活性的控制因子。由于电子结构的调制,Cu 3d轨道的d带中心从CuS的-2.07 eV增加到含S空位Al-CuS/TiO2的-2.03 eV,从而提高了吸附能,加强了电子转移(图4c)。由于S空位的贡献,Al-CuS/TiO2的d带中心从无S空位的-2.13 eV正向移动到有S空位的-2.03 eV,使Al-CuS/TiO2的Cu 3d轨道电子的能级更接近费米能级,从而增强了电子的活性。
在Al-CuS/TiO2的DFT模型上选择7个反应位点进行吸附计算(图4d)。CO2和*COOH分子吸附在S空位和Al附近的Cu位点上(图4e, f)。Al作为H2O的吸附位点,减少了Cu位点与CO2还原的竞争(图4g)。CO2和*COOH的最佳吸附位点都在靠近S空位和掺杂Al的Cu位点,这表明Al-CuS/TiO2打破了CuS原有的对称结构,有效调节了Cu活性位点的电子结构。当CO2的sp杂化轨道和*COOH的sp2杂化轨道靠近时,不对称的Cu位点将会在特定的d/s/p轨道上重新分配电子,调整杂化相互作用的能量,从而提高光催化CO2还原的速率和选择性。随后计算了Al-CuS/TiO2表面光催化CO2到CO过程的自由能变化(图4h)。CO生成的限速步骤是CO2加氢生成*COOH中间体。随后,*COOH进一步将质子/电子对偶联形成CO分子。研究了异质结形成、Al掺杂和S空位对能垒的影响。发现异质结的形成、Al掺杂和S空位都能促进能垒的下降。根据上述结果和结论,S空位不仅可以加速光生电子-空穴对的分离,将更多的光生电子转移到Cu的Cu位上,并且在Cu位上积累的光生电子驱动CO2还原半反应,还可以降低*COOH的能量势垒,加快响应速度。同时,局部不对称调控可以促进CO2分子的吸附和活化,优化CO2还原反应的反应途径。因此,Al-CuS/TiO2在可见光照射下表现出优异的光催化CO2还原性能。

图4:反应路径。a) Al-CuS/TiO2, b) CuS上CO2, H2O和TEOA蒸汽混合物共吸附的原位FTIR光谱;c) 不同样品的d带中心;d) 理论计算模型,e) CO2, f) *COOH, g) H2O在不同反应位点上的自由能(插图:最优位点的吸附模型);h) CO2光催化还原成CO的自由能。
为了解释光催化的机理,通过巴德电荷计算进行了系统的研究。Al掺杂和S空位使CO2分子积累更多的负电荷,有利于反应*CO2+e−+H+→*COOH和*COOH+e− H+→CO*+H2O的进行,通过比较不同Cu位点的吸附能,CO2和*COOH分子吸附在S空位和Al附近的Cu位点上(图5a, b),再次证明S空位和Al的引入可以调节CuS的电子结构,更有利于CO2和*COOH的吸附和活化,进一步促进了PCR的进行。
根据上述结果和结论,提出了Al-CuS/TiO2的高效CO2光还原的电荷转移机制(图5c及插图)。由于S空位和Al原子的引入,CuS的对称结构被破坏,周围的Cu暴露出来,有利于CO2在S空位和Al原子附近的Cu位点吸附。同时,在Al位点吸附附近的H2O。在可见光照射下,吸附的水开始分解并产生大量的H+,H+在CuS表面快速迁移,增加了PCR反应物的浓度。同时,Cu位点作为PCR开关,有效打开C=O键。使生成*COOH不再是质子-电子耦合的限速步骤。而*CO是*CO2到*COOH后自然生成的,然后以CO的形式释放。由于异质结优异的导电性和在TiO2与CuS之间形成内置电场,使得光生电子从TiO2向CuS快速迁移,保证了光生电子与空穴的复合速率降低,更多的光生电子被Cu位捕获,将CO2还原为CO。异质结的构建不仅可以加速光生电子-空穴对的分离,将更多的光生电子转移到Cu位点,并且Cu位点上积累的光生电子驱动CO2还原半反应,还可以降低*COOH的能量势垒,加快响应速度。因此,Al-CuS/TiO2在可见光照射下表现出优异的光催化CO2还原性能。

图5:理论研究。a) CO2和b) *COOH吸附在CuS、CuS/TiO2、Al-CuS/TiO2 (无S空位)和Al-CuS/TiO2 (有S空位)的Bader电荷;c) Al-CuS/TiO2的光催化机理(插图:CO2还原反应途径)。
综上所述,通过Al掺杂和S空位成功调整了CuS的对称结构和电子局域化范围。由于CuS对称结构的破坏,暴露出更多的金属Cu位,活性位点的电子结构受到调节,从而扩大了电子的定位范围。同时,Al和S空位周围的Cu活性位点促进了CO2和*COOH的吸附。TiO2加速了光生电子向CuS的迁移,并在活性位点积累,有效地打开了C=O键,降低了*COOH中间体的能垒,从而提高了光催化活性。掺杂Al原子增加了对H2O的吸附,提供了大量的H+,增加了反应物浓度。本文提出了引入S空位和Al掺杂破坏局部对称性,进而调控电子结构,促进CO2吸附和活化的方法。同时,该体系克服了光生载流子的快速重组速率,有效降低了*COOH形成的能垒,提高了动力学性能。从而为实现高活性、高选择性的光催化CO2还原提供了一条新的途径。
欢迎关注我们,订阅更多最新消息 “邃瞳科学云”推出专业的自然科学直播服务啦!不仅直播团队专业,直播画面出色,而且传播渠道多,宣传效果佳。
“邃瞳科学云"平台正在收集、整理各类学术会议信息,欢迎学会、期刊、会议组织方择优在邃瞳平台上进行线上直播,希望藉此帮助广大科研人员跨越时空的限制,实现自由、畅通地交流互动。欢迎老师同学们提供会议信息(会有礼品赠送),学会、期刊、会议组织方商谈合作,均请联系潘经理:18612651915(微信同)。
投稿、荐稿、爆料:Editor@scisight.cn
“邃瞳科学云”推出专业的自然科学直播服务啦!不仅直播团队专业,直播画面出色,而且传播渠道多,宣传效果佳。
“邃瞳科学云"平台正在收集、整理各类学术会议信息,欢迎学会、期刊、会议组织方择优在邃瞳平台上进行线上直播,希望藉此帮助广大科研人员跨越时空的限制,实现自由、畅通地交流互动。欢迎老师同学们提供会议信息(会有礼品赠送),学会、期刊、会议组织方商谈合作,均请联系潘经理:18612651915(微信同)。
投稿、荐稿、爆料:Editor@scisight.cn




















