
近日,随着吉利德(Gilead)、百时美施贵宝(BMS)、强生、传奇生物等药企陆续披露2024年Q3季度财报,全球已上市CAR-T产品在2024年Q3季度及整个前三季度的销售额已经揭晓。本文将对这些数据进行简单的汇总梳理。
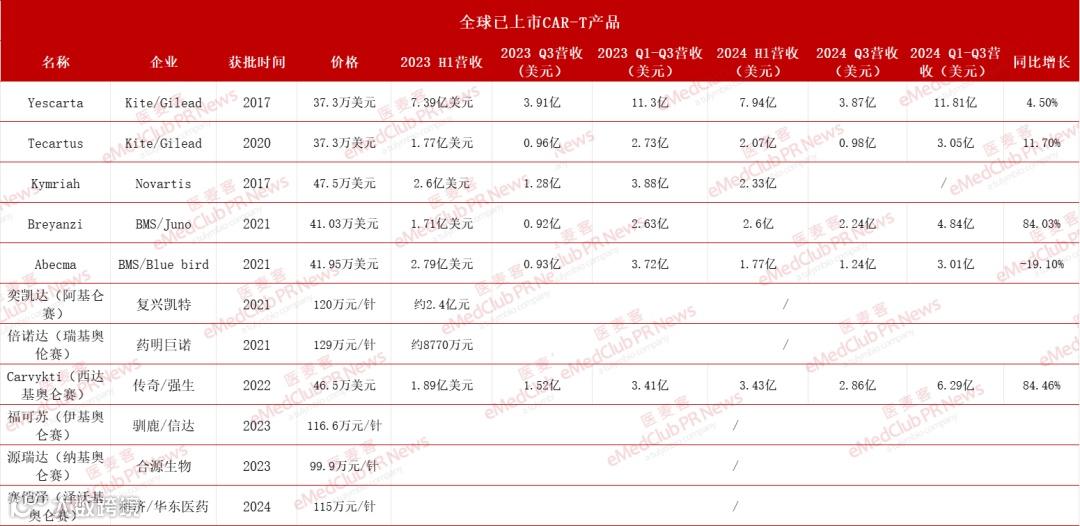
据统计,截至2024年Q3季度,全球已上市的CAR-T细胞疗法在前三季度的销售额达到29亿美元(约合人民币209.5亿),同比增长约21.9%(2023年同期销售额约为23.79亿美元),总体保持上升趋势。
总体来看,在CAR-T细胞疗法这一领域,国内外各大药企的竞争愈发激烈,新产品的上市和现有产品的适应症拓展等因素成为推动销售额增长的主要因素。在已披露销售额的几款CAR-T产品中,除了Abecma外,其他几款CAR-T产品前三季度销售额相较于2023年同期均有所增长。其中,Breyanzi和Carvykti展现出强劲的增长势头,销售额同比增幅均超84%。
Kite/Gilead
11月6日,吉利德公布了2024年Q3财报。财报显示,公司Q3营收75.15亿美元,其中肿瘤板块营收8.16亿美元,同比增长6%,但环比下降近3%。目前吉利德的抗肿瘤板块共有三款药物,分别是Tecartus和Yescarta两款CAR-T产品,以及一款ADC产品。
Yescarta是全球第二款获批上市的CD19 CAR-T,上市五年后,在2022年首次跨过10亿美元门槛。2023年销售额继续走高,同比增长24%达到15亿美元。但从今年的销售结果来看,Yescarta的增长开始减速,前三季度销售额为11.81亿美元,同比增长不到5%。
另一款CD19 CAR-T产品Tecartus在2024 Q3单季度销售额为9800万美元,前三季度销售额为3.05亿美元,同比增长为11.7%。
Novartis
诺华的Kymriah是全球首款获批上市的CAR-T细胞疗法,2024年上半年的销售额为2.33亿美元,Q3季度的销售额尚未公布。从上半年销售额来看,其同比销售额下降了约10%。出现下滑颓势可能是多方面因素导致,诺华曾表示,Kymriah作为上市最早、定价最贵的一款CAR-T疗法,新的竞争对手不断进入弥漫大B细胞淋巴瘤市场,对Kymriah的销售产生了直接影响。
尽管面临着激烈的市场竞争和疗效数据的挑战,诺华依然在积极寻求新的突破点,通过优化疗效和安全性、拓展适应症以及提升产能等措施,努力提升Kymriah的市场竞争力。
BMS 
10月31日,百时美施贵宝公布了2024 Q3业绩,前三季度总营收359.58亿美元,同比增长7%;研发投入79.68亿美元,同比增长17%。Breyanzi和Abecma是百时美施贵宝已上市的2款CAR-T疗法,在2024年前三季度总销售额约为7.85亿美元,同比增长约23.6%。
其中,Abecma今年前三季度的总销售额为3.01亿美元,与2023年同时间段销售额3.72亿美元相比有所下滑,考虑可能是面临着激烈的市场竞争等因素。然而,百时美施贵宝也在积极寻求新的增长点,通过拓宽适应症等措施,努力让Abecma重回增长轨道。反观其另一款CAR-T疗法Breyanzi则销售数据亮眼,Q3单季度收入2.24亿美元,同比增长143%,前三季度销售总额达4.84亿美元,同比增长84.03%,处于稳步增长。
此前,业内曾有观点指出,Breyanzi由于进入市场晚以及同靶点、同适应症竞争大的情况,其后续的销售额很难提高。但在2023年,Breyanzi给出了一手漂亮的销售业绩,全年销售额3.64亿美元,同比增长了100%。
从百时美施贵宝研发近况来看,Breyanzi销售额的稳步增长可能与其临床数据的支持、适应症的扩展、市场需求的增加等原因导致。2024年ASCO年会上,Breyanzi展示出其在广泛的B细胞恶性肿瘤中的显著临床意义效果。
值得一提的是,Breyanzi最近还获得了美国FDA的加速批准,用于治疗接受过两线或以上系统治疗的成人复发或难治性滤泡性淋巴瘤(FL)患者,以及至少接受过两线系统治疗(包括布鲁顿酪氨酸激酶(BTK)抑制剂)的复发或难治性套细胞淋巴瘤(MCL)患者。这一定程度上扩展了Breyanzi的使用范围,增加了其市场潜力。
传奇生物/强生
Carvykti是全球第2款BCMA CAR-T疗法,由传奇生物和强生合作开发,也是国内首个出海的CAR-T疗法。2022年2月,Carvykti获得美国FDA批准上市,用于治疗复发或难治性多发性骨髓瘤(R/R MM)患者。2024年8月,传奇生物西达基奥仑赛注射液(Carvykti)在中国获批上市。
2024年上半年,Carvykti实现了3.43亿美元的销售额,同比增长81.5%。10月,强生公布的第三季度财报显示,Q3季度Carvykti销售额为2.86亿美元,同比增长88.16%。
自获批以来,Carvykti凭借其显著的临床疗效和广阔的市场前景,销售额持续快速增长。特别的,今年4月,Carvykti在美获批二线治疗,成为首个且唯一获批用于MM患者二线治疗的BCMA靶向疗法,包括CAR-T、双抗和ADC(抗体偶联药)。
而后,其销售额增长强劲,前三季度已经达到6.29亿美元,同比增长了84.46%。这一增长得益于其在市场竞争中的优势,包括更广泛的适应症获批、更好的临床数据、更完善的市场覆盖以及更广泛的保险覆盖等。传奇生物的一位高管曾透露,在美国提供相关疗法的治疗中心中,Carvykti占据了大约80%的后线治疗市场份额。同时,美国超过90%甚至95%的保险公司会覆盖Carvykti。
今年下半年,随着产能的进一步扩大和新适应症的获批,Carvykti的市场表现有望进一步提升。业内人士预测,Carvykti被认为有望在2024年突破10亿美元大关。
结语
随着技术的不断进步,全球CAR-T细胞疗法赛道产品在不断涌现,市场也在不断扩大,为患者提供更多治疗选择的同时,也形成了更加复杂多变的竞争格局。
CAR-T细胞疗法作为新兴的生物技术治疗手段之一,长期以来的市场天花板始终难以打破。其如何降低治疗成本,或者扩大患者覆盖范围两大核心问题始终未能取得很好的突破。可以预见,其中任何一大问题得到很好的解决,都将显著促进整个CAR-T疗法产业的发展。
目前,CAR-T细胞疗法仅对血液瘤有着显著的疗效,而实体瘤占癌症病例的90%以上,疾病负担高且有着极大的未被满足的临床需求。尽管CAR-T疗法仍面临诸多挑战和不确定性,但其毋庸置疑的是,其仍具有巨大的应用潜力和前景。
未来,相信全球企业通过不断的技术创新、拓展适应症及成本控制,可以让很多患者不再“要而不得、望药兴叹”,从而进一步扩展市场,释放市场需求。同时,随着对适应症领域的进一步研究,CAR-T疗法有望在更广泛的治疗领域,如实体瘤、自免疾病等其他领域带来新的突破。
加速细胞和基因治疗的开发
Polyplus®提供GMP级转染试剂
病毒载体的生产是细胞和基因治疗产品生产过程中一个重要的环节,稳健的瞬时转染是保证高产量和可靠的病毒载体大规模商业化生产的关键。Polyplus®提供GMP级转染试剂,可用于临床病毒载体的生产。
Polyplus®是一家面向基因和细胞治疗市场的GMP级转染试剂供应商,提供一系列基于PEI的高品质转染试剂。公司开发的用于基因治疗和细胞治疗领域的病毒载体生产试剂PEIpro®和FectoVIR®-AAV已经越来越广泛的应用到了众多的临床试验中并成为了行业的金标准。其中PEIpro®-GMP是市面上第一款完全GMP级转染试剂。
PEIpro® 系列产品
PEI的生产遵循非常严格的质量控制和法律法规,有三个质量等级:研发级的PEIpro®用于工艺开发,更好质量等级的PEIpro®-HQ用于临床前研究和早期临床试验,最高质量等级即完全GMP级别的PEIpro®-GMP可用于临床病毒载体的生产(包括慢病毒,腺病毒,腺相关病毒等),满足细胞治疗和基因治疗的质量和监管要求。

专为悬浮体系生产AAV开发的
FectoVIR®-AAV
FectoVIR®-AAV 是新一代转染试剂,专为在悬浮和贴壁 HEK-293 衍生细胞体系中大规模生产rAAV而开发。FectoVIR®-AAV转染试剂保证更高的 rAAV 滴度,提高大规模生产的可放大性,拥有药品GMP级产品降低生产工艺的风险。FectoVIR®-AAV GMP级产品在经过验证的无菌工艺下生产,符合 ICH Q7、GMP指南第二部分。
与PEIpro®和其他竞争对手相比,FectoVIR®-AAV 在悬浮细胞中能生产更高滴度的rAAV病毒载体。与其他竞争对手相比,FectoVIR®-AAV可重复性地大幅提高 AAV 产量,可高达10 倍。

大规模瞬时转染需要在给定的时间范围内将大量转染复合物添加到悬浮细胞中。FectoVIR®-AAV 经过优化,可将复合物体积降低至1%,转染复合物的稳定性提高到3小时,易于转染复合物的转移和工艺放大。

FectoVIR®-LV
慢病毒载体被认为是同种异体或自体细胞疗法(如CAR-T)的首选载体。细胞治疗生产商通常使用瞬时转染系统生产这些载体,在工艺开发阶段进行放大。FectoVIR®-LV是下一代转染试剂,不含动物源成分,专为在HEK-293系统中提高LV的产率而设计。使用FectoVIR®-LV可以增加每批次生产的剂量数,以治疗更多的患者,同时降低生产成本。
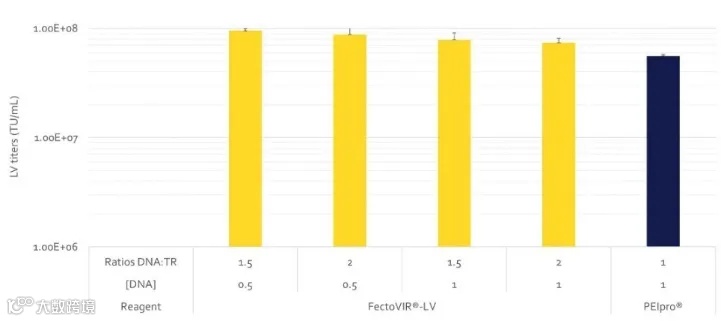
与其他市售用于慢病毒生产的转染试剂相比,FectoVIR®-LV可提高功能滴度达3倍。

FectoVIR®-LV在提高生产率的同时DNA用量可以减半。为了支持我们的客户,Polyplus提供了全面的DOE服务,以优化转染步骤的关键参数,达到更高的滴度。
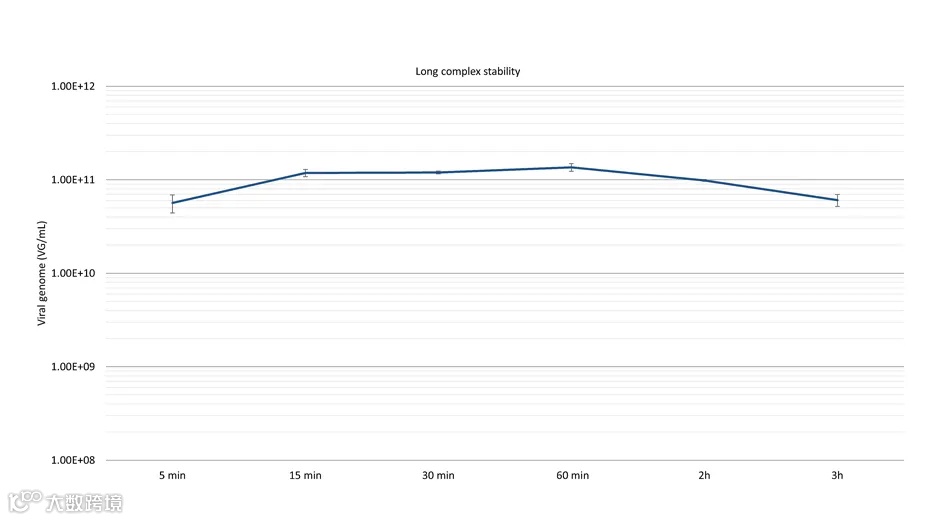
大规模瞬时转染的挑战包括在最佳时间范围内转移转染混合物。如果转染试剂不适合大规模生产,这一步骤可能成为一个限制。FectoVIR®-LV为大规模生产而设计,可减少复合物体积并提高复合物稳定性, 从而有足够的时间将混合物转移到大型生物反应器(>200 L)中。使用推荐的5%复合物体积和30分钟的复合物孵育时间,FectoVIR®-LV证明了其高效性,该条件可以进一步优化以符合您的工艺。Polyplus建议使用适合您系统的DOE研究。
Polyplus®
Sartorius旗下Polyplus,是一家为先进生物制品、细胞和基因治疗生产提供上游解决方案的领先供应商,涵盖从研发到商业化的各个阶段。经典的核酸递送产品组合是以工艺为中心的转染试剂、试剂盒和支持性服务,其中包括生物生产的行业标准,PEIpro®和FectoVIR®-AAV. 2022年,公司开始专注于上游生物工艺经济优化,整合了定制质粒载体设计,GMP转染试剂和质粒生产采用内部化供应链,旨在满足严格的科学和法规标准。总部位于欧洲,在美国与亚洲地区均有业务,Polyplus持续推进其全球业务发展。
扫描二维码添加Polyplus官方微信或者公众号搜索Polyplus 转染专家获取更多丰富的转染知识和产品信息!



