在药物研发中,一种手性分子的两种对映体可能呈现截然不同的生物活性——例如沙利度胺,其R型对映体可缓解妊娠呕吐,S型却会导致胎儿畸形。这种“镜像分子”的巨大差异,让手性分析成为化学、医药、材料等领域的核心技术。近日,发表于《Chem Soc Rev》的综述(DOI: 10.1039/d4cs01202j)系统梳理了手性分析的发展脉络,从基础概念到前沿技术,为我们揭开了分子“镜像密码”的解析之道。
一、认识手性:分子世界的“左右之分”
手性的本质,是分子的“镜像不可叠合性”——就像我们的左手和右手,看似相同却无法完全重合。这一概念最早由开尔文提出,而国际纯粹与应用化学联合会(IUPAC)进一步明确:手性分子不存在第二类对称元素(如镜像面、对称中心等),若分子能与镜像重合,则为非手性分子。
与手性密切相关的还有“立体异构性”。立体异构性指分子通过基团置换生成对映体(镜像异构)或非对映体(非镜像异构)的能力。1874年,范托夫提出sp³杂化碳原子连有4个不同取代基时会产生立体异构,这是人类首次认识到分子立体结构的重要性。
在实际研究中,科学家用“对映体过量(ee)”衡量手性样品的纯度,其计算公式为:ee(%)=[([R]-[S])/([R]+[S])]×100([R]、[S]分别为R型、S型对映体的摩尔浓度)。ee值越接近100%,说明样品中某一对映体的纯度越高,这一指标在药物研发中至关重要——多数手性药物只有单一对映体具有治疗活性,另一对映体可能无效甚至有毒。
手性分析的发展离不开两大历史里程碑:19世纪,工业化学家凯斯特纳在酒石酸纯化中意外发现光学惰性物质;随后,巴斯德通过手工分离,首次得到酒石酸的D型与L型对映体,奠定了立体化学的基础。而比奥发明的旋光仪,通过检测晶体对偏振光的旋转方向,开启了对映体过量评估的新纪元。
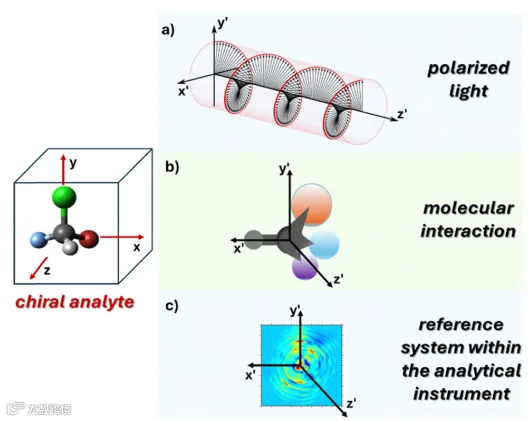
区分对映异构体需要利用特定参考系(x₀y₀z₀)确定原子的相对位置(xyz 坐标)。常见方法包括三类:(a)与偏振光发生相互作用或发射偏振光,(b)与另一种手性分子发生(非)共价相互作用,(c)在分析仪器内部建立参考体系。
二、手性区分的核心逻辑:三大途径破解“镜像难题”
要区分一对看似相同的对映体,核心是确定分子在特定参考体系(x'y'z')中的相对原子坐标(xyz),目前主要通过三大途径实现:
第一种途径是利用偏振光的相互作用。手性分子会对偏振光产生特殊响应,例如旋光仪通过检测线偏振光的旋转角度区分对映体,圆二色性(CD)光谱则通过测量分子对左右圆偏振光的吸收差异实现鉴别。这种方法无需引入其他物质,是最直接的手性分析思路。
第二种途径是借助已知手性分子的“桥梁作用”。将手性样品与已知构型的手性分子通过共价键或非共价作用结合,形成非对映体(非镜像异构的分子)。由于非对映体的物理化学性质(如溶解度、色谱保留时间)存在差异,可通过常规分析手段分离检测。例如色谱法中的手性固定相、核磁共振(NMR)中的手性衍生剂,均基于这一原理。
第三种途径是在仪器内部构建物理参考体系。部分先进仪器可通过特殊设计,在内部形成手性环境,让对映体产生不同响应。比如质谱中的离子迁移技术,通过向漂移管中通入手性气体(如(R)-2-丁醇),使对映体形成的离子因相互作用差异产生不同漂移时间,从而实现分离。
不过,手性区分也存在特殊挑战。例如外消旋体(R型与S型对映体等量混合)与纯对映体在固态性质(如熔点、溶解度)上存在差异,这源于同手性(R-R或S-S)与异手性(R-S)分子间相互作用的不同,但这种差异普适性低,难以作为常规分析方法。此外,“霍罗效应”会导致旋光与ee值呈非线性相关,干扰分析结果,这些都需要在实验设计中特别注意。
三、主流技术比拼:谁是手性分析的“主力军”
经过多年发展,手性分析已形成四大主流技术体系,各有优势与适用场景:
色谱法:ee测定的“金标准”
色谱法是目前手性分析中准确性最高的技术,主要包括气相色谱(GC)、高效液相色谱(HPLC)、超临界流体色谱(SFC)和毛细管电泳(CE)四种形式。其核心是“手性固定相(CSP)”——将手性分子(如环糊精、多糖、抗生素)固定在色谱柱内,当手性样品流经时,不同对映体与CSP的相互作用强度不同,导致洗脱时间(t_el)差异,通过峰面积即可计算ee值。
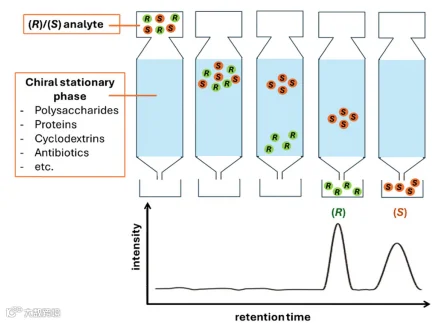
色谱法的优势在于“分离与分析一体化”,不仅能测定ee值,还能通过HPLC等制备级技术获取高纯度对映体。但它也存在明显局限:需针对不同样品优化固定相、流动相参数,分析时间较长(传统方法常需数十分钟)。不过,近年来研究者开发出多孔材料(如共价有机框架COFs、金属有机框架MOFs)作为新型CSP,大幅提升了分离效率,甚至实现了1分钟内分离兰索拉唑、氟比洛芬等药物的对映体,为高通量分析奠定基础。
手性光谱法:从“旋光”到“发光”的升级
手性光谱法利用分子对光的特殊响应实现分析,涵盖多种技术:旋光色散(ORD)通过检测线偏振光的旋转角度分析手性,无需分子含发色团,仪器成本低,但灵敏度较差;圆二色性(CD)光谱通过测量左右圆偏振光的吸收差异,信号分辨率高,可同时测定分子绝对构型与构象变化,广泛用于生物大分子(如蛋白质、核酸)分析,但需分子含发色团;振动圆二色性(VCD)则利用红外光探测分子振动模式,无需发色团,结合密度泛函理论(DFT)计算可解析复杂分子结构,不过信号弱、需大量样品;圆偏振发光(CPL)光谱关注分子发光的偏振特性,灵敏度高、非破坏性,适用于发光材料分析,但依赖分子的发光性能。
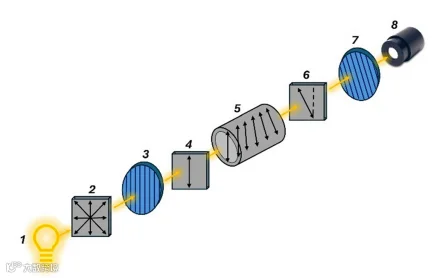
这类技术的共同挑战是“依赖校准曲线”——需获取纯对映体参考品,为每种样品单独构建曲线,分析效率低。为此,研究者开发出“立体动态探针”:这类分子含强发色团,且构象可快速互变,与手性样品作用后形成非对映体复合物,信号强度直接与ee值线性相关,大幅简化了校准流程。
NMR spectroscopy:“看不见的手性环境”
核磁共振(NMR)本身无法区分对映体,但通过引入手性试剂,可构建“手性环境”使对映体产生差异信号。常用试剂包括三类:手性衍生剂(CDA)与样品形成共价键,生成非对映体后通过化学位移(f,单位ppm)差异鉴别,如常用的Mosher酸可分析手性醇、胺;手性溶剂化剂(CSA)通过氢键、π-π堆积等非共价作用与样品结合,无需衍生化,操作简便;手性位移试剂(CSR)多为镧系金属配合物,能诱导样品产生显著化学位移变化,适用于难衍生化的分子。
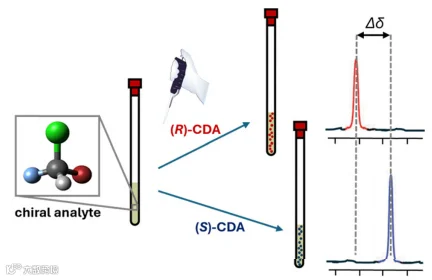
NMR的优势是可在溶液中直接分析,无需分离样品,还能提供分子结构信息。但它对样品浓度要求较高,部分试剂(如CSR)会导致信号展宽,影响定量准确性。
质谱:高灵敏度的“微量分析专家”
质谱(MS)凭借高灵敏度(可检测ppm甚至ppb级样品)、少样品前处理的优势,成为手性分析的后起之秀。其核心是让手性样品与手性选择剂形成非对映体离子,通过质荷比(m/z)、碎片离子强度或漂移时间(t_dr)差异实现区分。例如离子迁移质谱(IM-MS)向漂移管中通入手性气体,使对映体离子因碰撞截面(CCS)不同产生不同漂移时间,可分离氨基酸等小分子对映体。
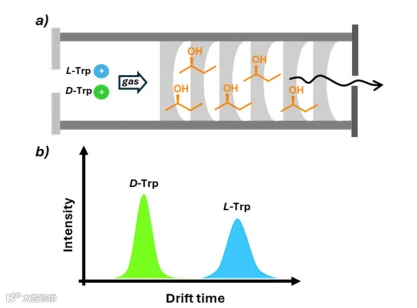
质谱的短板是“受电离条件影响大”——溶剂、浓度等因素可能干扰信号,需严格控制实验条件。但近年来,串联质谱(MS/MS)通过碰撞诱导解离(CID)增强信号重现性,光解离(PD)技术提升对映体区分度,使其在复杂样品分析中应用越来越广。
四、前沿技术突破:解锁手性分析的“新维度”
随着技术迭代,一批新兴方法正在打破传统局限,为手性分析带来新可能:
纳米光子学:信号增强的“超级放大器”
纳米材料的独特光学性质,让手性信号的检测灵敏度实现质的飞跃。例如金纳米颗粒、介电纳米结构可生成“超手性光”——其光学手性密度远超普通圆偏振光,与手性分子作用时能产生极强的信号响应。研究者利用金纳米平台构建传感器,将振动圆二色性(VCD)信号增强13个数量级,可同时测定复杂混合物中手性分子的浓度与ee值,为痕量分析提供了新方案。
晶体海绵法:无需结晶的“结构解析神器”
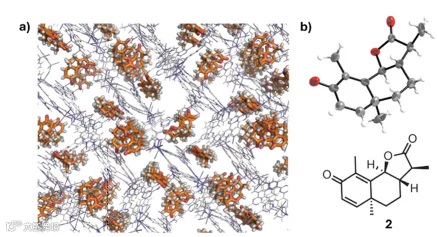
传统X射线晶体学需手性分子形成高质量晶体才能测定绝对构型,但多数天然产物、代谢物难以结晶。“晶体海绵法”的出现解决了这一难题:研究者将多孔金属有机框架(“晶体海绵”)预先结晶,再将难结晶的手性样品扩散到海绵孔道中,样品分子会在孔道内有序排列,通过单晶X射线衍射即可解析其结构。该方法仅需纳克至微克级样品,还能分析液体样品,已成功用于多种天然产物的绝对构型测定。
酶促方法:生物特异性的“精准筛选”
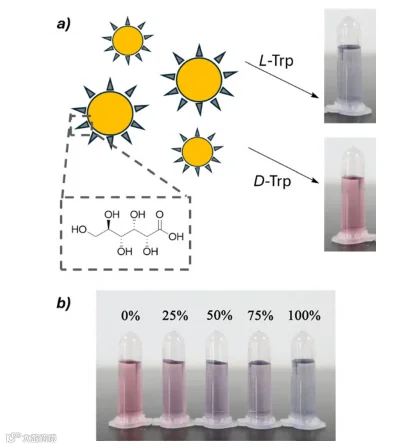
酶的立体特异性(仅与特定构型的手性分子反应)为手性分析提供了生物解决方案。例如脂肪酶可选择性水解一种对映体的酯类化合物,通过检测产物([P])或底物([SM])浓度变化,结合校准曲线即可计算ee值。这类方法操作简单、环境友好,且分析速度快——适配96孔板的高通量系统可在5分钟内完成多个样品分析,特别适用于药物合成中的实时监测。
分子旋转共振光谱:微波领域的“对映体鉴别师”
分子旋转共振(MRR)光谱利用微波辐射探测分子的纯旋转跃迁,具有极高的分辨率。通过“微波三波混合(M3WM)”技术,研究者可利用对映体偶极矩乘积(μₐμᵦμᵧ)的符号差异,实现精准的手性区分,ee测定精度达0.5%。更重要的是,它无需分离样品,可直接分析构象混合物(如香芹酮的不同构象),为复杂体系分析开辟了新路径。
五、未来展望:手性分析的“下一站”
尽管手性分析技术已取得显著进展,仍面临三大核心挑战:普适性不足(多数方法针对特定类型分子)、参考品依赖(部分技术需纯对映体校准)、复杂样品干扰(基质杂质影响信号)。针对这些问题,未来研究将聚焦三大方向:
一是开发“通用型”手性选择剂。目前的手性固定相、手性试剂多局限于特定官能团的分子,研究者正设计具有广谱识别能力的材料(如多功能化COFs、智能响应型聚合物),减少参数优化成本,提升方法普适性。
二是融合多技术优势。例如将机器学习与手性光谱结合,通过算法处理复杂数据,减少对纯参考品的依赖;将纳米光子学与质谱联用,同时实现信号增强与高灵敏度检测,满足痕量、复杂样品分析需求。
三是推动自动化与高通量。随着药物研发、材料合成向“高通量筛选”转型,手性分析需适配快速、自动化系统——例如流动注射-离子迁移质谱,可省去分离步骤,实现分钟级分析;微流控芯片结合手性传感,可同时处理数十个样品,大幅提升实验效率。
手性是自然界的基本属性,也是人类探索分子世界的重要窗口。从巴斯德的手工分离到纳米传感器的信号放大,手性分析技术的每一步突破,都在推动医药、材料、农业等领域的进步。未来,随着技术的不断融合与创新,我们必将更精准、更高效地解析分子“镜像密码”,为人类健康与科技发展注入新动力。


