
【研究背景】
电动汽车、规模储能等应用对锂电池能量密度、充电速度、温度适应性及寿命提出了更高要求,电解液优化已成为提升电池综合性能最有效的工程路径之一。然而,传统的电解液开发多依赖于“试错式”的配方筛选,面对日益复杂的功能需求,这种方法效率低下且缺乏理论指导。追根溯源,电解液的宏观性能(如离子电导率、界面稳定性)和电化学行为是根植于其微观的溶剂化结构,而该结构又是由电解液内部各组分的分子间相互作用竞争决定的。因此,厘清这些基本的相互作用,并建立“相互作用-溶剂化结构-电化学性能”的构效关系,是实现电解液理性设计的关键。
【工作简介】
近日,华南理工大学胡仁宗教授、朱敏教授团队在Materials Science and Engineering: R: Reports上发表了一篇重要综述,系统性地梳理了锂离子电池电解液中各种基本的分子间相互作用,并清晰地构建了其与溶剂化结构及最终电池性能之间的内在联系。该综述不仅总结了电解液中离子传输、界面化学等基础过程的机理,更从原子尺度深入分析了Li+-溶剂、Li+-阴离子、溶剂-溶剂、阴离子-溶剂四类相互作用的竞争与耦合关系,指明了通过调控这些相互作用来精准设计溶剂化结构并影响电解液行为的路径。这项工作为摆脱传统“试错”研发模式,实现自下而上的精准电解液设计提供了坚实的理论框架和前瞻性视角。本文第一作者为博士研究生陈金伟。
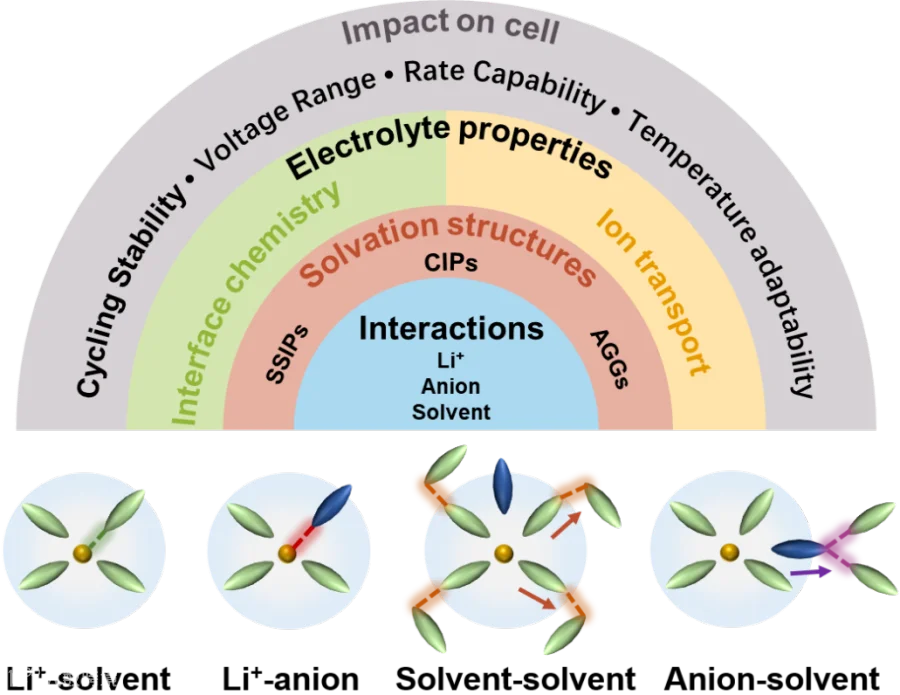
Figure 1 电解液组分间的相互作用及溶剂化结构-性能关系
【内容表述】
3.1 电解液的核心功能
电解质作为锂离子电池中离子传输的主要介质,架起了正极与负极之间的桥梁。在电极-电解质界面处,它通过实现电子传导与离子传导的相互转换来完成电荷平衡。这些过程涉及电解质的两个核心特性:传输特性与界面化学特性。传输过程包括从电极脱嵌的Li+在电解质中的溶剂化、其向对侧的液相扩散,以及进入界面前的脱溶剂化过程(图1)。综述详细分析了影响电解液中Li+传输速度的因素以及衡量这些因素的评价指标。
界面化学则涉及在两极形成具有离子导电性但电子绝缘性的固体电解质界面层,从而确保电解质的电化学稳定性及电极反应的高度可逆性(图2)。与界面形成有关的分子轨道理论和双电层理论被介绍,并阐明通常的界面结构和组分。进一步的,分析了界面膜的结构和组分特性对电池的不同方面性能的影响。
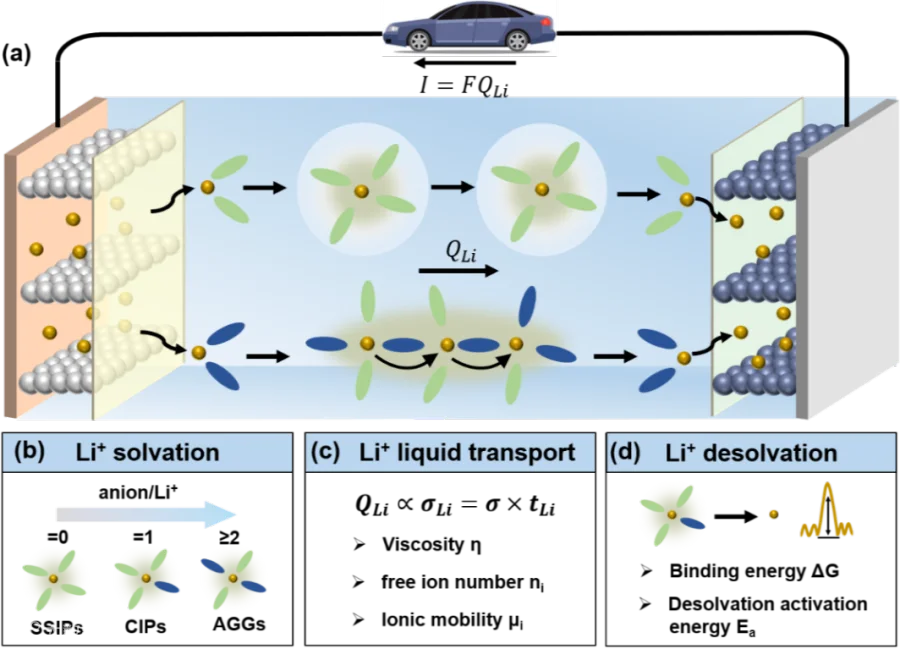
Figure 2 Li+在电解液中的传输过程及对应的评价指标

Figure 3 界面层性质与电池性能之间的关联
3.2 电解液组分间的基础相互作用
电解液的结构决定其在电池中的性能表现,特别是离子传输和界面化学行为。电解液中的粒子包括Li+阳离子、相应的盐阴离子以及各种溶剂偶极分子。由于锂离子具有较高的正电荷密度,而阴离子和偶极分子的电荷分布更为分散,因此Li+与其他粒子之间产生的相互作用相对较强,具体表现为Li+-偶极相互作用和Li+-阴离子相互作用。相比之下,阴离子与溶剂分子之间的相互作用(包括偶极-偶极相互作用和阴离子-偶极相互作用)则相对较弱。通过调控这些相互作用,可以改变电解液的结构,从而调节其性能。因此,理解这些相互作用如何影响电解液溶剂化结构并调控电化学行为具有至关重要的意义,这构成了电解质设计的底层逻辑基础。

Figure 4 Li+-溶剂相互作用
Li+-溶剂相互作用是溶解锂盐的根本动力。作用过强(如强极性溶剂EC)虽利于形成高电导的SSIPs结构,但会导致Li+脱溶剂困难,阻碍快充和低温性能。通过溶剂的静电势理论可以有效地预测不同溶剂对Li+的作用强度。选用弱溶剂、对溶剂分子进行氟化或增大空间位阻,可削弱此作用,促进阴离子参与配位,并降低脱溶剂能垒。

Figure 5 Li+-阴离子相互作用
Li+-阴离子相互作用在常规稀溶液中较弱,但在高浓度电解液或使用强结合能锂盐(如LiNO3,LiDFOB)时,会促进形成CIPs和AGGs。这会牺牲部分离子电导率,但其巨大优势在于能引导阴离子优先分解,形成富含无机物的界面膜。这种界面机械强度高、电化学稳定,能显著提升电池的循环寿命、高电压和高温耐受性。

Figure 6 溶剂-溶剂相互作用
溶剂-溶剂相互作用通常表现为氢键或偶极-偶极作用。这类“弱相互作用”可作为溶剂化结构的关键调节器。例如,通过设计溶剂-稀释剂间的氢键,可以“拉扯”Li+的溶剂化壳,加速脱溶剂;同样,利用PC与另一种溶剂的相互作用,可有效抑制PC在石墨负极的共嵌入,防止结构破坏。

Figure 7 阴离子-溶剂相互作用
阴离子-溶剂相互作用通常最弱,但通过引入阴离子受体(如含硼化合物)可显著增强这一作用。此作用能促进锂盐解离,提高Li+迁移数,某些条件下其还能改变界面双电层组成,诱导形成更优的界面膜。
这些相互作用对电解质整体性能的影响,可通过竞争-协同关系来理解。由于作用强度存在差异,对溶剂化结构影响最为显著的是Li+-阴离子与Li+-溶剂这两类相互作用,二者间的竞争与相对强弱共同决定了锂盐的解离程度,以及Li+溶剂化结构是溶剂主导型还是阴离子主导型。它们协同调控着电解质的离子电导率和Li+脱溶剂化难易程度。具体而言,当Li+-溶剂作用强至可实现锂盐完全解离时,较弱的Li+-溶剂作用则对应更高的离子电导率和更易发生的Li+脱溶剂化过程;而较强的Li+-阴离子作用虽有利于形成稳定的电极-电解质界面,却会因离子对的形成而降低Li+迁移效率。相比之下,阴离子-溶剂与溶剂-溶剂相互作用则通过竞争溶剂分子或阴离子,成为溶剂化结构的调控杠杆。增强阴离子-溶剂作用可解离离子对并降低阴离子迁移能力,从而提升锂离子迁移数;溶剂-溶剂作用则维系着电解质的物理状态和基本流动性,过强的溶剂-溶剂作用会增大溶剂粘度,提高Li+迁移阻力;而过弱的作用则会导致溶剂易挥发,降低电解质稳定性。总而言之,电解质的各项性能是这些相互作用竞争与协同的结果,任何单一相互作用的失衡都将导致特定性能指标的恶化。
3.3 电解液设计中的矛盾
在电解质设计中,我们通常期望在保持其他特性不衰退的前提下,提升某个甚至多个方面的性能。然而,由于各类相互作用间存在竞争关系,增强某一作用常会削弱另一作用。这导致与增强作用相关的性能得到改善,而与削弱作用相关的性能则出现衰减。相互作用调控中存在的固有矛盾,使得实现全面性能提升变得极为困难。最显著的是离子传输与界面稳定之间的矛盾。高的离子电导率通常依赖于SSIPs结构,而这易导致溶剂衍生的富有机的界面,可能带来高的界面阻抗和不够致密的界面膜。而阴离子衍生的富无机界面具有高强度,高电化学稳定性及低界面阻抗,但其却依赖于牺牲离子电导率的AGGs结构。其次,电解液的高低温性能兼顾同样是一大难点。低温性能依赖于三大关键:高离子电导率、低脱溶剂化能、低界面阻抗。需选用弱极性溶剂降低粘度,并通过富含高离子电导率无机物(如Li3N)的界面提升离子传导。高温稳定性则要求高沸点溶剂(如磷酸酯)和致密界面(如LiF/Li2O)来抑制分解。溶剂选择与界面设计存在固有矛盾:弱溶剂化溶剂虽利于低温却易挥发,而无机组分中高离子导与高稳定性难以兼得。最后,虽然弱化Li+-溶剂作用、促进阴离子配位(形成AGGs结构)能在实验上显著降低低温/快充时的界面阻抗,但理论计算表明更强的Li+-阴离子键本应增加脱溶剂能垒。这种表观矛盾暗示:观察到的性能提升可能并非源于脱溶剂步骤本身的简化,阴离子衍生的富无机物界面可能在催化脱溶剂过程中起到重要作用。目前对脱溶剂过程的微观机制仍缺乏直接实验证据,澄清阴离子的真实角色对进一步优化动力学性能至关重要。
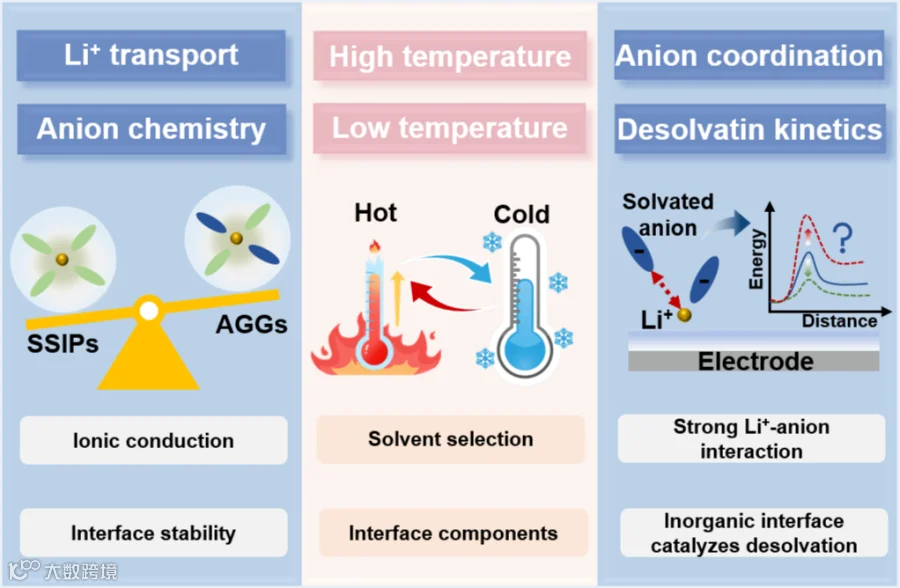
Figure 8 电解液相互作用调控中的矛盾
3.4 总结与展望
锂离子电池电解液的核心功能在于实现快速离子传输与构建稳定界面化学。电解液组分间相互作用通过竞争与协同方式共同塑造溶剂化结构,进而决定性影响离子传导效率与界面稳定性。这些微观相互作用构成了电解液性能的底层调控逻辑,其内在的竞争关系要求在设计过程中进行全局考量,唯有通过精准调控溶剂化结构,才能实现电解液综合性能的协同优化。
未来的电解液发展面临几大挑战:(1)在高电极负载下实现高功率性能,这要求实现数倍于当前水平的离子电导率与0.5-0.6的锂离子迁移数,但低粘度溶剂的使用常牺牲循环稳定性;(2)高电压/高温性能依赖富无机组分(LiF/Li2O)的致密界面,而传统高浓电解液方案又带来成本与低离子电导问题;(3)多功能集成需解决性能指标间的内在矛盾(如高低温性能冲突),关键在于通过解耦设计打破竞争性相互作用的制约;(4)基础认知层面需厘清脱溶剂化与界面演化的微观机制;(5)开发模式需借助计算模拟实现高通量筛选,加速理性设计。解决这些挑战需建立在对“相互作用-溶剂化结构-电化学性能”构效关系的深刻理解之上。
【文献详情】
Insights into the fundamental interactions within Li-ion battery electrolyte components and the solvation structure-property relationships[J]. Materials Science and Engineering: R: Reports, 2026, 167: 101134.
https://doi.org/10.1016/j.mser.2025.101134
文章来源:能源学人
《钠离子电池技术发展与产业前景研究报告》
▲以上报告由深水科技咨询制作
咨询电话:18115066088



