在医疗行业,产品研发与设备生产所需的高额投入成本,让众多企业深陷于如何将产品从研发阶段高效且顺畅地过渡至生产销售阶段的困境之中。
此时,企业面临一个关键抉择:究竟是自建生产线,还是寻求专业代工企业展开合作?

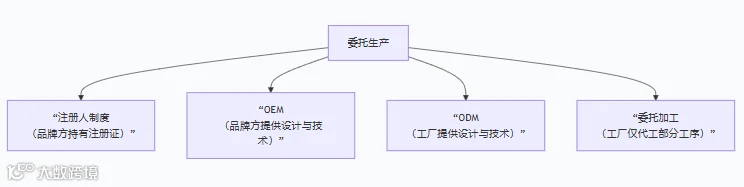
就医疗器械生产合作而言,典型模式涵盖委托生产、委托加工、OEM(原始设备制造商)、产学研医合作,以及在医疗器械注册人制度框架下的合作等。
那么,这些合作方式究竟存在哪些差异?又究竟哪一种合作模式更契合企业当前的发展阶段呢?
本文围绕平时常被问到的有关医疗器械委托生产、加工、合作等问题,进行汇总整理,供大家参考。
根据《医疗器械监督管理条例》第三十四条规定,医疗器械注册人、备案人可以委托具备相应条件的企业生产医疗器械。
委托生产——是指医疗器械产品的设计方或品牌方将产品的生产过程全部或部分,委托给具有相应生产资质的制造商。包括从原材料采购、生产加工到成品检验的整个流程。
作为医疗器械行业的从业者,很多企业老板或项目负责人可能更加专注于市场拓展,受限于资金、设备或专业人才等客观条件,无法自行建立生产线。
委托生产的合作方式能够将生产环节交给更加专业、成本更低的制造商,从而让负责人集中精力于自己擅长的领域,与此同时确保产品质量和生产效率。
《医疗器械生产监督管理办法》取消了“只能委托一家生产企业进行生产”的限制,目前是可以委托多家符合条件的生产企业进行生产的。
《医疗器械生产监督管理办法》中第三十二条规定:医疗器械注册人、备案人委托生产的,应当对受托方的质量保证能力和风险管理能力进行评估,按照国家药品监督管理局制定的委托生产质量协议指南要求,与其签订质量协议以及委托协议,监督受托方履行有关协议约定的义务。
受托生产企业应当按照法律、法规、规章、医疗器械生产质量管理规范、强制性标准、产品技术要求、委托生产质量协议等要求组织生产,对生产行为负责,并接受医疗器械注册人、备案人的监督。

OEM(原始设备制造商)和ODM(原始设计制造商)作为两种重要的生产合作模式,为企业提供了不同的解决方案。
➤OEM模式下,品牌商可以将产品的生产环节外包给专业的制造商,从而专注于品牌建设和市场拓展;(常被称为贴牌生产)
核心特征:
❶ 技术来自品牌方: 品牌方提供产品的设计图纸、技术参数、生产工艺及原材料要求。
❷ 工厂只负责生产: 受托工厂严格按照品牌方的要求,进行“来样加工”或“来料加工”。
➤而ODM模式则为缺乏设计能力的企业提供了从设计到生产的“一站式”服务。
核心特征:
❶ 技术来自工厂: 工厂不仅负责生产,还提供成熟的产品设计方案、技术文件甚至完整的医疗器械注册证。
❷ 品牌方“拿来即用”: 品牌方主要贡献在于品牌营销和市场渠道,可以直接选择工厂的现有产品方案,贴上自己的品牌进行销售。
OEM和ODM的主要区别在于,产品的设计责任和知识产权归属,到底在于品牌方还是生产方。
委托加工——通常指的是将医疗器械产品的某个生产环节或特定工艺委托给专业加工企业来完成。一般包括产品的零部件加工、组装、消毒、包装等。
如果你已经拥有一定规模的生产设备和生产线,但某些特殊工艺或零部件的加工需要特定的技术和设备,导致难以覆盖全部生产流程。
通过委托加工,企业可以弥补自身生产能力的不足,同时保持生产的灵活性和成本效益。

这种合作模式涉及高校、科研机构、企业以及医疗机构等多方主体,通过协同创新,推动医疗器械产品的研发和产业化。
高校和科研机构提供基础研究成果,企业负责产品开发和生产,医疗机构则提供临床需求和应用场景。
适用场景:适用于高端医疗器械的研发和创新,能够整合各方资源,促进技术突破和成果转化。

这是国家药品监督管理局推行的一项根本性制度改革。它允许符合条件的“注册人”在不自行生产的情况下,单独申请医疗器械注册证,然后委托给有资质的生产企业生产。
注册人负责产品的研发、注册和销售,而受托生产企业则负责产品的生产。
这种模式下,注册人可以是研发机构、企业或个人,而受托生产企业需具备相应的生产资质和能力。
适用场景:注册人将研发成果委托给有生产资质的企业进行生产,从而实现科技成果的产业化。
产学研医合作的重点在于技术研发和创新,强调从基础研究到临床应用的全链条合作。
合作流程包括科研项目的立项、研发、临床试验、成果转化等环节。
而医疗器械注册人制度下的合作的重点在于产品的注册和生产,强调注册人与生产企业之间的分工与协作。
合作流程主要涉及产品的研发、注册申请、生产委托、质量控制等环节。
1. 如何选择合作模式?
选择ODM: 如果您没有研发能力,希望快速上市,且对产品独家性要求不高。这是进入市场最快的方式。
选择OEM: 如果您拥有核心技术和产品设计,希望保护知识产权,并严格控制产品质量和一致性。
选择注册人制度: 如果您是研发机构或持有技术专利,希望完全拥有产品注册证和控制权,但不想自建工厂。
2. 代工合作中,最重要的法律文件是什么?
是 《医疗器械委托生产质量协议》 。这份文件必须严格按照《医疗器械监督管理条例》和《医疗器械委托生产质量协议编制指南》的要求制定。它明确了双方在质量管理体系中的责任划分,是飞检(飞行检查)的必查文件,也是出现质量问题时分担责任的核心依据。
3. 品牌方需要具备什么资质?
若采用OEM或注册人制度,品牌方必须持有《医疗器械注册证》/《医疗器械备案凭证》 和《医疗器械经营许可证》/《医疗器械经营备案凭证》。
若采用ODM,品牌方至少需要《医疗器械经营许可证》/《医疗器械经营备案凭证》,而产品注册证可能由工厂持有(需明确授权)。
4. 知识产权如何保护?
在OEM模式下: 品牌方需在协议中明确其提供的技术资料、配方、设计等属于商业秘密,并要求工厂承担保密责任。
在ODM模式下: 如果希望产品具有独家性,必须与工厂签订独家授权或买断协议,否则工厂可能将同一产品方案提供给多个品牌。
5. 质量责任由谁承担?
无论哪种模式,注册证持有人(品牌方)都是产品质量的第一责任人,对市场和质量问题负最终法律责任。
因此,品牌方必须对代工厂进行严格的质量体系审计,并持续进行监督和管理,不能做“甩手掌柜”。
6. 可以“免费拿证”或“快速拿证”吗?
这是一个巨大的陷阱。任何声称“不花钱拿证”或“远超常规速度拿证”的承诺都不可信。医疗器械注册流程严谨,需经过检测、临床(如需)、体系考核、药监局审评等环节,周期长、费用高。选择有技术实力和合规经验的合作伙伴,才是通往市场的正确道路。


最后
理解这些合作模式的差异,是企业成功布局医疗器械市场的第一步。关键在于明确自身定位与需求:您是技术的拥有者,还是市场的开拓者?在此基础上,选择最适合的模式,并通过严谨的法律协议明确权责,建立稳定、合规、互信的合作伙伴关系,方能行稳致远。
免责申明:本文图文均来自于网络,主要目的在于分享信息,版权归原作者所有,内容仅供读者参考,不作为任何用途。如有侵犯您的权益或版权请及时告知我们,我们将尽快删除!
about WEITAI

微肽集团
OEM/ODM化妆品一站式服务
冻干/护肤/械字号/消字号/特证
广州/长沙/佛山三大智能化工厂



