点击蓝字,关注我们

Pub Year:2025
DOI:10.1002/advs.202506107.
Background
1.研究背景:越来越多的文献表明,细胞间线粒体转移可调控健康与疾病状态下多个器官系统的生理功能,且具有治疗应用价值。食物免疫耐受已被充分证实。我们日常饮食中的植物含有线粒体,而线粒体的基本结构和功能在植物与动物中具有保守性。由于祖先内共生关系,植物和动物的线粒体在主要调控通路、生物能量代谢通路及化学底物通路方面具有共通性。然而,植物到哺乳动物的细胞间线粒体转移是否存在,以及其如何影响受体细胞功能,目前仍不明确。
2.本研究的主要发现:本研究证实,经口服给药的洋葱来源线粒体(O-Mit)可从肠道转运至肺部,并与巨噬细胞线粒体(M-Mit)融合。随后,O-Mit 中的 3,4 - 二羟基苯甲酸甲酯(MDHB)整合到 M-Mit 中,逆转 LPS 介导的 M-Mit 功能障碍,以及 LPS 诱导的白细胞介素 - 1β(IL-1β)、干扰素 -γ(IFN-γ)、白细胞介素 - 6(IL-6)、三磷酸鸟苷(GTP)、氧化型谷胱甘肽(GSSG)和线粒体超氧化物的过度产生。综上,口服 O-Mit 可通过调控 M-Mit 的能量代谢及动态活性,抑制 LPS 诱导的急性肺损伤(ALI)。这些发现揭示了植物线粒体在跨物种融合及调控肺部炎症中哺乳动物线粒体代谢通路方面的未知功能,为开发基于植物线粒体的转移疗法提供了启示。
Result & Figure
1.洋葱线粒体转移疗法抑制LPS诱导的小鼠急性肺损伤(ALI):
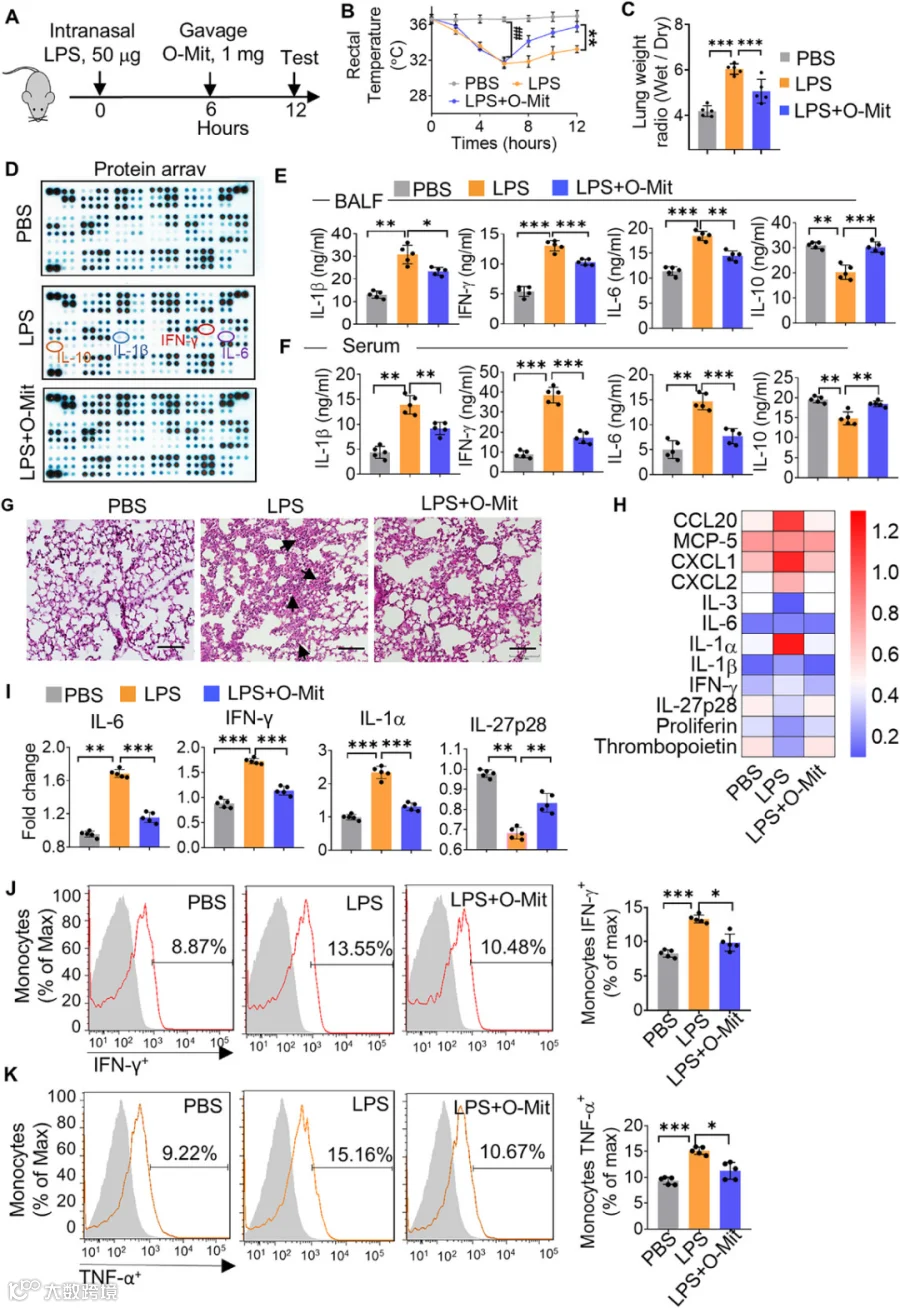
*图1:O-Mit可抑制脂多糖(LPS)诱导的小鼠急性肺损伤(ALI)。(A) 小鼠急性肺损伤(ALI)模型构建示意图。(B) 检测小鼠直肠温度。(C) 采用肺湿重/干重比值评估不同处理组小鼠的肺水肿程度。(D) 检测不同处理组 ALI 小鼠肺组织中细胞因子的表达。(E, F) ELISA检测不同处理组小鼠支气管肺泡灌洗液(BALF,E)和血清(F)中 IL-1β、IFN-γ、IL-6 和 IL-10 的水平。(G) 肺组织H&E染色。(H) 热图显示不同处理组小鼠细胞因子表达存在差异。(I) q-PCR检测肺组织中细胞因子基因的表达。(J, K) 流式细胞术(FACS)检测灌胃和未灌胃 O-Mit 的 ALI 小鼠肺单核细胞中 IFN-γ(J)和 TNF-α(K)的水平。
2.肺巨噬细胞以磷脂酸(PA)依赖性方式摄取O-MIT:
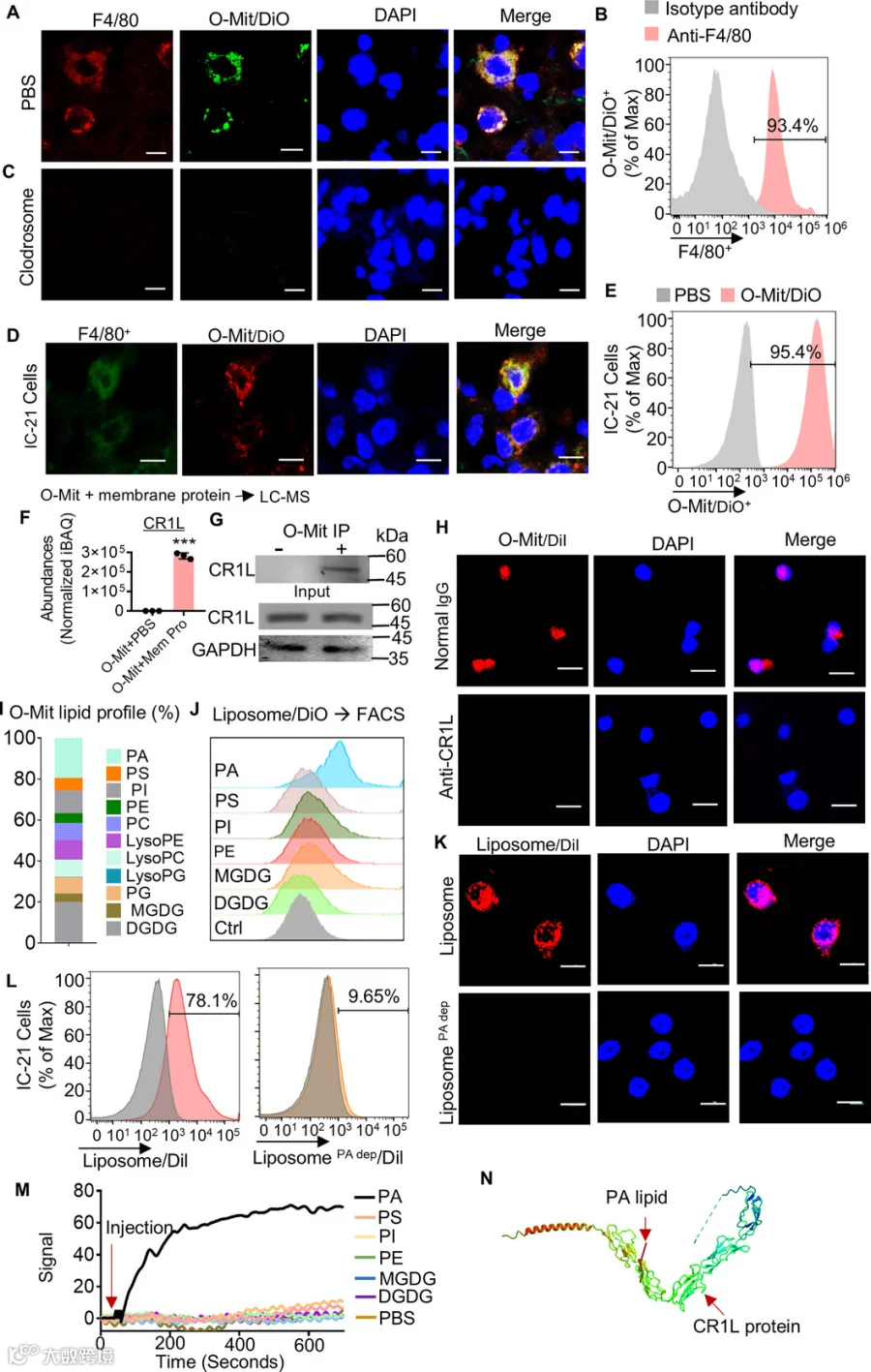
*图2:巨噬细胞摄取的O-Mit是通过 PA 和 CR1L之间的相互作用介导的。(A) 免疫荧光染色显示O-Mit/DiO与肺组织中F4/80+细胞共定位。(B) FACS分析用于量化F4/80+细胞在ALI小鼠肺组织中对DiO标记的O-Mit的摄取。(C) 免疫荧光染色显示在小鼠肺组织中未检测到 F4/80+细胞及 O-Mit/DiO。(D) 免疫荧光染色观察巨噬细胞对 O-Mit 的摄取情况。(E) 流式细胞术分析巨噬细胞对 DiO 标记 O-Mit 的摄取情况。(F) 采用液相色谱-质谱联用技术(LC-MS)分析与 O-Mit 相互作用的巨噬细胞膜蛋白。(G) 采用免疫共沉淀(CO-IP)检测O-Mit 与巨噬细胞膜蛋白 CR1L 的结合情况。(H) 免疫荧光染色观察巨噬细胞对 O-Mit 的摄取情况。(I) 通过 LC-MS 检测 O-Mit 的脂质谱。(J) 流式细胞术分析巨噬细胞对 DiO 标记脂质体的摄取情况。(K) 采用薄层层析法(TLC)分离 O-Mit 脂质,使用脂质体制备仪将分离后的 O-Mit 脂质制备为 PA 缺失脂质体(liposome PA dep)和非 PA 缺失脂质体;对脂质体进行 DiI 标记后与巨噬细胞共孵育,通过共聚焦显微镜观察巨噬细胞对脂质体的摄取情况。(L) 采用流式细胞术分析巨噬细胞对 DiI 标记的含 PA 与不含 PA 脂质体的摄取情况。(M) 将疏水芯片置于 Open SPR 仪器中,在芯片上固定不同脂质后注入 CR1L 蛋白,通过Open SPR观察信号变化。(N) 利用在线平台 HDOCK SERVER 模拟 AP 与 CR1L 蛋白的三维结构结合情况。
3.O-MIT与巨噬细胞线粒体的融合(M-MIT):
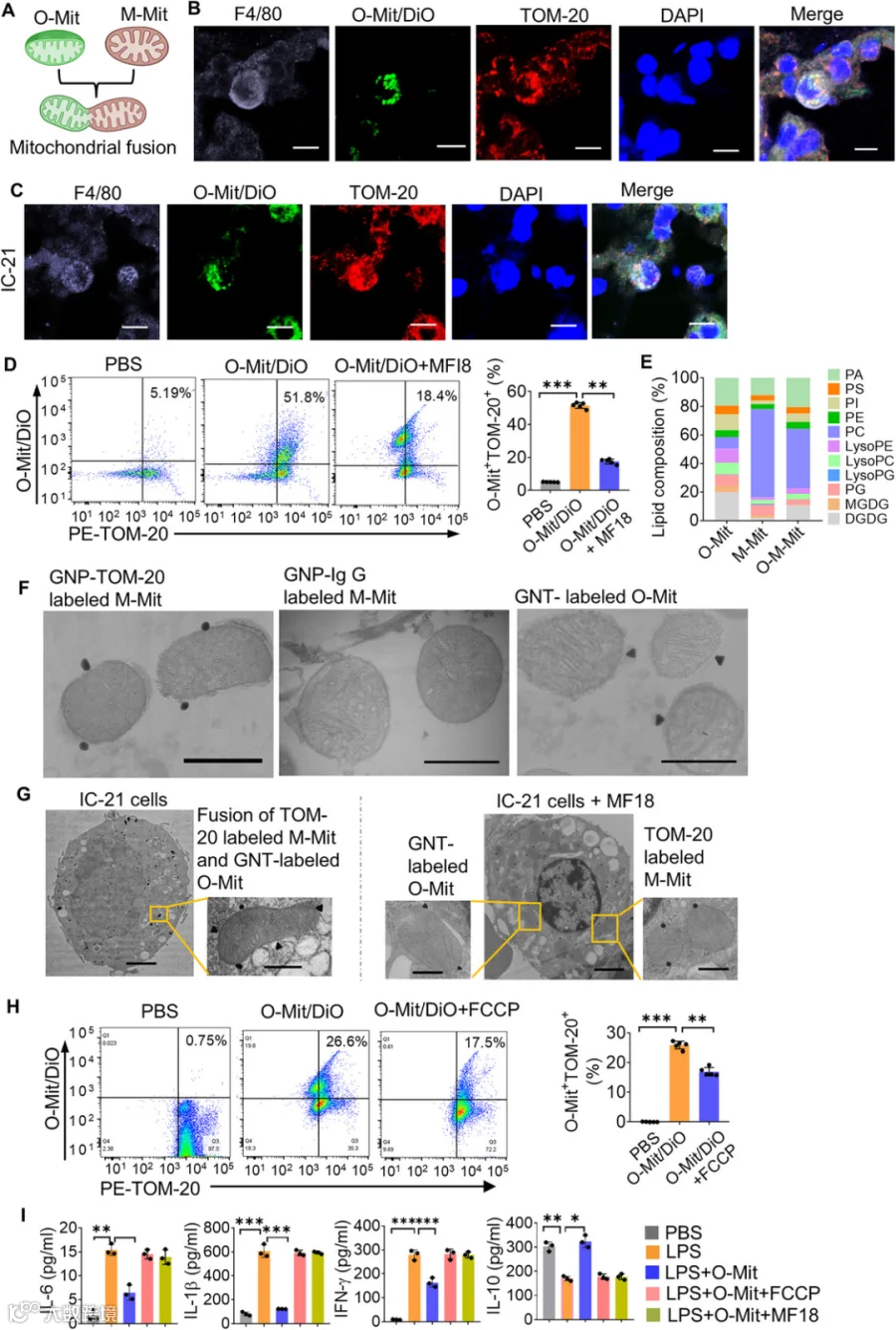
*图3:O-Mit与巨噬细胞线粒体(M-Mit)的融合。(A) 巨噬细胞摄取 O-Mit 后,O-Mit 与巨噬细胞线粒体(M-Mit)融合的示意图。(B) 对急性肺损伤(ALI)小鼠灌胃给予DiO 标记的O-Mit,取肺组织制作冰冻切片,用抗 F4/80 标记巨噬细胞、抗 TOM-20 标记线粒体(M-Mit)、DAPI 标记细胞核。共聚焦显微镜观察显示,急性肺损伤小鼠肺组织中,O-Mit 被巨噬细胞摄取并与线粒体融合。(C) 将 DiO 标记的 O-Mit 与巨噬细胞共孵育,用抗 F4/80 标记巨噬细胞、抗 TOM-20 标记线粒体、DAPI 标记细胞核。共聚焦显微镜观察显示,O-Mit 被巨噬细胞摄取并与线粒体融合。(D) 将DiO标记的O-Mit 与巨噬细胞共孵育 1 小时后,分离巨噬细胞的线粒体,用 PE-TOM-20 抗体标记线粒体。流式细胞术分析显示,O-Mit 与线粒体存在相互作用,且该相互作用可被线粒体融合抑制剂 MFI8 阻断(左图);O-Mit/DiO 与 TOM20 共定位的定量分析(右图)。(E)将 O-Mit 与巨噬细胞共孵育后,分离线粒体,通过流式细胞术分选 O-Mit/DiO 阳性线粒体(O-M-Mit),随后采用液相色谱 - 质谱联用技术(LC-MS)分析其脂质组成。(F)透射电镜(TEM)观察金球纳米颗粒(GNP)标记的线粒体(左)、GNP-IgG 标记的线粒体(中)和金三角纳米颗粒(GNT)标记的 O-Mit(右)。(G) 体外实验中,将 GNT 标记的 O-Mit 与巨噬细胞在 37℃下共孵育 1 小时,洗涤后用抗 Tom20 和 GNP - 蛋白 A 磁珠标记线粒体。巨噬细胞的代表性透射电镜图像(左)及巨噬细胞线粒体的放大图像(右)。(H) 流式细胞术分析 O-Mit 的活性及其对巨噬细胞线粒体融合的影响(左图);O-Mit/DiO 与 TOM20 共定位的定量分析(右图)。(I) 经 FCCP 或 MF18 处理后,O-Mit 无法抑制脂多糖(LPS)诱导的巨噬细胞细胞因子分泌。
4.O-Mit Rescue ALI小鼠肺部M-MIT功能障碍:
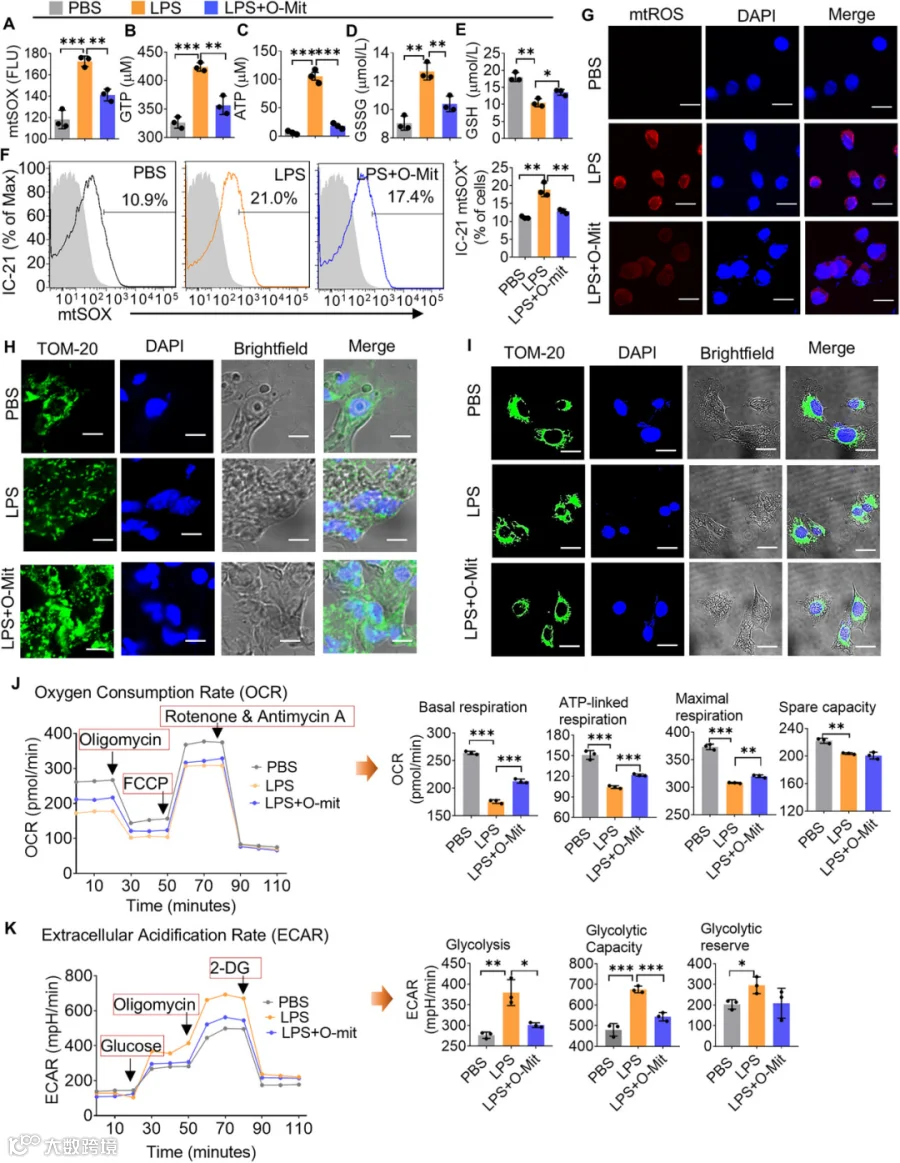
*图4:O-Mit调节肺中巨噬细胞的线粒体活性。(A-E) 将巨噬细胞 IC-21 与 LPS(1 μg/mL)共孵育 6 小时,随后用 O-Mit(1 μg/mL)处理。通过检测以下指标评估巨噬细胞线粒体活性:(A) 线粒体超氧化物(mtSOX)、(B) 三磷酸鸟苷(GTP)、(C) 三磷酸腺苷(ATP)、(D) 氧化型谷胱甘肽(GSSG)、(E) 还原型谷胱甘肽(GSH)。(F) 将巨噬细胞与 LPS 共孵育,用 PBS 洗涤后,用 O-Mit 处理。采用流式细胞术检测巨噬细胞线粒体超氧化物(mtSOX),结果显示 O-Mit 可降低 LPS 诱导的巨噬细胞 mtSOX 水平。(G) 将巨噬细胞与 LPS 共孵育,用 PBS 洗涤后,分别用 O-Mit 处理或不处理。共聚焦显微镜观察显示,O-Mit 可减少 LPS 诱导的巨噬细胞活性氧(ROS)生成。(H, I) 采用共聚焦显微镜观察线粒体形态:在急性肺损伤(ALI)小鼠肺组织(H)和巨噬细胞(I)中,LPS 可诱导线粒体碎片化;经 O-Mit 处理后,细胞内线粒体恢复正常形态。(J, K) 将巨噬细胞用 LPS 处理,PBS 洗涤后与 O-Mit 共孵育,采用 Seahorse 分析检测氧消耗率(OCR,J)和细胞外酸化率(ECAR,K)。结果显示,O-Mit 可降低 LPS 诱导的巨噬细胞线粒体 ECAR,同时提高线粒体 OCR。
5.O-Mit甲基 3,4-二羟基苯甲酸酯(MDHB)抑制 LPS诱导的肺部炎症:
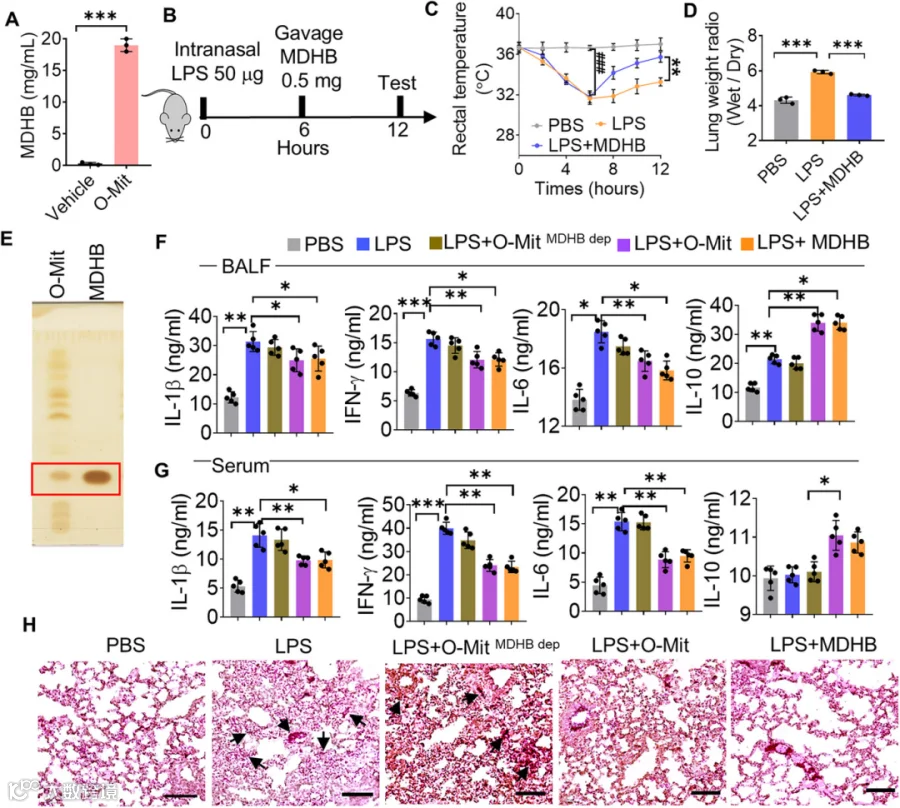
*图5:O-Mit中的甲基3,4-二羟基苯甲酸(MDHB)抑制LPS诱导的ALI小鼠。(A) 将 O-Mit 与巨噬细胞膜蛋白共孵育后离心沉淀 O-Mit,用 CTAB 裂解缓冲液裂解沉淀。对 O-Mit 的 CTAB 裂解液进行小分子液相色谱-质谱联用(LC-MS)分析,结果显示其中富含 MDHB(一种小分子物质)。(B) 实验示意图:对 C57BL/6J 小鼠鼻内给予 50 μg / 只的 LPS;6 小时后,以 0.5 mg / 只的剂量灌胃给予 MDHB;灌胃后 6 小时,检测小鼠体内的细胞因子水平。(C) 鼻内注射 LPS 后,每2小时记录 B6 小鼠的直肠温度。6 小时时,LPS 组与 PBS 组相比存在显著差异;6 小时时以 0.5 mg / 只的剂量灌胃给予 MDHB,6 小时后,MDHB 处理组小鼠与 LPS 组相比,体温存在显著差异。(D) 采用肺湿重/干重比值评估不同处理组小鼠的肺水肿程度。(E) 采用薄层层析法(TLC)分离 O-Mit 裂解液中的小分子物质;根据 MDHB 标准品的迁移位置,红色方框标注出 O-Mit 裂解液中的 MDHB 条带。(F, G) 对急性肺损伤(ALI)小鼠分别灌胃给予 O-Mit 裂解液、去除 MDHB 的 O-Mit 裂解液(O-Mit MDHB dep)及 MDHB;6 小时后,采用酶联免疫吸附试验(ELISA)检测小鼠支气管肺泡灌洗液(BALF,F)和血清(G)中 IL-1β、IFN-γ、IL-6 和 IL-10 的水平。结果显示,灌胃 O-Mit 裂解液和 MDHB 的 ALI 小鼠,其促炎细胞因子 IL-1β、IFN-γ、IL-6 水平降低,抗炎细胞因子 IL-10 水平升高;而灌胃去除 MDHB 的 O-Mit 裂解液的 ALI 小鼠,其细胞因子表达水平与未处理的 ALI 小鼠相近。(H) 急性肺损伤小鼠肺组织的H&E染色结果显示:灌胃 O-Mit 裂解液和 MDHB 后,小鼠肺部炎症显著减轻;但灌胃去除 MDHB 的 O-Mit 裂解液的 ALI 小鼠,其肺部炎症程度与未处理的 ALI 小鼠相近。箭头所示为肺泡腔和间质区域的炎症细胞浸润,以及肺泡壁增厚现象。
6.O-Mit MDHB挽救M-Mit功能障碍:
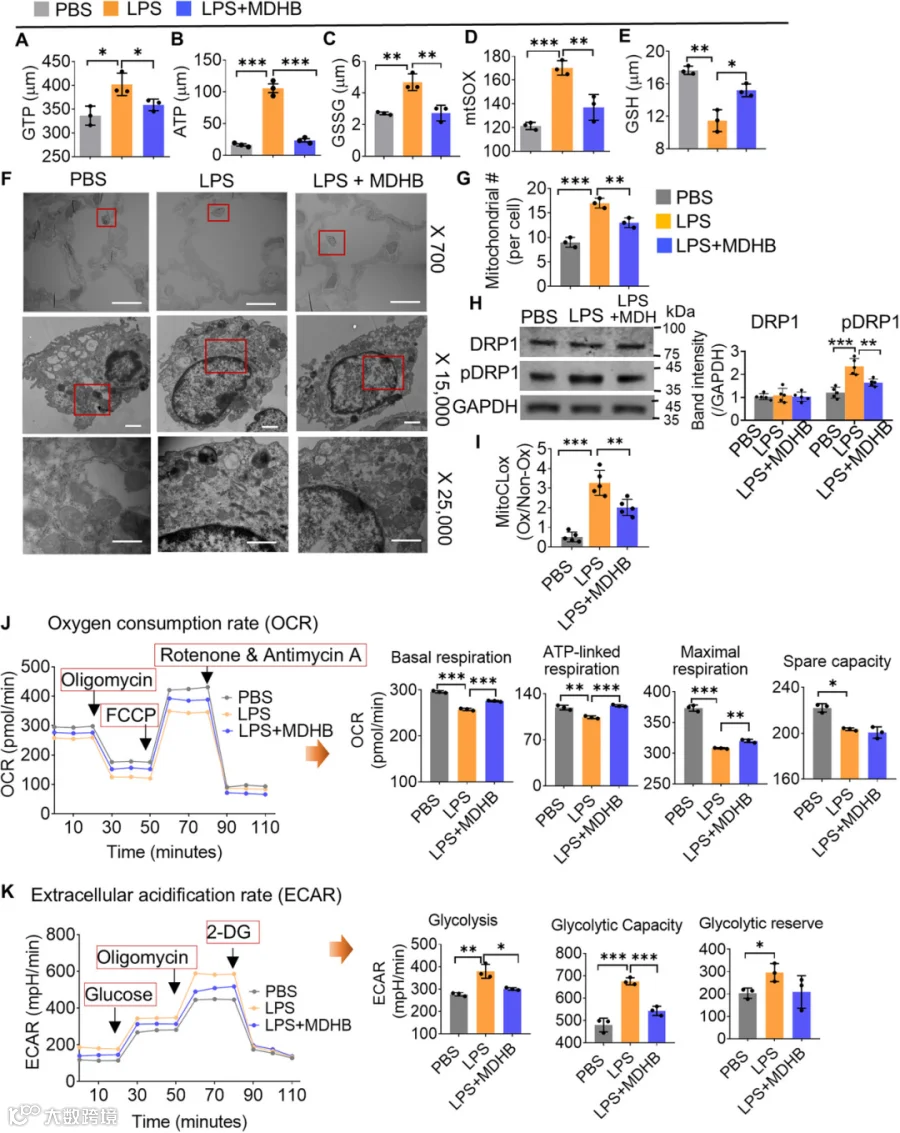
*图6:MDHB挽救LPS诱导的巨噬细胞线粒体功能障碍。(A-E) 将巨噬细胞 IC-21 与脂多糖(LPS,1 μg/mL)共孵育 6 小时,随后用 MDHB(0.5 μg/mL)处理。通过检测以下指标评估巨噬细胞线粒体活性:(A) 三磷酸鸟苷(GTP)、(B) 三磷酸腺苷(ATP)、(C) 氧化型谷胱甘肽(GSSG)、(D) 线粒体超氧化物(mtSOX)、(E) 还原型谷胱甘肽(GSH)。(F) 对急性肺损伤(ALI)小鼠灌胃给予 MDHB(0.5 mg / 只),6 小时后收集肺组织。采用透射电镜(TEM)观察小鼠肺组织内巨噬细胞的线粒体亚结构及数量。(G) 通过透射电镜计数灌胃与未灌胃 MDHB 的急性肺损伤小鼠肺组织中巨噬细胞的线粒体数量。(H) 采用Western blot检测灌胃与未灌胃 MDHB 的急性肺损伤小鼠肺组织中DRP1 及p-DRP1的表达水平。(I) 采用 MitoCLox 探针分析心磷脂过氧化水平:分离灌胃与未灌胃 MDHB 的急性肺损伤小鼠肺组织中的巨噬细胞,用 MitoCLox 染色后,通过酶标仪分别在 590 nm(非氧化状态)和 520 nm(氧化状态)处检测荧光强度;图表展示氧化状态(Ox)与非氧化状态(Non-Ox)的荧光强度比值。(J, K) 将巨噬细胞 IC-21 用 LPS 处理后,与 MDHB 共孵育,采用 Seahorse 分析检测氧消耗率(OCR,J)和细胞外酸化率(ECAR,K)。结果显示,MDHB 可降低 LPS 诱导的巨噬细胞线粒体 ECAR,同时提高线粒体 OCR。
7.MDHB通过结合线粒体ND1调节线粒体基因表达:
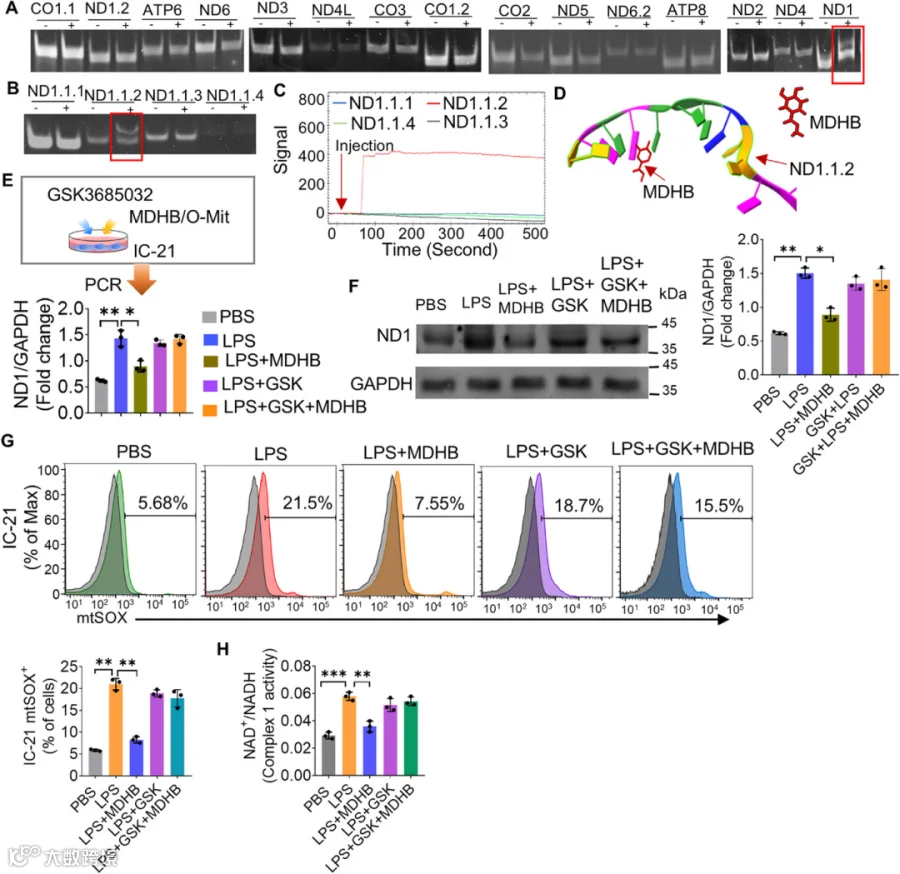
*图7:MDHB通过结合线粒体DNA(mtDNA)来调节线粒体基因表达。(A) 将小鼠线粒体 DNA(mtDNA)切割成不同大小的片段,随后分别与 MDHB 共孵育或不孵育。采用琼脂糖凝胶电泳比较切割后 mtDNA 的迁移情况,以分析 MDHB 与切割后 mtDNA 的结合作用;红色方框显示,与未加 MDHB 孵育的 ND1 片段相比,加 MDHB 孵育的 ND1 片段迁移速度更慢。(B) 将mtDNA 中的 ND1 基因扩增为 4 个片段(每个片段 50 bp),这些 ND1 片段分别与 MDHB 共孵育或不孵育。琼脂糖凝胶电泳分析显示,与未加 MDHB 孵育的 ND1.1.2 片段相比,加 MDHB 孵育的 ND1.1.2 片段迁移速度更慢(红色方框)。(C) 将 MDHB 固定在 Open SPR 芯片上,向芯片中注入 ND1 基因的不同 50 bp 片段。信号结果显示,注入 ND1.1.2 片段时,信号强度显著升高;而注入其他 MT-ND1 片段时,未观察到信号变化。(D) 为验证 MDHB 与 ND1.1.2 的结合作用,将两者的三维结构提交至 HDOCK SERVER 在线平台,并使用 Chimera 1.9 软件进行分析。分析结果显示,二者对接评分较高,表明 MDHB 与 ND1.1.2 之间具有较强的结合亲和力。(E) 先用 GSK3685032 处理巨噬细胞,随后用 LPS 刺激 2 小时;去除上清后,分别用 MDHB 或 GSK3685032 处理细胞;收集巨噬细胞提取 RNA,通过 PCR 分析线粒体 ND1 基因的表达水平。(F) LPS 可诱导巨噬细胞中线粒体 ND1 蛋白表达升高;但当 MDHB 与线粒体 ND1 基因结合后,LPS 诱导的巨噬细胞线粒体 ND1 蛋白表达被抑制。(G) 流式细胞术(FACS)分析结果显示,MDHB 可显著降低 LPS 诱导的巨噬细胞线粒体超氧化物(mtSOX)生成(上图);流式细胞术数据的定量分析(下图)。(H) LPS 刺激下,巨噬细胞中 NAD/NADH 比值升高,表明巨噬细胞处于氧化状态;但 MDHB 处理可逆转 LPS 诱导的 mtSOX 升高及 NAD/NADH 比值升高,使巨噬细胞内这些指标维持在适宜水平。

Reference
Xu Q, Teng Y, Huang Y, Mu J, Teng L, Qian H, Huang Q, Liu M, Zou Y, Zhang L, Merchant ML, Zhang X, Yan J, Zhang HG. Onion-Mitochondria Inhibit Lipopolysaccharide-Induced Acute Lung Injury by Shaping Lung Macrophage Mitochondrial Function. Adv Sci (Weinh). 2025 Oct 6:e06107.
注:本文内容仅为学术分享,若对原文内容理解有误,望请各位读者指正。
长按扫码关注

公众号丨水云天生物





