中国保健品出口日本:如何合规分类与准入?
日本市场对保健品需求旺盛,但其法规体系严谨复杂,产品分类与合规要求严格。中资企业欲顺利进入日本市场,必须清晰理解日本对药品、食品及保健功能食品的界定标准及相关法律法规[k]。
一、药品与食品的界定标准
根据日本《药品医疗器械等法》,凡用于诊断、治疗或预防疾病的物品,或影响身体结构与功能的物品,均被定义为“药品”[k]。而“食品”则指可食用且不具疾病治疗功能的普通消费品[k]。
判断进口产品属于药品还是食品,需综合评估以下四个要素,若任一条件符合,则可能被认定为药品,须接受更严格监管[k]:
- 成分本质:若产品含有日本列为“主要作为药品使用的成分”,则视为药品[k]。
- 标示功效:若包装、宣传中明示或暗示具有治疗、预防疾病或调节生理功能的效果,即使使用外语,也按药品管理[k]。
- 产品形态:如采用安瓿剂、舌下锭、喷雾剂等典型药品剂型,易被归为药品[k]。
- 用法用量:若明确标注服用时间、剂量、疗程等信息,将被视为药品[k]。
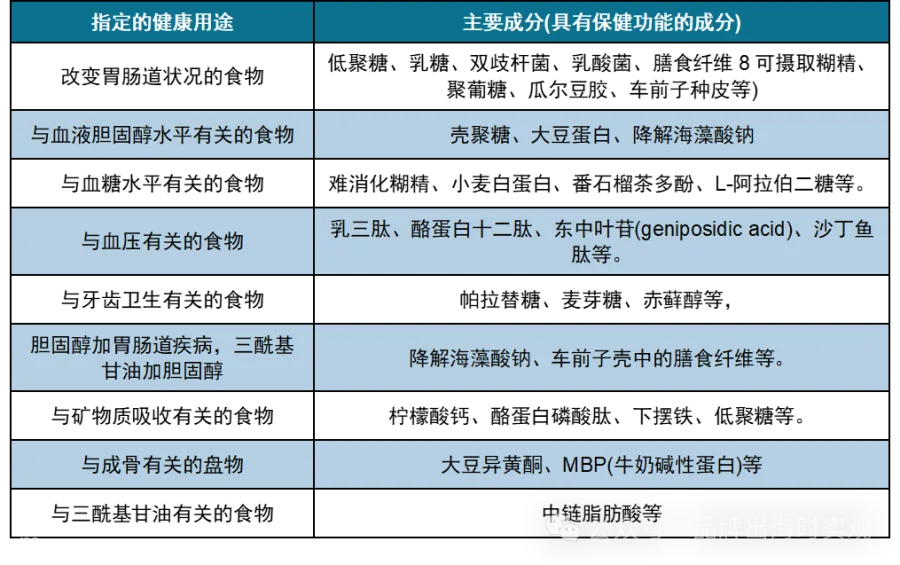
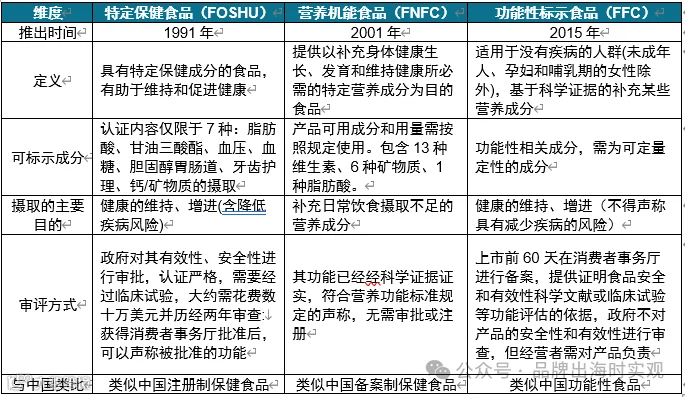
二、健康食品的三大分类:FOSHU、FNFC与FFC
日本将具备调节生理机能、预防疾病等功能的食品定义为“保健功能食品”,主要分为三类,监管强度依次递减[k]。
1. 特定保健用食品(FOSHU)
FOSHU为最早设立的保健食品类别,需经消费者厅、食品安全委员会及厚生劳动省三级审批,审批严格,仅允许单一健康用途声明(如“补钙”)[k]。该制度始于1991年,旨在应对饮食西化带来的慢性病高发问题[k]。

2. 营养机能食品(FNFC)
FNFC允许使用的成分为13种维生素、6种矿物质和1种脂肪酸,旨在补充日常营养不足[k]。无需审批,但需在产品上明确标示成分及每日摄入量,企业可直接合规上市[k]。
3. 功能性标示食品(FFC)
FFC于2015年设立,借鉴美国DSHEA法案,监管更为灵活[k]。企业可基于科学证据自主标示功能,无需事先审批[k]。
相较于FOSHU,FFC在健康声明和临床研究方面更具优势:
- 功能声明更广泛:涵盖骨骼、皮肤、睡眠、记忆、疲劳、肝脏等多方面,不再局限于代谢相关指标[k]。
- 研究要求更宽松:FFC只需证明产品相较于安慰剂的显著效果,无需阐明作用机理;配方变更也无需重复临床试验[k]。
三、适用的主要法律法规
保健功能食品作为食品类别,需遵守《食品卫生法》,完成安全性评估与检疫申报[k]。同时,营销宣传须符合《健康增进法》与《资源有效利用法》,禁止虚假、夸大或误导性表述[k]。
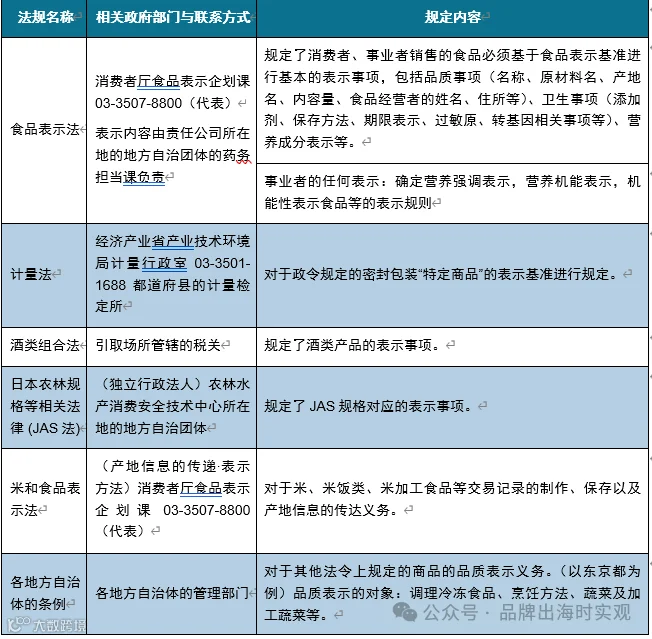

企业可向消费者厅食品表示规划科咨询通用法规问题,或通过所在地保健所获取具体产品合规指导[k]。


