
文献引用格式:董齐,熊思雨,周应山,等.生物医用纤维材料制造技术进展及应用研究[J].纺织科学研究,2024,(11):12-22.
生物医用纤维的创新与应用进展
董齐1a,熊思雨1a,周应山1b, 张兆威1a,2*
(1.武汉纺织大学 a.生物工程与健康学院; b.材料科学与工程学院,湖北 武汉 430020; 2. 湖北洪山实验室,湖北 武汉 430070)
摘要:纤维材料因其高比表面积和纳米结构所带来的特殊功能而成为研究的焦点。在医疗领域,纤维材料已经广泛应用于生物传感、治疗、药物递送和组织工程等多方面。本文综述了生物医用纤维材料制造技术的最新进展及其在生物医学领域的应用。探讨了多种纤维制造技术,包括基于微挤出的生物打印、微流体纺丝、湿法纺丝、干法纺丝、静电纺丝和近场静电纺丝等,详细分析了这些技术的设备要求、制造机制、关键加工参数、应用材料以及纤维结构和功能,评估了每种技术的优势与局限。探讨了纤维在组织工程、药物递送、伤口管理和生物传感器等领域的应用、前沿研究成果及面临的挑战,以期为生物医用纤维材料的理论和应用研究提供信息和技术支撑。
关键词:生物医用纤维;材料来源;制备加工技术;生物应用
前言
近年来,纤维材料在医疗领域的应用日益广泛,包括医用敷料、缝合线、口罩等产品[1-2]。随着材料科学、纳米技术和电子学的飞速进步,纤维材料被赋予了实时监测生理信号、药物递送、细胞移植以及神经记录/刺激等新功能。这些创新功能极大地推动了组织工程、可穿戴和植入式生物医学设备的发展[3-5]。
在绿色可持续发展理念的推动下,越来越多的天然高分子及其衍生物被开发应用于生物医学领域。这些材料因其优异的生物相容性、生物可降解性、仿生天然细胞外基质的结构、可持续利用和环保特性而受到重视[6-8]。同时,材料制造技术的迅猛发展使得纤维材料可以通过多种策略进行精确控制制造,包括基于微挤出的生物打印、微流体纺丝、湿法纺丝、干法纺丝、静电纺丝和近场静电纺丝等技术[9-10]。
当纤维直径从宏观尺度降至微米或纳米级别时,会展现出一系列特殊的理化特性,如增强的机械强度、高比表面积以及独特的表面功能[11]。这些显著特性使纤维在众多关键领域得到广泛应用,包括传感器、能量存储、催化、组织工程、药物递送和伤口愈合等[12-15]。本文评述了生物医用纤维材料的来源、分类、独特属性以及纤维的制造技术,并介绍了纤维材料在生物医学领域的应用,包括组织工程支架、药物输送系统、伤口愈合材料和生物传感器(见图1)。最后,对纤维制造技术及当前面临的挑战和未来发展潜力进行了讨论。

1 生物医用纤维材料的来源
目前常见的生物医用纤维材料来源包括两类:一类是天然高分子类,如纤维素及其衍生物、甲壳素及其衍生物(壳聚糖)、海藻酸、蛋白(丝素蛋白、羊毛角蛋白);另一类则是合成高分子类,如聚丙烯、聚氨酯[10, 16]。各材料性能不同,其适用的加工方式和应用领域也不同。
1.1 天然高分子
壳聚糖是一种常见的天然多糖。它是来自甲壳类动物外壳、骨骼的几丁质的N-脱乙酰衍生物。壳聚糖具有优异的生物相容性、生物降解性和抗菌性[17-18]。壳聚糖的阳离子特性,可以与各种阴离子糖胺聚糖形成聚电解质复合物,通过调节生长因子和细胞因子的活性在骨再生中发挥重要作用。同时,壳聚糖中的官能团也为生物活性分子提供结合位点,从而更好地支持细胞的生长。此外,壳聚糖的降解速率可以通过改变脱乙酰程度来调节,从而满足不同组织的再生需求[19]。壳聚糖纤维可制成隐形眼镜、人工皮肤、缝合线、人工透析膜和人工血管等组织工程支架[20]。
蚕丝蛋白主要来源于蜘蛛或蚕分泌的纤维。以蚕茧为例,它主要由丝素蛋白(SF)和丝胶蛋白 (SS)组成。SS拥有来自亲水性氨基酸的丰富活性基团,使得SF具有良好的机械和生物特性以及易于加工的特性,从而在生物医学领域展现出很大的吸引力[21-22],已应用在外科缝合线、人造组织、药物载体等多个领域[23-25]。
纤维素是由葡萄糖组成的天然高分子聚合物,是世界上蕴藏量最丰富的天然多糖类化合物[26]。常见的纤维素纤维材料包括棉、麻和纤维素制成的再生纤维(莱赛尔、莫代尔)。其中,棉因其纤维素含量高(接近100%)、柔软、亲水性强等优势,被认为是卫生保健领域里最为合适的基础材料之一,常用于伤口敷料、一次性卫生用品等[27-28]。
1.2 合成高分子
合成高分子通常表现出优异的机械性能、良好的加工能力、耐久性和化学稳定性,包括聚丙烯(PP)、聚四氟乙烯(PTFE)、聚酯(PET)、聚乳酸(PLA)、聚乙烯(PE)等。例如,聚乳酸(PLA)由丙交酯开环聚合得到可降解的聚合物,其聚合单体分为L-乳酸和D-乳酸[29]。PLA的降解产物可参与人体代谢,被广泛用于骨科植入物、缝合线和药物控释载体。
2 生物医用纤维材料的制造技术
为了制造天然高分子或合成高分子的纤维,已经发展出多种技术,包括基于微挤出式3D生物打印、微流体纺丝、湿法纺丝、干纺丝、静电纺丝和近场静电纺丝(见图2)。表1总结了每种纤维制造技术在纤维直径、形态以及各自的优势和局限性。
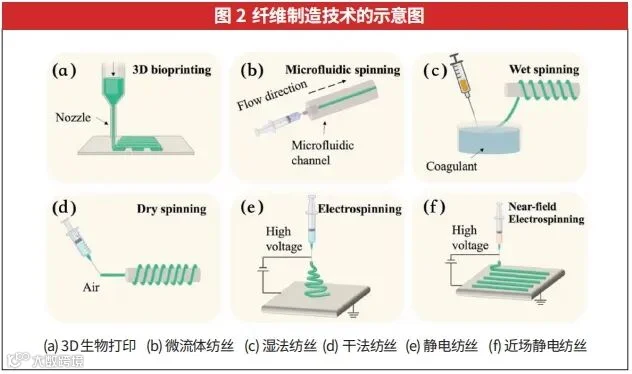
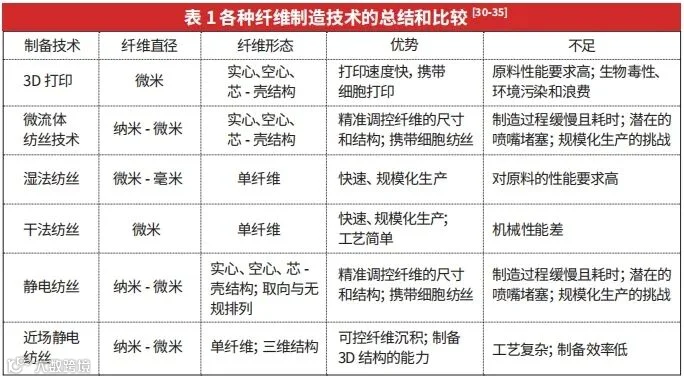
2.1 挤出式3D生物打印
近年来,3D生物打印技术在生物医学领域取得了显著进展。它融合了工程学、细胞生物学和材料科学的知识,通过逐层沉积含有活细胞和活性生物分子的生物墨水,最终构建出模拟天然组织或器官的3D支架[36]。 3D生物打印技术主要包括微挤压生物打印[37]、喷墨生物打印[38]、激光辅助生物打印[39]以及立体光固化成型[40]。其中,微挤出式3D生物打印以其成本低、适用性广以及构建复杂空心支架的能力,成为最常用的技术之一[41]。此外,微挤出的生物打印能够连续地打印出细丝或纤维,展现出其独特优势。
经过数十年的深入研究与发展,科学家们已经开发出多种适用于挤出式生物打印的生物墨水。这些生物墨水根据其来源,主要分为两大类:一类来源于天然材料,另一类则源自合成材料。表2列出了用于微挤出3D生物打印的聚合物的优点、缺点以及应用。
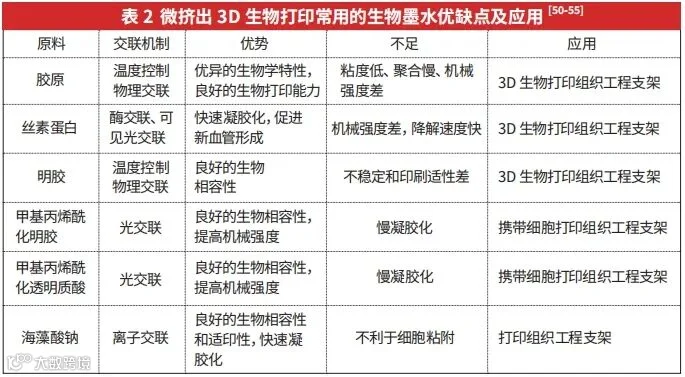
海藻酸盐或海藻酸是最早用于挤出式生物打印的生物材料。它是一种来源于海藻的生物多糖。海藻酸钠是最常见的水溶性海藻酸盐,可与钙离子溶液 (Ca2+)或镁(Mg2+)形成水凝胶。海藻酸钠的离子反应迅速(在几秒钟内),形成的水凝胶具有良好的机械强度和生物相容性[42-43]。在3D打印领域,海藻酸盐被用于制造组织工程支架,如藻酸盐/壳聚糖支架。尽管海藻酸盐的低粘度和较弱的机械性能限制了复杂结构的打印,但通过添加壳聚糖等材料可以提高打印墨水的粘度和结构稳定性[44]。例如,Wu等人采用3D生物打印技术,利用含有大鼠雪旺细胞的海藻酸盐/明胶水凝胶复合材料,成功制备了用于神经组织工程的神经支架[45]。Antich等人设计了一种新型透明质酸/海藻酸盐生物墨水,通过3D打印软骨组织用于软骨缺损的修复[46]。
甲基丙烯酰化明胶(GelMA)因其出色的生物性能被广泛用于支架材料,通过模拟天然组织的复杂结构来修复组织的复杂功能[47]。He等人通过同轴生物打印方法制造了具有可控形态的GelMA/海藻酸盐组合的水凝胶微纤维[48]。通过调整微流体的流速,GelMA微纤维的形态可以从直线变为波浪形,最终变为螺旋结构。清华大学教授王秀梅利用甲基丙烯酰化明胶(GelMA)/甲基丙烯酰化透明质酸(HAMA)的混合水凝胶,通过紫外光交联3D打印脊髓神经的取向结构,并在水凝胶中负载神经干细胞,用于脊髓神经损伤的修复[49]。
2.2 微流体纺丝技术
微流体纺丝制备纤维具备高表面积体积比、精确调控微/纳米级纤维的尺寸、成分和结构[56]。通过精确集成多相层流并在微通道环境中调节每个相的状态,制造出多功能的微/纳米级纤维。例如,圆形、扁平、沟槽、各向异性、空心、核壳、Janus结构、异质结构、直线、波形、螺旋和打结形态的纤维等[57]。
纤维材料的多样性主要源于多种固化方法。固化方法通常分为化学反应(如光聚合反应、化学交联反应)和物理固化过程(如离子交联反应、溶剂交换、非溶剂诱导相分离和溶剂蒸发),如图3所示。表3展示了微粒体纺丝常用的凝固方法和原料。
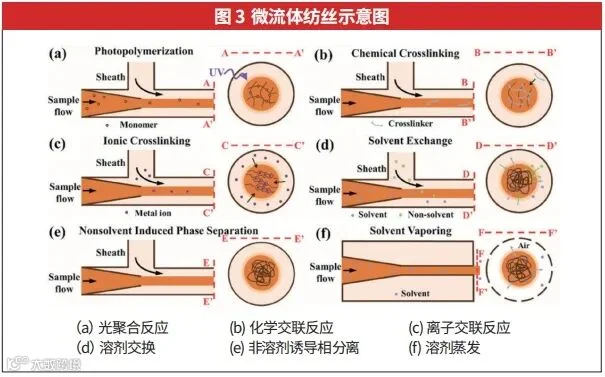
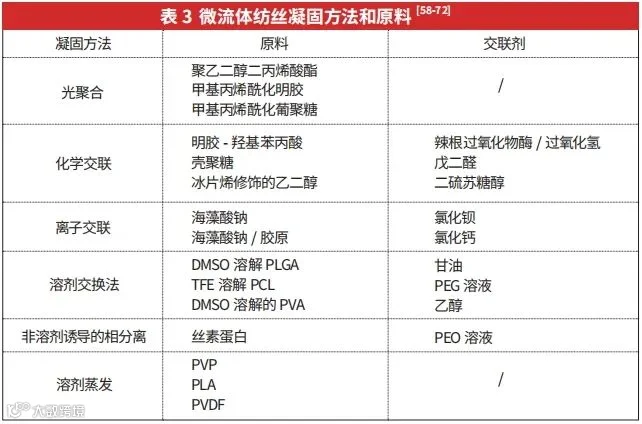
2.3 湿法纺丝
湿法纺丝技术分为“溶解—挤出—凝固—收集”4个步骤,如图4所示。在这一过程中,纺丝原液通过喷丝板直接挤出,进入混凝槽。槽内含有“差溶剂”“非溶剂”或“非溶剂/溶剂混合物”[73]。当细丝与浴槽接触后,由于溶剂与非溶剂之间的交换作用,细丝中的聚合物开始经历相转变,并凝结、凝固。经过一系列的漂洗以及加热辊(干燥拉丝辊)加工后,最终在旋转线轴上收集到的连续纤维,直径范围在数十到数百微米之间[74-75]。
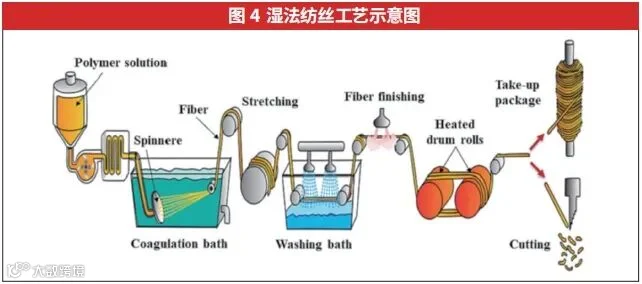
在湿法纺丝过程中,有几个关键参数对聚合物的凝结过程以及最终纤维形态产生显著影响。这些关键参数包括聚合物浓度和分子量、溶剂/非溶剂体系、溶液和凝固槽中的添加剂、加工温度、溶液进料速率、喷嘴直径以及卷绕速度[76]。湿法纺丝制备的纤维材料广泛应用于多种医疗领域,如药物输送系统[77]、血液透析[78]、修复受损的纤维环[79]、骨骼[80]以及肌腱组织工程[81]。
2.4 静电纺丝
静电纺丝能制造出纳米至微米级纤维,这一技术由Formalas在1934年发明。该技术涉及高压电源、连接针和接地的纤维收集器,如图5所示。在高压电场的作用下,聚合物溶液会形成带电射流,经分裂和蒸发后在收集器上形成纤维[82-83]。纤维特性受溶液特性、操作参数和环境条件等多种因素影响,其中溶液特性影响最大。通过调整参数,可制造出不同形态的纤维。静电纺丝纤维因其高比表面积、多孔结构等优点,在多个领域有广泛应用[84-85]。透明质酸、胶原蛋白等已成功通过静电纺丝技术被制成纤维。这些纤维因其良好生物相容性和仿生微结构被广泛用于组织工程领域,如表4所示。
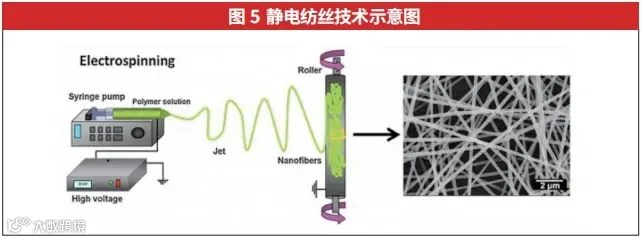

2.5 干法纺丝
干法纺丝是一种将聚合物先溶解在挥发性溶剂中,如乙醚或丙酮,然后挤出形成纤维的技术[74]。聚合物原液通过喷嘴形成射流,暴露于气体环境中。随着溶剂的蒸发,溶液浓度增加,细丝凝固成纤维。这一过程无需额外干燥步骤,纤维直接通过旋转辊收集。干法纺丝常用空气或氮气等惰性气体。溶液的制备对纺丝过程至关重要。溶液需要经过过滤,以获得适当的稠度、浓度和粘度[94]。纤维形态和性能受溶液特性和加工参数的影响。许多聚合物可以通过干法纺丝制成纤维,包括醋酸纤维素、PLLA [95]、聚氯乙烯、石墨烯、丙烯酸树脂、明胶和丝素蛋白[96]。
2.6 近场静电纺丝
近场静电纺丝(NFES)是一种从静电纺丝衍生的纤维制造技术,广泛应用于生物医学领域。与传统静电纺丝(针头与收集器间的距离通常大于50毫米)相比,近场静电纺丝利用稳定的直线射流,通过减少针头与收集器间距离(小于10毫米)来控制纤维的沉积方向[97]。近场静电纺丝设备包括高压电源、溶液供给系统以及移动收集平台。通过这些设备的协同工作,实现纤维排列和图案的精确控制[98]。NFES能生产微米级纤维,而静电纺丝偏向纳米级。NFES技术因其精确控制和高分辨率,在组织工程、传感器等领域展现出巨大潜力[99]。
3 功能性纤维在生物医学领域的应用
3.1 组织工程支架
组织工程领域是融合了生命科学和工程学原理的跨学科领域,旨在构建生物组织替代品,以恢复、维持或改善人体组织功能。支架作为组织工程的核心,为细胞提供必要的支持环境,直至形成新的细胞外基质(ECM)。理想的支架应具备良好的生物相容性、高孔隙率、适当的机械强度和可调节的生物降解性,以促进细胞行为的调控[100]。在组织工程中,材料的选择至关重要,包括天然材料(如胶原蛋白、丝素蛋白)和合成材料(如PLGA、PCL)[101]。静电纺丝技术因其能生产高孔隙率和高比表面积的纳米纤维而广受欢迎。这些纤维类似于天然ECM的原纤维,能有效促进细胞粘附和生长。此外,静电纺丝纤维的理化性质可调节,以满足不同组织的需求。文献已报道了多种用于皮肤、血管、软骨等组织的静电纺丝纤维支架[102]。除了静电纺丝,NFES和熔融NFES也被用于构建组织工程支架。它们能精确控制纤维沉积,模拟天然ECM结构。例如,通过熔融NFES制造的正交排列PCL纤维支架能诱导细胞沿纤维方向生长[103]。微挤压生物打印和微流体纺丝技术可用于制造具有细胞和生物材料时空分布的纤维结构。例如,基于GelMA、藻酸盐和聚乙二醇酯的混合生物墨水,通过多通道同轴挤出系统制造了具有人平滑肌细胞和脐静脉内皮细胞的多层管状移植物[104],用于模拟血管组织。这些技术的发展为组织工程领域带来了创新和进步。
3.2 药物递送
药物输送技术通过精确控制药物在生物体内的分布,以提升疗效和降低副作用。静电纺丝纳米纤维因其小尺寸和易吸收性广泛用于药物递送。静电纺丝技术利用高压电场将聚合物溶液或熔体转化为纤维,适用于药物的缓释递送,增强药物的溶解度和生物利用度[105]。药物分子可以通过同轴静电纺丝、共静电纺丝、多射流静电纺丝或静电纺丝等方式加载到纤维上[106]。同轴静电纺丝能够制备芯/壳结构的纳米纤维,调节药物释放速率;共静电纺丝将药物封装在聚合物溶液中,但需注意电场和溶剂对药物的影响;多射流静电纺丝能掺入多种药物,保护生物分子[107]。材料选择对药物释放至关重要,药物需通过纤维基质屏障后扩散至周围环境[108]。例如,Wei等人通过静电纺丝制备的PLGA纳米纤维支架掺入阿司匹林,实现了药物的持续释放,促进了BMSCs的增殖和成骨细胞分化[109]。Liu等人制备的阿魏酸负载麦醇溶蛋白纤维,通过调整涂层厚度来控制药物释放[110]。Dodero等人构建的含ZnO纳米颗粒的藻酸盐/PCL纳米纤维膜,展现了可控释放,促进了细胞活力和组织再生。微流体纺丝技术也因其能精确调节流体界面而广泛应用于药物递送[111],如Huang等人制造的布洛芬和BSA掺入的串珠微纤维,用于伤口愈合[112]。Ahn等人提出新方法增强超细纤维中药物包埋的特性[113]。通过静电纺丝和微流体纺丝等方法,实现了药物的有效控释和靶向递送,展现出广泛的应用潜力。
3.3 生物传感器
国际纯粹与应用化学联合会(IUPAC)将生物传感器定义为一种能提供特定分析信息的集成设备,包含生物识别元件。静电纺丝纳米纤维支架因其可控孔隙率、高表面积与体积比,被广泛用作生物传感器,增强了传感器的选择性、灵敏度和响应速度[114]。这些支架可通过静电纺丝功能聚合物或后改性纳米纤维表面敏感材料构建。例如,聚丙烯腈和聚丙烯酸等功能性聚合物可直接作为生物传感器的感应部分,而敏感材料后改性则通过物理沉积或化学交联实现[115]。电化学生物传感器由识别系统和换能器组成,静电纺丝纳米纤维支架可作为识别单元支撑。Zhang等展示了PVA/GQDs纳米纤维膜构建电化学生物传感器,用于检测H2O2和葡萄糖[116]。PVA纳米纤维膜也用于光学生物传感器,通过封装葡萄糖氧化酶实现对葡萄糖的高灵敏度检测[117]。将金属或陶瓷纳米颗粒掺入纳米纤维中,可提高表面积和灵敏度,加快电子转移。例如,通过静电纺丝制造的BCL@MOF纳米纤维,用于构建基于MOF纤维的生物传感器,对甲基检测表现出高灵敏度[118]。除了静电纺丝,其他技术如微挤出生物打印、熔融静电纺丝书写、微流体纺丝和湿法纺丝也被用于构建纤维生物传感器系统。Grigoryev等人使用湿法纺丝制造掺入单壁碳纳米管的藻酸盐纤维。这种纤维对湿度、pH值和离子强度表现出高敏感性[119]。Yu通过同轴微流体旋转构建螺旋藻酸盐微纤维,用于监测心肌细胞跳动行为,展示了基于力的生物传感器的潜力[55]。这些技术的发展为生物传感器领域提供了多样化的材料和设计,拓宽了其在医疗诊断、环境监测等多个领域的应用。
3.4 医用敷料
伤口愈合是一个复杂的过程,涉及止血、炎症、组织生长和再生四个阶段[120]。理想的伤口愈合材料需具备止血、抗菌、良好的贴合性、吸收多余伤口液体以及无痛去除等特点。纳米纤维膜因其大表面积、高孔隙率和可调节特性而备受关注[121]。纳米纤维膜的孔径通常在500纳米至1毫米之间,能够有效阻挡细菌侵入,为伤口提供保护屏障。同时,其表面积与体积比高,液体吸收能力强[122]。通过静电纺丝技术,可以将天然材料(如胶原蛋白、壳聚糖)和合成材料(如PVA、PCL、PLA、PLGA等)制成纳米纤维支架,展现出良好的愈合效果[123]。胶原蛋白因其与天然ECM结构相似而被广泛使用,但天然材料的机械强度和临床应用限制仍是亟待解决的挑战。合成材料如PLA和PLGA因其良好的生物相容性和可调节的理化性质而被开发。研究中,PLA被静电纺成掺入载有细胞因子IL-10的HA纳米颗粒的纳米纤维支架,实现细胞因子的受控释放,改善组织再生[124]。Khan等人开发的PLCL纳米纤维膜,通过同轴静电纺丝掺入ZnO纳米颗粒和精油,展现出抗菌和抗氧化活性,促进糖尿病伤口愈合[125]。Guo等人制造的ALA负载PCL纳米纤维膜,改善了伤口愈合,促进胶原蛋白分泌,阻碍疤痕形成。除了静电纺丝,微挤出生物打印技术也用于构建纤维支架,其孔径可控,细胞和生物活性成分分布精确。例如,基于GelMA和琥珀酰化壳聚糖的核/壳结构纤维支架,展现出优异的细胞活力和血管形成能力。微流体纺丝和湿纺技术也被用于制造伤口愈合纤维支架[126],如Yu等人展示的金属有机框架(MOF)封装的微纤维,通过可控释放铜和锌离子及维生素,增强受损组织修复[127]。另一项研究通过湿纺制备的藻酸盐微纤维,封装银离子并还原成银纳米颗粒,加快组织愈合速度。这些技术的发展为伤口愈合提供了多样化的材料和治疗方法。
4 结论和展望
尽管取得了显著成就,生物医用纤维材料制造技术仍面临诸多挑战。第一,材料选择方面,多限于常见天然或合成材料,如胶原蛋白、蚕丝、HA、PLA、PLGA、PCL等。这些材料虽易于加工成纤维,但其固有缺点,如天然材料的机械稳定性不足和合成材料的生物相容性问题仍需克服。第二,纤维支架的结构复杂性尚未达到自然组织或器官的水平,需要开发新型集成设备和技术,如结合静电纺丝与微流体纺丝技术,以更精确地模拟天然ECM结构,并实现细胞及生物活性成分的时空调控。第三,大多数技术限于二维支架制造,而三维支架能提供更优的仿生环境和机械支撑,促进复杂功能构建。因此,将纤维技术与纺织品制造方法结合,构建三维纤维支架,对生物医学应用具有重要意义。此外,纤维技术的临床转化同样面临挑战,转化效率缓慢。
尽管如此,这些技术有望解决未来生物医学生产中的挑战性问题。当前,技术的生产率难以满足临床研究和工业规模生产的需求,但多喷嘴静电纺丝装置的设计已显著提高生产率。例如,美普林再生医疗科技有限公司的ReDura静电纺丝支架已实现产业化,并获美国食品药品监督管理局(FDA)批准用于临床。然而,纳米/超细纤维的体内测试成本高、成功率低,未来需开发易于使用、成本效益高、对仪器要求低且符合行业标准的新型平台,以实现更准确的生物系统模拟和高度相关的体外体内研究。
参考文献见《纺织科学研究》2024年11月刊。
编辑丨董雅琪
微信公众号ID丨fzkxyj






