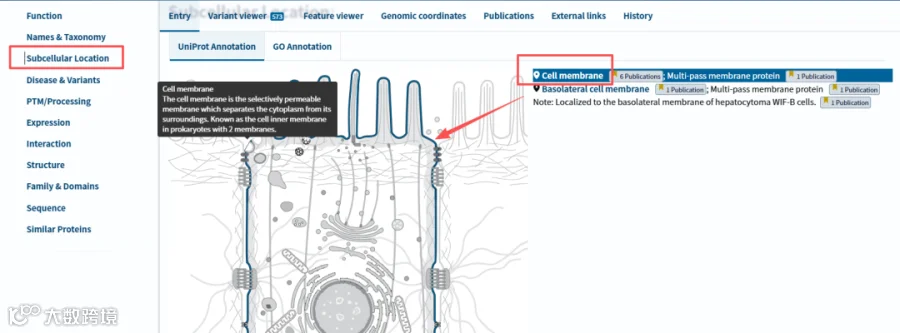
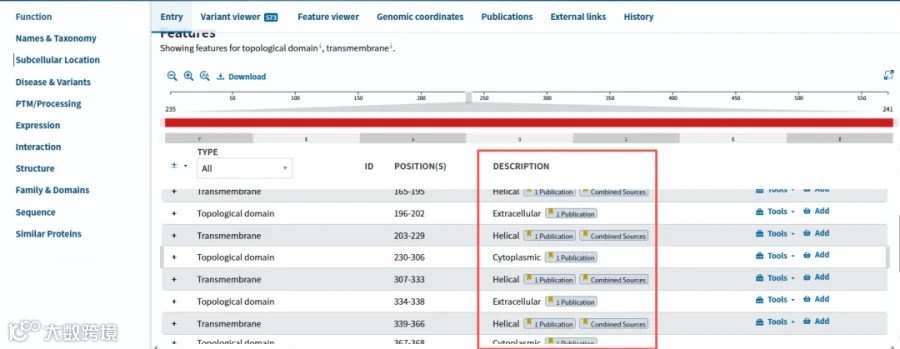
在 Western Blot(WB)检测多次跨膜蛋白时,制样避免高温煮样(如 95℃加热)的核心原因是:膜蛋白具有疏水性,高温加热后易发生聚集并形成二聚体或多聚体,甚至形成沉淀滞留在胶孔中,不能被抗体很好地识别,或导致识别后条带位置不在预期大小位置。
在一篇发表于《PLOS ONE》的Transmembrane protein western blotting: Impact of sample preparation on detection of SLC11A2 (DMT1) and SLC40A1 (ferroportin)文章中,作者聚焦于跨膜蛋白在WB检测中样品制备的关键影响因素,以铁代谢核心跨膜转运蛋白SLC40A1、SLC11A2为主要研究对象,结合单跨膜蛋白TfR1、胞质铁储存蛋白Ferritin H展开实验,证实高温煮样是跨膜蛋白 WB检测失败的核心原因。(详见原文)
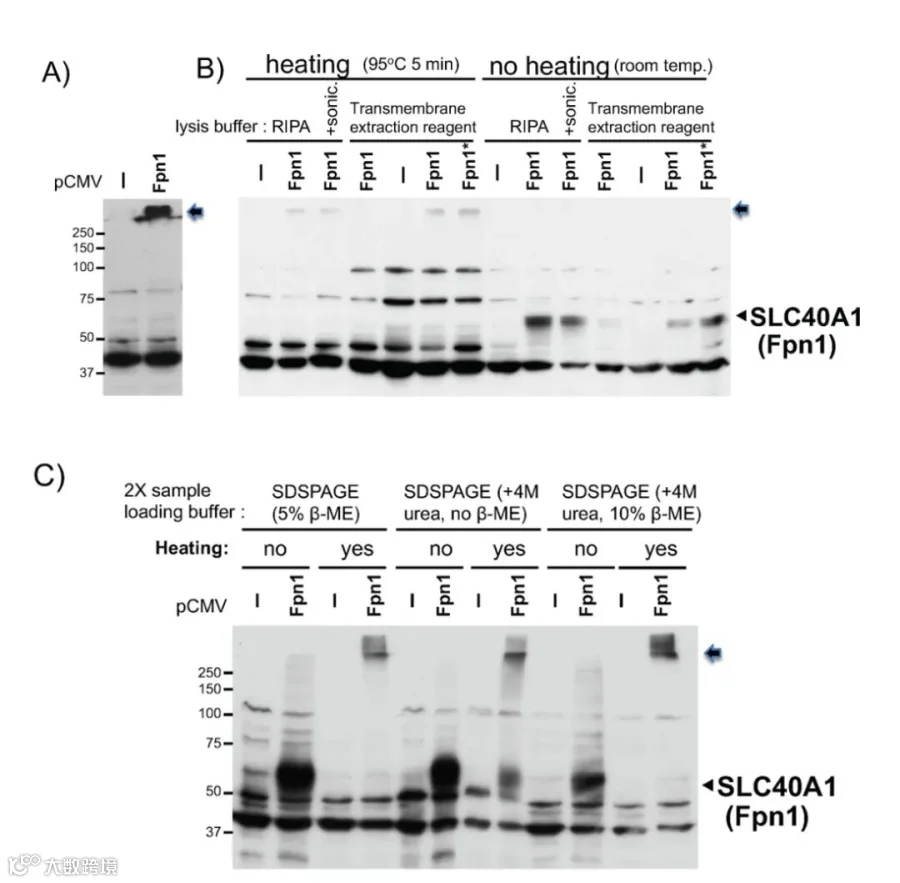
图 1 转染 Fpn1 的细胞样品加热 / 未加热处理后SLC40A1的 WB 对比。A)取 pCMV/pCMV-Fpn1 转染的 HEK293 细胞 RIPA 裂解液 25μg,与 2×SDS-PAGE 上样缓冲液混合后 95℃加热 5min 做 WB,箭头示滞留于分离胶顶部的 Fpn1 蛋白(B、C 同)。B)提取上述转染细胞的 RIPA 裂解液、RIPA + 冰浴超声裂解液、跨膜蛋白提取试剂裂解液,各取 15μg 制样后分 95℃加热 5min 和室温未加热组做 Fpn1 WB,三角箭头示转染的 Fpn1 条带。C)取上述转染细胞的 RIPA 裂解液,分别与含 5%β- 巯基乙醇、4M 尿素、5%β- 巯基乙醇 + 4M 尿素的 2×上样缓冲液混合,分加热 / 未加热组做WB,左侧标注蛋白分子量标准位。
图1结果表明转染 Fpn1的HEK293细胞样品经95℃加热5min后,Fpn1蛋白会滞留于分离胶顶部无法正常迁移;而未高温处理可检测到清晰的 Fpn1 特异性条带。更换 RIPA + 超声、跨膜蛋白专用提取试剂等裂解方式,或使用含尿素/不同β-巯基乙醇的上样缓冲液,均无法改善高温导致的 Fpn1 迁移异常,仅不使用高温处理是实现Fpn1有效检测的关键条件。
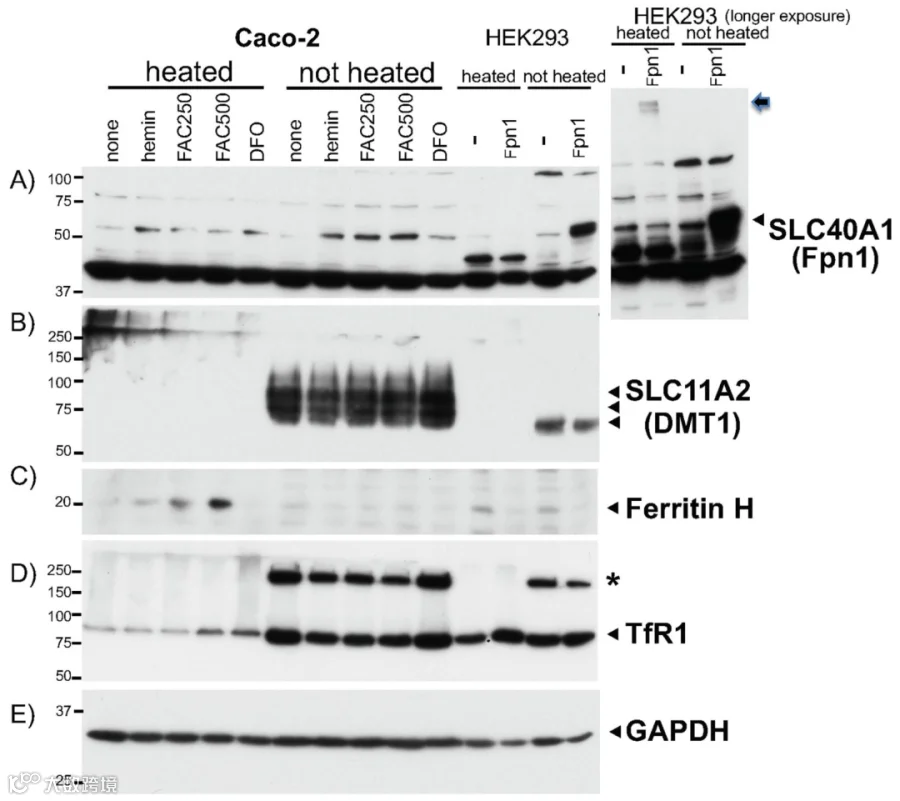
图 2 铁处理的 Caco-2 细胞在加热 / 未加热条件下Ferritin H与 TfR1 的 WB 对比。Caco-2 细胞经 50μM 血红素、250/500μM FAC、25μM DFO 处理 24h 或不处理,取 25μg 其全细胞裂解液,同时取 10μg pCMV/pCMVFpn1 转染的 HEK293 细胞裂解液,分 95℃加热 5min 和室温未加热两组,依次用抗 Fpn1、DMT1、Ferritin H、TfR1 及 GAPDH 抗体做连续 WB 检测。A)图旁附 HEK293 细胞 Fpn1 WB 放大结果,箭头示滞留于分离胶顶的转染型 Fpn1;D)中星号为仅未加热样品中出现的 TfR1 二聚体。
图2铁相关试剂处理的 Caco-2细胞及Fpn1转染的HEK293细胞样品,经加热/未加热后进行WB检测。结果表明Fpn1在未加热样品中条带更清晰,转染的Fpn1加热后滞留分离胶顶(多次跨膜);DMT1仅在未加热样品中可检测到(多次跨膜);Ferritin H则仅加热后能被有效检测(胞质);TfR1在未加热样品中条带信号更强,且能检测到仅存于未加热组的二聚体(单次跨膜)。


我们以SLC40A1为例,打开https://www.uniprot.org/官网,在搜索栏中输入SLC40A1,选择Human后网页会进行跳转。我们点击Subcellular Location选项后,能看到右边蛋白在细胞中的定位,并且下面的DESCRIPTION处能够看到其螺线结构,胞质和胞外对应的氨基酸序列。那根据这个我们就可以确定制样的方式啦。