糖尿病已成为全球范围内的慢性疾病之一,对人类健康构成了严重威胁。在中国,11.2%的成年人患有糖尿病,其中90%的患者为2型糖尿病(T2D)[1]。
近年来,随着连续血糖监控(CGM)技术的成熟,为血糖监控提供了更直接、更全面、更完整的血糖信息,其中血糖处于目标范围内的时间比例(time in range, TIR)由于定义直观、易于理解,于2019年美国糖尿病协会(ADA)指南“血糖评估”部分中被作为《国际共识》纳入,成为糖化血红蛋白(HbA1c)的有效补充指标[2]。TIR代表患者葡萄糖处于目标范围内(通常定义为3.9~10.0 mmol/L)的时间百分比,与糖尿病慢性并发症及心血管疾病死亡风险呈负相关,专家在共识中推荐维持在70%以上。
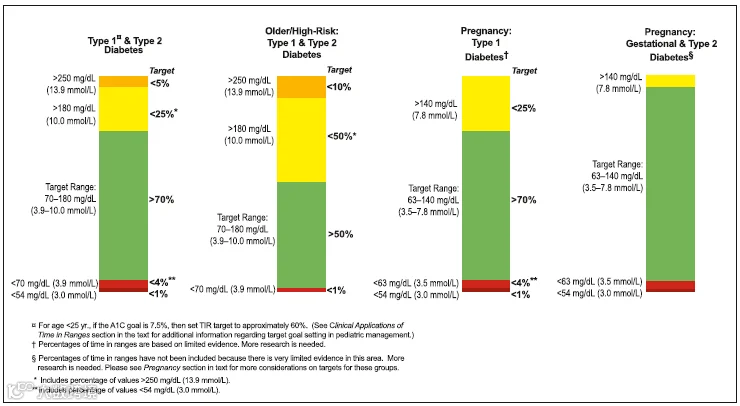
间充质干细胞移植作为一种有前景的糖尿病治疗手段,通过促进胰岛β细胞功能并减轻胰岛素抵抗来改善高血糖症状。已有临床研究证实其是一种安全有效的治疗策略,可减少T2D患者对外源性胰岛素需求并改善胰岛素抵抗情况[3]。然而,前期研究多聚焦于C肽水平、HbA1c等传统指标,对于TIR等反映患者短期血糖波动的数据仍然较少。
基于以上情况,中国解放军总医院开展了一项单中心、双盲、随机、安慰剂对照的II期临床试验,旨在评估脐带间充质干细胞对T2D患者处于TIR的影响[4]。

研究共纳入73名T2D患者,年龄在20-65岁,空腹C肽水平≥1ng/ml,HbA1c水平在7.0%至12.0%之间。患者入组前接受至少3个月胰岛素治疗,同时服用二甲双胍,病程不超过20年。治疗组患者接受脐带间充质干细胞静脉输注三次,剂量为1×106细胞/kg体重,每次输注间隔4周。在患者第一次输注前以及后续的第9周和48周对患者展开全面的评估,采集包括患者对胰岛素需求、HbA1c水平、空腹C肽水平、TIR等数据。
结果发现,接受脐带间充质干细胞输注的T2D患者表现出显著的血糖控制改善,除了经典的HbA1c指标显著改善,对外源胰岛素依赖减少以外,TIR在第9周和第48周时分别提升26.54% 和21.36%(基线58.16%),显著高于安慰剂组(15.84%和6.32%)。达到TIR≥70%且HbA1c<7%这一复合目标的患者数量显著多于对照组(9周:59.5% vs. 27.8%;48周:43.2% vs. 11.1%)。此外令人惊喜的是,脐带间充质干细胞治疗组的患者,在血糖变异系数(CV)、平均血糖波动幅度(MAGE)、血糖标准差(SD)等指标上改善更明显(P<0.05),表明其能有效稳定每日血糖波动,并且患者胰岛β细胞功能及对胰岛素敏感性均显著改善,与先前的临床研究结果一致。
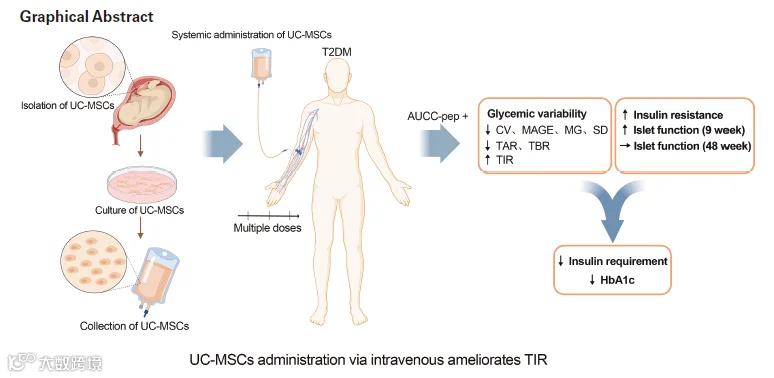
最后,研究人员还对疗效影响因素开展初步分析,发现患者C肽曲线下面积是脐带间充质干细胞疗效的独立预测因子,并且男性患者对治疗的反应可能优于女性。
以上研究成果,凸显了脐带间充质干细胞在治疗T2D中的潜力,显著提升T2D患者的TIR、降低HbA1c、改善血糖变异性及胰岛功能,且安全性良好。相信随着未来更多设计严谨的多中心、大规模临床研究的开展,间充质干细胞治疗有望为更多T2D患者带去福音。
参考原文:
[1] 中华医学会糖尿病学分会. 中国2型糖尿病防治指南(2020年版)[J]. 中华糖尿病杂志,2021,13(04):315-409.
[2] Battelino T, Danne T, Bergenstal RM, et al. Clinical Targets for Continuous Glucose Monitoring Data Interpretation: Recommendations From the International Consensus on Time in Range. Diabetes Care. 2019 Aug;42(8):1593-1603.
[3] Zang L, Li Y, Hao H, et al. Efficacy and safety of umbilical cord-derived mesenchymal stem cells in Chinese adults with type 2 diabetes: a single-center, double-blinded, randomized, placebo-controlled phase II trial. Stem Cell Res Ther. 2022;13(1):180.
[4] Zang L, Li Y, Hao H, et al. Efficacy of Umbilical Cord-Derived Mesenchymal Stem Cells in the Treatment of Type 2 Diabetes Assessed by Retrospective Continuous Glucose Monitoring. Stem Cells Transl Med. 2023 Dec 18;12(12):775-782.









