注:文中斜体下划线部分单独撰文介绍
较多化合物本身亲电性较弱,需要经适当的Lewis酸活化以强化亲电性,才能被亲核试剂顺利进攻。
1 酸催化亲核取代
对于部分亲核取代反应,若基团离去能力不佳,需额外加入Lewis酸等活化试剂增强其离去能力。较常见的如C-O键活化:醇羟基离去能力弱,加酸活化后离去能力增强,方可发生亲核取代(图1)。
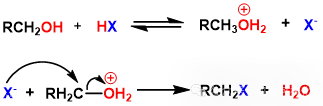
图1:H+活化羟基后发生亲核取代
原理可视为图2和图3。
图2:大兔子保护小兔子,即羟基离去能力弱,难直接发生亲核取代。
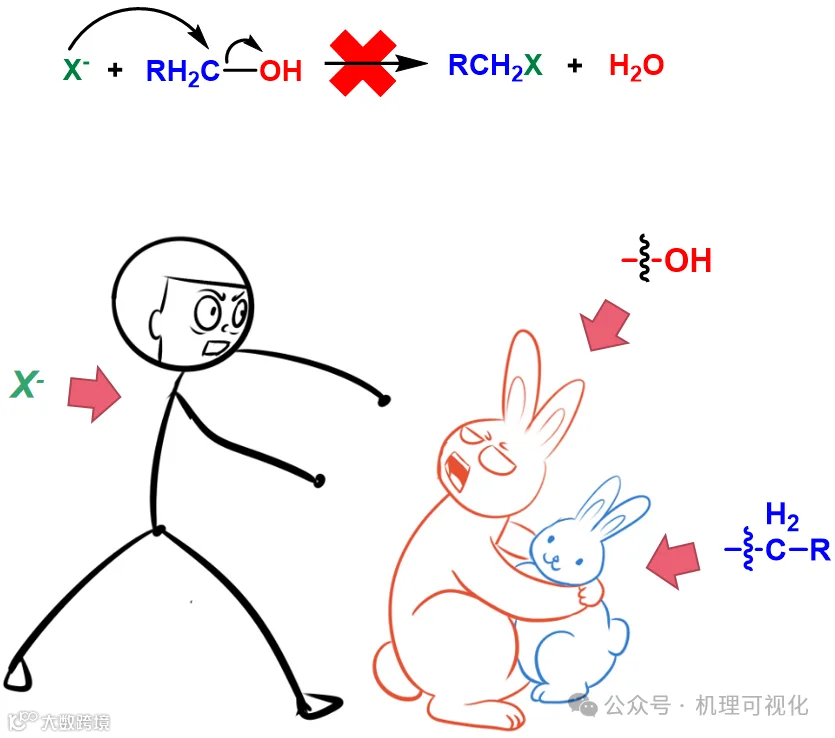
图2:大兔子保护小兔子(羟基离去能力弱,难直接发生亲核取代)
图3:“萝卜”引诱大兔子,抓住小兔子,即H+活化羟基后发生亲核取代。
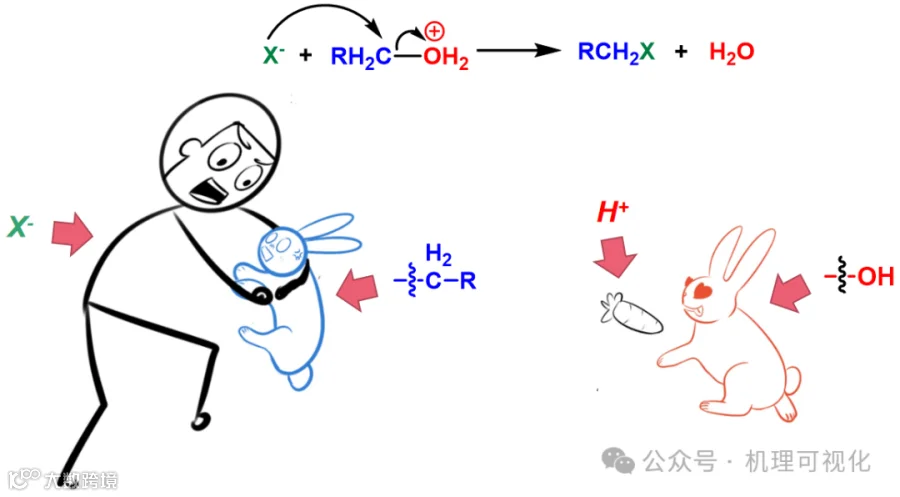
图3:引诱大兔子,抓住小兔子(H+活化羟基后发生亲核取代)
除质子酸外,PXn、SOCl2、p-Me-C6H5SO2Cl等均可作Lewis酸起到类似的活化效果;除醇C-O键外,醚、羧基C-O键均可经同样的过程活化。
2 酸催化亲核加成
部分羰基化合物(醛酮、α-β不饱和醛酮、羧酸及其衍生物)可在酸性环境下被亲核试剂进攻(图4),依据底物性质分别发生加成或加成消除反应。
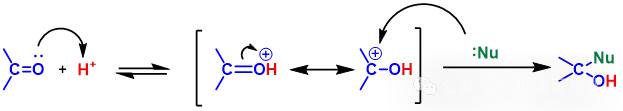
图4:H+活化羰基
在此类反应中,酸对羰基起到了亲电活化效果:被酸活化后,羰基C拥有了足够强的亲电性接收亲核试剂进攻。如图5:用萝卜引诱,进而成功捕获兔子。
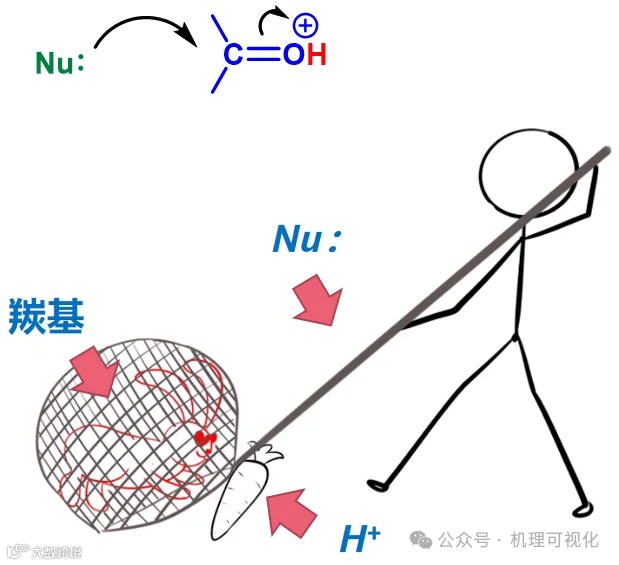
图5:“诱捕”(羰基被H+活化后顺利被进攻)
3 酸催化烯醇异构
羰基化合物可在酸性环境下发生“烯醇异构”,该过程可视为酸催化羰基亲核加成的分子内反应,亲核试剂为羰基α位C-H键电子(图6,图7),原理同图5。
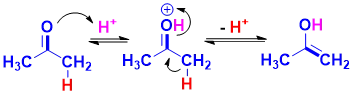
图6:烯醇异构
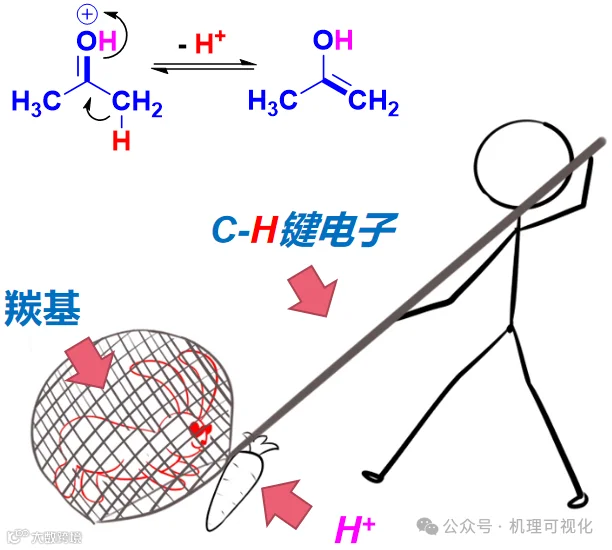
图7:“诱捕”(烯醇异构)
4 烯烃亲电加成
孤立烯烃因其富电子特性,难直接被亲核试剂进攻,但借助外界Lewis酸的活化,则可顺利发生亲电加成反应,原理同图5,见图8。
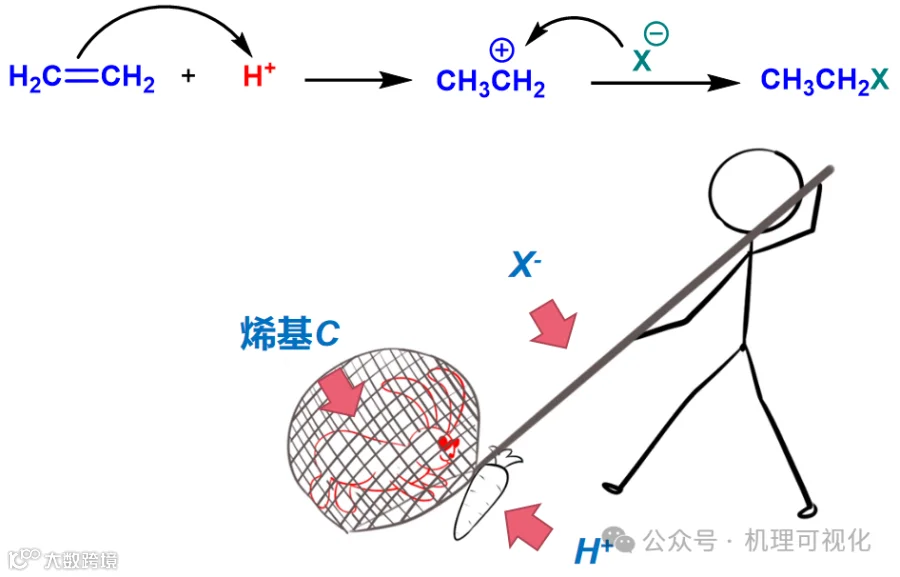
图8:“诱捕”(烯基被H+活化后顺利被进攻)
5 炔烃亲电加成
炔亲电性强于烯,理论上比烯烃更容易被亲核试剂进攻,不过对于较弱的亲核试剂如H2O,仍然需要在外界试剂的活化下发生反应,如使用Hg2+作活化试剂(图9),原理同图5,见图10。
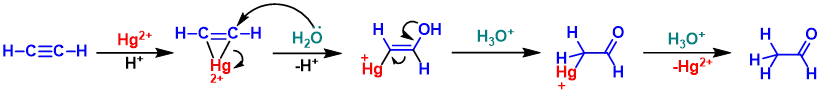
图9:Hg2+活化炔基
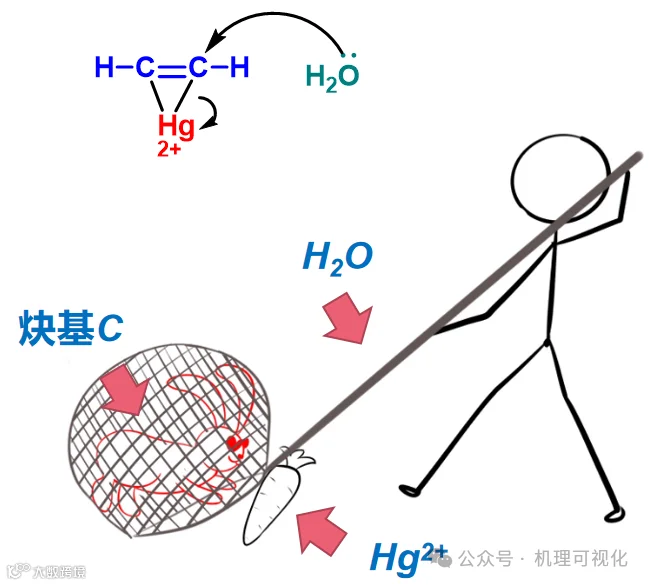
图10:“诱捕”(炔基被Hg2+活化后顺利被进攻)
6 Vilsmeier反应
在Vilsmeier反应中,三氯氧磷的作用就是为了活化酰胺羰基O并使之离去,进而有机会形成高亲电活性的Vilsmeier中间体(图11)。
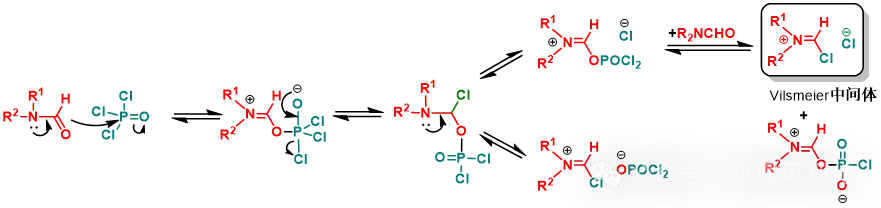
图11:三氯氧磷活化酰胺
随后,芳环对Vilsmeier中间体发生芳香亲电取代,再经水解得到产物(图12)。
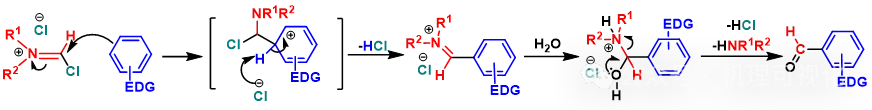
图12:芳环进攻活性Vilsmeier中间体
上述过程可理解为图13。
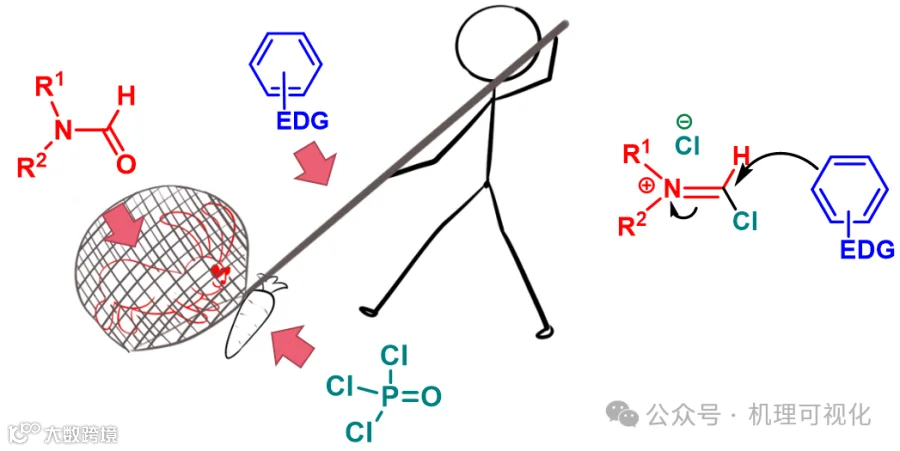
图13:“诱捕”(酰胺被三氯氧磷活化后顺利被进攻)
7 Bischler-Napieralski反应
将Vilsmeier反应引入分子内即Bischler-Napieralski反应(图14),原理同图13。
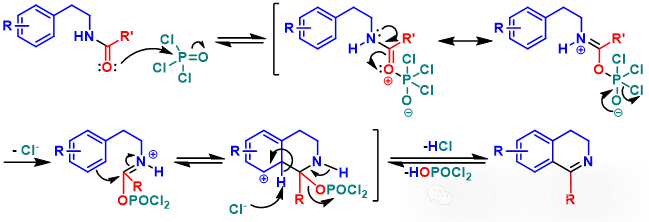
图14:Bischler-Napieralski反应
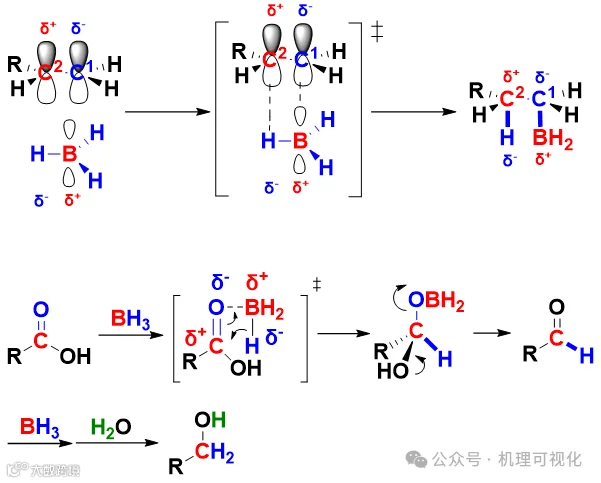
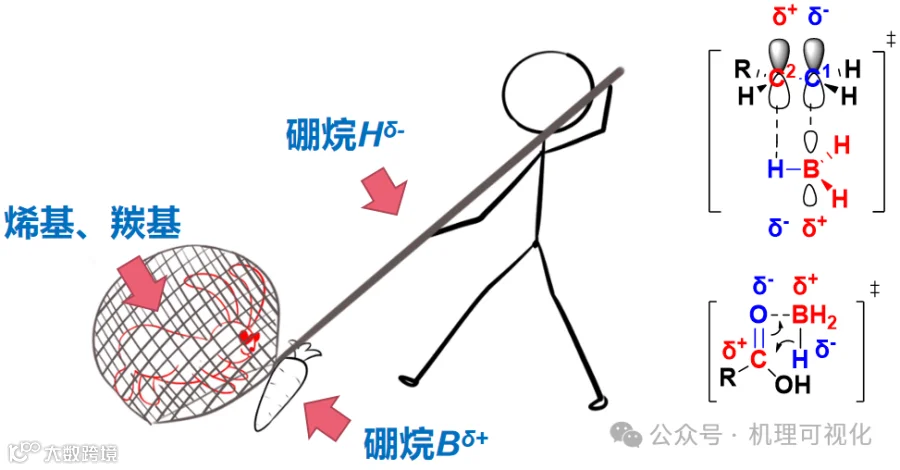
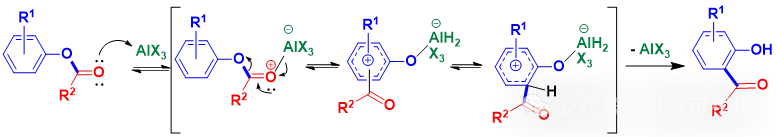
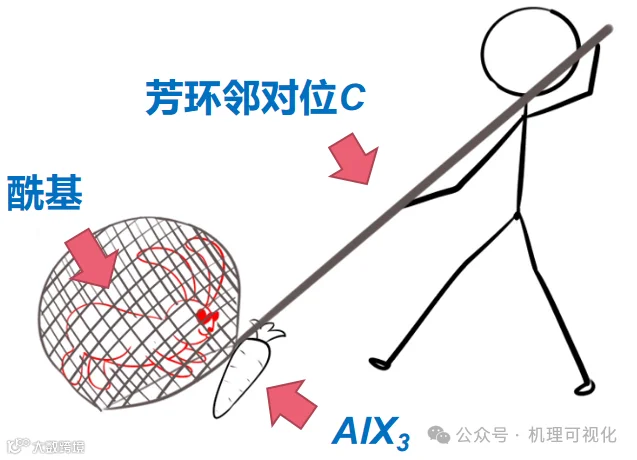
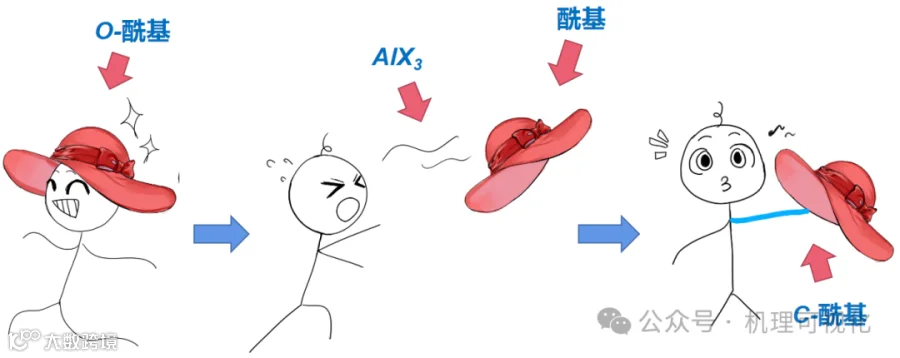
在Fries重排中,酚酯酰基受Lewis酸活化后解离,再被芳环邻对位攫取(图17)。原理可视为图18。