

《中国药典》2020年版四部通则1101规定:
无菌检查法系用于检查药典要求无菌的药品、生物制品、医疗器械、原料、辅料及其他品种是否无菌的一种方法。若供试品符合无菌检查法的规定,仅表明了供试品在该检验条件下未发现微生物污染。
无菌检查应在无菌条件下进行,试验环境必须达到无菌检查的要求,检验全过程应严格遵守无菌操作,防止微生物污染,防止污染的措施不得影响供试品中微生物的检出。单向流空气区域、工作台面及受控环境应定期按医药工业洁净室(区)悬浮粒子、浮游菌和沉降菌的测试方法的现行国家标准进行洁净度确认。隔离系统应定期按相关的要求进行验证,其内部环境的洁净度须符合无菌检查的要求。日常检验需对试验环境进行监测。
本次无菌检查风险评估对现有质量检验中心的无菌检查检验过程中的控制措施进行风险评估,以确定质量检验中心无菌检查各风险是否已经处于可接受范围,如仍存在中、高风险项目应制订合理的措施,使之降低至可接受范围。
相关法规
《药品生产质量管理规范》(2010年修订)对质量风险管理做出了以下规定:
第十三条 质量风险管理是整个产品生命周期中采用前瞻或回顾的方式,对质量风险进行评估、沟通、审核的系统过程。
第十四条 应当根据科学知识及经验对质量风险进行评估,以保证产品质量。
第十五条 质量风险管理过程所采用的方法、措施、形式及形成的文件应当存在风险级别相适应。
无菌检查概述
无菌检查流程
附图1 无菌检查流程图
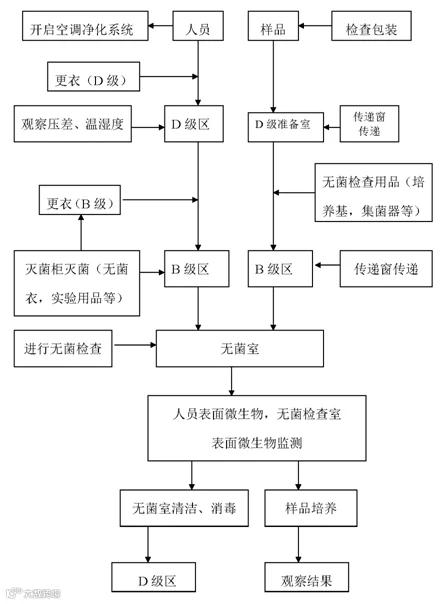
质量检验中心无菌检查样品准备设置于微生物检验实验室D级区域(D1准备室)。
质量检验中心已制定了相应的SOP明确规定样品和物料如何进入D区和B区。
· 实验准备工作
1.根据样品准备好培养基、集菌器、冲洗液等实验用品。
2.将无菌衣、手套、护目镜等放入更衣室内。
3.样品及其它实验用品由物流通道(传递窗)传入无菌检查室。样品及其它实验用品放入传递窗前,用消毒剂消毒,放入传递窗内经紫外灯和层流净化器消毒自净30分钟。
4.关闭紫外灯和层流净化器,开启无菌室的空气除菌过滤层流装置至少运行0.5小时。
5.操作人员由人流通道(更鞋室→更衣室→缓冲室)进入无菌检查室。操作人员进入更鞋室,换上拖鞋,洗手、消毒后,再进入更衣室,按《SOP-QC738人员进出实验室标准操作程序》中的更衣程序更衣,穿好无菌衣。
6.通过缓冲室进入无菌室,关上无菌室门,点燃酒精灯,着手进行实验。
7.无菌操作,均应在层流净化台上进行。
薄膜过滤法
供试管及阳性对照管:用剪刀除去样品铝塑组合盖的塑料部分,用75%乙醇棉擦拭瓶口橡胶塞外壁和瓶口缝隙,待干。打开集菌培养器包装,安装集菌培养器,将双芯针头快速过火焰不得过三次或火焰灼烧不超过三秒,然后插至0.9%氯化钠注射液(或其它规定的冲洗液)瓶塞上。开启电源,加入少量溶液润湿滤膜,关闭电源。将双芯针头快速过火焰不得过三次或火焰灼烧不超过三秒,然后插至供试品容器塞上,另一端插至冲洗液瓶塞上,开启电源,溶解样品,并将样品溶液加入集菌培养器。立即开动蠕动泵,将供试液抽干,冲洗次数及冲洗液量依供试品种类及量而异,应根据无菌检查方法适用性试验报告确定。完毕后,取下滤器顶部排气孔上的胶帽,将另一套胶帽套于集菌培养器底部的排液管口上,分别向三个培养器内加入硫乙醇酸盐流体培养基、胰酪大豆胨液体培养基和供阳性菌生长的培养基(一般为硫乙醇酸盐流体培养基)各100ml,用夹子夹紧塑胶管近端,剪断塑胶管远端,并将其插到排气孔上,取下集菌培养器,将供阳性菌生长的培养基管移入阳性菌接种室,加入相应的阳性菌液1ml(标准规定:≤100cfu/ml),作为阳性对照管,其余两管作为供试管。
阴性对照管:另取一个集菌培养器,各过滤规定量的稀释液或冲洗液,分别加入硫乙醇酸盐流体培养基和胰酪大豆胨液体培养基各100ml,作为阴性对照。若使用两个或两个以上批次的稀释液或冲洗液,则每个批次的稀释液或冲洗液均应进行阴性对照。如是生物制品,硫乙醇酸盐流体培养基的阴性对照管应有两份。
直接接种法
用剪刀除去样品铝塑盖的塑料部分,用75%乙醇棉擦拭瓶口橡胶塞外壁和瓶口缝隙及供试品溶剂,打开供试品溶剂。用灭菌的注射器吸取溶剂加入供试品容器以溶解供试品。用注射器吸取上述已完全溶解的供试品溶液,在酒精灯近火焰上方以右手握拳,小指为主拔开培养基管的塞子,管口通过火焰,移至火焰下侧沿着培养基管壁分别接种于硫乙醇酸盐流体培养基,胰酪大豆胨液体培养基及供阳性菌生长的培养基(一般为硫乙醇酸盐流体培养基),并轻轻摇匀。将供阳性菌生长的培养基管移入阳性菌接种室,加入相应的阳性菌液1ml(标准规定:≤100cfu/ml),作为阳性对照管,其余两管作为供试管。同时取相应溶剂分别做阴性对照。
结束工作
1.若两人同时操作,必须两人实验全部完成后方可一起清场。在实验过程中,无菌检查室的门严禁长时间处于打开状态。
2.将接种完毕的培养基由物流通道(传递窗)移出无菌室至培养室,于适宜温度的生化培养箱内培养。其中硫乙醇酸盐流体培养基管于30~35℃培养,胰酪大豆胨液体培养基管于20~25℃培养。如是生物制品,硫乙醇酸盐流体培养基管应有两份,一份于30~35℃培养,一份于20~25℃培养。
3.将实验用的一切物品由物流通道(传递窗)移出无菌室,洗净,烘干,备用。
4.操作人员实验结束后由人流通道(缓冲室→更衣室→更鞋室)退出无菌检查室。试验结束后,用消毒剂擦拭层流净化台,凳子,关闭空气除菌过滤层流装置,关闭无菌室、缓冲间的门,关上所有电源。
培养及观察
上述含培养基的供试管及阴性对照管按规定的温度培养不少于14天,阳性对照管培养不超过5天,应生长良好。培养期间应定期观察并记录是否有菌生长。如在加入供试品后、或在培养过程中,培养基出现浑浊,培养14天后,不能从外观上判断有无微生物生长,可取该培养液不少于1ml转种至同种新鲜培养基中,将原始培养物和新接种的培养基继续培养不少于4天,观察接种的同种新鲜培养基是否再出现浑浊;或取培养液涂片,染色,镜检,判断是否有菌。
结果判断
阳性对照管应生长良好,阴性对照管不得有菌生长。否则,试验无效。
若供试品管均澄清,或虽显浑浊但经确证无菌生长,判供试品符合规定;若供试品管中任何一管显浑浊并确证有菌生长,判供试品不符合规定,除非能充分证明试验结果无效,即生长的微生物非供试品所含。当符合下列至少一个条件时,方可判试验结果无效:
1.无菌检查试验所用的设备及环境的微生物监控结果不符合无菌检查法的要求;
2.回顾无菌试验过程,发现有可能引起微生物污染的因素;
3.供试品管中生长的微生物经鉴定后,确证是因无菌试验中所使用的物品和(或)无菌操作技术不当引起的。
4.在阴性对照中观察到微生物生长。
试验若经确认无效,应重试。重试时,重新取同量供试品,依法重试,若无菌生长,判供试品符合规定;若有菌生长,判供试品不符合规定。
根据《SMP-QA170 质量风险管理程序》所举失效模式与影响分析方法对无菌检查进行评估,并根据风险优先级,制订相应的控制措施。
失效模式与风险分析将风险的严重程度、风险发生的频率和风险的可检测性分别分为5个等级具体如下:
A. 严重程度(S)
严重程度根据对工艺参数和产品质量,法规符合性,质量数据的可靠性以及设备/系统功能的影响,设备或系统的失败可能只适用于上述4个方面中1个方面或多个方面,以影响最大的计算严重性等级。可分等级如下: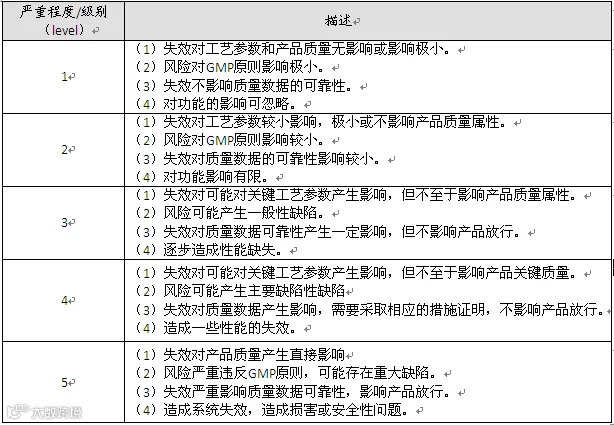
B.发生率(O)
测定风险产生的可能性。根据积累的经验、工艺/操作复杂性或其他来源数据,可获得可能性的数值。为建立统一基线,建立以下等级:
C. 可发现性(D)
在潜在风险造成危害前,判断发现的可能性,分级如下: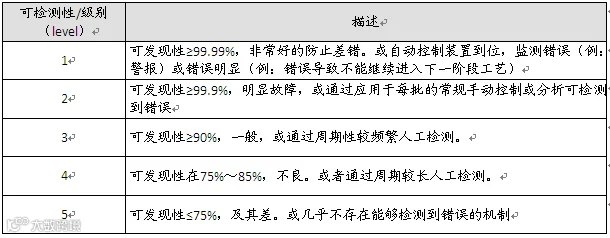
RPN优先值判定:(RPN=S×O×D)
A.高风险水平:RPN>27或严重程度= 5
此为不可接受风险。必须尽快采用控制措施,通过提高可检测性及/或降低风险产生的可能性来降低最终风险水平。措施和验证应首先集中于确认已采用控制措施且持续执行。
B.中等风险水平:27≥RPN≥15
此风险要求采用控制措施,通过提高可检测性及/或降低风险产生的可能性 来降低最终风险水平。所采用的措施可以是规程或技术措施,但均应经过验证。
C.低风险水平:RPN<15
此风险水平为可接受,无需采用额外的控制措施。
风险评估以质量检验中心起草各环节风险评估表,对相关风险进行初评,初评结束后再由专家进行审核,最终确定风险评估表见下表(表1 无菌检查风险评估表)
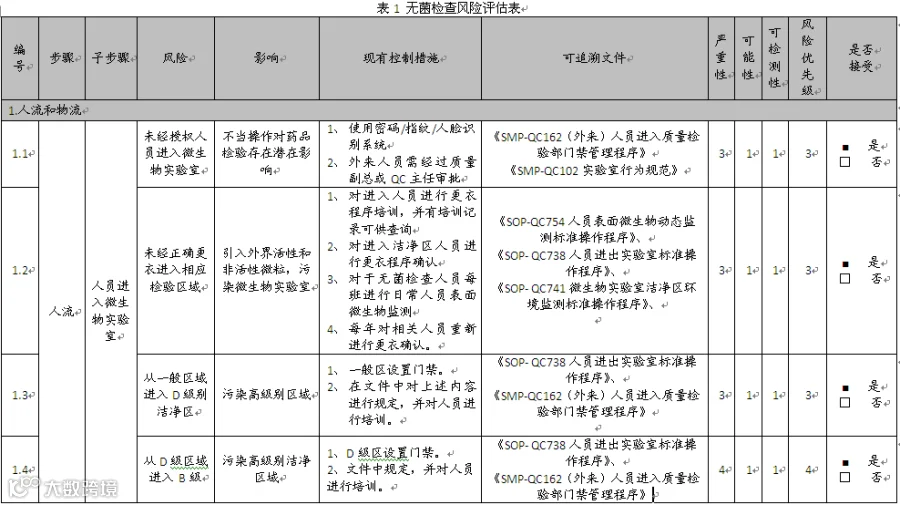
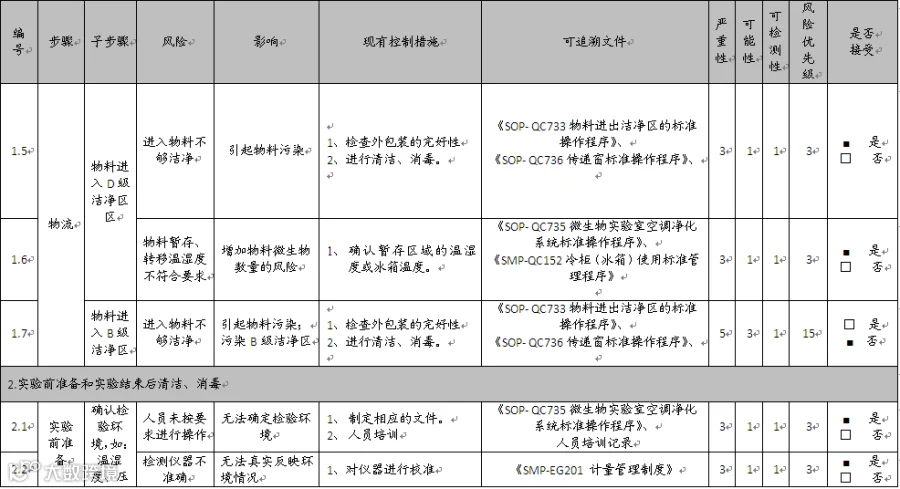
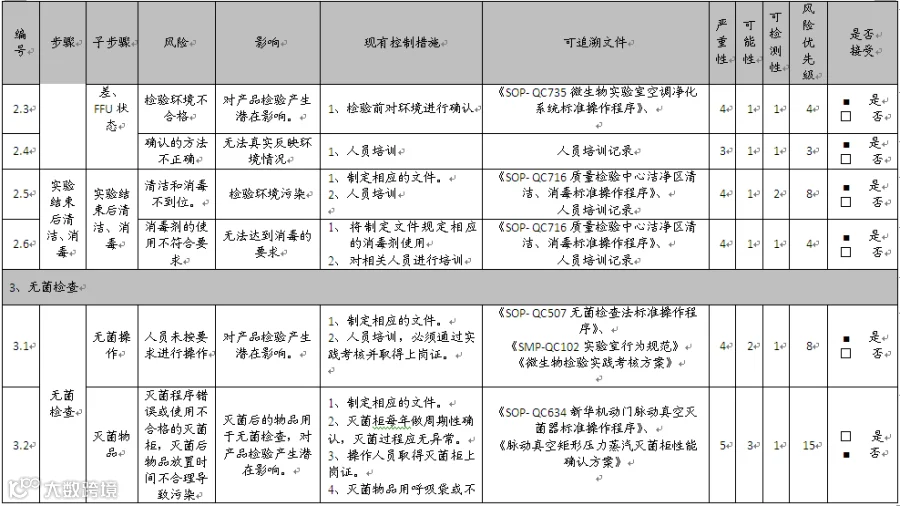
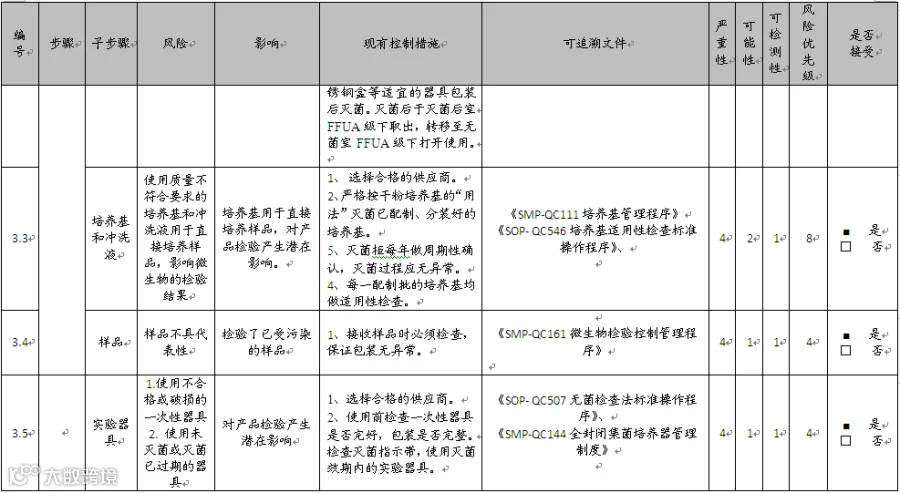
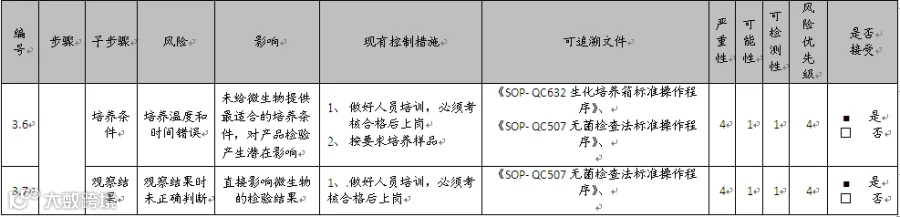
现对无菌检查的各个环节进行风险识别、风险分析、风险评估,细化风险,最终评定得出风险为40项,其中38项风险的优先级为“低”,2项风险的优先级为“高”,表明需要采取额外的措施。
根据“3.2”风险评估结果对无菌检查的关键步骤进行风险评估,并确定相应的风险优先级,根据风险优先级制订相应的措施,并对措施制定所能达到的预期效果进行风险评估,确定制订措施是否可接受。如严重程度为5时,导致的高风险水平,必须将其降低至RPN=5。
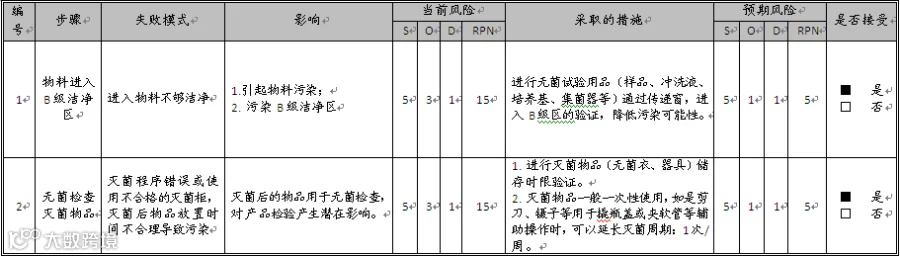
通过以上评估,识别出无菌检查的风险点,并通过制定相应的控制措施,本报告所评出的风险已得到有效控制。在今后的样品无菌检查、无菌检查的操作规程制定应遵照本报告的结果。
本评估报告批准后,还应根据后续验证的执行情况更新完成附件1:措施追溯矩阵,确保后续的确认措施均能够完成。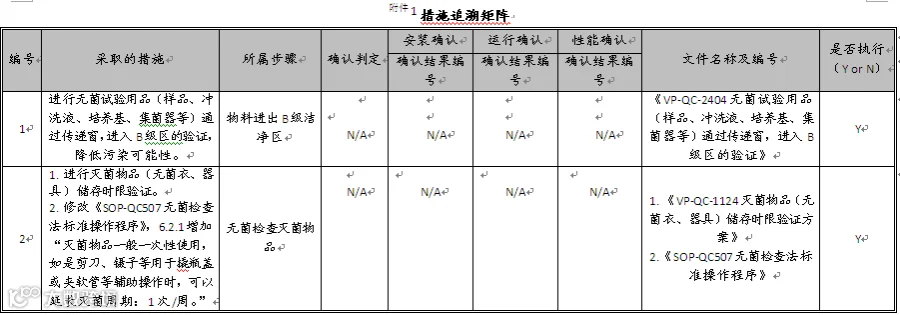

企业介绍
杭州澳亚生物技术股份有限公司(“澳亚生物”)是一家集产、学、研为一体,以无菌冻干粉针剂为主导产品的现代化制药企业。自1993成立以来,遵循“以人为本、质量为先”的可持续发展战略,澳亚生物已经逐渐从小型、简单的冻干生产,走向复杂、规模化的无菌生产模式,为客户提供全方位的无菌生产解决方案。








