eCTD由CTD发展而来。CTD(Common Technical Document)是国际公认的文件编写格式,用来制作一个向药品注册机构递交的结构完善的注册申请文件,是由ICH为了解决人用药在申请注册中格式和内容的统一,而决定采用的统一的注册申请文件格式。并在CTD的基础上加入了可扩展标记语言(XML)技术,将符合通用技术文档(CTD)规范的药品申报资料以电子化形式进行创建、审查、传输和归档,实现药品全生命周期的管理。
药品注册申报时申报企业按照规范编制结构化的药品电子申报资料,监管机构以电子化形式受理和审评,实现申报资料由递交到审评的规范化、标准化、信息化和电子化。

ICH范围内的所有国家和地区;
适用于化学药、生物药、植物药,原创药、仿制药等的所有人用药品;
适用于从申报临床研究开始至申报上市、上市后各种报告,包括进口上市在内的药品生命周期全程监控。

2000年在ICH核心成员中试行CTD初版金额相关技术指导原则;
2004年ICH发布第三版CTD,成为ICH成员国的现行通用规范;
2004年FDA公布CTD大纲;
2008年1月FDA开始要求人用药上市申报注册文件使用eCTD文件格式;
2009年6月EMA开始要求人用药上市申报注册文件必须使用eCTD文件格式;
2017年5月起FDA只接收eCTD提交的产品上市申报;
2018年5月起FDA只接收eCTD提交的DMF申报;
2018年10月FDA向ICH提议,对于ICH技术标准进行研发生产,并以eCTD格式制作申报文件,可以进行电子传送的仿制药产品,在ICH成员范围内开放市场。
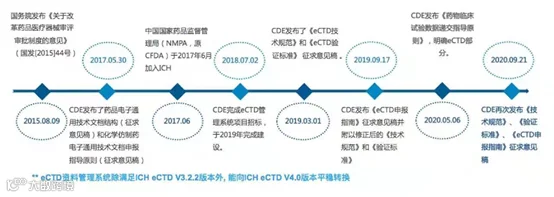
中国国家药品监督管理局(NMPA)于2017年6月加入ICH,2018年7月完成 eCTD 后台管理系统(验证,审阅,文档管理)招标,并于 2019 年相继发布了技术规范、验证标准和申报指南等规范。(短期内不大可能全面推开eCTD,但CDE已经开始着手准备了)

监管机构在评审时候遇到的痛点,包括以下几个方面:提交数量日渐增多;数据质量缺乏规范;统计和监测困难;数据量巨大;数据安全性和透明度要求增加。
(1)初级阶段:纸张形式
采用快递形式,运送大量的纸质文件;
将文件转换成PDF文件形式。
(2)中级阶段:光盘形式
在PDF文件中加入内装附件、书签和超链接;
加入外接附件、书签和超链接;
录制在光盘(CD/DVD)上进行传输。
(3)高级阶段:eCTD形式
将有超链接的文件汇编成XML架构系统;
通过保险连网传输给审批机构;
药企与审批机构实行CTD文件的双向电子传输。

(1)有利于全球研发申报
促进药品国内外同步申报,便于申报资料的重复利用,加快药品全球同步上市。
(2)提高药品申报成功率
依据eCTD技术规范和申报指南,通过eCTD申报软件,加快申报资料准备,有助自查和修改,及时更新法规变化,提高申报成功率。
(3)加速审评,缩短上市时间
电子化审评方式,大幅度提高审评效率,缩短审评周期,缩短药品上市时间。
(4)申报全生命周期管理
通过对申报资料全生命周期管理,实现对提交文档的历史追踪和版本管理,避免错报重报,便于现场检查和核查。

eCTD 是以XML为基础,规范和展示CTD文件的名称和架构。
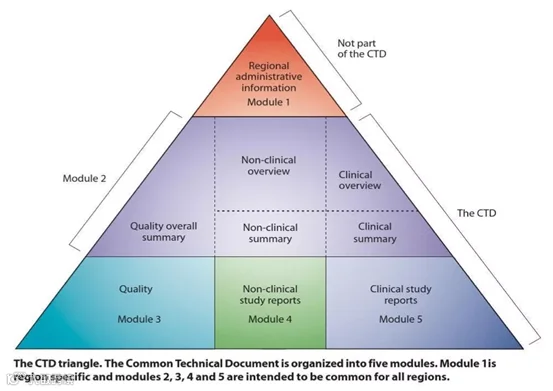
模块1 行政信息和法规信息:包括对各地区特殊的文件,例如申请表或在各地区被建议使用的标签,其内容和格式可以由每个地区的相关注册机构来指定。
模块2 CTD文件概述:
2.1CTD总目录;
2.2申请药品的一般介绍(药理作用、临床适应症);
2.3-2.7质量概要、临床前综述、临床综述、临床前研究列表总结和表格概要、临床研究概述。
模块3 质量部分:文件提供药物在化学、制剂和生物学方面的内容。
模块4 非临床研究报告:文件提供原料药和制剂在毒理学和药理学试验方面的内容。
模块5 临床研究报告:文件提供制剂在临床试验方面的内容。
(1)电子通用技术文档(eCTD)模型结构
eCTD新药申请首次提交的全套申报资料输出文件夹的结构示例(文件结构每个模块没有目录文件,取代的是index.xml主干文件),包括模块一至模块五的内容文件,2个骨架文件(XML文件),1个存放DTD相关文件的util文件及1个存放MD5值的文本文件。

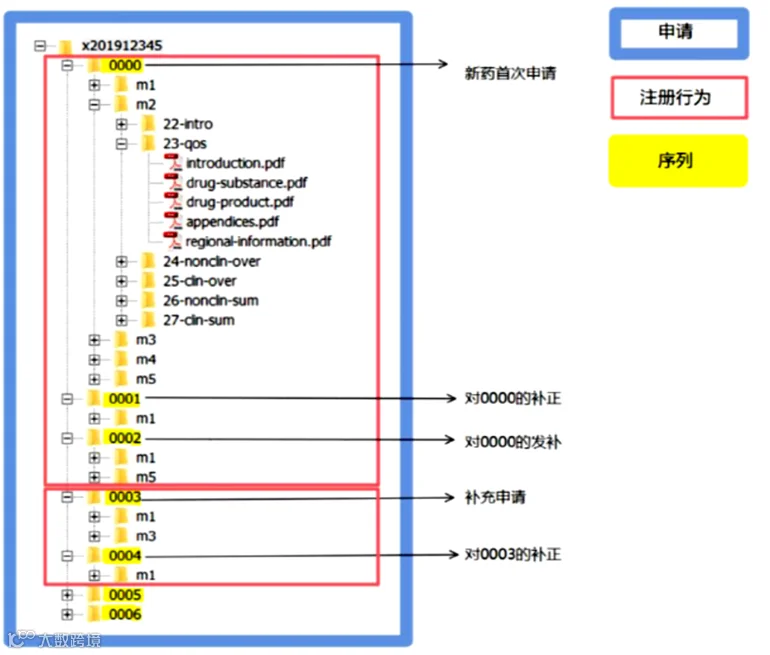
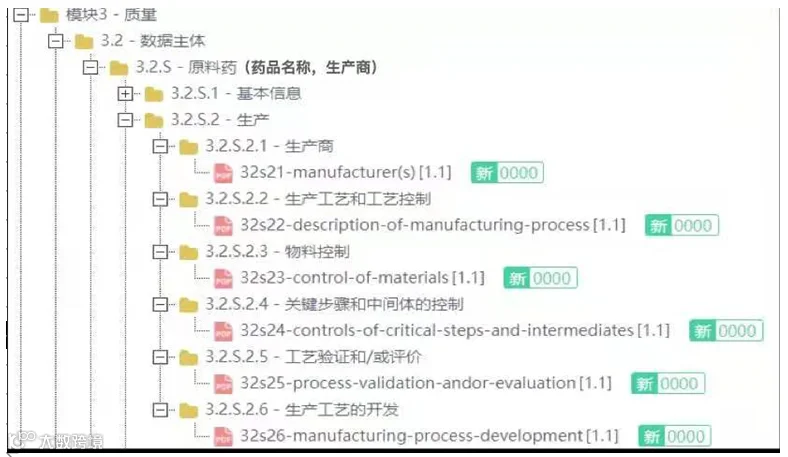

(2)eCTD申报资料结构
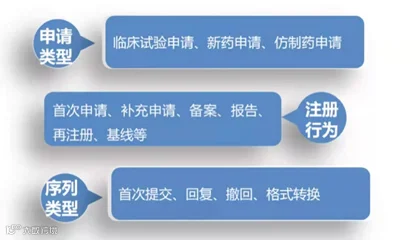
eCTD 申报资料由申请、注册行为和序列三个层级来定义。每个层级都包含一系列相关信息,即申请信息、注册行为信息和序列信息。
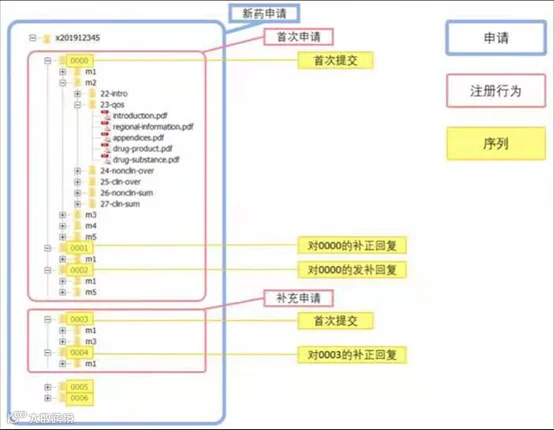
示例

1. Once eCTD, always eCTD;
2. 序列号应从0000开始,每次提交时须加1,并按先后次序提交,不得跳号提交;
3. 文件夹不允许存在空文件夹;不允许存在占位文档;
4. 不得对提交的申报资料中的文件进行任何压缩、加密处理;
5. 文件及文件夹命名允许使用字符要求、路径要求、字体大小、间距及颜色要求;
6.PDF标准:超过5页,需提供目录
(TOC/LOT/LOF/LOA)和书签;
7. PDF文件内容可复制、可检索要求;OCR
8. 建立书签和适当的超文本链接;
9. 应对提交的eCTD申报资料进行电子签章1.0说明函;1.2申请表;1.13申报资料真实性说明;
10. 3.2.R章节增加扩展节点:区域性药学信息模块4中4.2.X章节和模块5中5.3.1.x-5.3.5.x章节的文件应使用STF;
11. 建议提交基线;基线类型的注册行为对书签和超文本链接不做要求;
12. 外文资料要求:引入了“xml:lang”属性—语言属性设置为中文,对应的文件被识别为中文申报资料;外文参考资料将不受某些eCTD验证标准的约束;
13. 技术验证:错误:拒收;警告:说明函中解释;验证出版后,不能更改文件,否则Checksum会更改,被拒收;
14. 提交:CD-R/DVD+R/DVD-R,不得使用双面DVD;光盘封面;档案袋封面。



杭州澳亚生物技术股份有限公司(“澳亚生物”)是一家集产、学、研为一体,以无菌冻干粉针剂为主导产品的现代化制药企业。自1993成立以来,遵循“以人为本、质量为先”的可持续发展战略,澳亚生物已经逐渐从小型、简单的冻干生产,走向复杂、规模化的无菌生产模式,为客户提供全方位的无菌生产解决方案。


点击此处“转发”分享精彩内容




