

概述
无菌生产工艺是制药领域难度最大的工艺之一。由于许多药品无法实现最终灭菌,在配制、灌装、冻干、轧盖等暴露作业时就必须尽可能避免被微生物污染。
而影响产品是否无菌的因素相当多,诸如生产车间的设计及其设备布局、生产区的环境状况、所有与生产相关的设备及物料的污染状况、人员操作、行为规范和卫生状况等等,每一个环节对产品的无菌性都具有举足轻重的影响。为了确保无菌生产工艺系统无菌的可靠性和适应性,需通过培养基模拟灌装试验方法来对其进行验证。

无菌工艺模拟试验(培养基模拟灌装)即指用无菌培养基代替实际产品灌装来验证无菌生产线(区域)的无菌生产过程的验证方法。

《药品生产质量管理规范·无菌药品(2010年修订)》
第四十七条 无菌生产工艺的验证应当包括培养基模拟灌装试验。
应当根据产品的剂型、培养基的选择性、澄清度、浓度和灭菌的适用性选择培养基。应当尽可能模拟常规的无菌生产工艺,包括所有对无菌结果有影响的关键操作,及生产中可能出现的各种干预和最差条件。
培养基模拟灌装试验的首次验证,每班次应当连续进行3 次合格试验。空气净化系统、设备、生产工艺及人员重大变更后,应当重复进行培养基模拟灌装试验。培养基模拟灌装试验通常应当按照生产工艺每班次半年进行1 次,每次至少一批。
培养基灌装容器的数量应当足以保证评价的有效性。批量较小的产品,培养基灌装的数量应当至少等于产品的批量。
培养基模拟灌装试验的目标是零污染,应当遵循以下要求:
(一)灌装数量少于5000 支时,不得检出污染品。
(二)灌装数量在5000 至10000 支时:
1.有1支污染,需调查,可考虑重复试验;
2.有2支污染,需调查后,进行再验证。
(三)灌装数量超过10000支时:
1.有1支污染,需调查;
2.有2支污染,需调查后,进行再验证。
(四)发生任何微生物污染时,均应当进行调查。
胰酪大豆胨液体培养基(TSB)是一种广谱性培养基,特别对无菌工艺环境中源自人体的细菌、芽孢和真菌有良好的促生长效果,是无菌工艺模拟试验常用的培养基。
如果产品需充入惰性气体、储存在无氧条件,无菌操作在严格的厌氧环境中进行时(即氧气浓度低于0.1%)。应评估是否采用厌氧培养基,如硫乙醇酸盐液体培养基(FTM)或其他适宜的培养基。在厌氧的无菌工艺环境监控中反复发现厌氧微生物或在产品无菌检查中发现厌氧微生物时,需评估增加厌氧培养基。
用于模拟抑菌性产品的培养基,如有必要需评估抑菌性产品残存对其促生长能力及模拟试验结果的影响。
对于包含动物来源成分的培养基,应考虑培养基引入外源性病毒污染的风险,如BSE(可传染性海绵脑病)/TSE(疯牛病)的风险,亦可选用植物来源的培养基。
在灌装培养基期间应模拟所有类型和规定数量的干预。模拟试验应包含生产的初始、结束阶段和干预发生的时刻。大规模生产时,模拟试验的持续时间和实际生产相当,培养基灌装数量少于实际批量,因此模拟试验方法可采用但不限于以下几种方式:
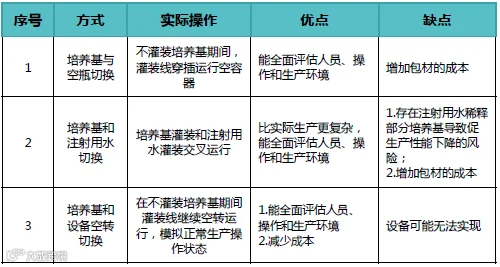
最差条件并不是指人为创造的超出允许范围的生产状况和环境。为了确认无菌工艺风险控制的有效性,应通过风险评估并结合无菌生产工艺、设备装备水平、人员数量和干预等因素来设计模拟试验最差条件。包括但不限于以下方面:
(1)人员
应充分考虑人员及其活动对无菌生产工艺带来的风险。如模拟生产过程的最多人数。参与人员应包括日常参与到无菌生产的全部人员,如生产操作、取样、环境监测和设备设施维护人员,同时应考虑以上人员交叉作业、班次轮换、更衣、夜班疲劳状态等因素。
(2)时限
在条件允许的情况下,适当考虑模拟实际生产操作过程中房间、设备、物料消毒或灭菌后放置的最长时间及最长的工艺保留时限等,如设备设施、分装容器、无菌器具灭菌后最长的放置时间等。
(3)灌装速度
模拟试验应涵盖产品实际灌装速度范围,基于无菌风险的角度分析评价灌装速度对工艺过程及其他方面的影响程度。例如采用最慢的灌装速度、最大的容器用以模拟最长暴露时间;或采用最快的灌装速度、最小的容器时,用以模拟最大操作强度/难度。
(4)环境
无菌工艺模拟试验期间环境的消毒处理应依据正常生产期间的消毒方法进行,避免过度消毒及消毒剂的过度使用。
在培养前,一般应对模拟灌装产品进行颠倒、轻摇以使培养基接触所有内表面,或倒置培养,培养时间至少14天,可选择两个温度进行培养:在20℃~25℃培养至少7天,然后在30℃~35℃培养至少7天。如选择其他培养计划,应有试验数据支持所选培养条件的适用性。在整个培养期间应连续监控培养温度。
(1)培养结束后,应对所有模拟灌装产品逐支进行无菌性检查,通常应在合适的照度下进行目视观察。
(2)在培养期间,应定期观察培养基的培养情况,如在培养期间发现异常情况时应做进一步调查。
(3)如在培养后检查中发现密封缺陷的灌装产品,应进行适当的原因调查并采取纠正措施。
(4)当灌装不透明的容器,应考虑将转移至透明容器观察的可能性,以确保阳性容器的发现。
(1)应考虑在无菌工艺模拟试验开始前及14天培养后按照现行中国药典方法对培养基进行促生长试验。
(2)根据所选择的培养基,按照中国药典要求进行促生长能力试验使用的菌种包括:白色念珠菌(CMCC98001)、黑曲霉(CMCC98003)、枯草芽孢杆菌(CMCC63501)、金黄色葡萄球菌(CMCC26003)、铜绿假单胞菌(CMCC10104)和生孢梭菌(CMCC64941)(必要时)等。除标准菌株之外,还可考虑加入环境监测和无菌检查中发现的典型微生物。促生长试验接种量应小于100CFU,按照中国药典要求培养,以证明培养基能够支持微生物的生长。
成功的无菌工艺模拟试验是允许正式生产的必要条件,但应注意其局限性。
(1)以现行药品GMP法规要求为准则,评价无菌生产过程的法规符合性,低于规范要求的无菌工艺过程,不能通过模拟试验来证实其无菌控制的合理性。
(2)虽然可通过培养基模拟灌装试验来评估无菌生产工艺的可靠性。但当产品无菌检查出现阳性时,不能以模拟灌装试验结果,排除生产过程所带来的污染可能性。


参考法规与指南:
⑴《药品生产质量管理规范·无菌药品(2010年修订)》
⑵《中华人民共和国药典》(2020版)
⑶《无菌工艺模拟试验指南》
⑷《药品GMP指南·无菌药品》
⑸《PDA technical Report No.22 ·Process Simulation for Aseptically Filled Products》(Revised 2011)

杭州澳亚生物技术股份有限公司(“澳亚生物”)是一家集产、学、研为一体,以无菌冻干粉针剂为主导产品的现代化制药企业。自1993成立以来,遵循“以人为本、质量为先”的可持续发展战略,澳亚生物已经逐渐从小型、简单的冻干生产,走向复杂、规模化的无菌生产模式,为客户提供全方位的无菌生产解决方案。


点击此处“转发”分享精彩内容




