
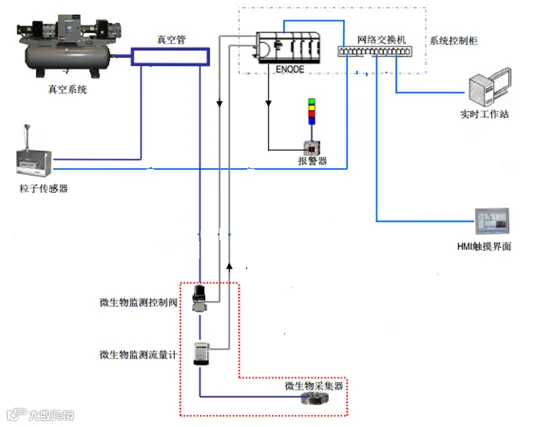
无菌制药生产过程需要进行环境监测,在关键生产环境通常会安装在线环境监测系统。在线监测系统(In process monitoring)能够及时发现所有人为干预、偶发事件及系统的损坏。由于在线监测系统可以做到不间断采样,因此系统不会漏掉任何单个的污染事件。通过将尘埃粒子传感器安装在靠近采样点的位置,可以减少采样管道中粒子的损失。在线实时监测软件可以追踪粒子事件发生的日志、地点及粒子的数据等诸多信息。
《药品生产质量管理规定(2010年版)》附录1 无菌药品
第十条 应当按以下要求对洁净区的悬浮粒子进行动态监测:
(一)根据洁净度级别和空气净化系统确认的结果及风险评估,确定取样点的位置并进行日常动态监控。
(二)在关键操作的全过程中,包括设备组装操作,应当对A级洁净区进行悬浮粒子监测。生产过程中的污染(如活生物、放射危害)可能损坏尘埃粒子计数器时,应当在设备调试操作和模拟操作期间进行测试。A级洁净区监测的频率及取样量,应能及时发现所有人为干预、偶发事件及任何系统的损坏。灌装或分装时,由于产品本身产生粒子或液滴,允许灌装点≥5.0μm的悬浮粒子出现不符合标准的情况。
(三)在B级洁净区可采用与A级洁净区相似的监测系统。可根据B级洁净区对相邻A级洁净区的影响程度,调整采样频率和采样量。
(四)悬浮粒子的监测系统应当考虑采样管的长度和弯管的半径对测试结果的影响。
(五)日常监测的采样量可与洁净度级别和空气净化系统确认时的空气采样量不同。
(六)在A级洁净区和B级洁净区,连续或有规律地出现少量≥5.0µm的悬浮粒子时,应当进行调查。
(七)生产操作全部结束、操作人员撤出生产现场并经15~20分钟(指导值)自净后,洁净区的悬浮粒子应当达到表中的“静态”标准。
(八)应当按照质量风险管理的原则对C级洁净区和D级洁净区(必要时)进行动态监测。监控要求以及警戒限度和纠偏限度可根据操作的性质确定,但自净时间应当达到规定要求。
(九)应当根据产品及操作的性质制定温度、相对湿度等参数,这些参数不应对规定的洁净度造成不良影响。
在线动态监测的目的是为了全过程的监督整个生产过程中环境发生的任何变动,干扰或者恶化,以便于我们能够对这批药品的生产过程做到心中有数,可以让消费者放心使用药品。从法规层面说,粒子主要监测的是0.5µm和5.0µm大小的粒径,其中0.5µm粒子能代表这个环境按照ISO 14644标准处于什么样的洁净等级;而5.0µm粒子是微生物超标的前兆,即微生物可能会粘附在这些粒子上形成菌落及菌落团漂浮于空气中。因此,当我们看到粒子超标,特别是5.0µm大颗粒超标时,就需要考虑环境是否有微生物污染可能性,但是5.0µm大颗粒无法代表其属性,即活性还是非活性。此时,我们就需要监测浮游菌,调查和鉴别这些浮游菌的数据来确认生产过程是否被微生物污染,从而确认这批药品是否可以放行。因此,对于一条无菌生产线,粒子和浮游菌都需要进行动态监测。
在线监测系统采样点的选择在考虑加工设备的性质、操作人员的行为以及产品的工艺流程的基础上基本上都放在风险最高,最容易受到污染的暴露位置,如药品暴露位置,容器暴露位置,生产暴露位置。通过对生产工艺及对产品在不同位置发生污染的风险评估,可以确定在线监测系统最有价值的采样点。下列因素在确定监测点的时候必须加以考虑:
✎.工作地点在何处;
✎.工作地点附近,产品暴露在空气中的可能性;
✎.生产的过程中,操作人员产生干涉的可能性。
一般来说,粒子采样探头的位置应当在关键点位置的一英尺(30cm)之内。为什么是一英尺呢?首先,粒子采样探头不能放在关键点正上方,虽然该位置是最反映关键点的环境状态的,但是关键点还是需要正上方的空气来保护关键点生产的。其次,也不能把粒子探头放在太靠近关键点的位置,因为关键点的生产操作可能会产生很多粒子,比如说灌装时出现的液滴。我们的粒子系统没有必要采集这些正常生产产品的粒子,这些数据会干扰我们对于环境监测的判断。因此,我们一般都放在距离关键点稍远一些位置。而一英尺的距离正好是一个高效过滤器的宽度,这个位置的选择正好能够是我们了解到同一片层流环境的关键点发生的情况。当然,我们粒子的采样高度是离关键点越近越好,但同时也要考虑到不要受到生产产生的粒子的影响,以及不要对正常生产造成干扰。
对于浮游菌监测高度的选择,由于微生物浮游菌是粘附在粒子上,或者有些芽孢是独立浮游在空气中的,故不需要担心生产过程会有微生物产生。因此,浮游菌采样头一般都靠近关键点,与关键点等高或稍高的位置来安装。因此,我们经常会在生产现场看到,粒子探头和浮游菌的采样头两者呈现一个高低的安装方式,粒子探头稍高,而浮游菌采样头稍低。
✎.浮游菌是否需要在全过程进行动态监测?
根据药品生产质量管理规范附录一无菌药品第十一条规定,应当对微生物进行动态监测,评估无菌生产的微生物状况。监测方法有沉降菌法、定量空气浮游菌采样法和表面取样法(如棉签擦拭法和接触碟法)等。动态取样应当避免对洁净区造成不良影响。成品批记录的审核应当包括环境监测的结果。
这里强调的是对无菌生产的环境必须进行动态监测来评估微生物状况,这个动态监测并未要求全过程进行。药品生产质量管理规范中还规定了“动态取样应当避免对洁净区造成不良影响”。企业应对采取的监测方法和程序进行评估。尤其要考虑到浮游菌采样过程及相关干预可能会对关键区的气流组织产生影响。所以,在关键操作中对微生物进行动态监测,浮游菌不需要进行全程动态监测。
对于无菌制药企业来说,产品的放行,需要建立在良好的环境监管计划以及有效的执行程序上。而环境监测是用来评估生产环境控制是否有效的一个工具,它从过去的十几年中从最开始的按一块块房间栅格的方式来执行,一直到后来更多的强调了风险评估,利用风险评估的工具来定义具有代表性的取样点位、方式方法,来进行更有效的环境监控。在线监控系统可以进行不间断采样,得到完整的更有意义的数据,对现场环境进行实时监测,及时发现所有人为干预、偶发事件及系统的损坏,以便于采取有效的解决措施;同时,自动化的采集系统对整个工作流进行监管,大大减少了由于人员操作带来的失误,对于无菌药品生产过程中的质量控制起着重要的作用。

杭州澳亚生物技术股份有限公司(“澳亚生物”)是一家集产、学、研为一体,以无菌冻干粉针剂为主导产品的现代化制药企业。自1993成立以来,遵循“以人为本、质量为先”的可持续发展战略,澳亚生物已经逐渐从小型、简单的冻干生产,走向复杂、规模化的无菌生产模式,为客户提供全方位的无菌生产解决方案。


点击此处“转发”分享精彩内容






