

MINTAB统计软件在产品质量回顾分析中
的应用案例
根据《药品生产质量管理规范(2010年修订)》第十章质量控制与质量保证第八节产品质量回顾分析第二百六十六条的要求,药品上市许可持有人(药品生产企业)应该每年对所生产的药品进行产品质量回顾分析,回顾分析的情形包括:成品的检验结果等。
本文以成品检验结果中的含量为例,对如何使用MINTAB统计软件进行统计分析进行了探讨。

1.含量背景数据资料
1.某公司生产的注射用XXXX企业注册标准规定的含量为8.6mg/支±5%(8.17~9.03)
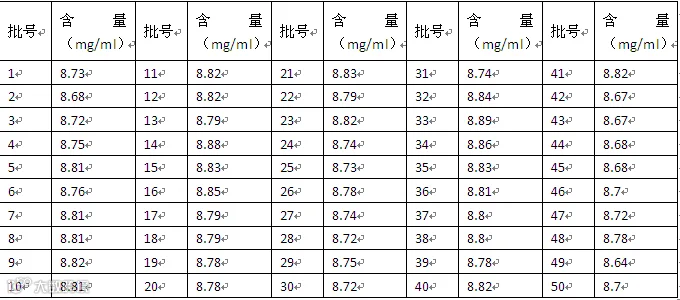
2.注射用XXXXX含量测定结果(2020年度,50批)

2.数据导入

3.单值控制图
1.统计(S)→基本统计量(B)→显示描述性统计量(D)
2.变量(V):选择C2含量,统计量(S):选择均值(M)、标准差(S)
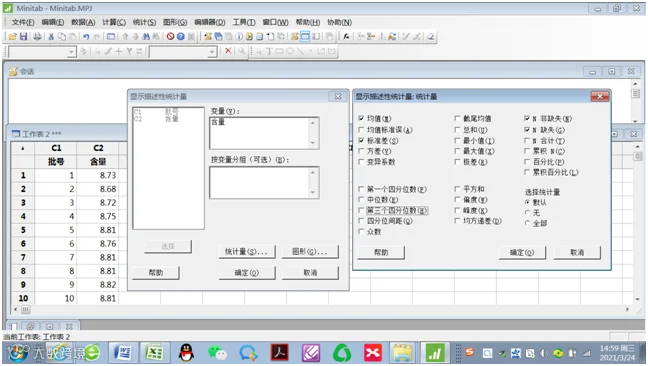
3.按“确定”,会话框出现平均值和标准差统计结果
| 变量 | N | N* | 均值 | 标准差 |
| 含量 | 50 | 0 | 8.7736 | 0.0590 |


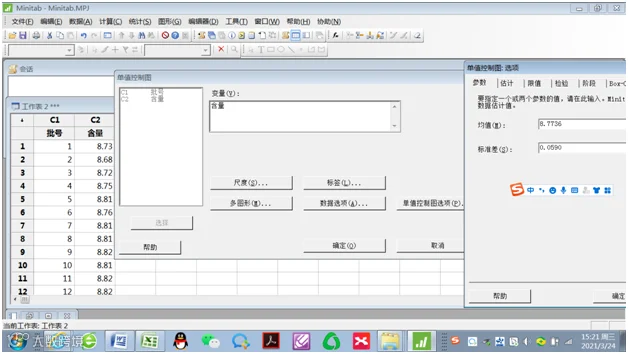
单值控制图选项(P):输入平均值8.7736,标准差0.0590

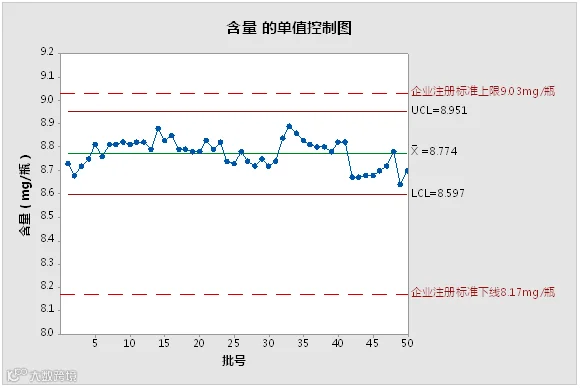
经统计,50批产品的平均值为8.774mg/瓶,3倍标准差的上下限8.951mg/瓶和8.597mg/瓶,所有批次产品含量均在±3s范围内。


1.统计(S)→基本统计量(B)→正态性检验(N)
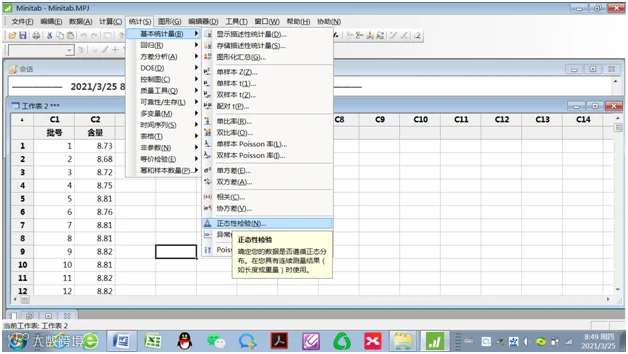
2.正态性检验
变量(V):选择含量;
正态性检验:默认“Anderson-Darling(A)”检验
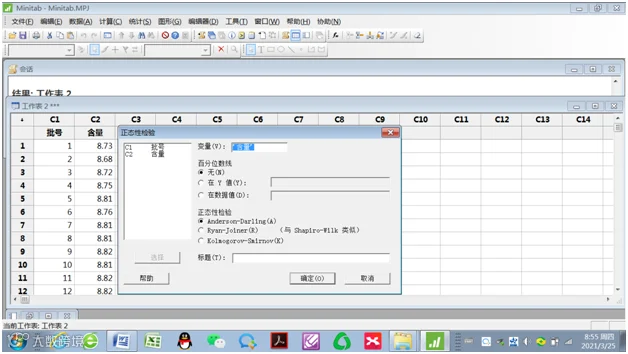
3.按“确定”,得到“含量的概率图”。
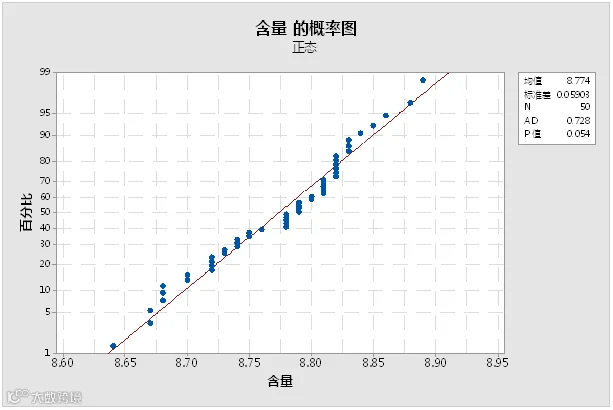
4.结果分析
P值=0.054>0.05,统计数据呈正态分布。

1.统计(S)→质量工具(Q)→能力分析(A)→正态(A)
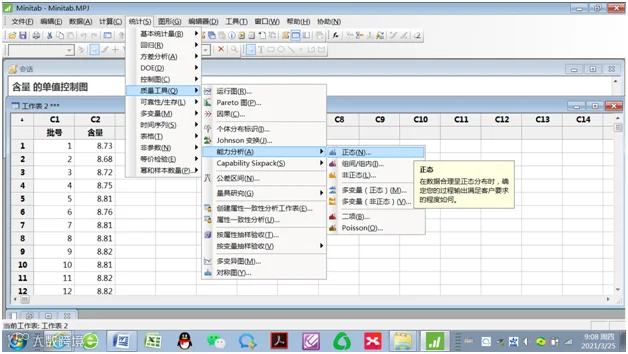
2.能力分析(正态分布)
数据排列为:单列(C):“含量”;子组大小(Z):1;规格下限:8.17;规格上限:9.03。
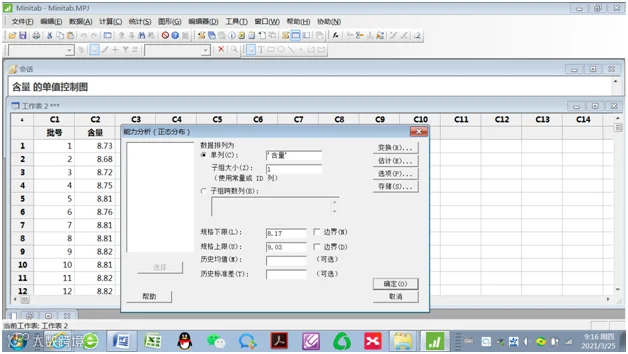
3.按“确定”,得到“含量的过程能力报告”。
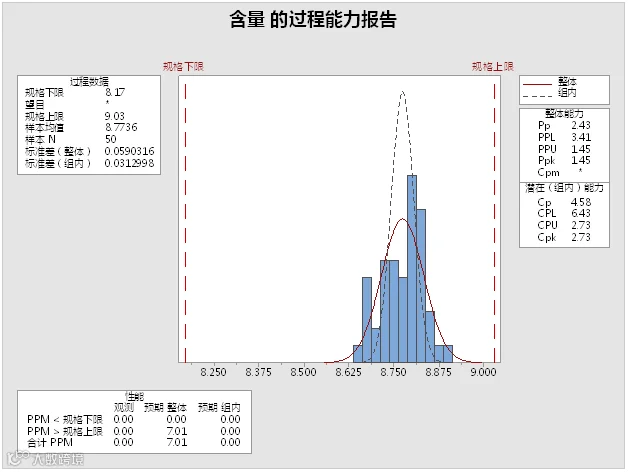
4.结果分析
(1)Cpk的评级标准
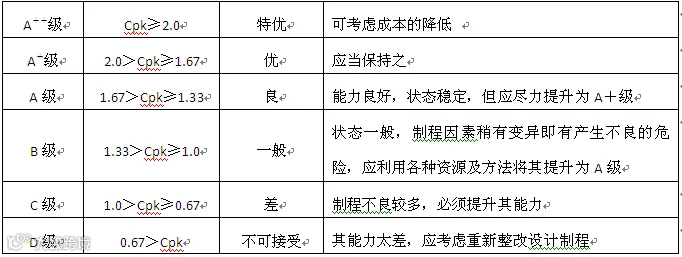
(2)结论Cpk=2.73,过程控制能力特优。药品生产不应考虑成本的降低,应继续保持其特优状态。

企业介绍
杭州澳亚生物技术股份有限公司(“澳亚生物”)是一家集产、学、研为一体,以无菌冻干粉针剂为主导产品的现代化制药企业。自1993成立以来,遵循“以人为本、质量为先”的可持续发展战略,澳亚生物已经逐渐从小型、简单的冻干生产,走向复杂、规模化的无菌生产模式,为客户提供全方位的无菌生产解决方案。









