
01
公司简介

杭州澳亚生物技术股份有限公司成立于1993年2月,是一家集药品研究开发、制剂生产及销售于一体的现代化生物医药企业。公司自成立以来,凭借“科技验证品质,诚信开拓未来”的企业宗旨,延续多年来委托生产(CMO)的专业经验,竭诚为客户提供一系列无菌制剂生产解决方案。
公司占地面积40000多平方米,拥有员工500多名,其中各类技术人员占50%以上,有一支热爱事业、勇于开拓和创新的专业团队。公司年产能力接近5亿瓶,是目前国内较大的无菌制剂职业委托加工企业。
公司现有12个无菌生产车间,包含7条冻干粉针剂生产线、4条预充针(卡式瓶)生产线及3条水针生产线,由17套药液配制过滤系统、IMA及星德科等14条高速洗烘灌联动生产线、星德科及B+S等4条预灌封(卡式瓶)生产线、18台不同规格冻干机(总冻干面积678.3㎡)、18台高速轧盖机等核心设备组成。





目前,澳亚的商业化委托加工客户横跨祖国大江南北。涵盖了多家国内著名的大型头部药企,所生产的药品都是与人民群众健康息息相关,服务于基层医院的常用药品。中国生物制药市场在全球市场的带动下,经历了革命性的崛起,催生了市场对生物类新药和复杂剂型的需求。澳亚生物的一站式中试平台,服务于产品生命周期的“实现”阶段,实验室小试到中试转化到商业化放大一条龙服务,降低生物制品,复杂剂型、新型给药和治疗方式下制剂生产断层的风险。
目前澳亚生物已经在为客户提供服务的产品涉及了目前行业最先进的产品和剂型,包括单/双克隆抗体,GLP1长效胰岛素,多肽类药品,脂质体,SiRNA小核酸类药品等。在西林瓶灌装和冻干的基础上,新增卡式瓶、预灌封等新型给药模式,同时涉足脂质体、纳米混悬剂、微球、微晶等21世纪最前沿的制药途径。
澳亚生物始终遵循“创新、挑战、勇气、竞争”的企业精神,致力于研究和生产高质量,优疗效的化学类和生物类药品,为保障民生,发展民族医疗产业添砖加瓦,为国产高端药品走向世界而努力。
未来,澳亚将借助杭州的医药小镇经济和上海张江、苏州纳米园研发的群体优势,继续深耕发展一个致力于孵化产品上市,面向国内外制药企业和研发机构的,集开发、生产、物流、注册等委托服务为一体的技术服务平台,成为国内无菌制剂CMO的龙头企业之一。

● 无菌注射剂【冻干粉针制剂和小容量水针(除菌过滤和终端灭菌)】的商业化委托生产
● 上市许可持有人制度(MAH)下的委托生产
● 中试孵化平台(临床样品委托生产)
● 冻干曲线的开发与优化
● 无菌生产质量管理培训
● 西林瓶冻干粉针剂(2-50ml)
● 西林瓶水针(2-50ml)
● 卡式瓶水针(1.5ml,2.5ml,3ml和5ml)
● 预灌封水针(1ml标准型,1ml细长型,2.25ml,3ml)

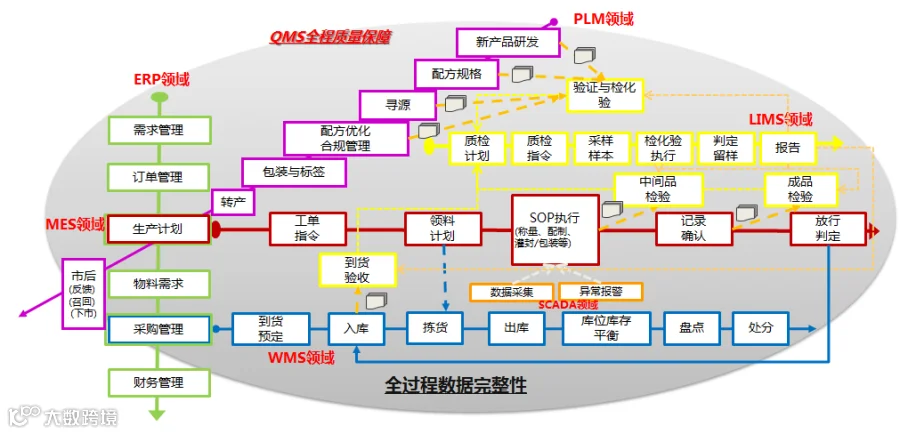
鉴于无菌药品生产的特殊性,企业在质量保障方面投入大量的人力与物力资源,质量保障体系的人员占企业员工人数的30%。公司投资建设了独立的无菌培训中心,让生产、质量培训更接地气、更接近实战。通过工艺流程管控、人员培训和信息化系统的辅助,在数据可靠性、质量体系建设、生产现场风险控制等方面,建立了成熟的管理、运营模式。
以药品质量为核心因素,打造信息化透明化的智慧工厂、实验室系统、生产系统、CCTV+AI智慧监管。






02
会议详情

09:00-09:40
我国药品集采政策调整重塑医药产业未来
耿鸿武 清华大学老科协医疗健康研究中心,执行副主任
09:40-10:20
已上市药品变更政策解读
朱明 海南省药品和医疗器械审评服务中心药化审评服务科科室主任
10:20-10:25
优质批文/项目发布
10:25-10:45
轻松一刻
10:45-11:25
主题待定
宣建伟 中山大学教授
11:25-12:05
主题待定
海南省药品查验中心

14:00-14:10
主题待定
王波 药融圈创始人
14:10-14:40
我国药品出海现状与思考
陈永法 中国药科大学教授
14:40-15:10
中国药企出海策略与经验分享(拟)
回爱民 惠正奇医药创始人、董事长兼CEO、前复星医药执行总裁
15:10-15:15
优质批文/项目发布
15:15-15:35
轻松一刻
15:35-16:05
无菌制剂国际化考量
宋庆国 健进制药副总裁
16:05-16:35
制剂国际化路径探讨和常见问题分享
孟晓峰 海昶生物联席总裁
16:35-17:05
中国药企商业化出海的机遇与挑战——平台型出海合作案例分享
何社辉 科兴制药拓展中心高级总监

09:00-09:30
委托生产质量管理体系建设要点及常见问题
谢海燕 丽珠医药集团质量管理总部总经理
09:30-10:00
药品生产技术转移一药品注册常见问题分析
王老师 原浙江省药监专家,国家GMP检查员
10:00-10:30
优质批文/项目发布
10:30-10:50
轻松一刻
10:50-11:20
药品数据完整性核查要点
胡淼 原国家药品生产检查组长
11:20-11:50
MAH质量合规之路:委托生产质量合规锚点与挑战
黄跃东 常州四药制药有限公司首席审计官
14:00-14:40
药品上市后变更质量研究策略探讨
刘峰 四川省药品检验研究院化学药品检验研究所所长
14:40-14:45
优质批文/项目发布
14:45-15:25
新规下,药物警戒检查要点与常见问题分析
苗会青 海南省药物警戒中心副主任
15:25-16:05
GMP符合性框架下的药品生产工艺验证考量
唐道生 国家药品GMP检查员、注册核查员

09:00-09:30
纯B证企业的突围发展方向思考
点苍鹤 医药云端工作室创始人、知名医药市场准入及营销模式、合规咨询专家
09:30-10:00
药品委托生产共线风险评估与防控(拟)
张新 中国医药教育协会制药技术专委会专家委员;制药工程正高级工程师,六西格玛黑带
10:00-10:30
优质批文/项目发布
10:30-10:50
轻松一刻
10:50-11:20
浅谈药品注册现场检查应关注的风险点(拟)
田老师 国家药监局核查中心原学术委员会副主任委员、主任药师、专家级检查员
11:20-11:50
技术转移工作的误区分析与管理突破
吴军 药品制造系统工程与GMP专家
14:00-14:40
药品上市许可持有人产品立项方向及策略
赵忠卫 深圳奥祺生物医药有限公司总经理
14:40-15:20
CMO的选择及日常管理
叶非 深圳华润九新药业有限公司质量总监
15:20-16:00
药品生产B/C证的监管要求与案例分享
刘德富 联邦制药集团质量总监

09:00-09:30
药品质量控制检验过程中的风险解析
彭继烽 广东省汕头市药品检验所原所长、国家药品(G M P)检查员、广东省药品审评专家
09:30-10:00
我国制药用水系统的最新法规动向与核查要求
张功臣 国家药典委2020版、2025版《中国药典(2016Y447、2022Y29)制药用水标准体系课题特邀专家
10:00-10:30
优质批文/项目发布
10:30-10:50
轻松一刻
10:50-11:20
实验室OOS调查
刘伟强 原上海市食品药品监督管理局认证审评中心GMP副部长,原国家食品药品监督管理局GMP高级检查员
11:20-11:50
液体除菌过滤工艺验证的合规要求及概述
彭瑛 默克工艺解决方案验证实验室负责人
14:00-14:40
2025年版《中国药典》微生物污染控制体系新增指导原则概况
林丽英 广东省药品检验所原微生物室主任
14:40-15:20
2025年版《中国药典》分析方法验证指导原则解读
杨伟峰 原浙江省食品药品检验研究院化药所副所长,主任药师
15:20-16:00
2025年版《中国药典》二部凡例主要内容解析
刘海静 陕西省食品药品检验研究院首席专家

实事求是,以人为本
尊重流程,注重效率








