一
湿热灭菌中常用术语
用于评估灭菌器空载条件下空气去除和蒸汽穿透的一种试验(例如,Bowie-Dick 测试法,DART,Lantor Cube,Browns 测试法),此类灭菌器用于多孔/坚硬物品类装载的灭菌。
采用生物指示剂来证明整个装载(被灭菌品)始终能达到所规定生物杀灭时间(FBIO值)的试验。它是性能确认的组成部分。
为评估真空条件下灭菌器腔室中是否有空气渗入而进行的试验。
在规定的灭菌条件下,使所用生物指示剂的数量下降一个对数单位,或杀灭90%所需的时间。在湿热灭菌中,D值需注明参照温度,即以DT 表示。例如,一个 D121℃=1.4分钟的生物指示剂系统,表示在 121℃下,杀灭90%的芽孢需要 1.4 分钟。
指灭菌器的参照测试点(通常是排水口)达到最低灭菌温度开始,到装载中最难灭菌点(冷点)均达到灭菌温度之间的时间间隔。它体现了灭菌器去除装载中空气并对其加热的能力。通常要求将热穿透探头放置在多孔/坚硬装载中才能对此进行评估。
二
湿热灭菌常见的灭菌程序
1、预真空程序:
饱和蒸汽最常见的灭菌程序是预真空程序。该程序是在灭菌阶段开始之前通过机械真空泵或蒸汽喷射器将空气从腔室中抽走。预真空程序尤其适用于可以包藏或夹带空气的装载物,比如软管、过滤器和灌装机部件。在制药行业中,脉动真空程序常用于难以去除空气的多孔/坚硬装载的灭菌。
灭菌程序开始之前,对装载的处理是很重要的。如果每次抽真空至 0.1 个大气压,那么每个脉冲将使灭菌器内的空气减少 90%或者 1 个对数单位。三次脉冲(抽真空-充蒸汽)可获得3个对数单位的下降值,有效地将空气去除了 99.9%。为了使装载处于正常状态,可能另需正压脉冲(充蒸汽至高于大气压,以避免空气进入腔室)。通过这个方法,提高去除空气的效率,这样平衡时间就会缩短。在制定灭菌程序时,要准确地确定脉冲的次数和抽真空的压力(抽真空的速率在一些多孔物质的装载中也应当被考虑)。
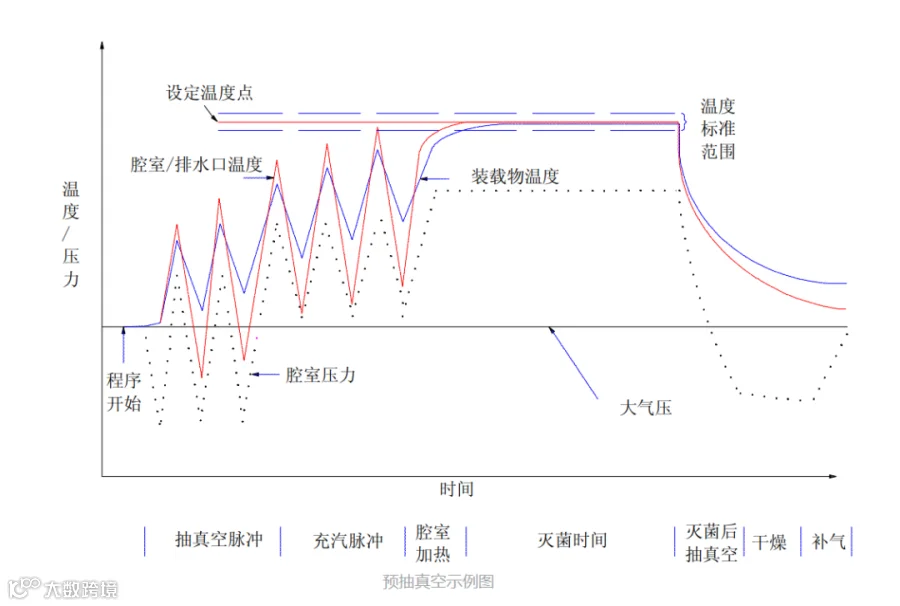
2、重力置换程序:
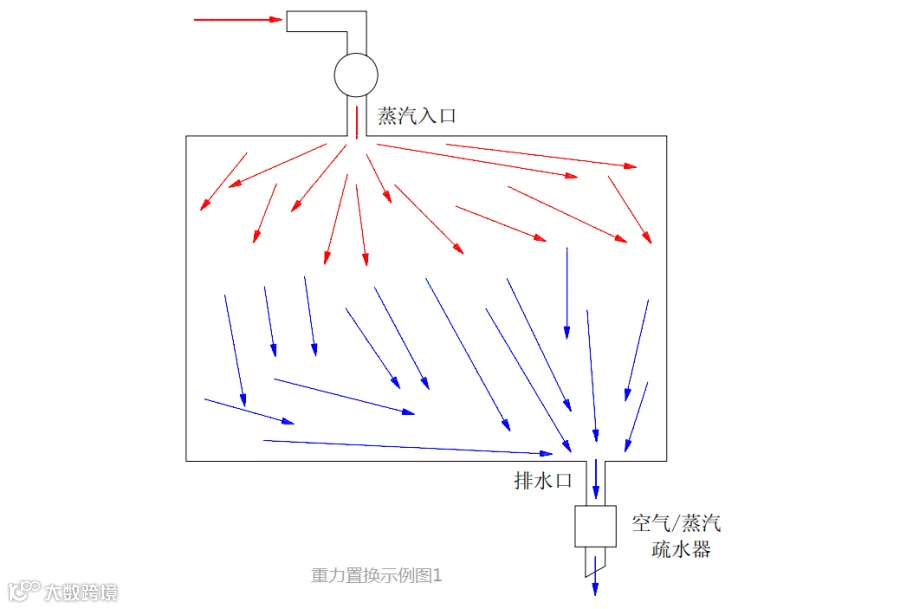
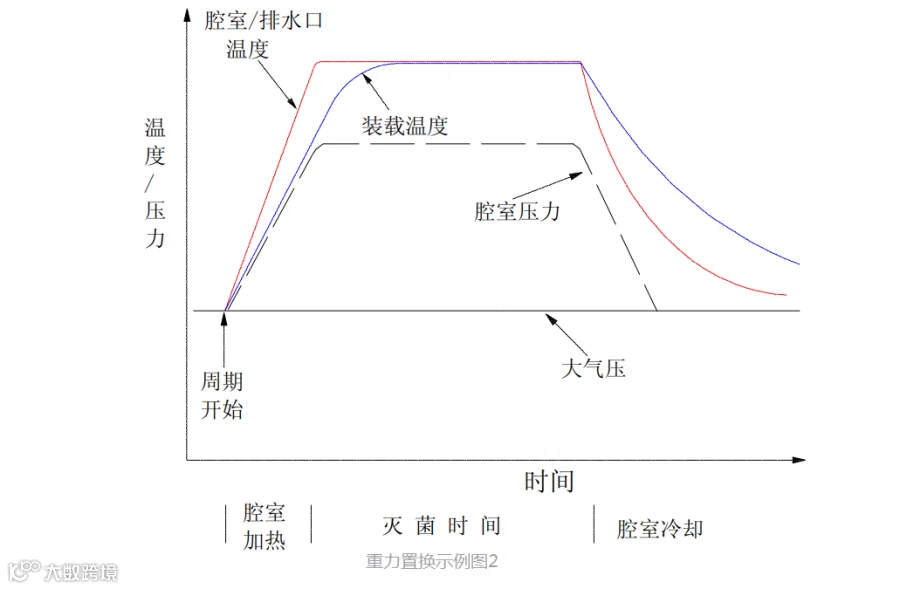
典型的重力置换程序建立在如下理论基础上:腔室中的冷空气比进入的蒸汽重,因而将下沉到腔室的底部。蒸汽进入灭菌器腔室迫使空气从腔室底部的排水管排出(和冷凝水一起通过蒸汽疏水阀排出)。排除空气成功与否取决于疏水阀的正确运行和适当的蒸汽分布。蒸汽通过导流板或散流器(例如多孔管)注入灭菌器腔室。如果蒸汽进得过快或分布不合理,装载的顶部或周围可能会夹带空气层。如果进汽过于缓慢,空气受热而扩散入蒸汽中,从而使排除空气更加困难。
三
湿热灭菌温度选择
灭菌效果的目标是实现规定的无菌保证水平(SAL)。对于无菌药品,一般要求达到SAL 10^−6,即使最顽强的微生物也被灭活至百万分之一以下的残留概率。要达到如此严格的无菌水平,通常需要足够的温度和时间组合,以确保将产品初始生物负荷降至安全水平。灭菌过程中的微生物灭菌率通常用L值表示——这是一个与温度相关的参数,用于量化某温度下相对于参照温度的杀灭效力。以121℃为参照(Tref=121℃,常取Z=10℃),则121℃下灭菌1分钟定义为1个等效灭菌时间单位。当温度偏离121℃时,可以通过公式计算其等效效力:L(T) = 10^((T−Tref)/Z)。例如,在Z=10℃的条件下,120℃下灭菌1分钟的效力约相当于在121℃下灭菌0.79分钟,而122℃下灭菌1分钟则相当于121℃下1.26分钟。由此可见,略高于121℃的温度会提高杀灭效率,略低则降低效率。国内目前对于无菌器具多采用121℃过度灭菌法进行灭菌。
在过度杀灭程序的确认过程中,最常采用生物指示剂是嗜热脂肪地芽孢杆菌;也可采用其他对湿热灭菌耐热性强的微生物,所选则菌株应当符合相应的法规要求。
所选用生物指示剂的数量应比产品或物品的生物负荷高,耐热性应比生物负荷强。只能采用芽孢来做蒸汽灭菌程序的挑战性试验。这些孢子必须达到一定的纯度(基本没有生长态菌、微小的残骸和团块),有确定的耐热特性,其母代菌株应该从公认的菌种库购买。
多孔/坚硬装载是指以直接接触饱和蒸汽来实现灭菌目的的物品。当蒸汽在被灭菌物品的表面冷凝时,发生热量转移。(与灌装液体容器的灭菌不同,湿热蒸汽通过传导/对流作用,将能量传递给容器中的内容物)。
制药工业中使用的多孔/坚硬装载包括真正的多孔物(如筒式过滤器和包装的织物)和坚硬物品(如不锈钢器皿和灌装机部件)。不管装载物的内容是什么,通常不建议采用对每类物品建立特定灭菌程序的做法,而是建立标准化的能够获得最低无菌保证的灭菌程序。
多孔/固体物品包括但不局限于下述内容:
过滤器(各种滤膜、筒式过滤器,和深层过滤器)
胶塞和其他封闭用聚合材料
管道和软管
工作服
清洁设备
设备易损件
注:过滤器应按供货厂商的建议选择灭菌时间、灭菌压力、灭菌温度等。
对于湿热灭菌来说,有两种常用的灭种程序:预真空程序和重力置换程序。预真空程序灭菌程序通常用于多孔/坚硬物品,而重力置换程序常用于液体产品。
确认开始前,要确认装载的类型和方式并有相应记录。应考虑灭菌效果和生产效率的以下方面:
装载不能接触腔室的内壁;
采用有孔的架子,以尽可能减小金属容器平面间的接触以及与灭菌车之间的接触,必要时可采用可调节式的支架;
为方便去除空气、排冷凝水(如将桶倒置)和蒸汽穿透,要明确装载物的方位并有相应记录;
质量大的装载应放置在灭菌器中较低的架子上,以尽量减少冷凝水所致的潮湿;
对于多孔/坚硬装载物而言,控制灭菌器中物品的数量是十分重要的。如果预期装载物的量是变化的,则需要确定最小和最大的装载量。应当有评估确认最难装载方式每年进行周期性确认,对于其他的装载方式应当在ccs中明确再验证的周期;
应有适当的装载指南,方便操作人员查阅;

建立灭菌程序的关键因素是确定运行参数,以满足灭菌工艺设计的目标并确定它们属关键因素或重要因素。下列出了工艺参数需考虑的问题:
过程 |
参数 |
需考虑的问题 |
全过程 |
夹套的温度和(或)压力 |
夹套温度不能超过或者明显低于腔室的灭菌温度。要控制温度以避免过热或者过冷。通常系重要参数 |
升温阶段 |
真空/脉冲的次数、范围和持续时间(如果使用) |
决定去除多孔物品中空气和达到适当平衡的时间。通常是关键参数 |
真空速率 |
可以设定,以保护包装完整性;但不具有代表性。是可能的重要参数 |
|
充蒸汽的正脉冲次数、范围和持续时间(如果使用) |
充入蒸汽的正脉冲是灭菌前为装载创造灭菌条件的有效方法。通常是重要参数 |
|
腔室加热时间 |
对于饱和蒸汽灭菌器而言,它与所供的蒸汽相关;可设报警线,对非正常的加热时间报警 |
|
灭菌阶段 |
灭菌时间 |
每个灭菌程序均需验证,并需监控/记录的关键参数 |
灭菌阶段温度设定值 |
这是验证过程中确认的关键控制点 |
|
灭菌阶段 |
灭菌阶段温度波动值 |
对灭菌程序是重要的控制参数 |
灭菌阶段排水畅通,或腔室温度不受影响 |
每个灭菌程序均需验证,并需监控/记录的关键参数。 |
|
装载探头的温度 |
在多孔或固体物体的灭菌中没有广泛应用.不作为日常控制参数,但在性能确认(PQ)中用于评估热穿透。。 |
|
灭菌期间的腔室压力 |
对于饱和蒸汽灭菌,可用以确认饱和蒸汽灭菌的条件:是一个依赖于控制系统可能的关键因素。 |
|
装载探头最低F0值 |
如采用装载探头,这是一个关键参数。 |
|
冷却阶段 |
压力下降的速率 |
可以设定,以保护包装(如:呼吸袋)和过滤器的完整性;但不具有代表性。是可能的重要参数。 |
干燥时间 |
下列因素可能会提高干燥效率:加热、高真空、脉冲或这些因素的组合。装载有特定干燥要求时,它是灭菌程序的重要参数。 |
|
补气速率 |
可以设定,以保护包装(如:呼吸袋)和过滤器的完整性;但不具有代表性。是可能的重要参数。 |
灭菌后冷却阶段的物品需要尽可能的干燥,避免潮湿导致有可能的微生物滋生,灭菌后物品的干燥程度评估可以通过目测或比重法进行检测,并制定合理的可接受标准,如目视无肉眼可见明显液滴、无明显潮湿织物。
为了提高灭菌后装载干燥度,在冷却阶段中可采用以下方法:提高真空度、升高夹套加热的温度、增加脉冲真空次数和时间的方式或这些方法的组合来提高物品干燥程度。同时在物品准备和装载的摆放方式上也需要进行开发和试验,如物品在灭菌前尽可能干燥、优化呼吸袋的摆放方式,调整容器开口的朝向,优化无菌包装的方式用于提高通透性。
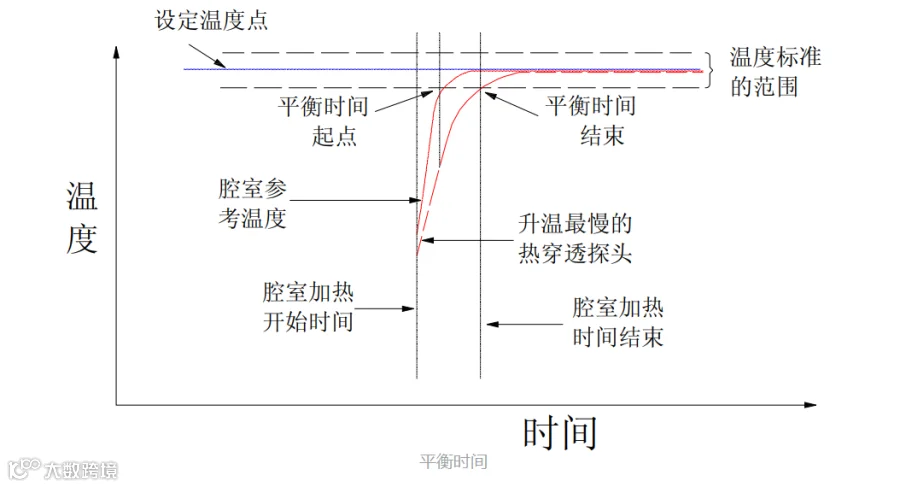
平衡时间代表去除空气和升温并使装载达到适当灭菌条件的能力。如果平衡时间过长即使最终达到了设定的灭菌温度,平衡时间的延长也表示去除空气或加热能力的不足。在建立灭种程序过程中,应采取预防措施,尽可能减小平衡时间,这点十分重要。通常可以采用以下方法:
确认物品正确放置,能有效去除空气(如胶管不受挤压)。
增加真空或蒸汽脉冲(即充蒸汽)的次数、速率。
提髙真空脉冲的真空度。
优化装载方式。
评价物理杀灭时间FPHY和生物杀灭时间FBIO的一致性
对于一个灭菌程序而言,当一个生物指示剂的生物杀灭时间可测量时,在同一位置测得的物理杀灭时间和生物杀灭时间应该是相等的。灭菌程序生物指示剂确认的要求是验证样品的生物指示剂试验呈阴性结果;这就要求物理的标准灭菌时间FPHY比较大。在这一物理标准灭菌时间条件下,无法测定生物指示剂的生物杀灭时间 FBIO,因为BI在额定灭菌区的范围以外。杀灭生物指示剂所需要的热量可以通过计算得到。如果实际的灭菌时间明显低于所需的物理杀灭时间 FPHY,灭菌试验将导致生物指示剂呈现阳性的结果。
物理和微生物结果之间的一致性是灭菌验证中最重要的部分。对于蒸汽穿透或热穿透困难的产品来说,仅凭温度和压力测量得到的物理数据尚不能证明已经达到了设定的灭菌要求。例如,物理测量法不能完全证明产品(比如注射器的内腔、针头的保护罩或滤膜)达到了灭菌要求。同样,如果忽略杀灭生物指示剂所需要的物理参数,那么生物指示剂的杀灭并不足以证明一个灭菌程序的适用性。生物挑战的结果应与物理数据相一致,反之亦然。

按照赋予被灭菌品的杀灭时间来衡量,应当从物理和生物二个方面来证明最低的合格灭菌程序的合理性。为了保证最低可接受灭菌程序结果的一致性,为确保有一个安全余地,日常运行的灭菌程序一般使用高一些的灭菌温度和长一些的灭菌时间。
1.1热分布
热分布确认的主要目的是证明整个装载区加热介质的分布是均匀的。为了测试热分布情况,温度探头应置于装载区,但不能与装载物或灭菌器硬件(例如灭菌车、支架、托盘)相接触。应有详细描述具体温度探头位置的图形。
在热分布确认试验中,应确认关键和重要的操作参数并有相应的文件和记录。灭菌程序灭菌阶段的合格标准包括:
每个探头所测得温度的变化范围
不同探头之间测得的温度变化范围
探头测得的温度与设定温度之间的差值
夹套温度的变化
1.2热穿透
热穿透确认的目的是证明所需的热量已经转移到装载(比如液体)或材料的表面。应采用热穿透数据来计算物理杀灭时间 FPHY。应将热穿透温度探头置于液体容器中的冷点,或经确定多孔/坚硬物品升温最慢,即最难灭菌的位置。
对于热穿透特性不同的产品组成的多孔/坚硬装载(通常称为混合装载物),探头应置于每个类型中具有代表性的装载物中。对于只有一种类型物质组成的多孔/坚硬装载物(如胶塞),可以均匀分布。每个确认装载的温度探头的位置,以及选择此位置的理由及评估,均应有相应的文件及记录。
2.1挑战系统中生物指示剂数量和耐热性的确定
可以用半对数模式来确定生物指示剂确认中所用生物指示剂的特性(如数量、耐热性)。所需的杀灭时间应在灭菌程序开发过程中确定。通过以下公式可以设计出生物指示剂,以证明实际上灭菌程序已达到了所需要的杀灭时间。
Log NF = − F(T,z)/DT + Log N0
F = 灭菌程序设计过程中期望获得的灭菌致死率
D = 挑战试验中BI(生物指示剂)的耐热性
N0 = 生物指示剂的起始浓度
NF = 灭菌程序结束后,生物指示剂的存活数量。为了方便计算,如果将生物指示剂杀灭,可以认为存活数小于1,在此等式中,可以NF=100表示。
注:这些计算假设灭菌程序是在理想条件下(如空气完全移除、纯饱和蒸汽、生物指示剂数量/耐热性没有变化)。应注意,计算的杀灭时间(F值)是灭菌程序的最低杀灭时间,而物品从最低合格灭菌程序获得的杀灭时间F值要大得多。
2.2生物指示剂的使用和放置
为了评价FPHY和FBIO之间的关系,生物指示剂应靠近温度传感器放置。在放置温度探头和BI指示剂的时候,要注意避免人为地增加或减少某一区域空气的去除或者蒸汽的穿透。例如在实际的验证过程中有线温度验证探头刺破呼吸袋进入物品内部是否会提高冷空气的排出和纯蒸汽的进入。

PDATR1中提高为了得到有代表性的结果,也许有必要在装载中放置两个相同的物体,其中一个插入温度探头,另外一个则含有生物指示剂。但笔者认为这个方式应当经过充分的评估并考虑法规的符合性。
应在试验方案中清楚地明确物理和生物确认的合格标准。这些标准应根据待灭菌产品的类型、采用的灭菌方法、适当的法规要求以及在灭菌程序开发时确定的运行参数等确定。
物理确认的合格标准示例如下:
用热穿透探头测得超过设定温度的最短及最长时间
F0的下限及上限
灭菌阶段结束时的最低F0值
灭菌阶段的最低和最高压力
饱和蒸汽温度和压力之间的关系
灭菌阶段腔室的最低和最高温度
热穿透温度探头之间的最大温差或F0的变化范围
热分布试验中温度探头间的最大温差
最长平衡时间
物品的干燥程度
夹套温度的变化
生物确认合格标准示例如下:
微生物挑战试验中,孢子的对数下降值符合预期标准
规定的阳性和阴性对照符合设定要求
01 药品生产质量管理规范(2010年修订)无菌药品附录
02《中国药典》通则1421《灭菌法》、9207《灭菌用生物指示剂指导原则》
03《化学药品注射剂灭菌和灭菌工艺研究及验证指导原则》
04《药品GMP指南- 无菌制剂》10.2湿热灭菌
05 PDA技术报告(TR1、TR30和TR48)
06 GB 8599《大型压力蒸汽灭菌器技术要求》
07 EN285《消毒蒸汽灭菌器大型灭菌器》
08 EMA《药品、活性物质、辅料和内包材灭菌指南》
09 ISO17665《医疗器械灭菌过程的开发、验证和常规控制要求》
结语:最后笔者想说想要通过湿热灭菌达到相应的无菌水平绝不是简单的延长灭菌时间就可达到的,需要合理的装载方式、经过科学的设计的参数并通过验证、设备的定期维护保养、合格的纯蒸汽、定期的再确认、持续的装载优化以及尽可能的参数优化、操作人员严格的按已验证的方式进行灭菌等。

实事求是,以人为本
尊重流程,注重效率



