
两套不同检测系统甲状腺激素测定结果的可比性分析
王建琼,牛 华,陈 玲,张 芹,平竹仙
(云南省第一人民医院检验科,云南昆明650032 )
摘 要:目的 对 Abbott Architect ci16200 全自动生化免疫分析仪(雅培系统)和Roche Cobas e601 全自动免疫分析仪(罗氏系统)检测甲状腺激素的结果进行对比分析。方法 分别采用雅培系统[化学发光微粒子免疫分析(CMIA)]和罗氏系统[电化学发光免疫分析(ECLIA)]对 93 例血清标本进行甲状腺激素[甲状腺素(T4)、游离甲状腺素(FT4)、三碘甲腺原氨酸(T3)、游离三碘甲腺原氨酸(FT3)、促甲状腺激素(TSH)]的检测,并对结果进行分析。结果 两套检测系统检测T4、FT4、T3、FT3、TSH的结果具有良好相关性,相关系数分别为0.960、0.962、0.976、0.900、0.999(P<0.01),但两套检测系统测定结果的差异有统计学意义(P<0.05)。结论 两套检测系统测定甲状腺激素的结果不可比。
关键词:甲状腺激素; 检测系统; 可比性
DOI: 10.3969/j.issn.1673-4130.2014.21.040 文献标识码:A 文章编号:1673-4130 (2014)21-2953-02
甲状腺激素是由甲状腺滤泡上皮细胞通过摄取碘合成和分泌的一种糖蛋白[1],是评价甲状腺功能的特异、灵敏的指标[2]。临床上以甲状腺功能五项指标[甲状腺素(T4)、游离甲状腺素(FT4)、三碘甲腺原氨酸(T3)、游离三碘甲腺原氨酸(FT3)、促甲状腺激素(TSH)]最为常用。目前对于甲状腺激素的检测方法较多,常用的有放射免疫分析法、酶联免疫吸附法、化学发光免疫分析法、时间分辨荧光免疫分析法以及电化学发光免疫分析等[3]。对于同一项目采用不同的免疫分析系统测定的结果是否存在差异,是否具有可比性,以及实验室之间的检测结果是否可以相互认证,是否能达到一致,这些都是值得进行研究和探索的问题。而对雅培(CMIA)和罗氏(ECLIA)进行甲状腺激素(T4、FT4、T3、FT3、TSH)检测结果的可比性研究鲜有报道,为此,本研究通过两套免疫检测系统对93例标本进行T4、FT4、T3、FT3、TSH的检测并对其结果进行比较分析,现将报道如下。
1 资料与方法
1.1 一般资料 2014年1~2月云南省第一人民医院门诊或住院患者93例血清标本。
1.2 仪器与试剂
1.2.1 仪器 Abbott Architect ci16200 全自动生化免疫分析仪[简称雅培系统,采用化学发光微粒子免疫分析(CMIA)],Roche Cobas e601全自动免疫分析仪[简称罗氏系统,采用电化学发光免疫分析(ECLIA)]。
1.2.2 试剂 雅培系统使用配套的雅培试剂及校准品;罗氏系统使用配套的罗氏试剂及校准品。在测定中分别使用伯乐质控品和罗氏质控品作日常质控,以保证测定结果均在良好的质量控制系统下获得。
1.3 方法 所有对象均为清晨空腹状态采血,使用含有分离胶(红色头)的真空采血管抽取静脉血3~4mL,以3000r/min离心10min后,分离血清上机检测。
1.4 统计学处理 相关性检验采用Excel2003软件进行直线相关分析。计量资料采用x±s表示,采用SPSS19.0统计软件包进行统计分析,不同的检测系统检测结果均数比较采用配对t检验,P<0.05为差异有统计学意义。
2 结 果
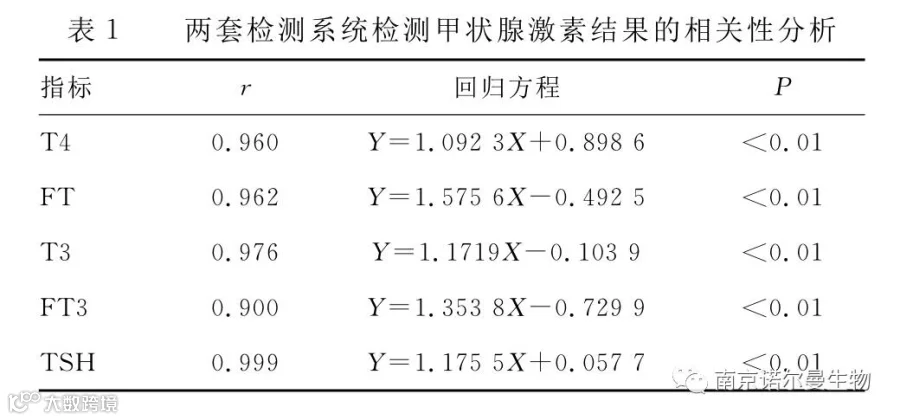
2.1 两套系统检测甲状腺激素结果的相关性分析结果 数据采用Excel2003软件以制作线性回归方程(X:雅培系统;Y:罗氏系统),结果见表1
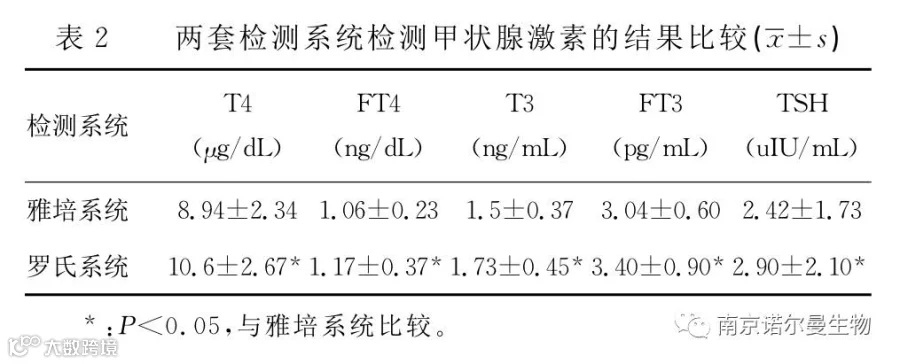
2.2 两套检测系统检测甲状腺激素结果的比较 见表2。
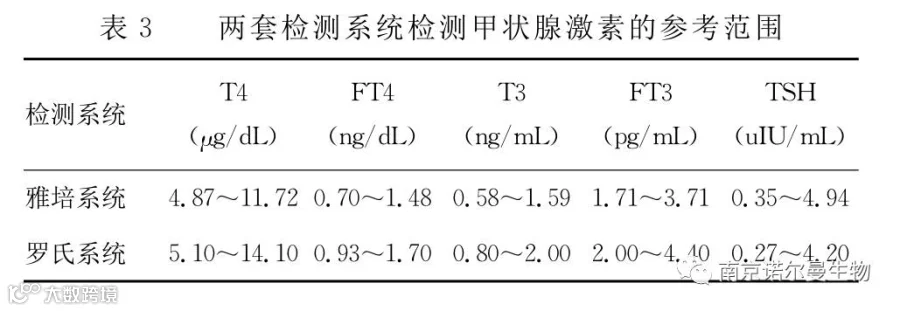
2.3 两套检测系统检测甲状腺激素的参考范围 见表3。
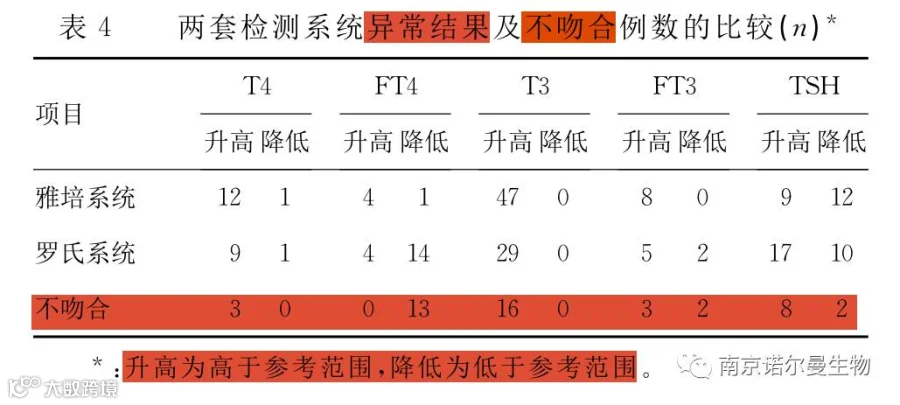
2.4 两套检测系统检测93份血清标本甲状腺激素的异常结果比较 分别采用两套检测系统检测93份血清标本的甲状腺激素,检测结果存在明显差异,见表4。
3 讨 论
在临床实际检测工作中,甲状腺激素各指标的检测经常会受到多种因素的影响而造成检测结果的偏差,进而影响临床诊断和判断,延误甲状腺疾病患者的早期治疗[4]。国外文献有报道,在医疗水平较高的发达国家中,也有各种类型的甲状腺功能紊乱的患者没有得到及时正确的诊断而延误治疗,其比例超过10%[5]。因此,采用适当的方法检测甲状腺激素对甲状腺疾病的诊断具有十分重要的意义。
雅培系统采用了CMIA法,主要用于测定蛋白质、病毒抗原等大分子物质,标本与微粒反应后,利用磁场分离未反应的物质,以吖啶类(N-磺酰基)羧基氨基化合物作为标记物,H2O2和NaOH作为预激发液和激发液,吖啶酯发生氧化还原反应恢复到基态时发光,根据发光强度通过预先确定好的时间读取化学发光发射的量计算分析物的浓度[6-7]。
罗氏系统运用了ECLIA法,该方法是一种新的小分子标记免疫分析技术,是电化学发光和免疫反应结合的产物[8]。ECLIA法直接以[Ru(bpy)3]2+标记抗体,反应时标记物直接发光,且[Ru(bpy)3]2+在电极表面的反应过程可以周而复始地进行,产生许多光子,使光信号得以增强。ECLIA方法有较高的诊断灵敏度和特异性,试剂稳定性好、保存时间长,且排除了人为误差[9-10]。
对于不同的检测系统而言,甲状腺激素的检测结果是否存在差异,是否具有可比性,对于同一家医院具有两种分析系统其检测结果又是否能够达到一致,这些都是值得研究人员去探讨和分析的问题,这是质量管理的目标,同时也是检验人员、卫生管理机构、所有厂商等共同的愿望和努力的方向[11]。从本文研究结果显示,雅培系统和罗氏系统检测甲状腺功能五项指标(T4、FT4、T3、FT3、TSH )的相关系数均大于0.900,尤其是T3、TSH的相关系数大于0.975,且P<0.01,说明两套检测系统检测甲状腺功能五项指标的相关性良好。但是从表2中可以看出两套检测系统检测甲状腺激素的结果差异有统计学意义(P<0.05)。另外,表4的结果也证明两套检测系统检测甲状腺激素的结果存在不吻合的情况。以上结果说明,虽然雅培系统和罗氏系统检测甲状腺激素的结果有良好的相关性,但检测结果不可比。
造成同一项目检测结果不可比的原因主要是检测原理、仪器性能、试剂来源不同、试剂成分和参考范围的不同。由于检测过程中与相应的抗原、抗体、载体、底物、发光剂等依次结合的顺序不同,均可造成检测结果的差异,且由于两种免疫检测体系试剂所包被的抗体存在差异,抗体的差异性可导致识别和结合分子抗原位点的差异性,因而造成了检测结果的最终差异,而这一差异会给临床医生和患者正确解读检验报告并将检验结果用于诊疗带来困难。因此,雅培系统和罗氏系统检测的甲状腺激素结果不可互认。
参考文献
[1] 王兰兰,许化溪.临床免疫学检验[M].北京:人民卫生出版社,2012.
[2] 董作亮.两种促甲状腺激素受体抗体检测方法的临床应用比较[J].天津医科大学学报,2008,14(3):297-298.
[3] 孟保福.全自动电化学发光免疫法检测甲状腺功能5 项指标的临床应用及评价[J].国际检验医学杂志,2008,29(6):542.
[4] 欧阳彬.电化学发光免疫分析检测血清促甲状腺激素在甲状腺功能减退中的应用[J].中国民康医学,2010,22(9):1116-1118.
[5] Feldt-Rasmussen U.Analytical and clinical performance goals for testing autoantibodies to thyroperoxidase, thyroglobulin,and thy-rotropin receptor [J].Clin Chem,1996,42(1):160-163.
[6] 何洁文,王勋松.罗氏电化学发光检测法与微粒子酶免疫法检测泌乳素的比较[J].海南医学,2010,21(1):106.
[7] 马寄晓,刘秀杰.实用临床核医学[M]. 北京:原子能出版社,2002:97-117.
[8] 宫尚鸿. 磁酶免方法检测甲状腺激素及临床应用[J].临床和实验医学杂志,2007,6(9):142-143.
[9] Sehott M,Hermsen D,Broecker-Preuss M.Clinical value of the first at Jtol/I,tlted TSH receptor a atoantibody assay for the di-agnosis of Groves′disease(GD):an international muhieentre tR-RAI[J] .Clin Endocrinol,2009,71(8):566-573.
[10]郎江明. 临床免疫诊断学[M] .广州:广东科技出版社,2003:11.
[11]陶义训.免疫学和免疫学检验[M].2版.北京:人民卫生出版社,1977:174.
(收稿日期: 2014 - 09 - 28 )




