
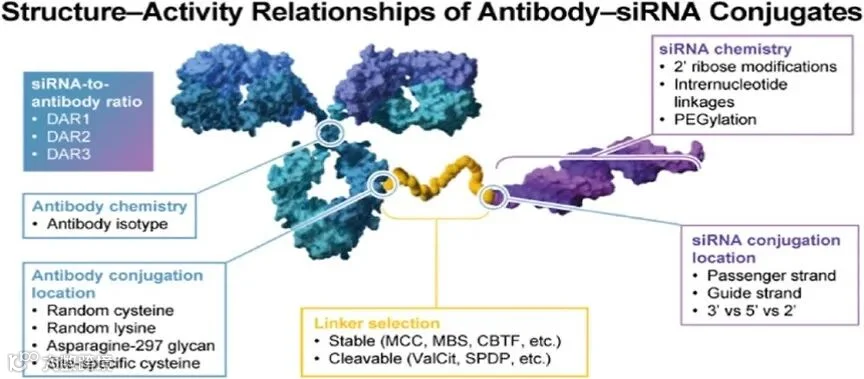
图1:抗体与siRNA偶联物的构效关系(图片来源:参考文献1)
抗体与寡核苷酸的应用与优势
抗体和寡核苷酸是生物医药领域中两类强大且多样化的分子,抗体能够高特异性识别并高亲和地结合多种细胞表面靶标,因此已被广泛应用于治疗和药物递送中,比如近几年来如火如荼的抗体药物偶联物(ADC),但其本身对于细胞内药物靶点则力有不逮;反观寡核苷酸(如小干扰RNA/siRNA,反义寡核苷酸/ASO和磷酰二胺吗啉寡聚物/PMO)则是通过调控基因表达,包括mRNA降解、剪接调控以及外显子跳跃,在多种疾病治疗中展现出了良好效果。在过去25年间,已有超过16种寡核苷酸药物获批(参考文献2),为疾病治疗提供了新的选择。
寡核苷酸的挑战与解决方案
siRNA是一种双链RNA,通过与RNA诱导沉默复合体(RISC)结合,特异性降解靶mRNA来抑制基因表达。但siRNA面临着容易被核酸酶降解、穿膜困难以及可能引发免疫反应等挑战,为提高其稳定性,通常会对其进行2’-O-甲基化或磷硫酰化的修饰,并通过生物信息学优化序列以减少脱靶效应(见图2)。
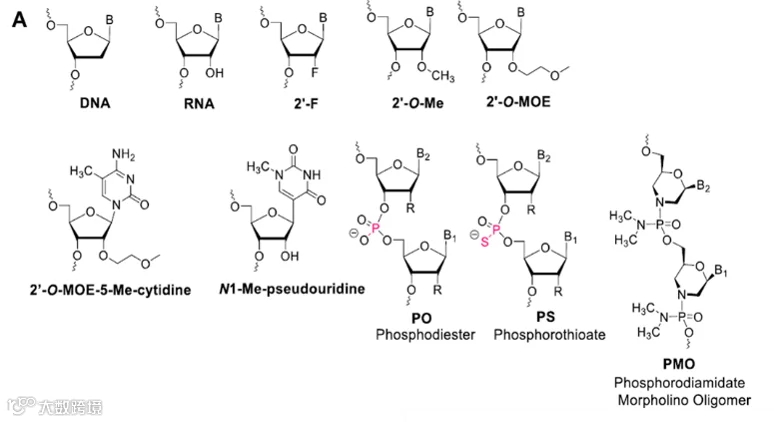
图2:天然DNA和RNA以及一些已获批并用于治疗的相关化学修饰(图片来源:参考文献2)
而ASO作为一种单链寡核苷酸,面临类似的降解和递送挑战,通过硫代磷酸酯修饰或纳米颗粒载体包裹等方式可增强其稳定性以及提高细胞摄取。
PMO则是一种不含核糖和磷酸的反义寡核苷酸类似物,虽然在化学稳定性上有优势,但其穿膜效率却相对较低,一般会通过与细胞穿透肽(CPP)偶联或进行化学修饰,来提升其递送效率。除了上述的改进策略以外,与抗体进行偶联形成AOC分子则在这些寡核苷酸上都展现出增强稳定性和提高特异性的特点。
AOC策略:突破递送障碍
AOC(抗体-寡核苷酸偶联物)结合了抗体的靶向与内吞能力来解决寡核苷酸在跨细胞膜递送方面的挑战。在一些报道中显示,AOC在体外及小鼠模型中均表现出良好的药效,抗体与反义寡核苷酸(ASO)的偶联物在中枢神经系统疾病中的应用也取得了一定进展。然而,目前AOC的构效关系(SAR)尚缺乏系统性研究报道。值得关注的是AOC领军企业Avidity Biosciences于近期在J Med Chem. 连续发表了两篇分别关于PMO 和 siRNA AOC的结构活性关系(SARs)的文章(参考文献1和3),详细探讨了AOC的构建方法、连接子选择、偶联位点及DAR(药物与抗体比率)对活性的影响,并进行了系统的构效关系分析。此外,在上一篇文章中,我们对AOC的主要偶联方法、主要竞争格局以及临床试验状态进行了分析,有兴趣的读者可以参见:解码抗体-寡核苷酸偶联,赋能创新生物偶联药开发。
01
AOC的偶联策略及其对疗效的影响
该研究探索了抗体-siRNA偶联物(AOC)的偶联策略,涉及的偶联方案包括使用部分还原抗体链间二硫键暴露半胱氨酸(Cys)巯基,使其与siRNA连接子-马来酰亚胺偶联,生成DAR1的抗体-siRNA偶联物。此外,文章还探讨了在抗体的Asn297和赖氨酸(Lys)位点进行偶联的策略,结果显示通过Cys偶联的AOC表现出更好的血浆稳定性。另外,作者还比较了链间随机Cys偶联与thiomAb定点Cys偶联的DAR1 AOC的血浆稳定性,结果表明二者具有相似的血浆稳定性(见图3)。虽然随机链间Cys具有不用抗体改造的优势,但是其也存在抗体还原后游离Cys可能导致的聚集和二硫键重排问题。为了解决这一问题,作者在还原后采用DHAA(脱氢抗坏血酸)氧化和NEM (N-乙基马来酰亚胺)封端处理,确保DAR1偶联物的稳定性。结果表明,NEM封端有效消除了游离Cys,确保AOC在储存期间不会形成二聚体。这一优化策略在不同抗体上表现略有差异,但游离Cys封端处理具有广泛适用性。
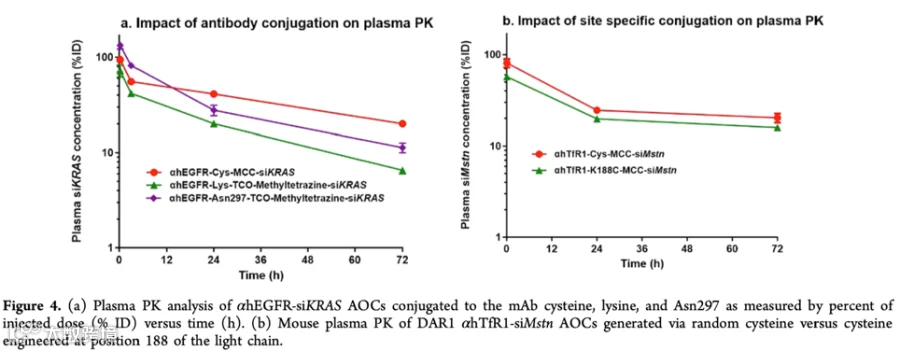
图3: 不同偶联方式AOCs的血浆PK. (图片来源:参考文献1)
02
siRNA的化学修饰与药效
siRNA在体内给药后易受内外切酶降解,影响其在靶组织中的积累和持久性,通过化学修饰,如2′-F、2′-OMe、2′-MOE及硫代磷酸酯(P-S)替代,可以有效提升其稳定性。研究显示,通过将这些修饰应用于siRNA,可以显著改善其在肌肉组织中的稳定性和药效,尤其是通过糖修饰(如UNA、LNA)和P-S的组合,可以实现长达8周的基因敲低效果(见图4)。
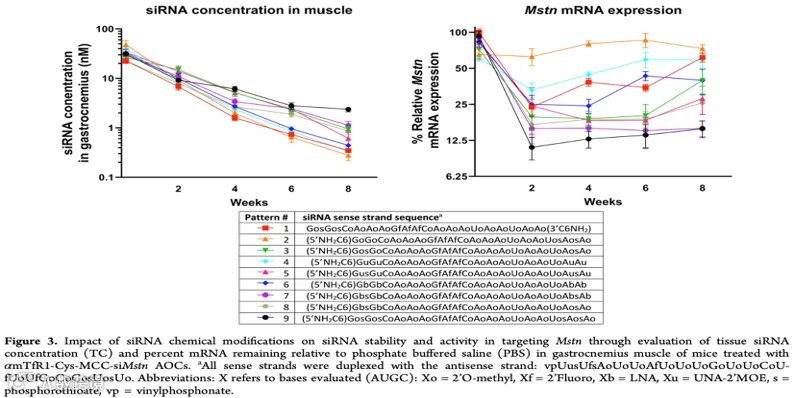
图4:不同化学修饰对siRNA AOC在小鼠中的稳定性及活性的影响(图片来源:参考文献1)
03
DAR对疗效的影响
文章中,作者制备了DAR为1、2和3的siRNA AOC来研究DAR值对疗效的影响。结果显示,随着DAR的增加,AOC的血浆清除率加快(见图5.a&b),特别是DAR2的清除速度约为DAR1的五倍,这主要是由于肝脏的非生产性摄取(Nonproductive uptake)增加,导致肌肉中的药物输送和活性的降低,更高的DAR还会改变偶联物的物理化学性质,如尺寸和负电荷密度的变化,影响与血浆蛋白的相互作用。对于PMO AOC,较高的DAR(如DAR9.7)在降低抗体剂量的情况下,依然能够有效递送相同量的PMO,并显著提高了心脏中的外显子跳跃效果(见图5.e),这表明在不同应用中,DAR的优化对于提高AOC疗效、生产效率和成本效益都具有重要意义。
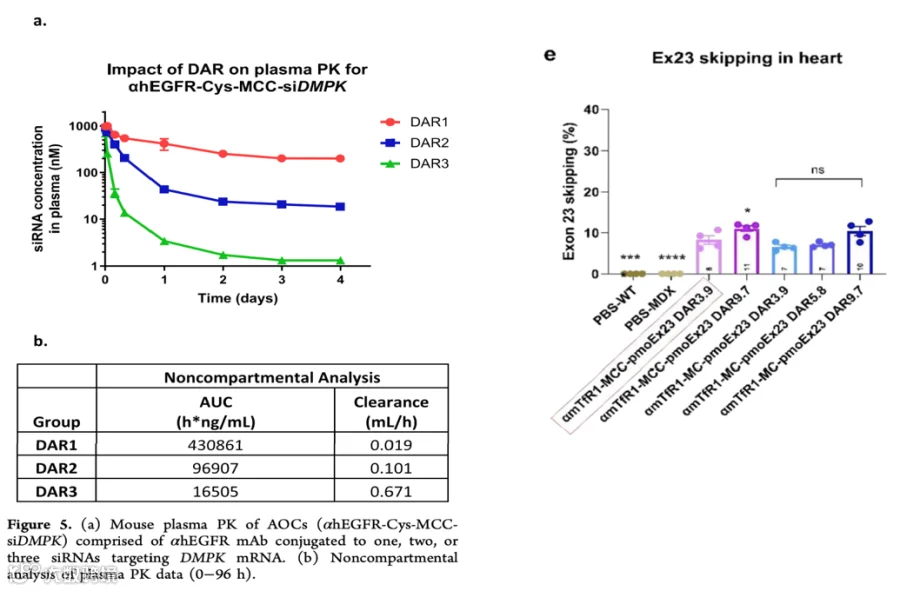
图5: 不同DAR值AOC在小鼠血浆的PK(a & b) (图片来源:参考文献1);不同DAR值AOC (PMO)对心肌细胞中外显子跳跃的影响(图片来源:参考文献3)
04
连接子类型对疗效的影响
该研究探讨了可裂解和不可裂解连接子对AOC药代动力学和疗效的影响,通过对比多种连接子,发现虽然连接子在siRNA血浆清除率上的影响不大,但优化连接子结构和空间位阻(如增加双甲基基团)可以提高其在循环中的稳定性,从而减慢AOC的清除速度(见图6)。在PMO AOC的研究中(参考文献3),不同连接子在药效上的差异较小,这说明了连接子的影响具有一定的局限性。
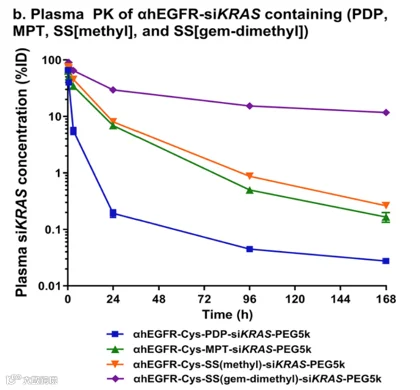
图 6:含有不同可裂解连接子的AOC在小鼠血浆中的PK(参考文献1)
05
siRNA和PMO连接子位置对疗效的影响
研究还探讨了连接子在siRNA连接位置对稳定性和敲低效率的影响,结果显示,连接子在siRNA的正义链的3′或5′端对不同组织(如肌肉、心脏、肝脏和肺)的mRNA敲低效果无显著影响。然而,当连接子位于正义链的骨架中间(如第8位或第14位)时,低剂量下敲低效率下降,表明这些位置可能干扰RISC装载。相比之下,5′端连接子在肝脏和肌肉中的敲低效果优于中间位置的连接子(见图7)。此外,当剂量超过1 mg/kg时,siRNA浓度升高并未进一步提高敲低效率,提示其他因素如细胞类型和递送机制对疗效有影响。
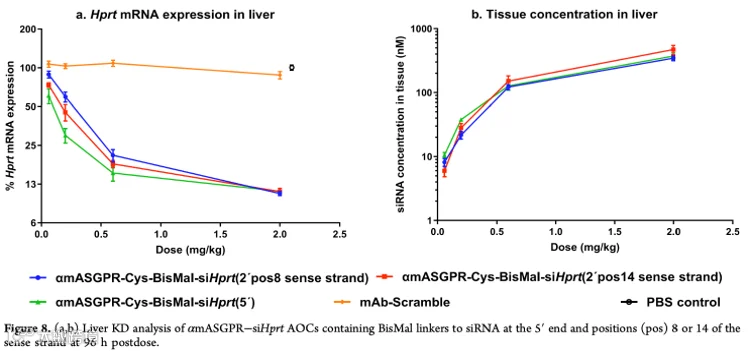
图7:连接子位于siRNA不同部位对AOC在肝脏中对相关基因敲低效果的影响 (图片来源:参考文献1)
在PMO AOC的研究中则比较了PMO在3′端和5′端的接头位置对外显子跳跃效力的影响(见图8),结果表明,尽管差异不大,3′端接头的PMO外显子跳跃效力略优于5′端接头的PMO。虽然5′端接头的PMO在组织中浓度稍高,但其效力较低,可能是由于5′端接头体积较大影响了其进入细胞核与目标前mRNA(pre-mRNA)结合的能力。
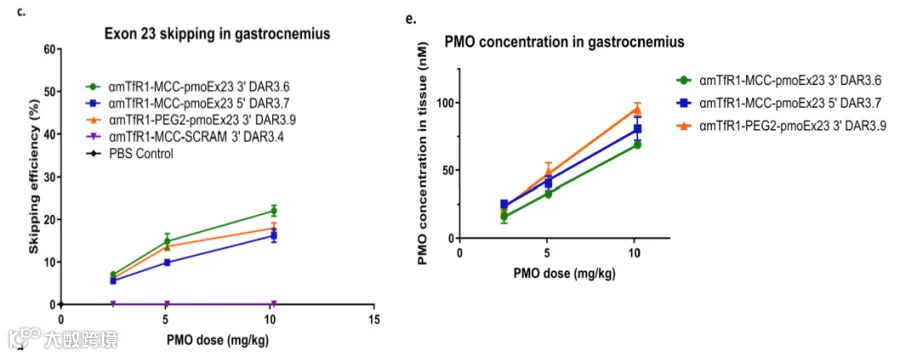
图8:PMO偶联位点对外显子跳跃效率的影响(图片来源:参考文献3)
06
PEG对AOC活性的影响
本研究还探讨了PEG对siRNA AOC活性和药代动力学的影响,PEG可以提高分子溶解度、减少非特异性蛋白结合、提供保护以减少酶的作用从而减少清除率。对比PEG位于siRNA内部或外部的AOC,PEG位置或大小对血浆PK无显著影响,但将PEG放置在siRNA外部提高了基因敲低效果并增加了肿瘤中的组织浓度,这表明PEG能增强siRNA的稳定性和亲水性(见图9a)。此外,PEG化的AOC在较低剂量下达到了与无PEG AOC更高剂量相似的组织浓度和敲低效果(见图9b)。
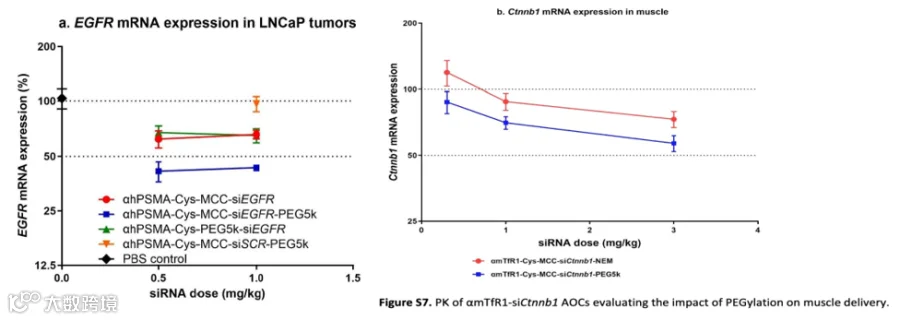
图9:PEG修饰对基因敲降效果的影响(图片来源:参考文献1)
07
siRNA生物偶联在不同抗体亚型中的适用性
研究探讨了siRNA偶联在多种亚型抗体中的适用性(见表1),结果显示,不同抗体亚型在siRNA偶联效率及DAR分布上存在差异,尤其是hIgG4生成的主要是DAR2。不同连接子的使用(如MCC和BisMal)也会影响DAR分布,尽管各抗体亚型的DAR1产率不同,但通过优化都可以获得足够的纯DAR1用于临床前研究。
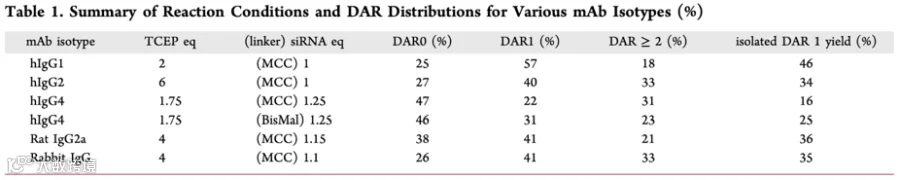
表1:各种 mAb 亚型的偶联反应条件和 DAR 分布总结 (图表来源:参考文献1)
08
总结
下表中,我们总结了PMO AOC与siRNA AOC的结构活性关系(SAR)对比表,以帮助读者快速阅读:
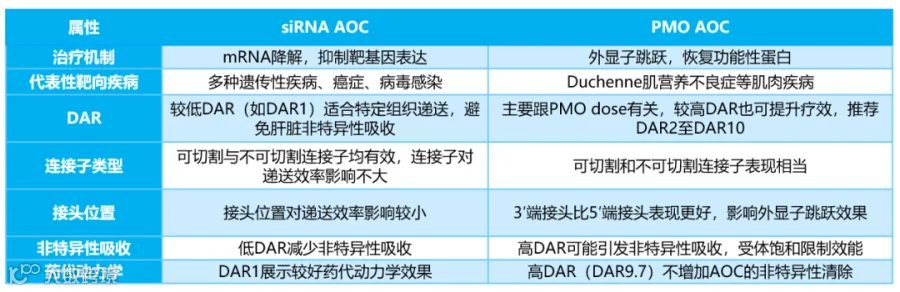
AOC策略为克服寡核苷酸药物递送障碍提供了新的思路,通过结合抗体的靶向性和寡核苷酸的基因调控功能,能够有效提升药物疗效和稳定性。未来,随着构效关系研究的进一步深入,AOC有望在基因治疗领域发挥更大的作用。
药明合联:全球领先的生物偶联药CRDMO
药明合联在生物偶联药领域的技术和经验涵盖了包括ADC在内多种多样的偶联药物,迄今已经成功交付了11000多个偶联药物分子(截止2024年6月30日)。特别值得一提的是:药明合联拥有具有自主知识产权的偶联技术:WuXiDARx™。采用该技术无需对抗体进行工程化改造,对要偶联的抗体兼容性强,工艺简单,并且根据载荷(payload)的毒性大小以及DAR值的需求,可以灵活采用WuXiDAR2™, WuXiDAR4™, 或者WuXiDAR6™技术。另外药明合联还与亚洲和美国的几家拥有创新偶联技术和/或连接子/载荷的生物技术公司达成战略合作,客户可以根据自己的项目需求不仅可以使用药明合联自己的偶联技术,还可以通过药明合联使用这些合作伙伴的创新偶联和/或连接子/载荷技术。
作为全球领先的生物偶联药CRDMO,药明合联至今已成功交付了超过400个 AOC 产品(截止2024年6月30日),我们的专业技术团队在AOC领域拥有深厚的专业知识和丰富的项目经验,了解更多AOC相关信息,请点击如下卡片。
欲了解更多关于药明合联的技术和服务能力,欢迎访问公司官网:https://wuxixdc.com
也欢迎通过如下两种方式联系我们:
Email:wuxixdc_info@wuxibiologics.com
Web:https://wuxixdc.com/contact-us/
参考文献/资料:
1. Cochran M, et al. Structure-Activity Relationship of Antibody-Oligonucleotide Conjugates: Evaluating Bioconjugation Strategies for Antibody-siRNA Conjugates for Drug Development. J Med Chem. 2024 Sep 12;67(17):14852-14867.
2. Egli M, Manoharan M. Chemistry, structure and function of approved oligonucleotide therapeutics. Nucleic Acids Res. 2023 Apr 11;51(6):2529-2573.
3. Cochran M, et al. Structure-Activity Relationship of Antibody-Oligonucleotide Conjugates: Evaluating Bioconjugation Strategies for Antibody-Phosphorodiamidate Morpholino Oligomer Conjugates for Drug Development. J Med Chem. 2024 Sep 12;67(17):14868-14884.


关于药明合联
药明合联生物技术有限公司(股票代码:2268.HK)是全球领先的生物偶联药合同研究、开发和生产企业(CRDMO),专注于提供抗体偶联药物(ADC)等生物偶联药端到端服务,涵盖抗体或其他偶联药中间体、连接子/化学有效载荷、偶联原液及制剂等研发和GMP生产领域。如需了解更多信息,请访问:www.wuxixdc.com


![[技术探析] 解码抗体-寡核苷酸偶联:探索siRNA与PMO AOC在药物开发中的生物偶联策略](https://cdn.10100.com/user/cdc0e06b2088a5534210277c7993cbc8_180x.png)