
2017年3月17日,药品审评中心公布了2016年度药品审评报告。2016年,CFDA批准了206件药品生产(上市)注册申请(中药2件、化学药品188件、生物制品16件),批准了3666件药物临床试验注册申请(中药84件、化学药品3311件、生物制品271件)。
通过对2012~2016年审评报告的对比,我们可以挖掘到生物制品行业哪些趋势?
生物制品新药数量略有增加
新药 |
进口药 |
|
2012年 |
29 |
17 |
2013年 |
12 |
3 |
2014年 |
10 |
2 |
2015年 |
14 |
8 |
2016年 |
16 |
8 |
表1 2012~2016年生物制品批准上市情况
生物制品临床试验数量大幅增加
时间 |
临床试验 |
生物等效性试验 |
2012年 |
62 |
/ |
2013年 |
49 |
0 |
2014年 |
110 |
0 |
2015年 |
88 |
/ |
2016年 |
271 |
/ |
表2 2012~2016年生物制品批准临床情况
生物制品审评正在解决积压
时间 |
新受理申请数 |
审评完成 |
2012年 |
456 |
533 |
2013年 |
526 |
408 |
2014年 |
458 |
523 |
2015年 |
567 |
543 |
2016年 |
410 |
646 |
表3 2012~2016年新申请受理与审评完成情况
2012~2015年,完成审评并呈送总局审批的注册申请与新受理申请大致相当,2016年审评加速,而申报减少。
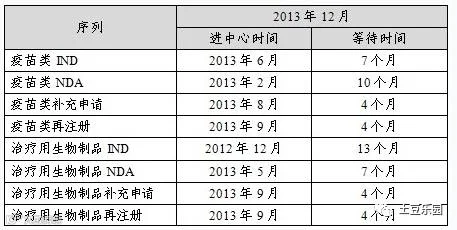
2012年,生物制品审评的时限压力很大。2013年,生物制品各审评通道的排队等待时间为4~13个月。2016年,疫苗临床试验申请已基本实现按时限审评,其他申请应该仍然存在排队现象。
2013年生物制品各审评通道启动审评情况
新受理生物制品申请较为平稳
时间 |
预防用IND |
预防用NDA |
治疗用IND |
治疗用NDA |
补充 |
进口 |
复审 |
2011年 |
27 |
5 |
100 |
24 |
259 |
3 |
9 |
2012年 |
41 |
3 |
114 |
22 |
244 |
20 |
8 |
2013年 |
40 |
17 |
173 |
24 |
261 |
11 |
6 |
2014年 |
37 |
9 |
149 |
28 |
225 |
6 |
4 |
2015年 |
57 |
8 |
175 |
27 |
283 |
10 |
6 |
2016年 |
23 |
5 |
157 |
7 |
204 |
11 |
1 |
表4 2011~2016年新申请受理情况
优先审评
2016年药审中心根据总局《关于解决药品注册申请积压实行优先审评审批的意见》(食药监药化管〔2016〕19号,以下简称19号文),共将12批193件注册申请纳入优先审评程序,其中生物制品注册申请22件,占比11.4%,远远超过药监总局国产药品数据库中生物制品1%的比例,1647件国药准字S/164490件。
优先审评理由包括:“适用于治疗因慢性肾脏病(CKD)引起的贫血,包括接受透析与未接受透析治疗的患者”、“儿童用药”、“病毒性肝炎”、“与现有治疗手段相比具有明显治疗优势”、“罕见病”等。
重要治疗领域新品种
2012年,注射用重组人凝血因子IX,用于血友病治疗。单纯从血液中提取的制品难以满足血友病的治疗,本品以重组技术开发的品种,按照优先审评程序加快审评。第一个重组人IX因子的进口注册,为我国乙型血友病患者提供了特异性治疗用药物。
2014年,Sabin株脊髓灰质炎灭活疫苗(sIPV),我国自主研发的全球首个Sabin株脊髓灰质炎灭活疫苗(单苗),填补了我国在脊髓灰质炎灭活疫苗生产领域的空白,消除了目前计划免疫规划中数千万剂使用的口服脊髓灰质炎减毒活疫苗潜在的致病危险(疫苗株或衍生株引发的相关病例),安全性更好。药审中心按特殊审批程序完成了该疫苗上市注册申请的审评,有效配合了WHO全球根除脊髓灰质炎病毒的行动计划。同时,该疫苗的批准上市,对我国乃至全球,特别是发展中国家消灭脊髓灰质炎都会产生积极的影响。
2015年,Ebola疫苗:我国自主研发的重组埃博拉疫苗,也是全球首个2014基因突变型埃博拉疫苗。药审中心按“特别审评程序”完成了该疫苗临床试验申请的审评,获得了世界卫生组织(WHO)、西非国家和国际社会的一致好评。
2015年,口服I型III型脊髓灰质炎减毒活疫苗(人二倍体细胞):WHO全球消灭脊髓灰质炎战略免疫规划推荐的常用疫苗,药审中心按照“特别审评程序”完成审评并批准了该疫苗的注册上市,为实现WHO全球消灭脊髓灰质炎战略免疫规划和相关疫苗的可获得性奠定了基础。
2015年,肠道病毒71型灭活疫苗:我国自主研发的1类新药疫苗,用于刺激机体产生抗肠道病毒71型(EV71)的免疫力,预防EV71感染所致的手足口病。药审中心按“特殊审评程序”完成了该疫苗审评并经总局批准上市,对有效降低我国儿童手足口病发病率和重症死亡率具有重要意义。
2015年,贝伐珠单抗注射液:批准用于非小细胞肺癌的一线治疗。相对于单纯接受化疗治疗,以该品种为基础的一线治疗可显著延长患者的无疾病进展生存期。该品种新扩展新适应症的批准,为肺癌患者带来了新的治疗手段。
2015年,聚乙二醇修饰干扰素:我国第一个国产上市的聚乙二醇(PEG)修饰干扰素品种,其及时完成审评并批准上市,打破了国外进口同类产品垄断中国市场的局面。
2015年,聚乙二醇化重组人粒细胞刺激因子注射液:批准用于非骨髓性癌症患者在接受易引起临床上显著的发热性中性粒细胞减少症发生的骨髓抑制性抗癌药物治疗时,降低以发热性中性粒细胞减少症为表现的感染的发生率。两家国内企业获批该产品上市,可提高患者对该药物的可获得性。
2016年,聚乙二醇干扰素α2b注射液:为重组人干扰素α2b与聚乙二醇结合形成的长效干扰素,适用于治疗慢性丙型肝炎成年患者(患者不能处于肝脏失代偿期)。该药品为我国自主研发的首个长效干扰素,可有效提高患者用药的可及性。
2016年,托珠单抗注射液:为人源化单克隆抗体,通过与具有可溶性和膜结合性的白细胞介素-6受体结合,抑制信号传导和基因激活,适用于治疗全身型幼年特发性关节炎(sJIA),可显著改善对非甾体类抗炎药及全身性糖皮质激素治疗反应不足的活动性sJIA患者的美国风湿学会评分并降低激素用量。该药品本次增加适应症,主要用于儿科患者,为我国儿科患者提供了首个疗效及安全性明确的治疗药物,解决了临床长期无药可用的问题。
2016年,13价肺炎球菌结合疫苗:为通过化学方法将肺炎球菌多糖与蛋白载体结合制备的多糖蛋白结合疫苗,将多糖的非T细胞依赖免疫转变为T细胞依赖的免疫,适用于预防6周龄至15月龄婴幼儿由13种肺炎球菌血清型引起的侵袭性疾病(包括菌血症性肺炎、脑膜炎、败血症和菌血症等)。该药品为我国首个上市的可用于婴幼儿主动免疫的13价肺炎疫苗,较7价肺炎球菌结合疫苗有更高的血清型覆盖率。
本文经“土豆乐园”微信公众号授权转载,“阅读原文”可查看原始链接 《透过审评看生物制药,2012~2016》。
2016年度药品审评报告:http://www.cde.org.cn/news.do?method=viewInfoCommon&id=313842



