导语
近几个月,药明合联(WuXi XDC)合作伙伴捷报频传,礼新医药与美国肿瘤精准疗法公司Turning Point针对Claudin 18.2创新抗体偶联药物(ADC)LM-302达成总价超10亿美元海外独家授权合作,普众发现与OnCusp Therapeutics就CDH6抗体药物偶联物达成海外许可协议,这些授权交易为中国新药出海添上了浓重的一笔,也证明了中国创新力量在ADC领域的崛起。
ADC药物为何成为近年来全球创新研发的焦点?其中又存在哪些机遇与挑战?7月29日-30日,由药明合联、多禧生物和佰傲谷BioValley共同举办的XDC及多抗新型药物全球创新峰会将在杭州举行(点击文末左下角阅读原文了解会议详情)。届时,药明合联首席执行官李锦才博士将以“国际领先的一体化XDC研发生产服务平台”为题发表精彩演讲。本文中,李锦才博士就ADC赛道面临的技术挑战进行了深入解读,更多精彩内容敬请期待会议现场报告。
ADC正处于爆发式的增长期。从2019年开始连续三年三款ADC药物被批准上市,美国、中国、欧洲企业都在加速布局ADC药物,越来越多的专注于ADC药物研发的公司相继成立,投融资和各种授权交易火热,国内外各种行业会议纷纷设置ADC的专题报告和讨论,ADC赛道已成为业界备受瞩目的焦点。
我们看到全球涌现了一批研发企业投身于ADC药物研发,致力于通过差异化的创新解决未满足的临床需求。我不认为这是一种‘泡沫现象’,主要是因为目前临床上证明了ADC药物具有很高的成药性,之前积累的一些市场需求在短时间内被释放出来了,带动了行业的爆发式增长。”
在李锦才博士看来,即便是很成熟的靶点,如果能够在连接子和小分子毒素上进行创新,都可能产生差异化的临床治疗效果。研发企业既可以选择基于已知靶点,在连接子或者毒素上进行创新,也可以选择基于成熟的连接子和毒素,在靶点上进行创新。偶联技术的出现拓宽了原有传统单抗单一的成药方式,为研发企业探索差异化创新之路提供了方向。
1. ADC药物在研发生产过程中最大的挑战?
传统上讲ADC药物的难点是:治疗窗口比较窄,往上一点,毒性太大;往下一点,效果不好。经过近些年的发展,这个方面取得了比较大的进展,很多方面的技术慢慢成熟之后治疗窗口相对比较宽了,但是这样的挑战持续存在,每一个ADC项目都要持续关注治疗窗口是不是足够宽,安全性和有效性永远都是最重要的考虑因素。从技术上确保治疗窗口相对较宽,其中一个很重要的因素就是偶联工艺要非常地稳定,做出来的产品均一性、一致性要非常高,否则会影响它的效果和安全性。这一点也是我们药明合联(WuXi XDC)能够为客户提供价值的地方,我们打造了相应的技术平台WuXiDAR4™ (DAR=4),能够帮助客户优化药物抗体比显著提升治疗窗口,提高ADC产品的均一性和DAR值的可控性。另外,在前期ADC候选药物筛选的环节上,药明合联和药明生物的其他兄弟部门合作,能够帮助客户在早期阶段做大量的优化和筛选,包括我们的高通量偶联筛选,帮助客户挑出来成功概率最高的ADC药物。
另外,ADC的工艺和生产在产业化过程中都是非常具有挑战性的。因为ADC药物是大分子和小分子的组合,工艺开发和分析的工作量非常大,大概是传统抗体的2倍。另外由于高活、高毒的特性,ADC生产对厂房设备设施也有非常严格的要求,产业化的成本相对比较高。这些挑战也是为什么ADC药物的研发生产外包比例要比普通生物药更高,因为大部分公司都没有能力完整地从头做到尾。
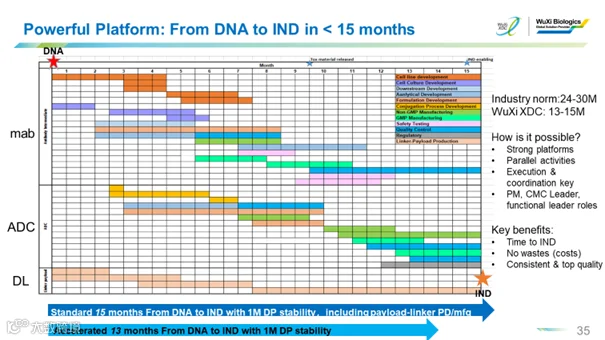
然而,通过高度集成ADC所需要的平台和技术,能够以最快的速度推进项目,这是药明合联作为专注于生物偶联药服务的CRDMO公司,对ADC行业、对客户非常重要的赋能。能够以最快的速度把项目推向临床,对做创新药的公司来说尤为重要。我们能够在200公里内提供端到端服务,完成所有的新药发现、临床前研究、CMC开发生产、临床申报,真正做到了一站式服务,简化并高效地帮助全球客户开发高质量的包括ADC在内的生物偶联药物。由于供应链的缩短和各功能块的高效整合,从蛋白质的DNA合成到ADC的临床申报(IND),药明合联一般仅需15个月即可完成,相比业界时间缩短近一半,为客户新药尽快上市提供了极大帮助。
我们有几个非常好的案例,其中一个是欧洲的初创型公司,有很好的产品线,他们在全球范围最后选择了药明合联的一体化技术平台来做这个项目。客户找到我们是因为这个项目的工艺比较独特,包括偶联后面的纯化,还涉及到用酶,整个工艺比较复杂,他们非常希望能够有一个一体化的技术平台以最快的速度把项目推进临床。后来我们用不到一年半的时间,帮助客户把这个项目成功地推向了临床,并且公司在项目仍然处于临床试验阶段的时候就被收购了。
还有一家我们从2012年左右就开始合作的客户,他们有比较独特的ADC的技术,后来也把这个分子的中国权益授权给了一家中国公司。我们帮助这两家公司分别在国内和国外同时推进项目,尤其在2021年,该项目在国内和国外的临床上都获得了非常好的数据,现在我们正在帮助客户以最快的速度将这个项目推向BLA,期待产品能够尽快在中美两地上市。
2. ADC赛道的创新和差异化?
首先从大方向来看,ADC的扎堆不像单抗那么拥挤。很多时候,我们看起来像是大家都扎堆到了几个相同的靶点上,但实际上它跟单抗的做法不太一样,即使是同一个靶点,还是完全可以做出来创新的产品。对于ADC赛道而言,创新的定义跟其他领域有所差异。主要是因为它有三个部分,抗体、连接子、毒素,这三个部分中的任何一个部分创新都可能带来临床疗效上的差异,从这个角度来说ADC创新更多元化。我们也看到众多的ADC公司在其中的一部分或多部分都有比较深度的钻研,比如聚焦于ADC靶点发现或抗体优化,或者毒素连接子的优化。
对于研发企业而言,药物研发最重要的还是要考虑临床获益。不管是新的靶点还是新的毒素、连接子,都要以终为始,考虑它最终希望达到的效果,以及可能的临床适应症,从一开始就有比较明确的方向。针对适应症的竞争也日益激烈,如何选择适应症,设计临床试验,使得产品能够尽快上市,同时避免同质化,这些也越来越重要。
在具体筛选候选药物的过程中,有很多其他的技术点需要关注,比如ADC分子是不是足够稳定,在CMC、产业化上是不是能够比较顺利地推进。当然,创新药研发要有国际化视野,考虑到未来产品可以走到国际市场。相应地,药品监管机构对于ADC药物也有多重相关法规。
3. ADC一体化平台面临什么样的挑战?
药明合联的目标是赋能客户,通过开放式、一体化的偶联制药技术平台,加速和变革全球偶联药的发现、开发和生产进程。既要保质保量又要以最快速度交付项目,其实是我们建设这个平台的挑战之一。
ADC药物涉及非常多的学科以及各种不同的技术背景,需要有完全不同的独特要求的厂房,要把这些都集中到一个公司里,这不是一件容易的事情。药明合联目前拥有三大基地,分别是位于上海的研发/工艺部、常州的小分子基地以及无锡新区的偶联原液和制剂生产基地。上海的研发基地主要负责前期研发项目和技术平台建立,如前述的WuXiDAR4™技术平台。常州的小分子基地,不仅具备催化氢化、流体化学、生物催化、化学催化等强大的技术能力,且拥有丰富的小分子研发,生产和分析方法开发的经验。无锡偶联园区负责ADC及其他偶联药物的GMP生产和灌装,拥有国际一流的生物偶联药及制剂灌装、成品制剂及工艺开发、冻干工艺优化、放大平台和GMP生产能力。质量体系符合美国FDA、欧盟EMA及中国NMPA的要求,满足临床I、II、III期及将来的商业化生产需求。


偶联药连接子及毒素研发和生产平台
此外,还有一个更大的挑战就是每一个项目都需要非常好的整合能力。每一个ADC项目在推进的过程中需要有很多不同的团队参与,做好相互之间的协调,应对各种可能会出现的技术挑战以及其他可能发生的问题。药明合联正是通过同步进行多项研发环节无缝衔接调动了不同团队之间的资源和能力,大幅缩短了项目时间。
例如,单克隆抗体的工艺开发,载荷连接子的工艺开发和ADC偶联工艺开发是同步进行的,这节省了大量的时间。这种创新做法只有在同一个质量体系下,每个功能块都拥有强大的平台技术能力,以及跨功能团队的无缝衔接和配合,才能得以真正实现。这样的无缝衔接在项目计划、项目预算阶段就充分体现了优势,也在执行过程中,尤其是遇到技术或项目进度方面的挑战时(比如新冠疫情期间),整体项目的管理,协调和相互支持等方面起到至关重要的的作用。这种高度整合、一站式的服务还在很多方面起到了成本节约的作用,比如生产批次的大小、时间等不会出现错位或因为估算不准导致的过度浪费等问题。


药明合联生物偶联药专用GMP生产平台
截至2022年4月30日,药明合联已赋能全球近200家合作伙伴加速研发和生产生物偶联药,进行和完成的各类项目高达240个,其中包括26个已提交IND的项目和8个处于II/III期临床试验的项目。
除了传统意义上的ADC药物,药明合联也提供其它新型生物偶联药的研发和生产服务,包括多肽偶联药物(PDC)、抗体寡核苷酸偶联物(AOC)、抗病毒偶联药物(AVC)、抗体-siRNA偶联物(ARC)等。正如药明合联的英文名WuXi XDC的寓意,X 代表未知和未来,以及“偶合天下药”的无限可能。
关于药明合联

- 滑动查看更多药明合联介绍 -
注:本信息不构成药明生物的信息披露或投资建议