
本期导读
抗体药物偶联物(ADCs)是一种由不同药物偶联程度组成的高异质性混合物。根据偶联位点、偶联率、连接子和药物的不同,ADC表现出不同的效价、药代动力学和毒性。从支持偶联工艺过程的开发,到鉴定非特异性偶联位点,保障工艺批次间的一致性,偶联位点分析和偶联率分析对于ADC结构表征来说至关重要,关乎到药物质量的管理。
那么,如何进行偶联位点的鉴定呢?
业内常常采用肽谱图法。这种技术通过酶解ADC分子的蛋白部分,产生一系列肽段,然后利用液相色谱-质谱(LC-MS/MS)分析这些肽段,从而确定偶联修饰的确切位置。
但由于药物偶联肽段带有完整的载荷,其MS/MS二级谱图质量较差,有时难以采集到确定偶联位点的关键特征碎片离子。
同时,疏水性载荷的存在导致偶联肽段与未偶联肽段的质谱电离效率存在差异,偶联占比的计算也可能受到影响。
目前,传统肽图方法在定性地鉴别偶联位点和定量地测量偶联率方面仍然面临挑战。

业内有偶联位点分析的新解法吗?
近期药明生物分析科学团队在Journal of Pharmaceutical and Biomedical Analysis期刊上发表了关于基于质谱技术实现抗体药物偶联体偶联位点定性定量表征的文章。
Drug deconjugation-assisted peptide mapping by LC–MS/MS to identify conjugation sites and quantify site occupancy for antibody-drug conjugates,可点击左下角【阅读原文】查看英文原文。
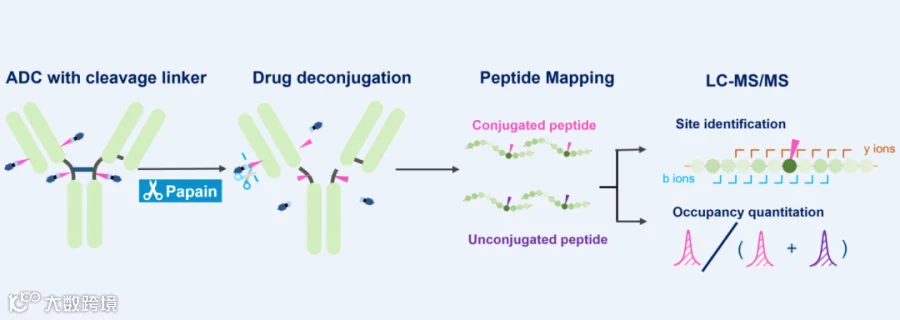
文章提出了一种简单易行的药物解偶联辅助肽图谱法,适用于含有可裂解连接子的抗体药物偶联体(ADCs)偶联位点鉴定和偶联率分析。
方法通过移除高疏水性的药物部分,显著提高了偶联肽段水平的偶联率定量准确性和肽段二级质谱碎裂质量。方法能够用于工艺开发和稳定性期间样品多个关键质量属性的追踪。
点开视频,了解药明生物分析科学团队如何为产品质量控制和申报保驾护航,加速生物药研发之旅。
1
优化样品前处理方法
上下滑动查看更多

相对于传统肽图检测方法,该方法在样品前处理过程中,引入了木瓜蛋白酶。通过将ADC样品与木瓜蛋白酶一起孵育,切割连接子-载荷药物上的酰胺键,从而降低偶联肽段的疏水性并增加肽段在质谱中的带电能力。
经过木瓜蛋白酶处理后的ADC分子再经过变性、还原、烷基化和换液后,酶解成合适长度的肽段进行LC-MS/MS检测。由于载荷药物已被木瓜蛋白酶释放,肽段的整体分子量及疏水性降低,含有连接子的肽段更容易在二级质谱上获得的关键b/y离子,更容易鉴定到偶联位点。另外,通过比较含连接子残基的偶联肽段提取离子流峰面积与偶联/非偶联肽段的总峰面积可以计算该肽段的偶联率。
连接子与载荷药物间的切割是本分析方法的第一步,也是最关键的一步。本文探索及优化了木瓜蛋白酶的酶解条件,使蛋白部分的非特异性酶切尽可能地减少,同时保证载荷药物部分被充分的切割及释放。
本方法通过优化酶解温度和底物-蛋白酶比例得到最佳条件,最大化释放载荷药物的同时几乎不引起木瓜蛋白酶的非特异性切割。在解偶联步骤后直接添加盐酸胍抑制木瓜蛋白酶的活性,让操作更加直接和简便。
2
提高偶联位点鉴定率
在本方法中,木瓜蛋白酶将较大的连接子-载荷药物切割为较小的二肽连接子残基,降低了分子量和疏水性,进一步降低质谱检测关键碎片离子的难度,提高了偶联位点鉴定率。
经过切割的连接子残基在二级质谱碎裂后往往能完整地保留在肽段上,可以被数据处理软件顺利鉴定为特定氨基酸位点上的“翻译后修饰”。此外,这种偶联切割分析方法能够区分铰链区肽上两个潜在的结合位点中的任意一个发生偶联的单偶联组分,从而实现对肽段上特定位点的偶联占有率计算。
3
提高位点偶联率定量精度
通过连续三天对同一ADC样品采用偶联切割分析方法分别制备三次,并采用LC-MS/MS进行分析。对比所有9次实验结果,发现结合水平的日内和日间精密度标准偏差均在3.5%以内,这体现了该方法具有较高的精密度。根据ADC产品的结构对称性,通过将总和结合水平倍乘,可计算出所有日间样品的平均DAR值为4.40,所有样品DAR值的标准偏差为 0.8%。DAR值与标准HIC-UV方法测得的结果 (4.28) 相差仅2.8%,比例非常接近。
4
该解法在多质量属性监控中的应用
上下滑动查看更多

使用分析工具监测在加速条件下ADC产品质量的变化对深入理解分子质量属性至关重要。而这种能够在一次分析中提供多个属性信息的方法,有潜力替代多个并行测试,简化分析过程并加速产品开发进度。
本分析方法可以用于分析热加速条件下ADC样品来监测多种质量属性的变化,包括位点偶联率、DAR、连接子水解率和其他翻译后修饰变化。我们将模型 ADC 样品在40℃下进行 总计14天的热加速处理。将第 0、1、3、7 和 14 天的样品与对照样品进行对比,可发现偶联位点占有率和平均 DAR 值没有显著变化,结合位点LC: Cys214、HC: Cys223和HC: Cys229处的连接子的琥珀酰亚胺逐渐开环水解,同时发现铰链区HC: Cys232处的连接子水解率则几乎没有变化。本结果与先前的研究具有一致性。
同时,分析方法也可以保证良好的模型 ADC样品的序列覆盖率,其中重链覆盖率达到99.6%,轻链覆盖率达到100%,仅有一个亲水性短肽(HC:324CK325)未被覆盖。在保证良好序列覆盖度的前提下,该方法也可同步用于翻译后修饰的监控,如脱酰胺化,氧化,蛋白N端谷氨酰胺环化等。
5
结语
综上,运用木瓜蛋白酶酶解偶联切割分析方法,能够显著提高偶联位点的鉴定能力,提高位点偶联率定量的准确性,力保产品质量。
对于该方法来说,连接子类型和载荷药物的结构理解以及对ADC解偶联条件的优化都至关重要。此外,该方法仅使用便于应用的常见试剂,操作更加方便快捷,还可同时用于监测多个ADC质量属性。实际上,任何一种可裂解连接子的裂解机制都能用于载荷药物的释放。通过释放载荷药物部分,有助于我们更准确地分析位点偶联率并鉴定偶联位点。
随着越来越多含可裂解连接子的ADC进入市场或临床试验阶段,我们相信偶联切割分析方法作为一种创新解法,通过提供详细且特定的偶联位点,帮助ADC的发现、工艺开发和质量控制,赋能合作伙伴高质量加速产品落地。

关于药明生物质谱卓越中心
(Mass Spectrometry CoE)
结构表征研究是生物制药产品质量研究和质量标准制定的前提及基础。质谱卓越中心经过多年潜心打磨,打造了一个国际级领先水平的生物制药质谱结构表征平台。结构表征研究是生物制药产品质量研究和质量标准制定的前提及基础。凭借丰富的质谱经验和先进的仪器,专注于对行业内难点问题进行探索和攻坚,在ADC偶联位点鉴定和准确定量,复杂分子二硫键链接鉴定,序列变异体深度分析,复杂O糖糖型分析及位点鉴定,CIEF-MS/CZE-MS电荷异质性在线分析,残留蛋白高灵敏度PRM-MS定量分析等技术研究上处于国际领先水平,并能为客户提供专业的解决方案。
中心迄今已完成超过700种治疗性蛋白分子的分析支持,为包括单抗、双抗、融合蛋白、酶、抗体偶联药物、疫苗和多肽类药物等多种分子提供全套质谱测试技术平台,助力医药早期发现,工艺开发和各期临床研究,高效高质赋能客户,提供一站式解决方案。
如果您对药明生物分析科学服务感兴趣,
欢迎扫描下方二维码填写
我们的工作人员会尽快联系您





关于药明生物
药明生物(股票代码:2269.HK)是一家全球领先的合同研究、开发和生产(CRDMO)公司。公司通过开放式、一体化生物制药能力和技术赋能平台,提供全方位的端到端服务,帮助合作伙伴发现、开发及生产生物药,实现从概念到商业化生产的全过程,加速全球生物药研发进程,降低研发成本,造福病患。
药明生物在中国、美国、爱尔兰、德国和新加坡拥有超过12000名员工。通过药明生物的专业服务团队,以及先进技术和精深洞见,公司为客户提供高效经济的生物药解决方案。截至2024年6月底,药明生物帮助客户研发和生产的综合项目高达742个,其中包括16个商业化生产项目(不包括8个新冠项目和1个非活跃项目)。
药明生物将环境、社会和治理(ESG)视为业务发展和企业精神的重要组成部分,并致力于成为全球生物药CRDMO领域的ESG领导者,例如应用更绿色环保的新一代生物制药技术和能源等引领行业发展。公司成立了由首席执行官领导的ESG委员会,全面落实ESG战略并践行可持续性发展承诺。更多信息,请访问:www.wuxibiologics.com。


媒体关系 PR@wuxibiologics.com
业务垂询 info@wuxibiologics.com






