1.CUT技术的前世今生
2017年1月,来自美国Fred Hutchinson癌症研究中心的Steven Henikoff 团队,使用微球菌核酸酶(Micrococcal Nuclease)MNase进行染色质切割,替代了ChIP-seq中的超声打断,开发了CUT&RUN技术。(Skene et al., 2017)
2018年4月,研究人员继续改进CUT&RUN,使用洋地黄皂苷(Digitonin)对细胞膜进行“打孔”,从而可以无需提前分离细胞核 (Skene et al., 2018)。
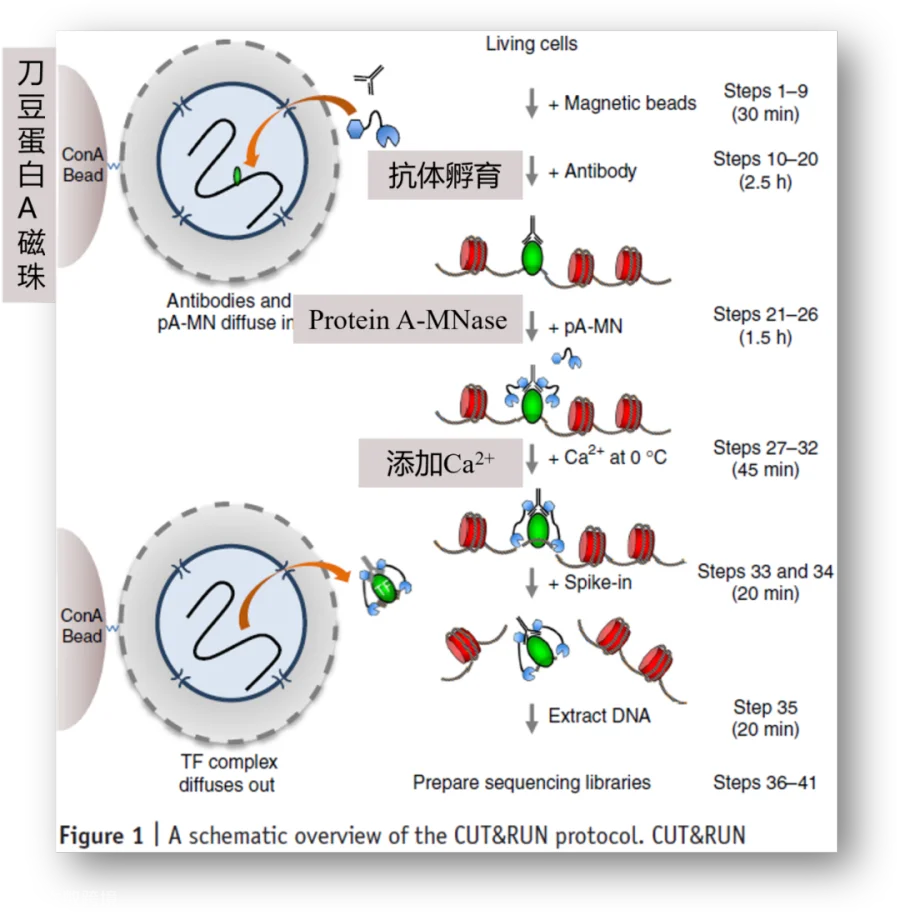
2. CUT&Tag问世
2019 年4月 Steven Henikoff 团队在 Nature Communications 杂志上发表了题为“CUT&Tag for efficient epigenomic profiling of small samples and single cells” 的论文,第一次提出了 CUT&Tag 方法。
这种方法用来研究蛋白质与DNA相互作用的技术,利用Tn5转座酶的特点,在切割染色质的同时直接插入接头,极大地缩减了建库时间,且对样本量要求更低,所需测序深度也更低。

Nature曾发文, 表示CUT&Tag是最具有发展前景的新技术之一,作者重点指出了 CUT&Tag技术有望揭示在胚胎发育的过程中,基因组结构和染色质修饰如何决定细胞命运。
3. CUT&Tag技术原理
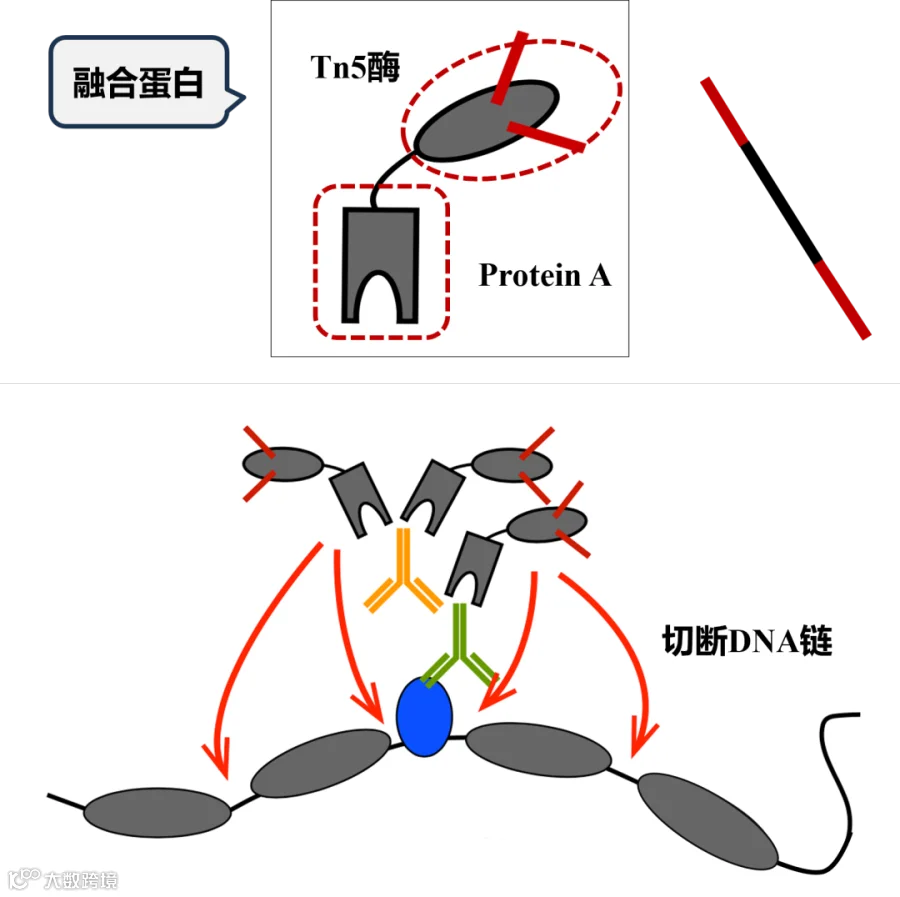
用基因工程改造方法做出来的结合了ProteinA和Tn5转座酶这两种蛋白质的功能的融合蛋白是实验的核心。
在这个融合蛋白中ProteinA的部分是负责实验中的一抗和二抗结合,也就是负责把Tn5酶拉到目标蛋白质所吸附的染色质DNA位置附近。
Tn5的部分则执行转座酶的功能,切断附近的DNA链。并且这个Tn5酶是被事先结合好了标签DNA序列的,所以被Tn5酶切断的染色质DNA片段会被加上标签DNA序列,并且因为切下来的DNA片段两端已经带了标签DNA序列,它就很容易被PCR扩增,再进一步加上建库接头,成为后面深度测序的文库,被用于深度测序(Kaya-Okur et al., 2019)。
4. CUT&Tag实验流程
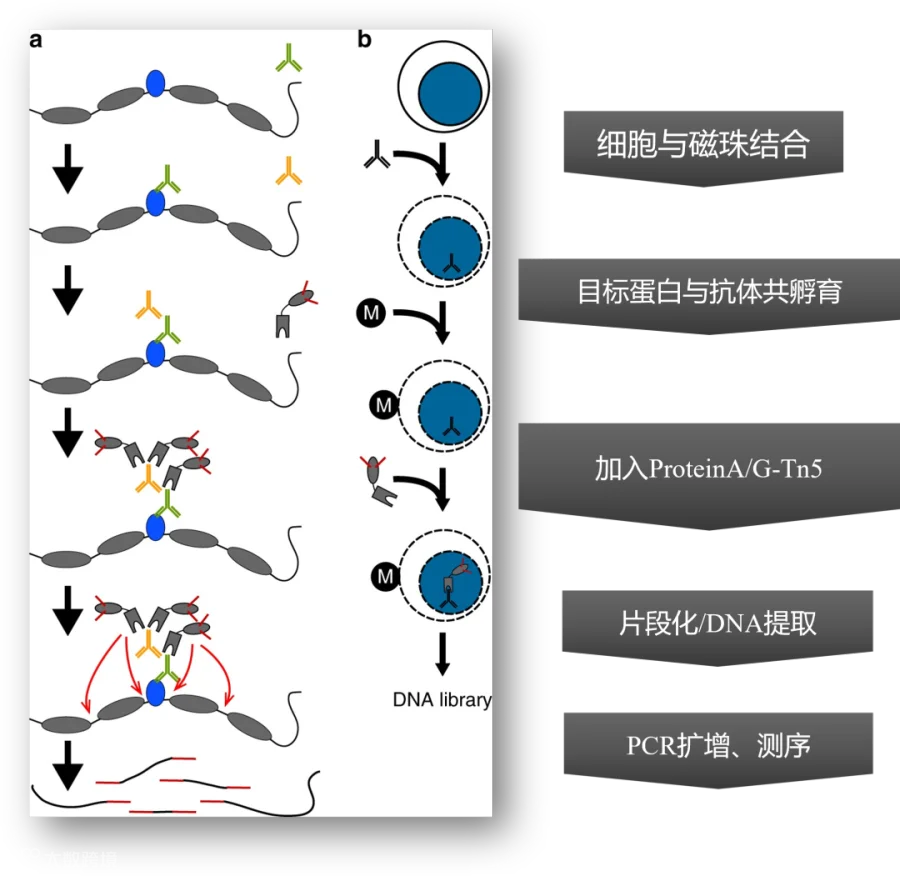
(1)利用刀豆素A包被的磁珠(ConA磁珠)与细胞结合,从而捕获细胞,刀豆蛋白A是一种凝集素,它可以粘住细胞,之所以实验中要用刀豆蛋白A的磁珠来粘住细胞,原因是在整个实验的多步反应中,要做多步的孵育和清洗,利用磁珠吸附细胞,可以使回收细胞的操作变得方便。
(2)细胞膜和核膜做通透化处理,透化的目的是让细胞膜和核膜产生小洞,这可以让后面要用到的酶和抗体等物质进入细胞核。
(3)加入针对目标蛋白的一抗,这个一抗会透过细胞膜和核膜进入细胞核,然后就可以结合在目标蛋白上。然后再加上二抗,二抗结合在一抗上,加入二抗的目的是为了放大信号。
(4)接下来,加入ProteinA和Tn5转座酶的融合蛋白,其中ProteinA结合到抗体上包括之前的一抗和二抗,这样目标蛋白结合到它识别的染色质DNA序列上,抗体结合到目标蛋白,ProteinA结合到抗体,ProteinA又连着Tn5酶,这样Tn5酶就出现在了被目标蛋白吸附的染色质DNA序列的旁边;
(5)再接下来加入Mg离子,Mg离子能够激活Tn5转座酶的酶活性,于是Tn5转座酶切断DNA链,并且在切断的DNA链的两端加上标签序列,最后把核酸抽提出来,对有标签序列的DNA片段进行PCR扩增,然后进行高通量测序(Kaya-Okur et al., 2019)。
5.ChIP-seq技术原理
首先通过染色质免疫共沉淀技术(ChIP)特异性地富集目的蛋白结合的DNA片段,并对其进行纯化与文库构建;然后对富集得到的DNA片段进行高通量测序。通过将获得的数百万条序列标签精确定位到基因组上,从而获得全基因组范围内与组蛋白、转录因子等互作的DNA区段信息。
6. ChIP-seq实验流程
(1)甲醛交联整个细胞系(组织),即将目标蛋白与染色质连结起来;
(2)分离基因组DNA,并用超声波将其打断成一定长度的小片段;
(3)设置分组:严格的ChIP实验包括三组,实验组以及两个对照(input-DNA和IgG-control),分别为阳性对照和阴性对照
(4)添加与目标蛋白质特异的抗体,该抗体与目标蛋白形成免疫沉淀免疫结合复合体;
(5)去交联,纯化DNA即得到染色质免疫沉淀的DNA样本,准备测序;
(6)将准备好的文库进行高通量测序。
7. CUT&Tag与ChIP-seq优势对比
ChIP-Seq(Chromatin Immunoprecipitation Sequencing)因能真实、完整地反映靶蛋白与DNA序列的结合情况,因而成为研究DNA-蛋白相互作用的经典方法。但ChIP-Seq继承了ChIP的难点与局限性:需要大量细胞投入(100万左右),甲醛交联易导致假阳性或假阴性,整体实验步骤复杂耗时长,测序数据背景信号高等,这些难点使得研究变得较为困难。
与传统的ChIP-seq相比,CUT&Tag技术优势明显:
(1)无需免疫共沉淀和超声破碎,一般不需要甲醛交联,因此细胞起始量低;
(2)性价比高:背景噪音低、信噪比高,所需测序深度少;
(3)实验重复结果一致性好,peak-calling的效率更高;
(4)使用Tn5转座酶代替传统的超声打断,靶向性更强。

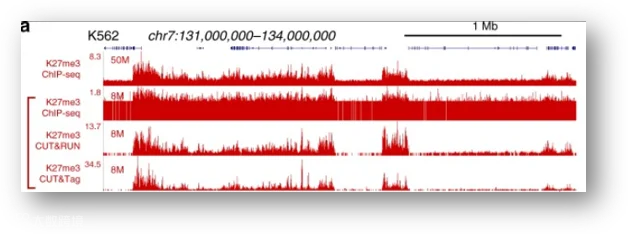
从测序结果来看,显示的是ChIP-seq/CUT&RUN/CUT&Tag三种方法得到蛋白与染色质结合峰的比较,第一行是ChIP-seq方法测序深度达到50M reads的时候,reads在这一段染色质上的覆盖情况,第二行还是ChIP-seq的方法,但是测序深度下调到8M reads的情况,第三行和第四行分别是CUT&RUN/CUT&Tag这两种方法测序深度,各测8M reads的情况,横轴是把这3M的染色质展开;
每张图中,峰的高低是覆盖在相应位置上resds数量的多少,一个位置覆盖的reads数目越多,峰越高,峰所在的位置也就是目标蛋白吸附的染色质的位置;
从图中可以看出,峰所在的染色质的位置是高度一致的,也就是说三种方法测到的蛋白质吸附的染色质位置是一致的,另一方面,当取8M reads的测序深度的时候,ChIP-seq方法的背景很高,ChIP-seq要把测序深度提高到50M reads,信号才能看得比较明显,而CUT&Tag在8M reads的时候背景信号已经很低,这说明CUT&Tag的信噪比要比ChIP-seq更高。
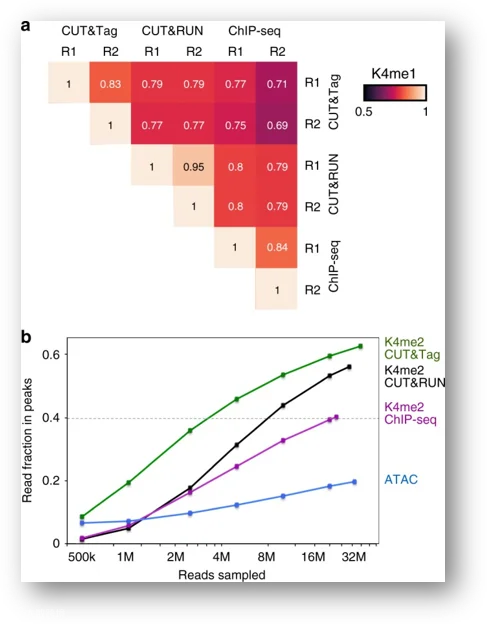
相关性热图表明,CUT&Tag的两个重复样品表现出更高的组内相关性;从peak calling可以看出,在测序数据量相同的情况下,CUT&Tag的peak Region内的数据量更多,信号更强。
8. 送样指南
新鲜细胞
(1)按照上述细胞数量要求转移适量细胞至1.5 mL离心管;
(2)使用封口膜封好离心管,用碎冰保持管周边温度在4℃左右,迅速送至公司。
冻存细胞
(1)根据计数结果,使用冻存液重悬细胞沉淀,因解冻过程有损失,故每个冻存管中要求细胞数量大于50,000-80,000个,数量以我司解冻后计数为准;
(2)把冻存管放到程序降温盒内,再把程序降温盒放到-80℃的冰箱里,以保护细胞不被损伤(无程序降温盒的老师可以用梯度降温流程代替);
(3)-80℃降温24h 后,即可使用干冰运输。(细胞冻存液配方:90%胎牛血清+10%DMSO)
动物组织
(1)取下新鲜组织,立即剔除结缔组织和脂肪等杂质;
(2)用预冷的 PBS 溶液漂洗,将组织表面的血渍冲洗干净;
(3)如果组织体积较大,将组织切成长宽高均≤0.5cm 的小块;
(4)将处理好的组织样本混合均匀后保存于 1.5ml 离心管中,每管 20mg-40mg 左右(每个样本分装 2 管);
(5) 迅速置于液氮中速冻,然后转移至-80℃冰箱中保存;
(6)为确保实验的顺利,建议样品备份 1-2 份,以防部分样品降解重新取材、制备或送样。
(7)运送方式:将冻存管置于密封性好的塑料袋中,用胶布缠到冰袋上,并在泡沫盒中装入足量的干冰,进行运输。
植物组织
(1)从植物体上,取下新鲜组织。取材后需用清水将材料表面的灰尘或泥土冲洗干净,吸干;
(2)如果组织体积较大,应在冰上将组织剪切成小块或薄片,然后放入 1.5ml 离心管中,每管50mg 左右每个样本分装 2 管),准确标记样品名称;
(3)迅速置于液氮速冻,然后转移至-80℃冰箱长期保存;
(4)为确保实验的顺利,建议样品备份 1-2 份。
注意事项
送样前,尤其寄送新鲜细胞时,请提前与销售人员沟通。
参考文献:
Skene, P., Henikoff, J. & Henikoff, S. Targeted in situ genome-wide profiling with high efficiency for low cell numbers. Nat Protoc 13, 1006–1019 (2018).
Michael P Meers, Terri D Bryson, Jorja G Henikoff, Steven Henikoff (2019) Improved CUT&RUN chromatin profiling tools eLife 8:e46314
aya-Okur, H.S., Janssens, D.H., Henikoff, J.G. et al. Efficient low-cost chromatin profiling with CUT&Tag. Nat Protoc 15, 3264–3283 (2020).
Kaya-Okur, H.S., Wu, S.J., Codomo, C.A. et al. CUT&Tag for efficient epigenomic profiling of small samples and single cells. Nat Commun 10, 1930 (2019).
Seven technologies to watch in 2023.PMID: 36690758 DOI: 10.1038/d41586-023-00178-y.
Methods for ChIP-seq analysis: A practical workflow and advanced applications .PMID: 32240773 DOI: 10.1016/j.ymeth.2020.03.005.

领克生物致力于新一代高通量测序技术(NGS)的应用和推广、生信分析、临床辅助诊断、产前检测、转化医学研究等领域。
业务包括单细胞多组学测序、基因组重测序、外显子测序、WGBS、RRBS、转录组测序、LncRNA测序、miRNA测序、ATAC-seq、CUT&Tag、Hi-C、4C-seq、m6A测序等前沿技术服务、各类组学数据的个性化分析服务以及临床疾病的辅助诊断、产前检测等。

欢迎咨询了解~
电话:0871-65399960
邮箱:service@biolinker.com



