
导语

肺癌(Lung cancer)是世界上最常见和最致命的癌症,非小细胞癌(Non-small cell lung cancer,NSCLC)约占所有肺癌的85%。大约90%的肺癌死亡是由肿瘤转移引起的。肿瘤来源的外泌体可能通过传递转移相关分子来潜在地促进肿瘤转移。然而,外泌体长链非编码RNA (lncRNA)在肺癌转移中的作用和潜在机制仍不清楚。因此需要研究清楚肺癌转移的潜在机制,寻找癌症诊断和治疗的早期生物标志物。
2023年10月台湾国立成功大学医学院临床医学研究所的研究者在期刊Journal Of Experimental & Clinical Cancer Research (11.3/Q1)上发表了文章“Exosomal long noncoding RNA MLETA1 promotes tumor progression and metastasis by regulating the miR-186-5p/EGFR and miR-497-5p/IGF1R axes in non-small cell lung cancer”。该研究通过外泌体LncRNA测序(LncRNA-seq)用于鉴定长链非编码RNA,采用Western blot、qRT-PCR等方法研究发现lnc-MLETA1是一种重要的外泌体lncRNA,可在肺癌细胞中介导串扰,促进癌细胞转移;可能作为肺癌诊断和治疗的预后生物标志物和潜在的治疗靶点。


外泌体lncRN-seq实验设计

样本:人肺腺癌细胞CL1-0和CL1-5
测序:外泌体LncRNA-seq,Illumina NovaSeq 6000,PE150

文章研究思路

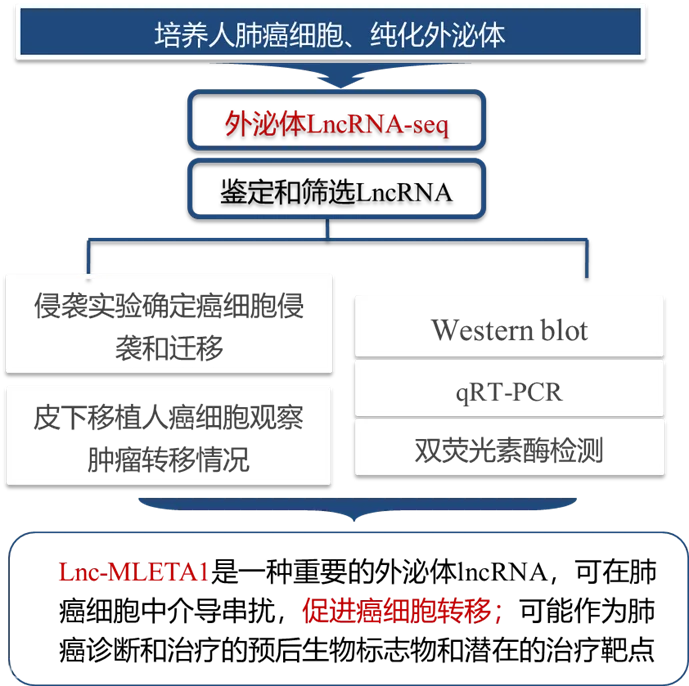

主要结果

一、lnc-MLETA1在体外促进肺癌细胞的迁移和侵袭
近年来,许多研究表明外泌体miRNA能够促进肿瘤转移[1-2]。然而,外泌体lncRNAs对细胞运动和肿瘤转移的影响尚不清楚。因此,作者试图来探索外泌体lncRNAs是否可以改变肺癌细胞的运动。
为了鉴定外泌体中可能在细胞运动中起作用的lncRNA,制作者对CL1-0和CL1-5外泌体进行了LncRNA测序。结果表明,与CL1-0外泌体相比,一种新的lncRNA ENST00000563763在CL1-5外泌体中表达上调,将其命名为lnc-MLETA1(转移性肺癌细胞衍生的外泌体传递LncRNA 1)。
接下来,作者使用qRT-PCR分析确认了几种lncRNA在CL1-0和CL1-5细胞及其外泌体中的表达。结果显示,与CL1-0细胞和外泌体相比,lnc-MLETA1在CL1-5细胞和外泌体中的表达最高。此外,通过qRT-PCR分析比较了lnc-MLETA1在低转移性和高转移性肺癌细胞中的表达,发现Lnc-MLETA1在高转移性肺癌细胞中的表达显著上调,表明lnc-MLETA1可能与迁移和侵袭能力有关。
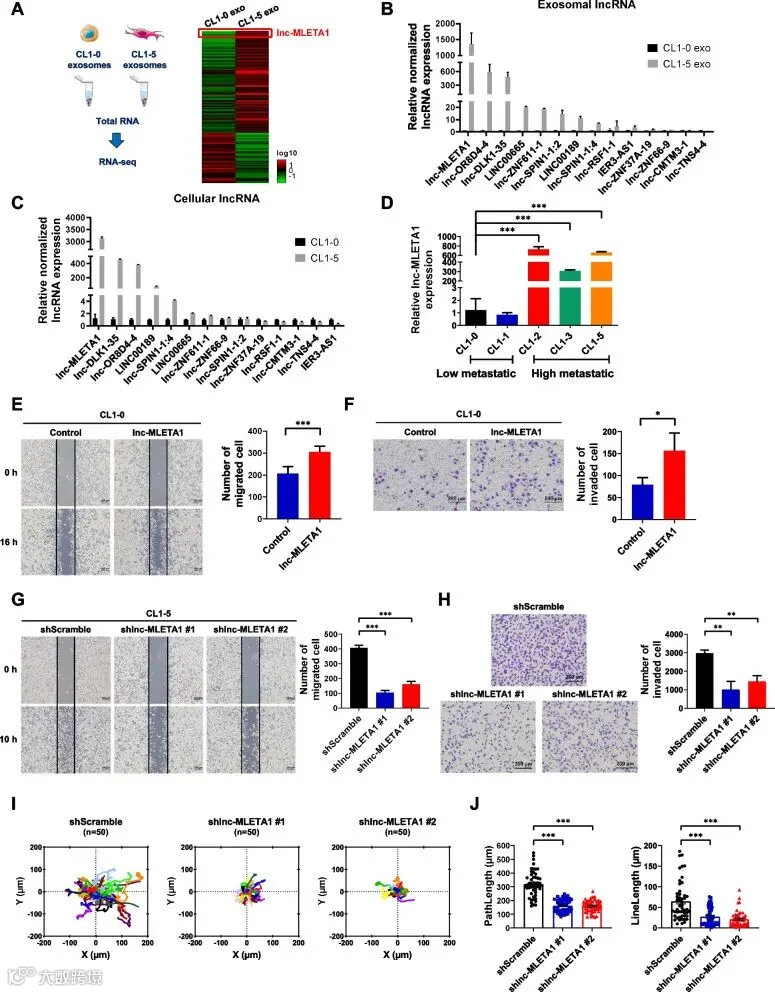
Fig1.lnc-MLETA1 promotes migration and invasion of lung cancer cells in vitro
二、lnc-MLETA1通过miR-186-5p-EGFR和miR-497-5p-IGF1R轴促进细胞运动
为了探索lnc-MLETA1介导的细胞运动的潜在机制,作者对lnc-MLETA1敲低和对照组CL1-5细胞进行了RNA测序。热图显示在778个差异表达基因中,前50个基因增加和减少最多。与对照组CL1-5细胞相比,lnc- MLETA1敲低的细胞中有315个基因上调,463个基因下调。
为了进一步阐明lnc-MLETA1对全局转移相关基因变化的影响,作者对lnc-MLETA1敲低的CL1-5细胞进行了基因集富集分析(Gene set enrichment analysis,GSEA)。结果表明lnc-MLETA1参与转移过程并调控转移相关基因的表达。此外,GSEA结果显示miR-186-5p和miR-497-5p的靶基因特征在下调基因中显著富集,表明lnc-MLETA1调节miR-186-5p和miR-497-5p靶基因的表达,可能肿瘤支持转移。
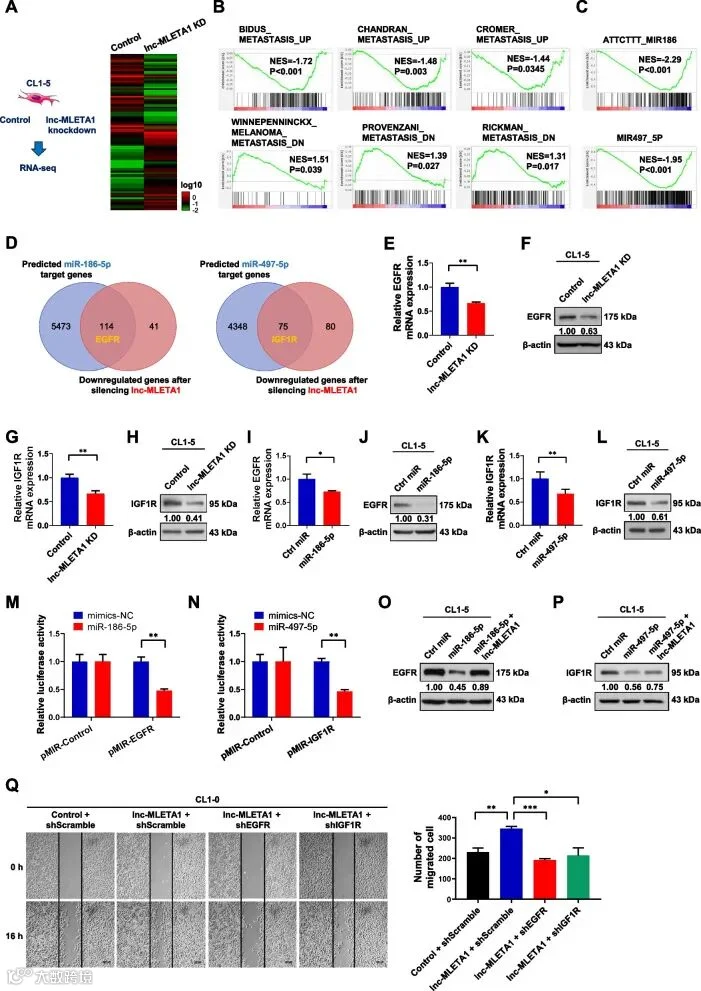
Fig2. lnc-MLETA1 promotes cell motility through the miR-186-5p-EGFR and miR-497-5p-IGF1R axis.

总结

综上所述,作者发现新的lncRNA——lnc-MLETA1,它在高度转移癌细胞及其外泌体中表达上调,过表达促进癌细胞迁移,相反,敲低lnc-MLETA1会减弱肺癌细胞的运动和转移。机制上,lnc-MLETA1通过海绵化miR-186-5p和miR-497-5p促进癌细胞运动,调节EGFR(表皮生长因子受体基因(原癌基因))和IGF1R(胰岛素样生长因子1受体)的表达。研究结果表明,lnc-MLETA1在肺癌转移中起着至关重要的作用,可能作为肺癌诊断和预后的生物标志物和肺癌治疗的潜在靶点。
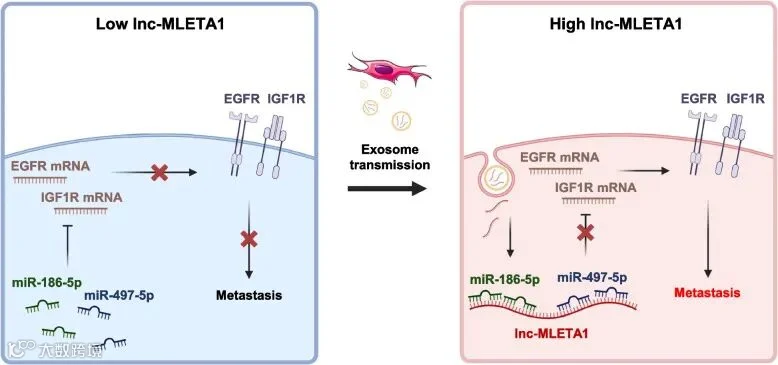
Fig5.Schematic diagram of lnc-MLETA1-based regulatory mechanism in lung cancer metastasis

参考文献

Rodrigues G, Hoshino A, Kenific CM, Matei IR, Steiner L, Freitas D, et al. Tumour exosomal CEMIP protein promotes cancer cell colonization in brain metastasis. Nat Cell Biol. 2019;21(11):1403–12.
Yang B, Feng X, Liu H, Tong R, Wu J, Li C, et al. High-metastatic cancer cells derived exosomal miR92a-3p promotes epithelial-mesenchymal transition and metastasis of low-metastatic cancer cells by regulating PTEN/Akt pathway in hepatocellular carcinoma. Oncogene. 2020;39(42):6529–43.

领克生物致力于新一代高通量测序技术(NGS)的应用和推广、生信分析、临床辅助诊断、产前检测、转化医学研究等领域。
业务包括单细胞多组学测序、基因组重测序、外显子测序、WGBS、RRBS、转录组测序、LncRNA测序、miRNA测序、ATAC-seq、CUT&Tag、Hi-C、4C-seq、m6A测序等前沿技术服务、各类组学数据的个性化分析服务以及临床疾病的辅助诊断、产前检测等。

欢迎咨询了解~
电话:0871-65399960
邮箱:service@biolinker.com


