导语
近年来,间歇性禁食(Intermittent Fasting)方案在全球愈发流行。此前研究显示禁食可改善肠道、肌肉和造血系统等体细胞干细胞功能,但对皮肤等外周组织的影响未知。而且,间歇性禁食导致身体生理变化,这些变化如何传递到外周组织以及特定生态位成分是否影响干细胞命运也大多未知。此外,成体干细胞代谢特性独特,其在禁食时的反应机制也不明确。
皮肤中的毛囊由毛囊干细胞(Hair Follicle Stem Cells,HFSC)周期性激活驱动生长、退行和休止,形成毛发。临床观察发现,极低热量饮食减肥患者可能脱发,但现代间歇性禁食方案对毛囊再生和毛发生长的影响不明,而HFSCs行为明确且毛发可见,使毛囊成为研究间歇性禁食对体细胞干细胞和组织生物学影响的理想系统。
2024年12月研究人员在期刊CELL(IF=45.5)上发表题为“Intermittent fasting triggers interorgan communication to suppress hair follicle regeneration”的文章。该研究揭示了间歇性禁食对组织再生的抑制作用,并确定了在营养供应不稳定期间消除激活的 HFSC 并停止组织再生的器官间通讯。

一、实验设计
1. 动物实验:实验动物选用 C57BL/6J、K15CrePGR、AdipoQ CreERT 等多种基因编辑小鼠,3 - 10 周龄成年雌雄小鼠,饲养于特定无菌环境。
(1)间歇性禁食方案:限时喂养16/8 TRF(Time-Restricted Feeding)组每天 8 小时进食、16 小时禁食;ADF(Alternate-Day Fasting) 组 24 小时禁食与 24 小时进食交替,AL(Ad Libitum)组为对照。从特定时间点开始对小鼠实施,持续观察至156天(P156),期间监测小鼠毛发再生、食物摄入及代谢状态等。
(2)细胞层面操作:通过 EdU(5-ethynyl-2′-deoxyuridine)注射标记增殖 HFSCs,观察其激活与凋亡;利用荧光激活细胞分选(Hluorescence-Activated Cell Sorting,FACS)技术分离不同状态 HFSCs 及表皮干细胞(Including Epidermal Stem Cells,EpiSCs),进行基因表达分析;
(3)采用基因敲除小鼠(如 K15CrePGR;TSC2、AdipoQ CreER;Atgl fl/fl、Lhx2CreER;Cpt1a fl/fl 等)研究特定基因在禁食诱导 HFSCs 凋亡中的作用;还进行了肾上腺切除术、交感神经消融等手术操作,并配合相应药物处理(如 6 - 羟多巴胺、肾上腺素、皮质酮、维生素 E、CB - 839 等),以探究不同因素对毛囊再生的影响机制。
(4)检测方法:运用苏木精-伊红(Hematoxylin and Eosin,H&E)染色观察毛囊形态;免疫组织化学法检测多种蛋白表达;采用代谢笼分析小鼠代谢状态;进行葡萄糖耐量测试评估代谢健康;利用透射电子显微镜观察 HFSCs 超微结构;通过气相色谱-质谱法分析脂肪细胞脂肪酸组成;测量激素、血糖及游离脂肪酸(FFAs)水平;运用 MitoSox 和 TMRM 检测线粒体活性氧(Reactive Oxygen Species,ROS)及膜电位;采用 Annexin V - FITC / DAPI 检测细胞凋亡;结合 RNA - seq 及相关生物信息学分析研究基因表达变化。
2. 人体实验
(1)实验对象:招募 49 名 18 - 60 岁健康东亚华裔成年人,男女皆有,无特定疾病及用药史等。
(2)实验分组与干预:随机分为正常饮食(ND)、18/6 限时饮食(TRD)和能量限制饮食(ERD)三组,分别给予相应饮食方案,持续 12 天左右,期间监测血糖等代谢指标。
(3)检测指标:在实验前后刮取头皮特定区域毛发,测量毛发长度、直径及密度以评估毛发生长变化;采集血清样本检测血脂、C 肽等代谢指标。
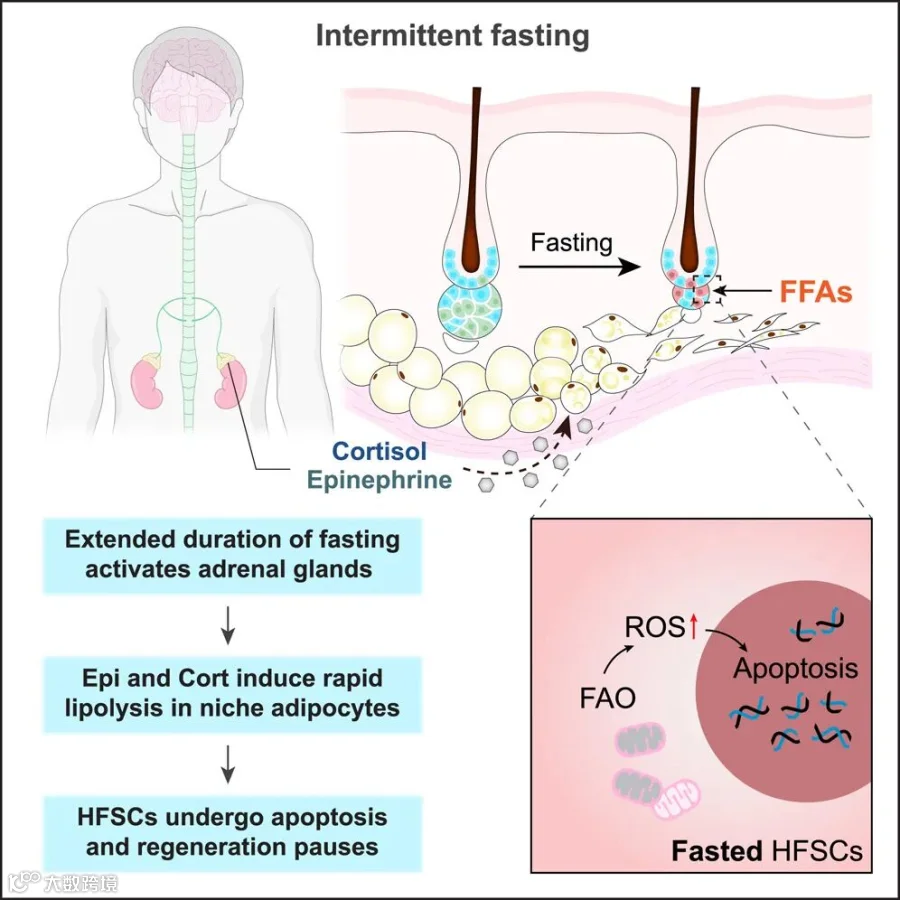
二、主要结果
1. 间歇性禁食抑制毛囊再生
采用 16/8 限时喂养(TRF)和隔日禁食(ADF)两种方案对成年 C57BL/6 小鼠进行处理,从出生后第 60 天(P60)开始,此时小鼠背部皮肤毛囊处于休止期。实验期间小鼠剃毛后持续观察至 P156,发现与自由进食(AL)组相比,TRF 和 ADF 组小鼠毛囊再生明显受损,毛发仅部分再生,组织学染色显示其毛囊停滞于休止期/早期生长期。同时,代谢笼监测表明禁食方案有效执行,且间歇性禁食小鼠葡萄糖耐量增强,体现出其虽对毛囊再生有抑制作用,但在代谢方面存在益处。
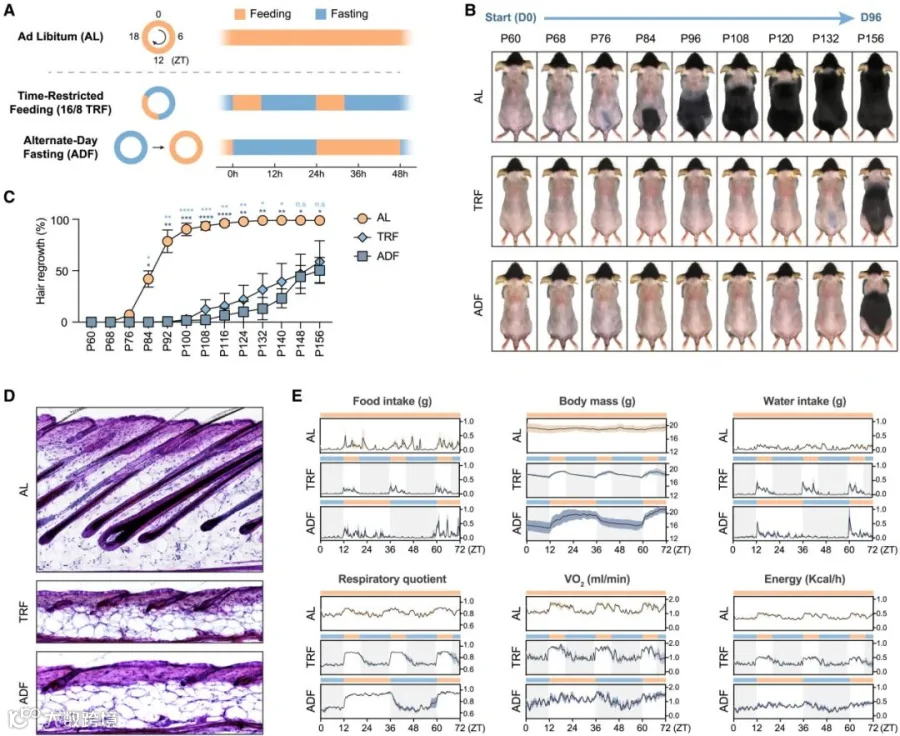
Figure 1 Intermittent fasting inhibits hair follicle regeneration
2. 间歇性禁食选择性诱导活化HFSCs凋亡
作者研究发现间歇性禁食并不抑制 HFSCs 的激活,但会选择性诱导激活的 HFSCs 凋亡。在 ADF 方案下,小鼠毛囊干细胞在禁食期凋亡增加,在喂食期又有新的激活,如此反复导致毛囊生长受抑;通过标记追踪实验表明,凋亡的 HFSCs 多为之前激活的细胞,且 ADF 使激活的 HFSCs 大量减少。人工激活毛囊干细胞后再实施 ADF,凋亡的 HFSCs 增多,毛囊再生延迟。长期(8 个月)实施间歇性禁食(TRF)会导致小鼠背部皮肤部分区域秃发,HFSCs 数量、毛囊长度及 HFSCs 区域大小均显著降低。总之,间歇性禁食使 HFSCs 经历激活与凋亡循环,短期影响毛囊再生进程,长期则造成 HFSCs 缺失和毛囊退化。
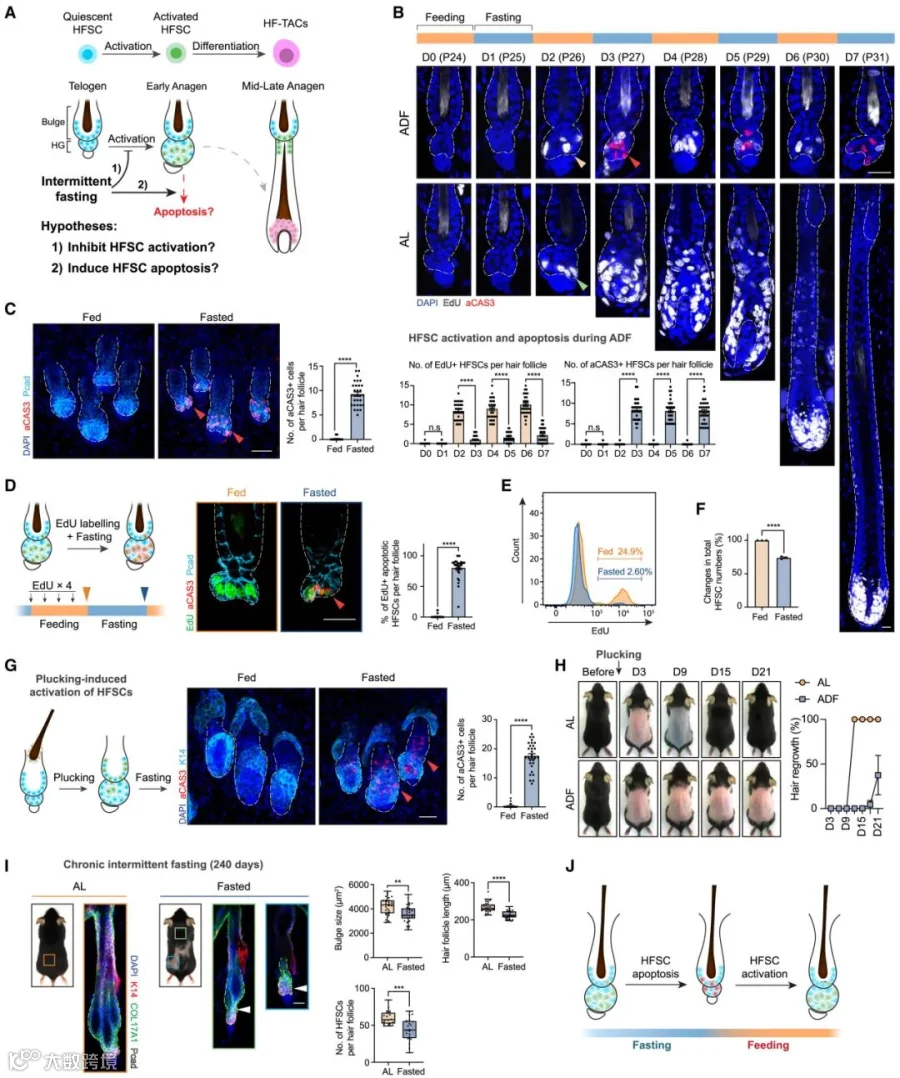
Figure 2 Intermittent fasting induces apoptosis in activated HFSCs
3. 延长禁食时间会导致干细胞死亡
实验表明,TRF 和 ADF 组小鼠平均每日卡路里摄入量与 AL 组相比无显著降低,说明 HFSCs 凋亡并非由总卡路里摄入减少所致。随着禁食时长增加,HFSCs 凋亡现象加剧,8 小时禁食时毛囊凋亡信号少,16 小时及更长时间禁食则出现大量凋亡 HFSCs,且再喂食后凋亡消失。调整 TRF 禁食时长后发现,延长每日喂食窗口(缩短禁食时间)可使小鼠毛发近乎正常生长,反之则毛发再生延迟更明显,且昼夜禁食对毛囊再生影响相似,表明 HFSCs 凋亡和毛囊再生缺陷主要由禁食时长决定,而非卡路里摄入或昼夜节律变化,且禁食时间越长,缺陷越严重。
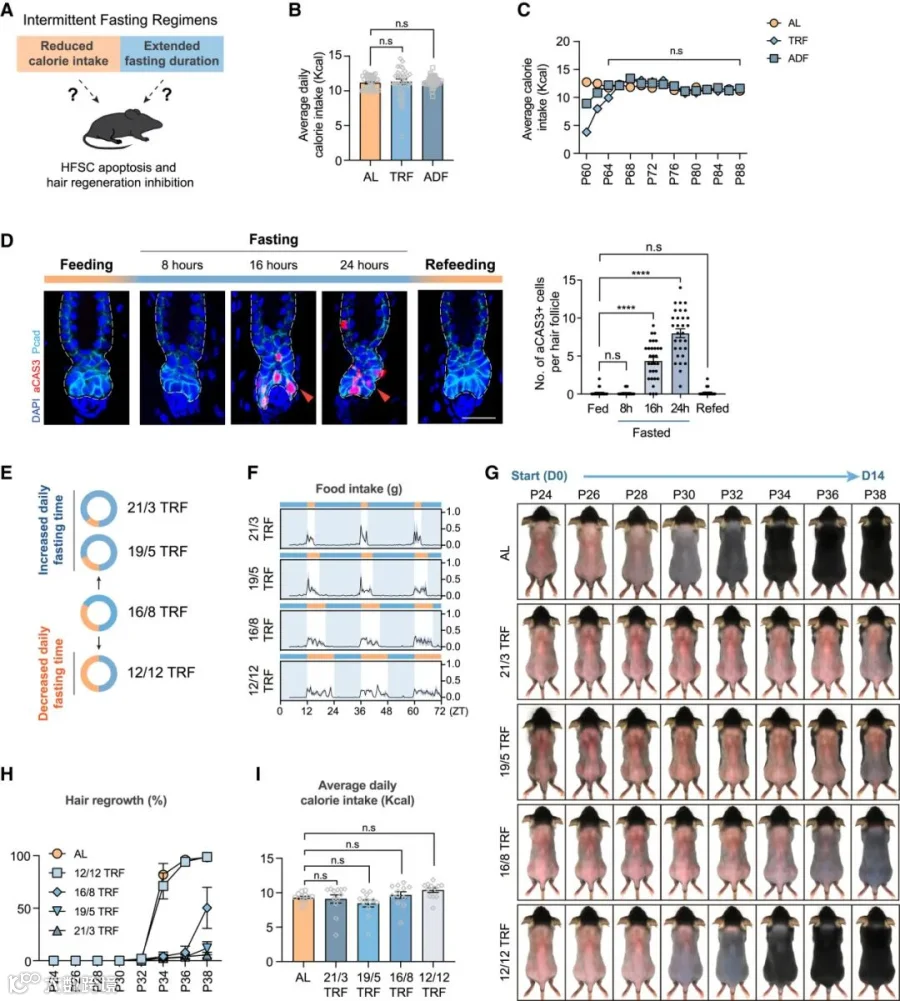
Figure 3 Extended duration of fasting induces HFSC death and inhibits hair follicle regeneration
4. 脂肪细胞诱导的脂肪分解驱动HFSC凋亡
作者首先排除了 HFSCs 凋亡依赖 mTORC1 营养感知机制这一可能。随后发现,禁食会促使皮肤真皮层脂肪细胞发生脂解,释放大量游离脂肪酸(FFAs)至微环境,且脂肪降解现象在禁食 16 小时后显著,与 HFSCs 凋亡出现时间吻合,再喂食后两者均停止。通过基因敲除小鼠模型证实,抑制脂肪细胞脂解或 HFSCs 脂肪酸氧化(FAO),均可减少 HFSCs 凋亡,缓解毛囊再生抑制,且阻断 FAO 的 HFSCs 依赖谷氨酰胺代谢维持生存。此外,皮内注射脂肪细胞中主要的 FFAs 可诱导 HFSCs 凋亡,而不影响 EpiSCs。综上,皮肤脂肪细胞脂解及 HFSCs 中 FAO 是间歇性禁食期间 HFSCs 凋亡的关键因素。
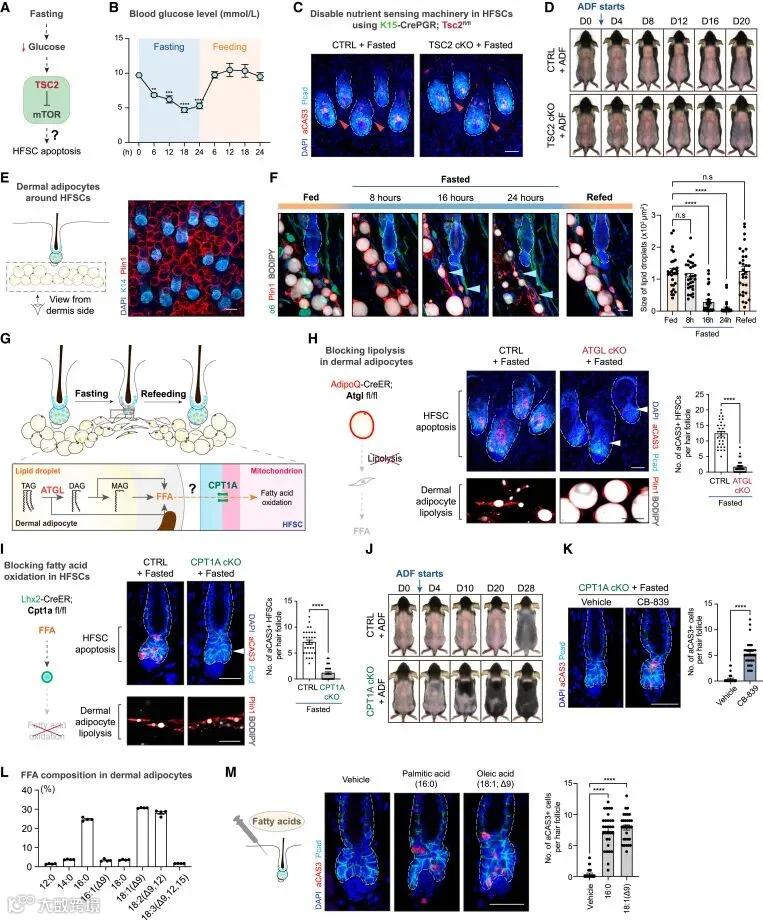
Figure 4 Fasting-induced lipolysis in niche adipocytes drives HFSC apoptosis
5. 禁食会激活肾上腺以阻止组织再生
研究发现交感神经在其中作用不显著,虽禁食时其有轻度激活,但去除交感神经后,脂肪细胞脂解和 HFSCs 凋亡仍存在,毛发再生抑制未恢复。而肾上腺在这一过程中起关键作用,禁食时血浆中瘦素降低,促使肾上腺释放皮质酮和肾上腺素,其水平在禁食 12 小时后显著变化,与脂肪细胞脂解和 HFSCs 凋亡同步,再喂食后恢复正常。体外实验表明,生理浓度的这些激素可诱导脂肪细胞脂解,体内皮内注射更高浓度也有相同效果且能诱导 HFSCs 凋亡,而在特定基因敲除小鼠或使用拮抗剂时,可减少脂肪细胞脂解和 HFSCs 凋亡,肾上腺切除小鼠则完全阻断了这些现象,毛囊再生对禁食不再敏感,表明肾上腺激活释放激素通过脂肪细胞信号传导消除激活的 HFSCs 并抑制毛囊再生。
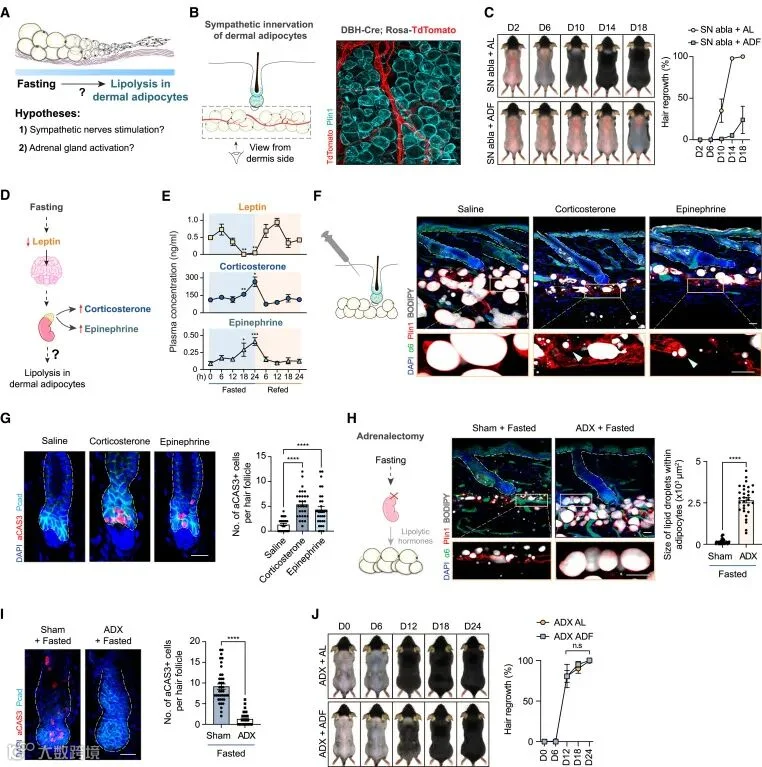
Figure 5 Fasting activates adrenal glands to induce lipolysis in niche adipocytes and apoptosis in HFSCs
6. 禁食诱导HFSCs中线粒体活性氧(ROS)升高
对禁食小鼠 HFSCs 进行 RNA - seq 分析发现,其糖酵解途径下调、脂肪酸代谢上调,氧化应激反应等相关通路改变显著,提示细胞氧化应激可能与 HFSCs 凋亡有关。实验检测到禁食 24 小时后 HFSCs 线粒体 ROS 升高、膜电位降低,透射电镜显示线粒体受损、8 - 氧鸟嘌呤染色表明 DNA 氧化损伤增加,进一步证实了氧化应激与凋亡的关联。与抗凋亡的表皮干细胞(EpiSCs)相比,HFSCs 抗氧化基因表达低,使其更易受 ROS 损伤。而外用抗氧化剂维生素 E 或过表达过氧化氢酶可有效防止 HFSCs 凋亡,缓解毛囊再生抑制,表明增强 HFSCs 抗氧化能力可抵御禁食诱导的损伤。
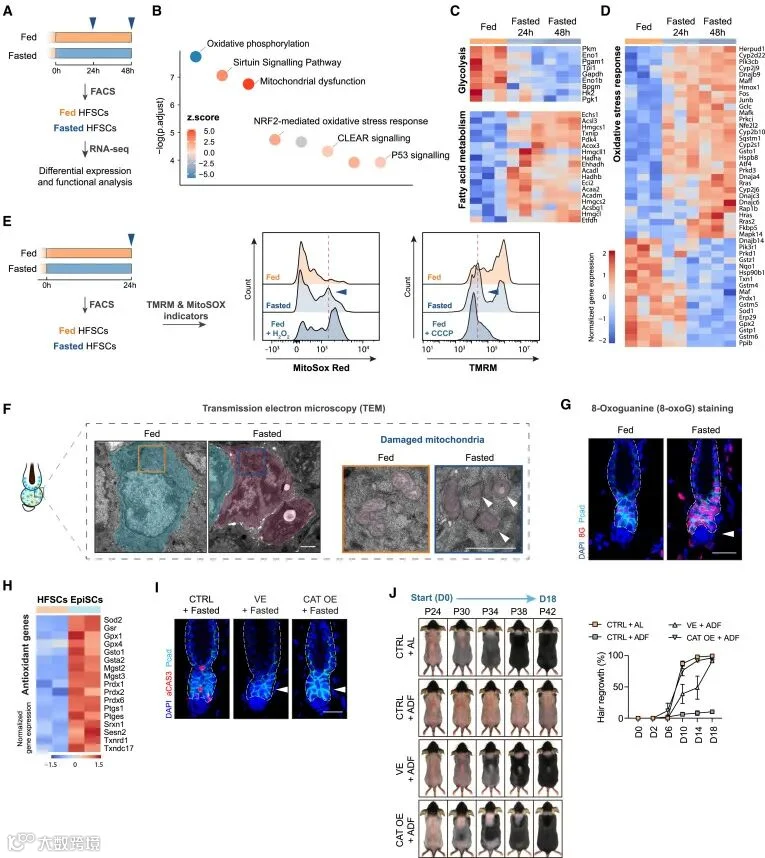
Figure 6 Elevated ROS in HFSCs leads to apoptosis, and enhancing antioxidant capability prevents HFSC apoptosis upon fasting
7. 人类细胞和临床试验中代谢转换及间歇性禁食对毛发生长的影响
在细胞层面,用游离脂肪酸(FFAs)处理HFSCs后,其ROS 水平升高、线粒体损伤加剧且凋亡增加,在人毛囊外植体模型中也观察到类似结果,表明人 HFSCs 在利用 FFAs 时也会出现类似小鼠的不良变化。在临床试验中,招募 49 名健康年轻人进行分组饮食干预,结果显示间歇性禁食(18/6 TRD 组)显著抑制人毛发生长,平均生长速度较正常饮食组降低 18%,虽毛发密度无明显变化,但再生毛发变短变细,且 18/6 TRD 组禁食 18 小时后血液中脂解激素水平升高,提示人体中可能存在与小鼠相似的机制,即间歇性禁食影响 HFSCs 和毛发生长。
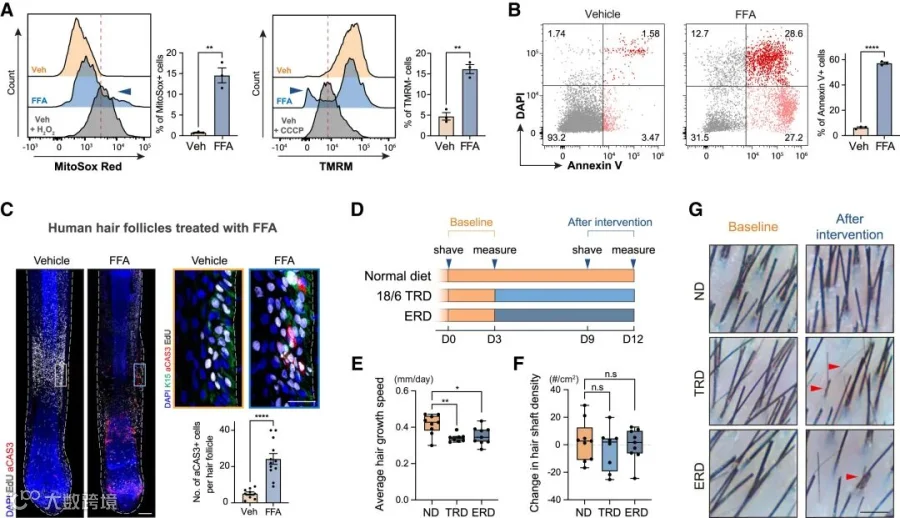
Figure 7 Metabolic switching to FAO induces HFSC apoptosis and inhibits hair growth in humans

领克生物科技(昆明)有限公司致力于下一代高通量测序技术(NGS)、生物信息学分析、转化医学研究等领域的应用和推广。
服务项目包括单细胞多组学测序、基因组重测序、外显子测序、WGBS、转录组测序、LncRNA测序、miRNA测序等,优势项目包括单细胞多组学、Smart-seq2、ATAC-seq和CUT&Tag等前沿技术服务,并且能够进行各类组学数据的个性化分析服务等。

欢迎咨询了解~
电话:0871-65399960
邮箱:service@biolinker.com


