呼吸道病原体,尤其是不断出现的新型病毒和细菌,对全球公共健康构成持续威胁。然而,现有疫苗大多针对特定病原体设计,当病原体发生突变或出现新的病原体时,其保护效果往往有限,因此开发能够提供广谱保护的疫苗具有重要意义。
2026年2月19日,美国斯坦福大学Bali Pulendran教授团队,在国际顶级期刊Science发表题为:Mucosal vaccination in mice provides protection from diverse respiratory threats的研究论文。研究人员开发了基于鼻腔给药的黏膜疫苗:通过脂质体包裹TLR4 激动剂GLA 和TLR7/8 激动剂3M-052(GLA-3M-052-LS),并联合模型抗原ovalbumin (OVA)/流感核蛋白NP。该策略不仅诱导强烈抗原特异性免疫,还在小鼠模型中实现了对多种呼吸道威胁的长期保护。


一
研究方法
动物模型:C57BL/6 小鼠,鼻腔接种GLA-3M-052-LS 脂质体佐剂+ OVA / 流感NP抗原
病原体挑战:SARS-CoV-2、SARS-CoV、SCH014 冠状病毒、流感PR8病毒、金黄色葡萄球菌、鲍曼不动杆菌及尘螨哮喘模型
检测技术:流式细胞术、ELISA、Luminex、病理分析,联合BD Rhapsody单细胞多组学平台(scRNA-seq、scATAC-seq、空间转录组)解析免疫机制


二
主要结果
1.鼻腔疫苗可提供广谱且持久的保护
小鼠接种后21天至3个月内,面对 SARS-CoV-2、SARS-CoV、SCH014 冠状病毒挑战时,表现出:
体重下降减轻
肺部病毒载量显著下降
肺组织炎症和损伤明显减轻
该疫苗还有效降低 金黄色葡萄球菌 和 鲍曼不动杆菌 肺部负荷,静脉感染同样受控,说明保护并不局限于呼吸道。
即使在既往有感染史的小鼠中,疫苗仍能诱导广谱非特异性保护,提示形成了持久免疫记忆。
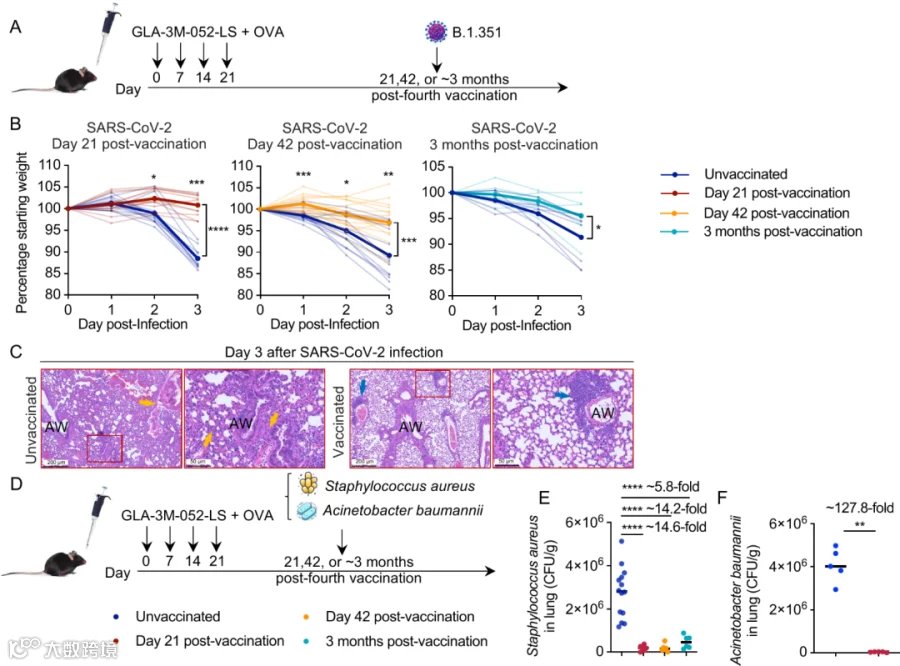
Fig. 1: 鼻腔给药的 GLA-3M-052-LS + OVA 疫苗对 SARS-CoV-2、PR8 流感病毒、金黄色葡萄球菌和肺炎链球菌感染提供了强效且持久的保护。
2.疫苗诱导长期局部免疫记忆
接种后,肺部先天免疫细胞如肺泡巨噬细胞 (AMs)、树突状细胞、单核细胞短期内被活化。
尤其是 AMs,在接种后 90 天仍保持高抗原呈递能力,形成长期“免疫警戒”。
肺组织中大量 组织驻留记忆 T 细胞 (TRM),包括 CD4⁺ 和 CD8⁺ T 细胞,可持续分泌 IFN-γ、IL-2、TNF-α,建立长期局部防御。
单细胞转录组和染色质可及性分析显示,疫苗重塑肺部免疫细胞表观遗传状态,增强抗原呈递与抗病毒基因表达。
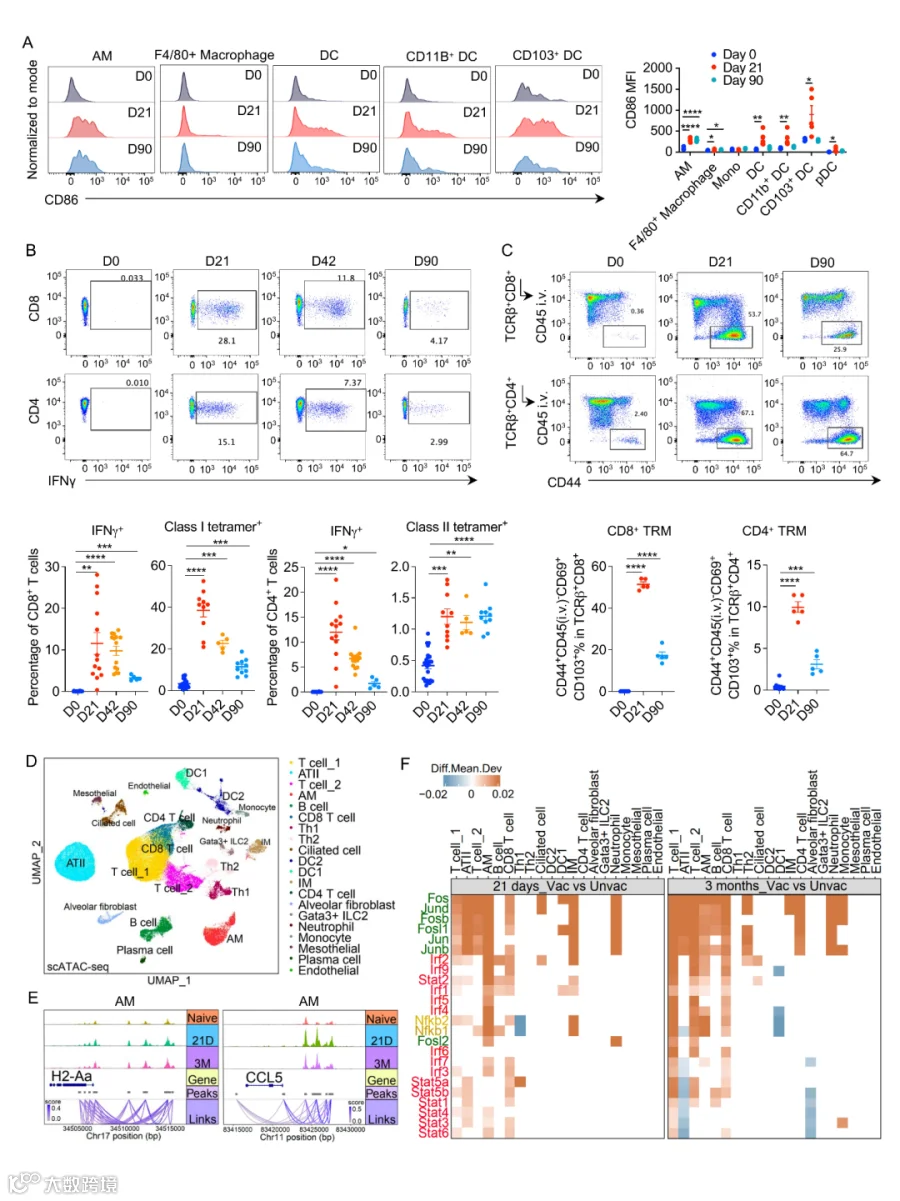
Fig. 2: 鼻腔 GLA-3M-052-LS + OVA 疫苗可诱导 强烈且持久的抗原特异性组织驻留记忆 T 细胞 (TRM) 反应,同时激活先天免疫,并驱动肺泡巨噬细胞的协同表观基因组重编程。
3.抗原特异性 T 细胞驱动肺部整合免疫
长期保护依赖抗原 OVA 的存在,单用佐剂仅有短期效果。
同时耗竭 CD4⁺/CD8⁺ T 细胞 会完全消除对病毒和细菌的保护作用,证明 T 细胞是核心效应。
抗原特异性 T 细胞调控肺泡巨噬细胞和树突状细胞功能,提高抗原呈递能力,塑造肺部整合免疫网络。
RANKL 信号在 T 细胞调控先天免疫中关键,阻断会削弱保护效果。
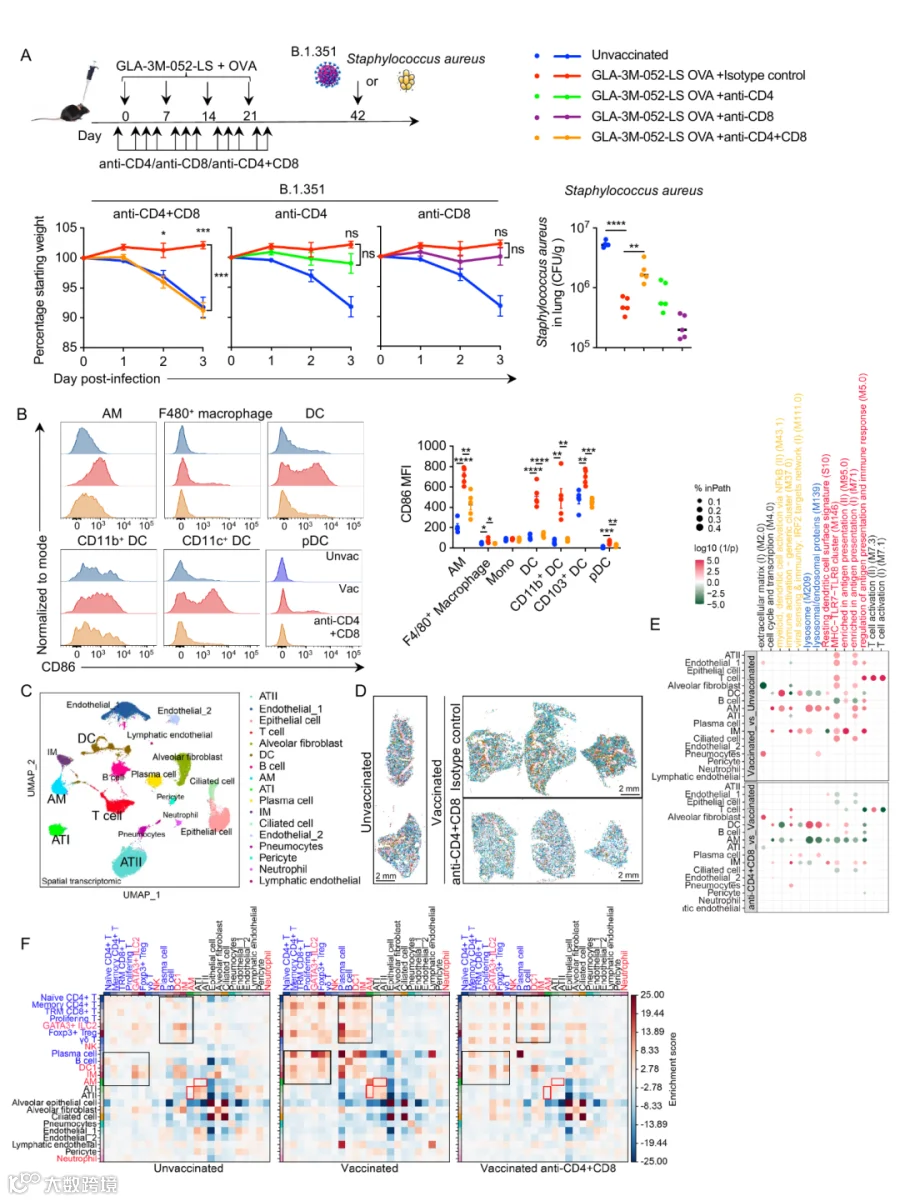
Fig. 3: 抗原特异性T细胞协调 先天免疫细胞与肺上皮细胞之间的相互作用。
4.肺泡巨噬细胞驱动疫苗诱导的非特异性保护
GLA-3M-052-LS + OVA 接种后,AMs 发生长期表观遗传重编程,形成“训练型”状态。
AMs 吞噬和活化能力显著增强:
高效摄取 S. aureus、坏死细胞、感染肺上皮
上调 CD86、MHC-I/II
加强免疫细胞趋化与局部组织修复
AMs 的训练状态通过调控局部微环境,实现早期非特异性广谱防御。
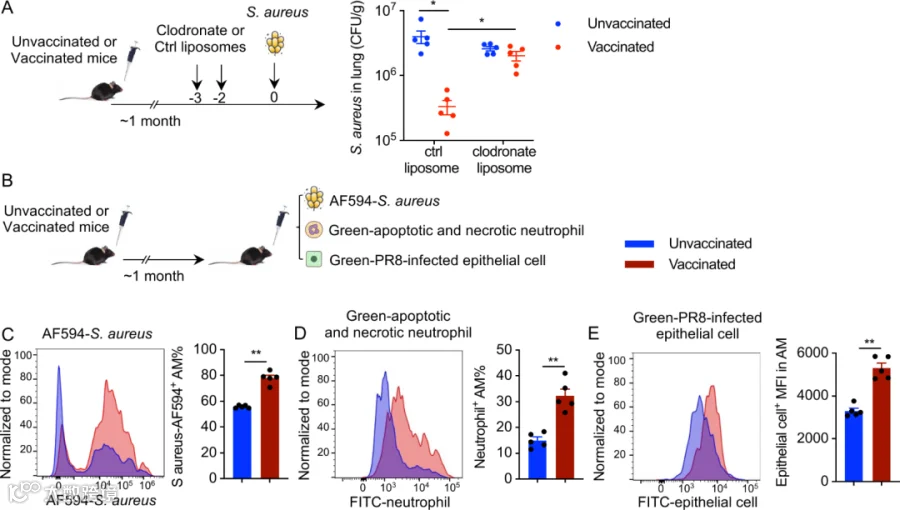
Fig. 4: 疫苗接种后 肺泡巨噬细胞吞噬功能增强,有助于疫苗诱导的 非特异性保护性免疫。
5.促进肺部三级淋巴结构形成并协调免疫
接种后,肺部形成类似淋巴结的结构化微环境:
T 细胞区/B 细胞区与病毒蛋白共定位
NP tetramer⁺ CD8⁺ T 细胞迅速积累
BAL 液中 HA 特异性 IgG/IgG2c 水平升高
同时,促炎因子如 IL-6、CXCL10、CCL2、GM-CSF 水平下降,提示快速控制感染同时抑制炎症风暴。
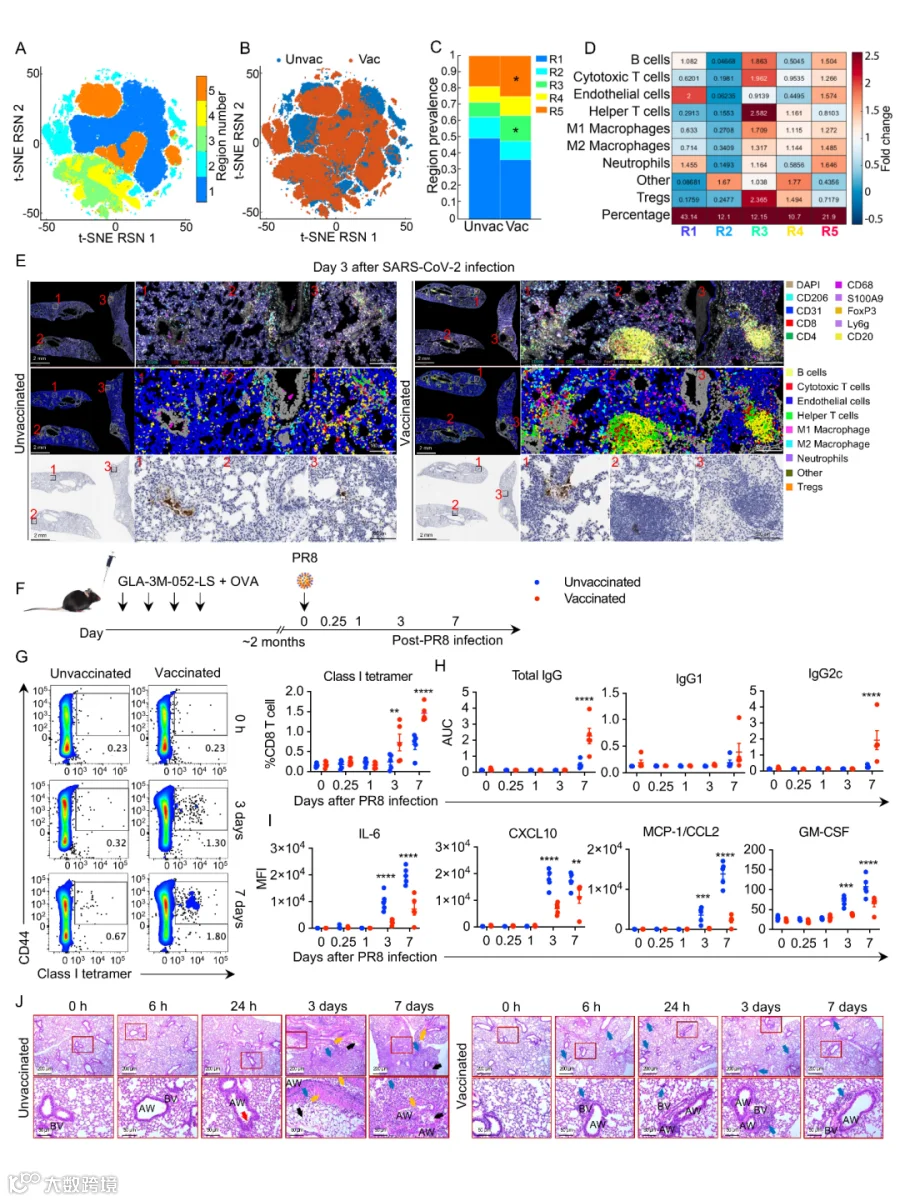
Fig. 5: 疫苗接种促进 感染后的肺部三级淋巴结构 (TLS) 快速形成,并调控炎症反应。
6. 对过敏性哮喘的长期保护
在尘螨诱导的哮喘模型中,疫苗接种小鼠:
肺部嗜酸性粒细胞和 ILC2 浸润减少
Th2 细胞分泌的 IL-4、IL-5、IL-13 降低
血清 IgE 水平下降
PAS 染色显示黏液分泌显著减少,保护至少维持三个月。
T 细胞耗竭或转移实验验证,保护完全依赖抗原特异性 T 细胞。
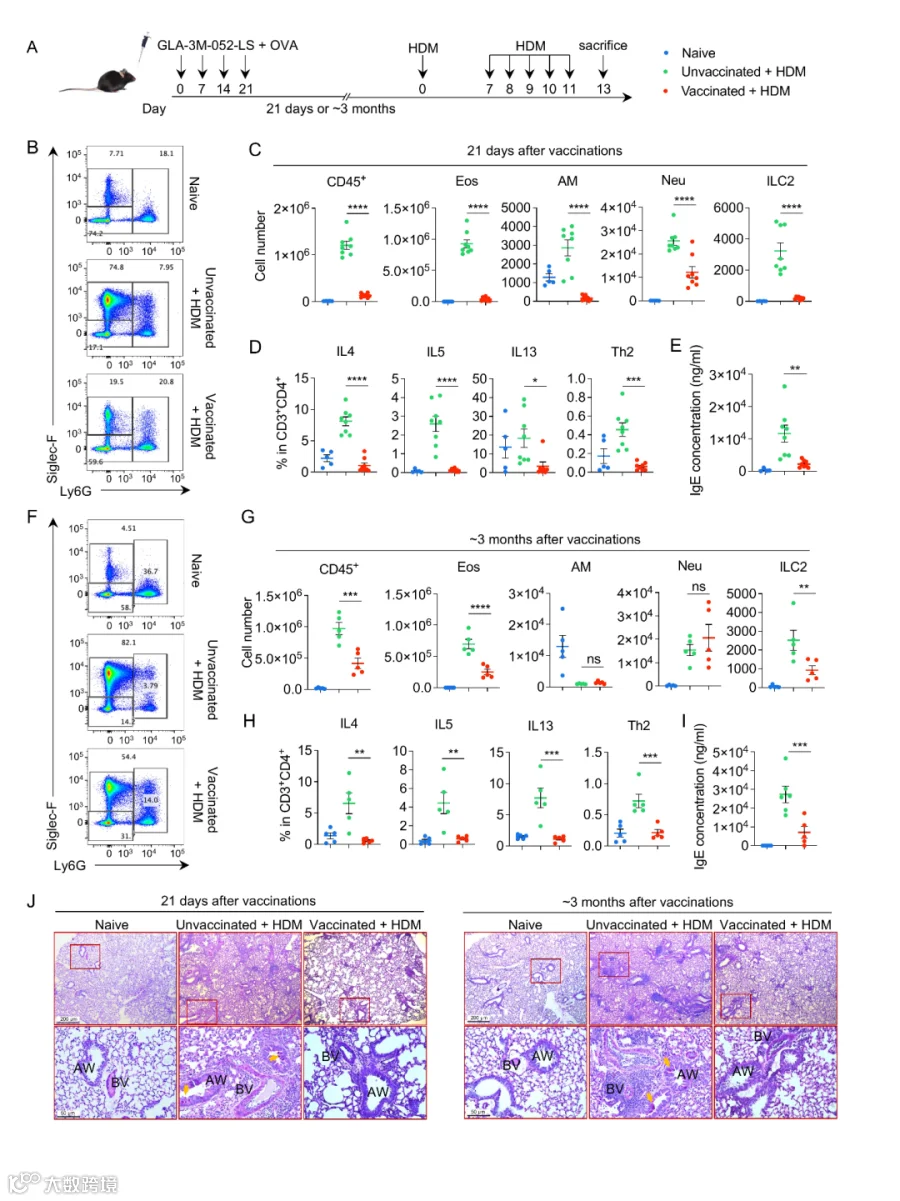
Fig. 6: 鼻腔GLA-3M-052-LS+OVA疫苗对过敏性哮喘提供强效且持久的保护。

三
小结
这项研究通过鼻腔黏膜疫苗策略,结合TLR激动剂+抗原:
诱导持久的抗原特异性TRM
训练肺泡巨噬细胞实现早期广谱防御
重塑肺部局部免疫微环境,形成TLS
同时控制Th2炎症,实现对过敏性哮喘的长期保护
💡 科学意义:该策略为开发通用型呼吸道疫苗提供了新思路,不仅针对病毒和细菌,也对过敏性疾病具有保护潜力,通过整合抗原特异性T细胞与先天免疫形成“肺部整合免疫网络”,实现广谱、持久、局部免疫防御。
领克生物已引进BD Rhapsody单细胞平台,为广大科研工作者提供全方位科研服务支持!