

乳腺癌患者来源的PDO被认为是评估潜在药物有效性的理想模型。 目前乳腺癌治疗的主要挑战是癌细胞对传统抗肿瘤疗法产生耐药性。
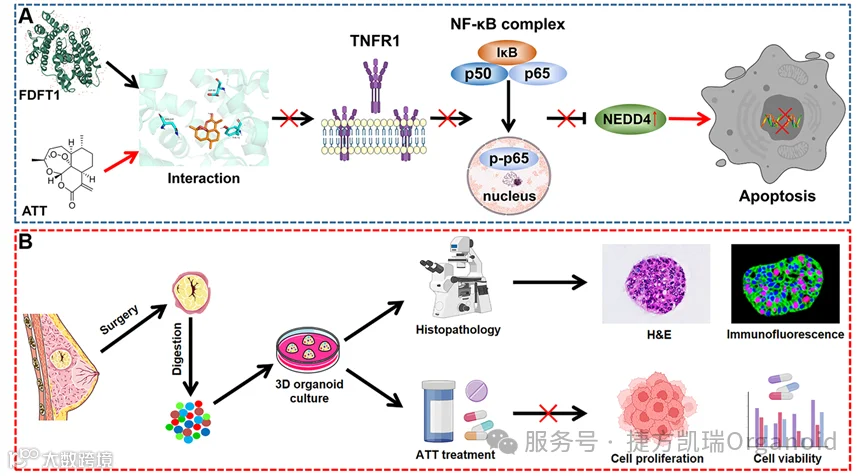
1. 分子对接鉴定出FDFT1是ATT的潜在相互作用蛋白
通过SEA和CDOCKER方法,表明ATT与FDFT1具有良好的结合能力。
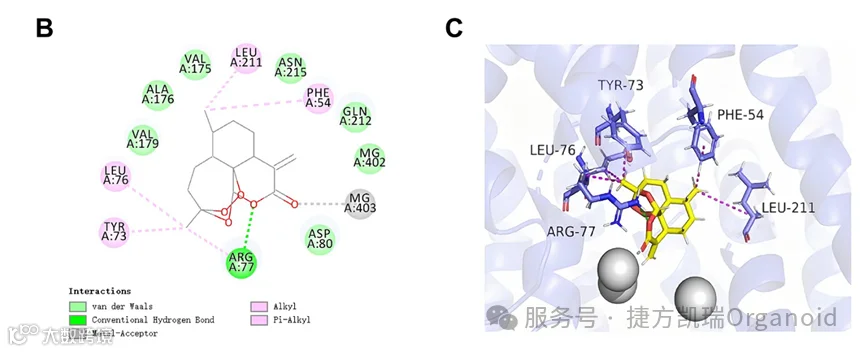
2.ATT与乳腺癌细胞中的FDFT1相互作用
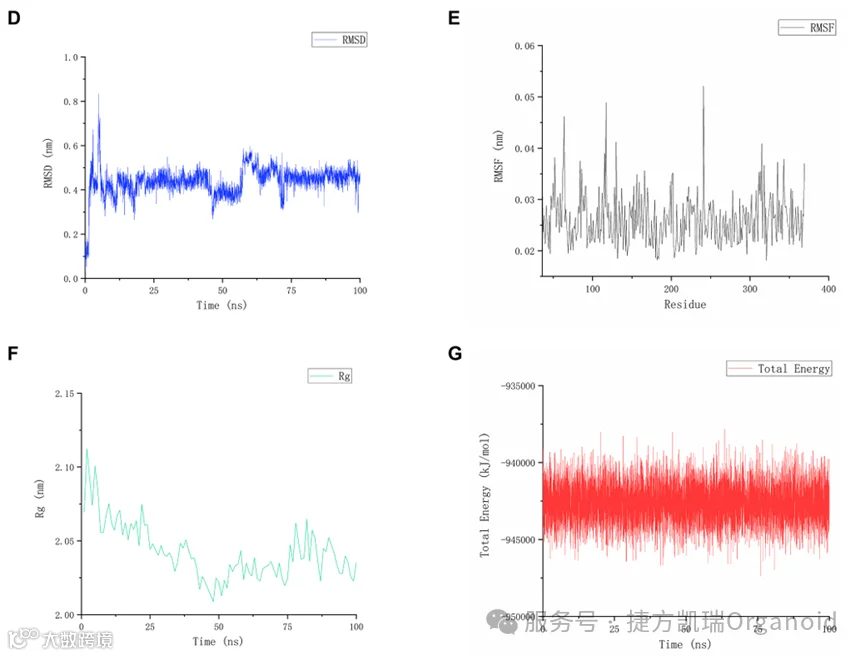
通过分子动力学模拟和其他实验方法证明了ATT与FDFT1在乳腺癌细胞中的稳定结合。
3.ATT以FDFT1为靶点,通过调节TNFR1/NF-κB/NEDD4通路诱导乳腺癌细胞凋亡
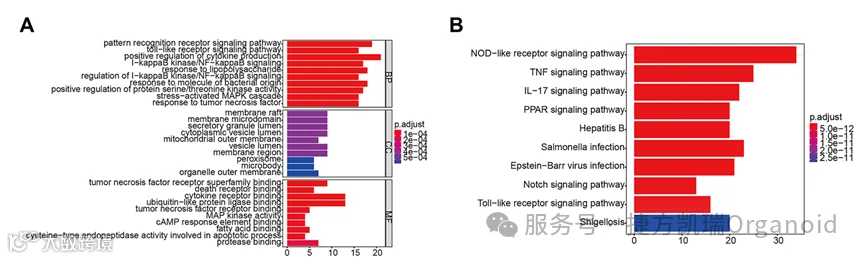
FDFT1的敲低诱导了检测到的乳腺癌细胞中NEDD4的表达和凋亡。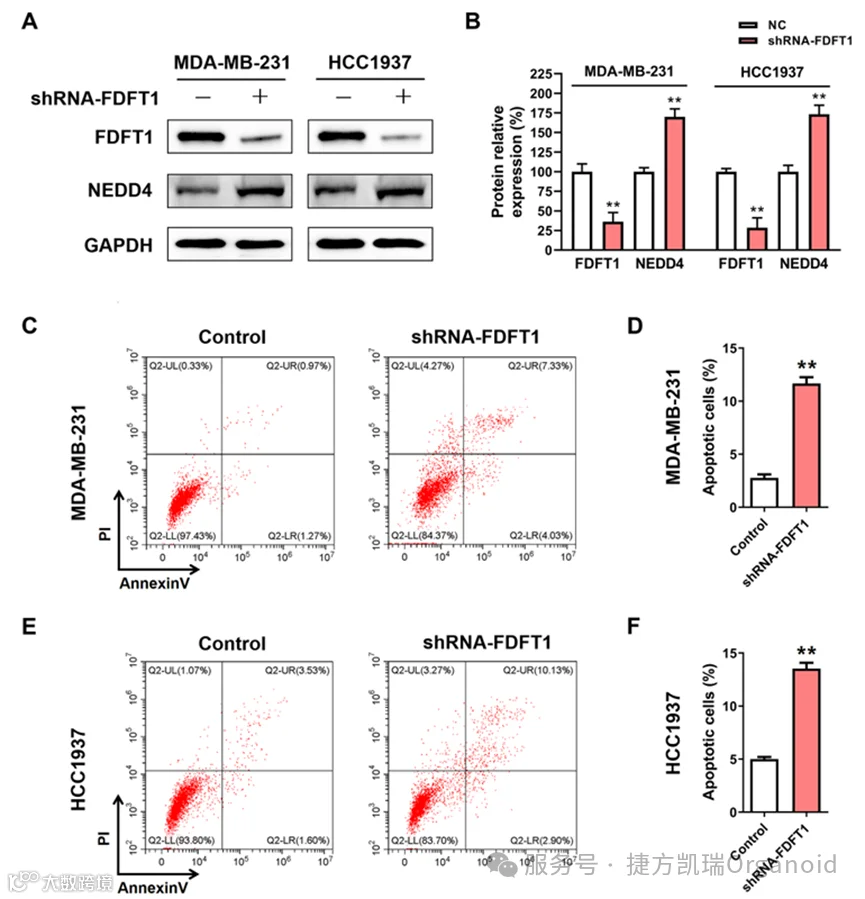 为了探究FDFT1如何调控NEDD4的表达,从TCGA数据库中获取乳腺癌样本的表达谱数据,GESA分析发现FDFT1参与了TNF和NF-κB信号通路的调控。
为了探究FDFT1如何调控NEDD4的表达,从TCGA数据库中获取乳腺癌样本的表达谱数据,GESA分析发现FDFT1参与了TNF和NF-κB信号通路的调控。
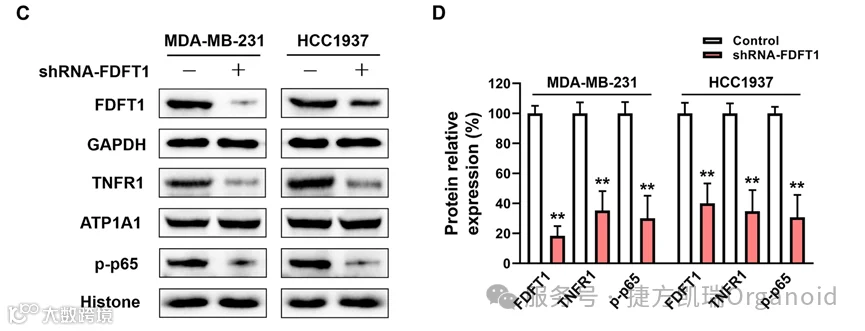
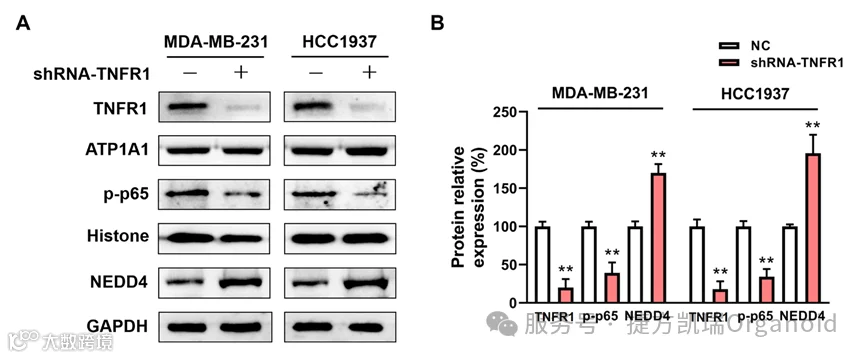
 在乳腺癌细胞中沉默TNFR1后,细胞核内RelA(NF-κBp65亚基)水平显著下调,而NEDD4水平被诱导,进一步证实了TNFR1/NF-κB通路对NEDD4表达的调控作用。
在乳腺癌细胞中沉默TNFR1后,细胞核内RelA(NF-κBp65亚基)水平显著下调,而NEDD4水平被诱导,进一步证实了TNFR1/NF-κB通路对NEDD4表达的调控作用。
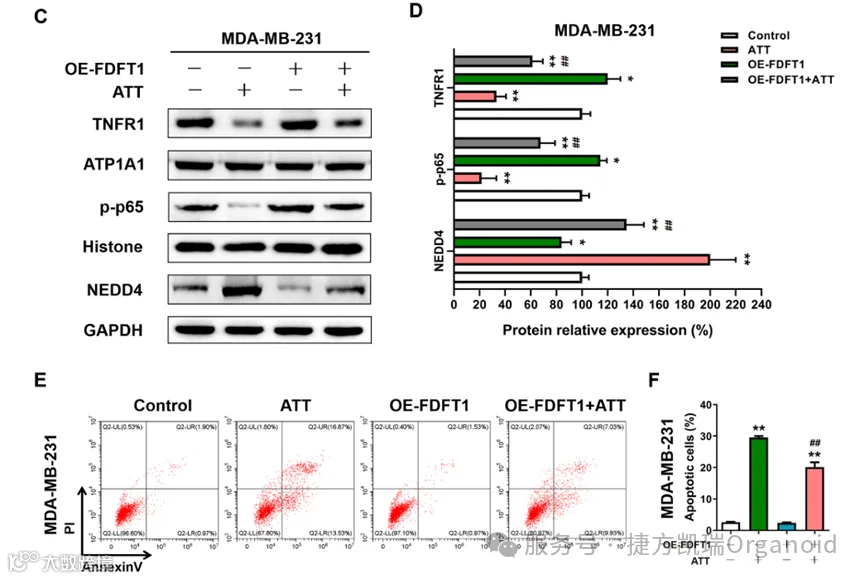
发现ATT刺激乳腺癌细胞时,FDFT1的表达受到干扰,导致与上述FDFT1敲低相似的效应,即NEDD4表达上调和细胞凋亡。过表达FDFT1能够逆转ATT的这种效应,进一步支持了ATT通过调控TNFR1/NF-κB/NEDD4通路来靶向FDFT1并诱导乳腺癌细胞凋亡的假说。
4.乳腺癌PDO的建立及组织学表征
进一步应用PDO来评估ATT治疗乳腺癌的临床疗效,对原发性肿瘤和类器官切片进行了H&E和免疫荧光分析,以确认PDO中的肿瘤病理并评估PDO是否保留了与原始肿瘤相似的组织结构。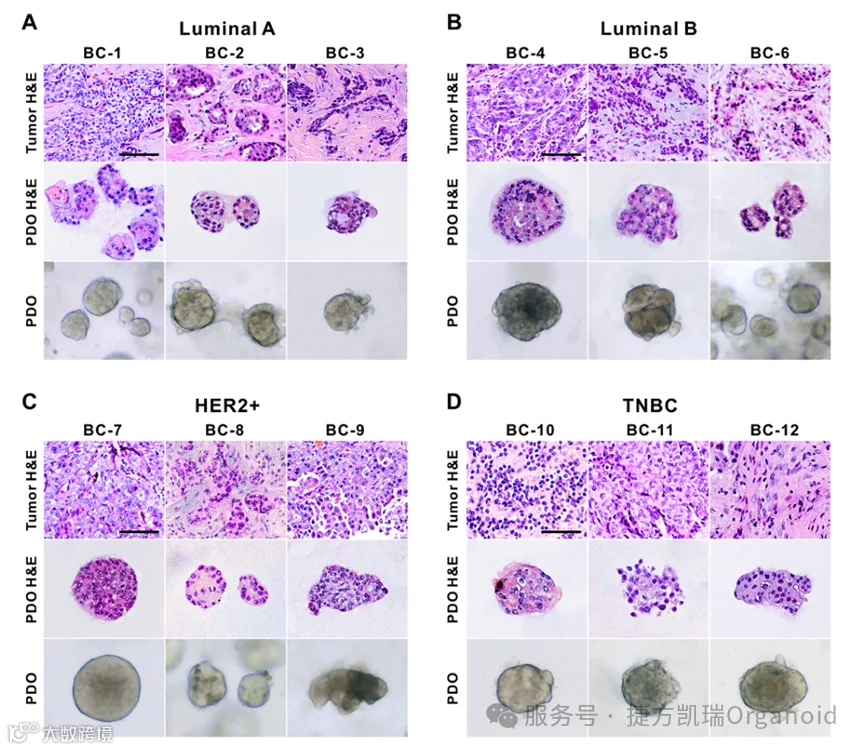 利用一组乳腺癌特异性生物标志物如ER、PR、HER2和Ki-67将乳腺癌分为四种亚型,包括管腔A、管腔B、HER2富集和TNBC,结果表明PDO的表型保留了原始组织病理学乳腺癌亚型。
利用一组乳腺癌特异性生物标志物如ER、PR、HER2和Ki-67将乳腺癌分为四种亚型,包括管腔A、管腔B、HER2富集和TNBC,结果表明PDO的表型保留了原始组织病理学乳腺癌亚型。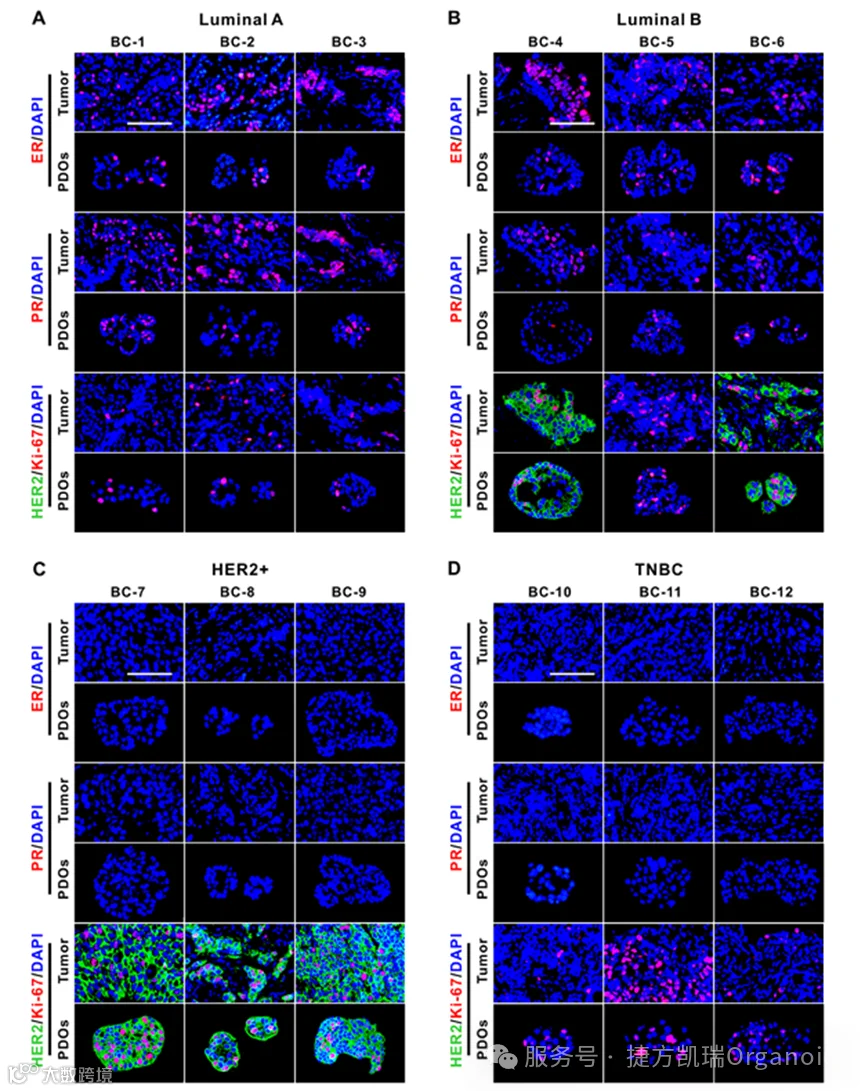 综上所述,PDO在组织学特征、激素受体状态和HER2表达模式方面与原始患者保持一致,是一种高度准确的模型。
综上所述,PDO在组织学特征、激素受体状态和HER2表达模式方面与原始患者保持一致,是一种高度准确的模型。
5.ATT表现出更广泛的抗乳腺癌功效和良好的安全性
为了评估ATT在乳腺癌临床病例中的疗效,用不同药物浓度处理PDOs,并评估其活力和表型变化。随着ATT处理浓度的增加,不同亚型的PDOs的生长受到显著抑制。在最高处理浓度(20µM)下,结构崩解和PDOs边界不清等表型变化被认为是ATT诱导细胞死亡的迹象。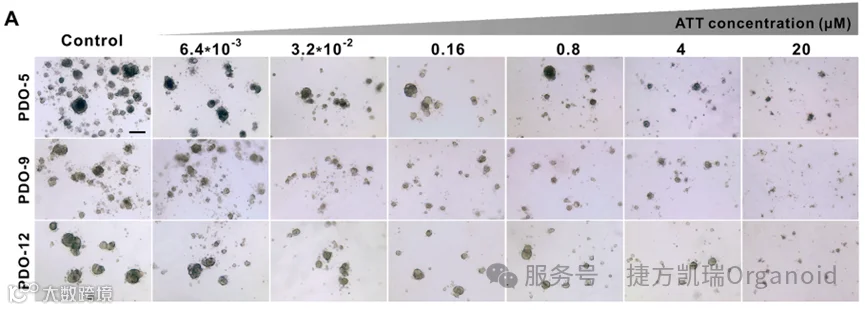 选择了三种常用于乳腺癌治疗的化疗药物(紫杉醇、盐酸阿霉素和多西他赛)作为治疗对照。药物敏感性试验表明,ATT和化疗药物对PDOs均有良好的治疗作用。但三种化疗药物对不同个体来源的PDOs的疗效存在差异。
为评估这些药物的安全性,我们评估了ATT和三种化疗药物对正常乳腺类器官的毒性。药物安全性测试显示,ATT对正常乳腺类器官的损伤小于三种化疗药物(1µM和5µM浓度)。综合来看,ATT对乳腺癌具有良好的治疗效果和良好的安全性,有望成为临床上可行的治疗选择。
选择了三种常用于乳腺癌治疗的化疗药物(紫杉醇、盐酸阿霉素和多西他赛)作为治疗对照。药物敏感性试验表明,ATT和化疗药物对PDOs均有良好的治疗作用。但三种化疗药物对不同个体来源的PDOs的疗效存在差异。
为评估这些药物的安全性,我们评估了ATT和三种化疗药物对正常乳腺类器官的毒性。药物安全性测试显示,ATT对正常乳腺类器官的损伤小于三种化疗药物(1µM和5µM浓度)。综合来看,ATT对乳腺癌具有良好的治疗效果和良好的安全性,有望成为临床上可行的治疗选择。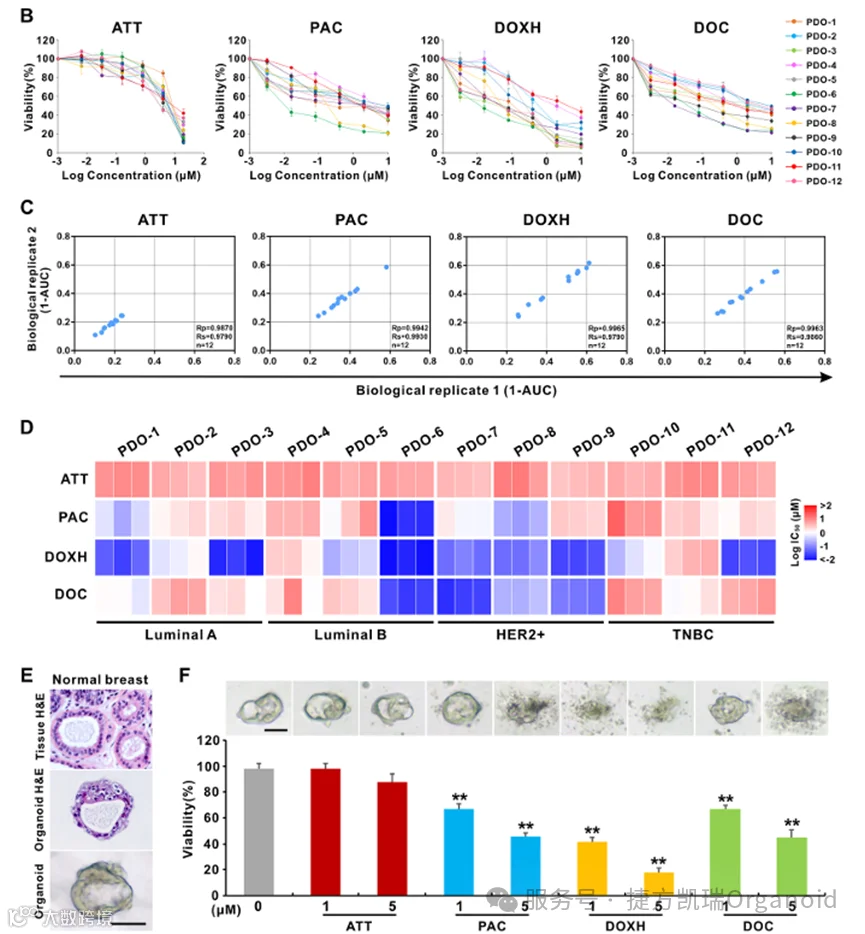
6.ATT抑制乳腺癌PDO的增殖
采用Calcein-AM/PI荧光双染法检测ATT对PDOs的细胞毒作用。5μMATT处理5天后,与对照组相比,Luminal(PDO-5)、HER2+(PDO-9)和TNBC(PDO-12)亚型患者的类器官均出现了不同程度的细胞死亡。细胞增殖实验进一步证实,ATT能显著减少PDOs中的EdU阳性细胞数量,表明其抑制了PDOs的增殖。与ATT相比,紫杉醇、盐酸阿霉素和多西他赛等化疗药物也表现出对PDOs增殖的抑制作用,且部分药物的抑制作用更强。不同组别的EdU/Hoechst荧光强度对比也支持了ATT和化疗药物对PDOs增殖的抑制作用。综上所述,ATT能有效抑制PDOs的细胞活力和增殖,与部分化疗药物的抑制效果相近或具有相当的潜力。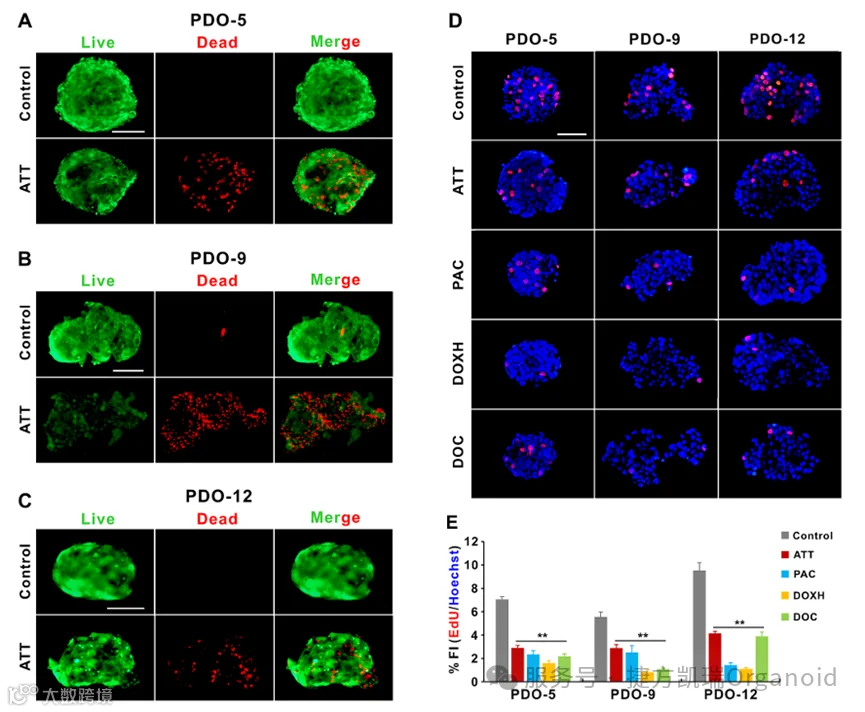
ATT作为一种抗肿瘤药物,不仅具有显著的抗癌效果,还展现出良好的安全性。先前的研究已表明ATT能有效杀死人类癌细胞,同时对小鼠的肝脏和肾脏无明显的细胞毒性。在本研究中,进一步证实了ATT对正常乳腺类器官无明显毒性,与传统化疗药物相比,其安全性更为突出。此外,本研究还揭示了ATT的作用机制,即FDFT1是ATT的直接靶点,ATT通过靶向FDFT1并调控TNFR1/NF-κB/NEDD4通路来诱导乳腺癌细胞凋亡。更重要的是,ATT对不同病理亚型的乳腺癌PDOs(患者源性类器官)的生长均表现出广谱抑制作用。综上所述,ATT作为一种有效、安全且具有潜力的乳腺癌治疗候选药物,值得进一步研究和开发,有望成为乳腺癌患者的一种辅助治疗手段。
捷方凯瑞提供乳腺癌类器官培养基试剂盒和类器官构建服务,后续老师对类器官构建比较感兴趣,欢迎咨询!
Chen D, Li G, Luo L, et al. Artemisitene induces apoptosis of breast cancer cells by targeting FDFT1 and inhibits the growth of breast cancer patient-derived organoids.Phytomedicine. 2024;135:156155. doi:10.1016/j.phymed.2024.156155

 扫码添加小助手
E-mail: info@jfkrorganoid.com
公司网址:http://www.jfkrorganoid.cn/
扫码添加小助手
E-mail: info@jfkrorganoid.com
公司网址:http://www.jfkrorganoid.cn/






 在乳腺癌细胞中沉默TNFR1后,细胞核内RelA(NF-κBp65亚基)水平显著下调,而NEDD4水平被诱导,进一步证实了TNFR1/NF-κB通路对NEDD4表达的调控作用。
在乳腺癌细胞中沉默TNFR1后,细胞核内RelA(NF-κBp65亚基)水平显著下调,而NEDD4水平被诱导,进一步证实了TNFR1/NF-κB通路对NEDD4表达的调控作用。









 扫码添加小助手
扫码添加小助手


