


部分研究结果

研究目的
谱系可塑性与治疗抵抗:晚期前列腺癌在AR通路抑制剂(如恩杂鲁胺)治疗压力下,常通过谱系可塑性发生适应性转变,从AR阳性的腺癌(CRPC-AR)转变为AR低表达或阴性的、高度耐药的亚型,尤其是CRPC-NE。这种转变是治疗失败和疾病进展的主要原因。谱系可塑性通常由可逆的表观遗传重编程驱动,这为开发逆转耐药性的疗法提供了理论可能。
NSD2(又称MMSET)是催化组蛋白H3第36位赖氨酸二甲基化(H3K36me2)的关键酶。H3K36me2是一种与转录激活相关的组蛋白修饰,且已知能拮抗抑制性标记H3K27me3(由EZH2/PRC2复合物催化)。NSD2是否在CRPC-NE的谱系可塑性和耐药性中发挥核心作用?靶向NSD2能否逆转这一过程并恢复药物敏感性?
部分结果
1. 建立了模拟人CRPC异质性的小鼠来源类器官模型
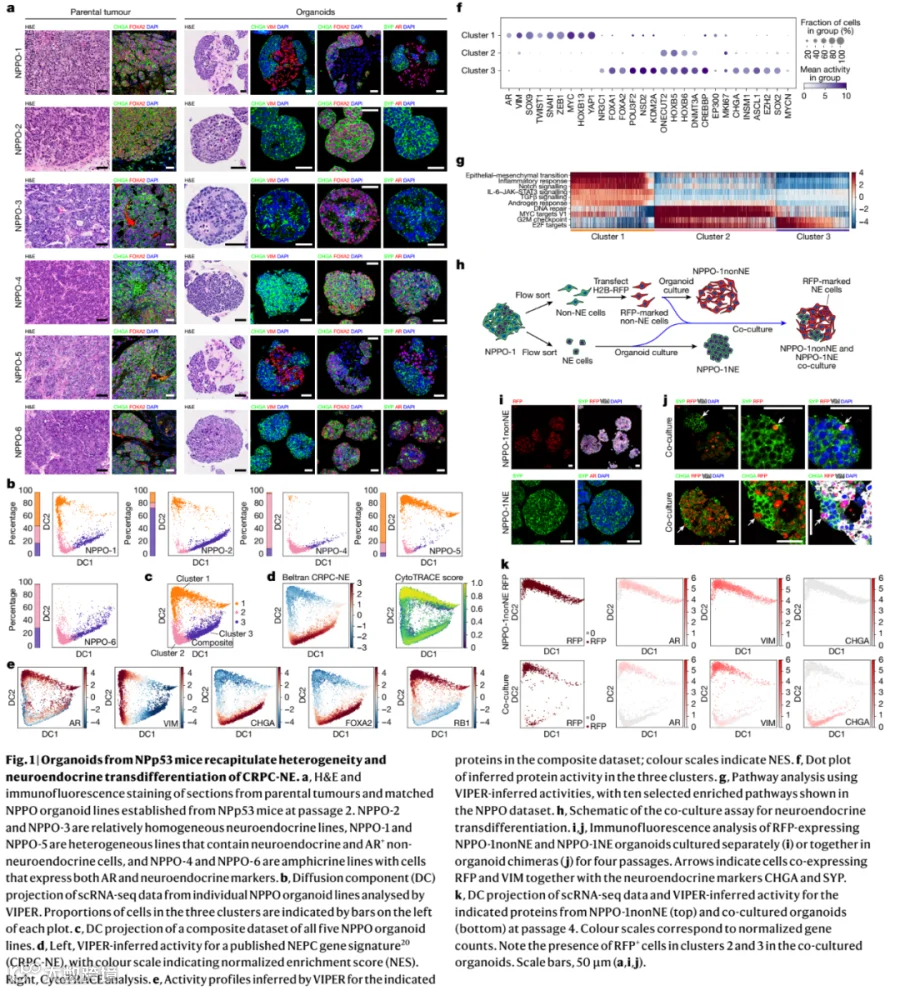
2. NSD2与H3K36me2在CRPC-NE中特异性上调并与不良预后相关
在NE类器官细胞中,H3K36me2水平显著升高,而抑制性标记H3K27me3水平降低。NSD2(而非NSD1或NSD3)在CRPC-NE中特异性高表达,且其蛋白水平和酶活性在NE类器官中升高。
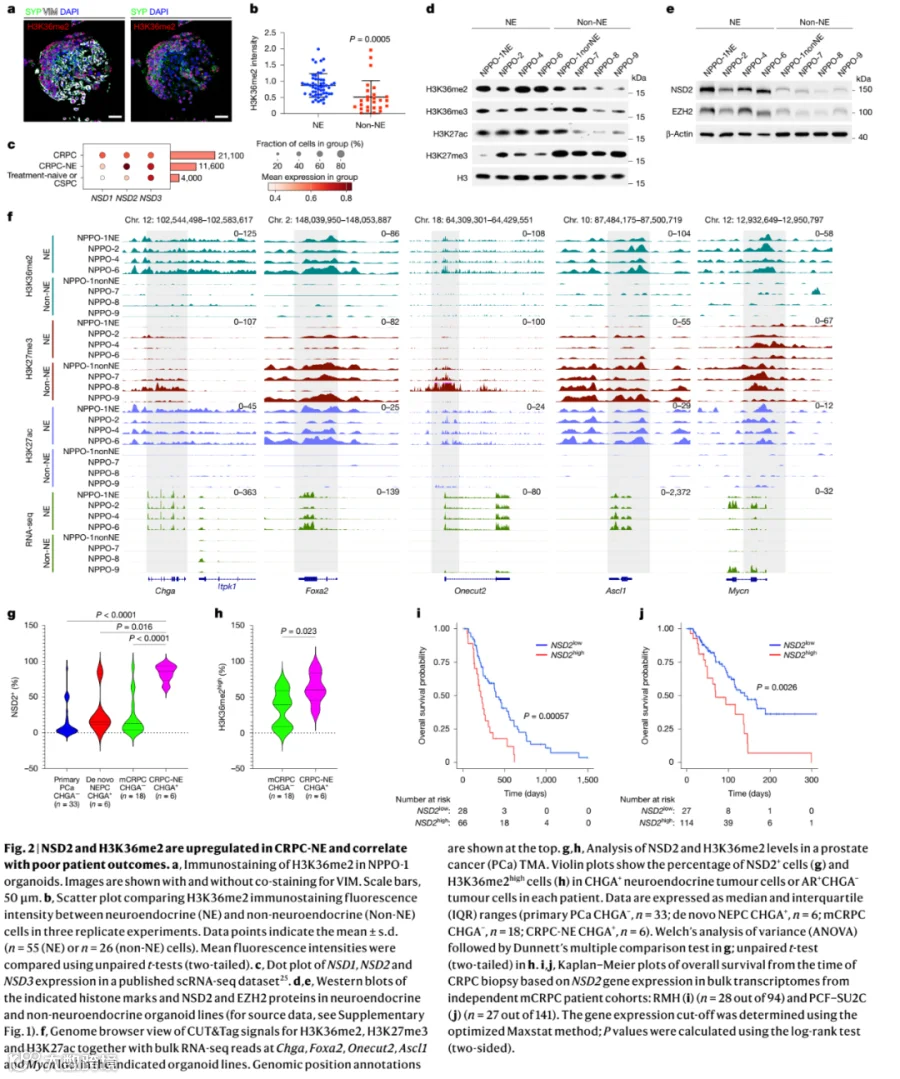
3. 类器官模型验证了NSD2是维持NE表型所必需的
在NE类器官(NPPO-1NE, NPPO-2)中,通过CRISPR-Cas9敲除Nsd2,导致:NE标记物(如CHGA, SYP)丢失。AR重新表达。组织学上向腺癌样表型逆转。
CUT&Tag分析显示,敲除Nsd2导致全基因组水平的H3K36me2丢失和H3K27me2增加。NE特异性增强子(由H3K27ac和H3K36me2标记)的染色质可及性降低,这些增强子调控着ASCL1、FOXA2等关键NE分化因子。
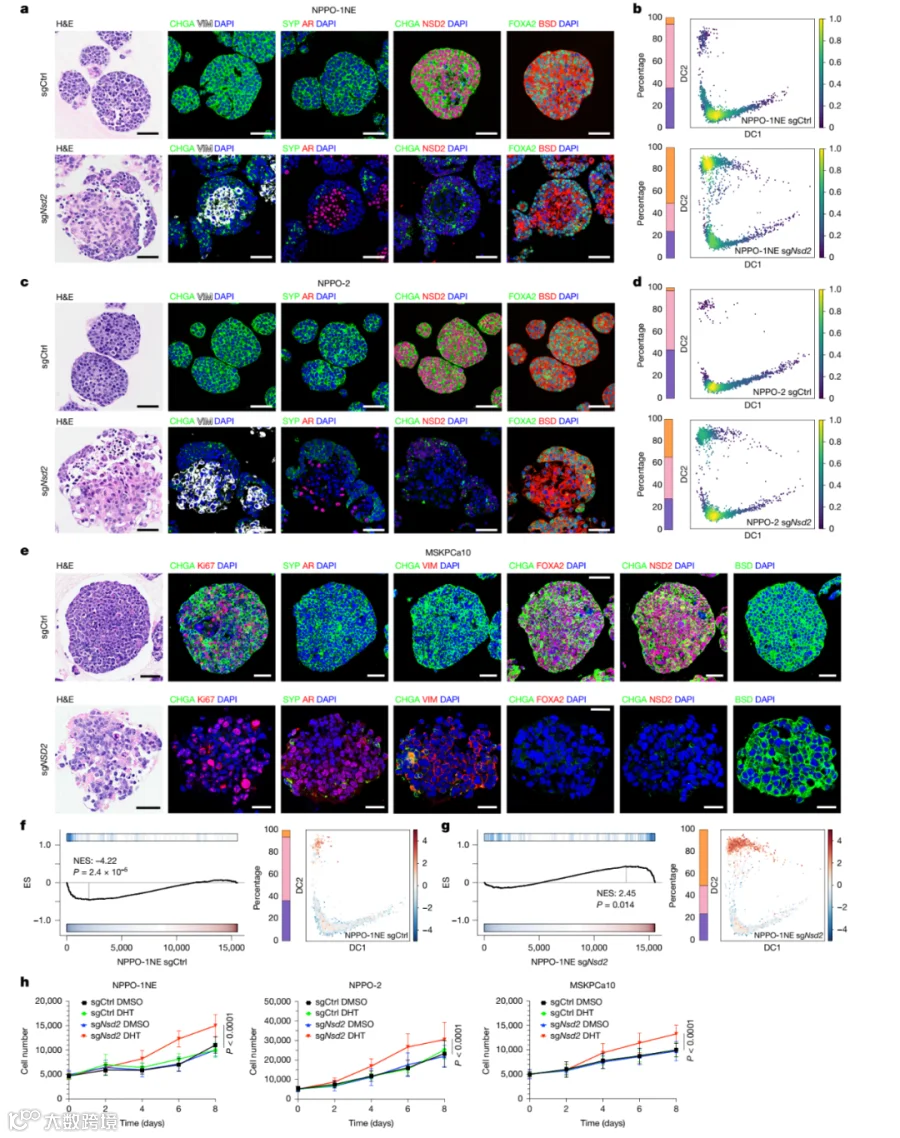
4. NSD2缺失恢复了对恩杂鲁胺的敏感性
Nsd2敲除或表达显性负效突变体H3.3K36M后,原本对恩杂鲁胺高度耐药的NE类器官,生长被显著抑制(IC50降至~3 μM或更低.
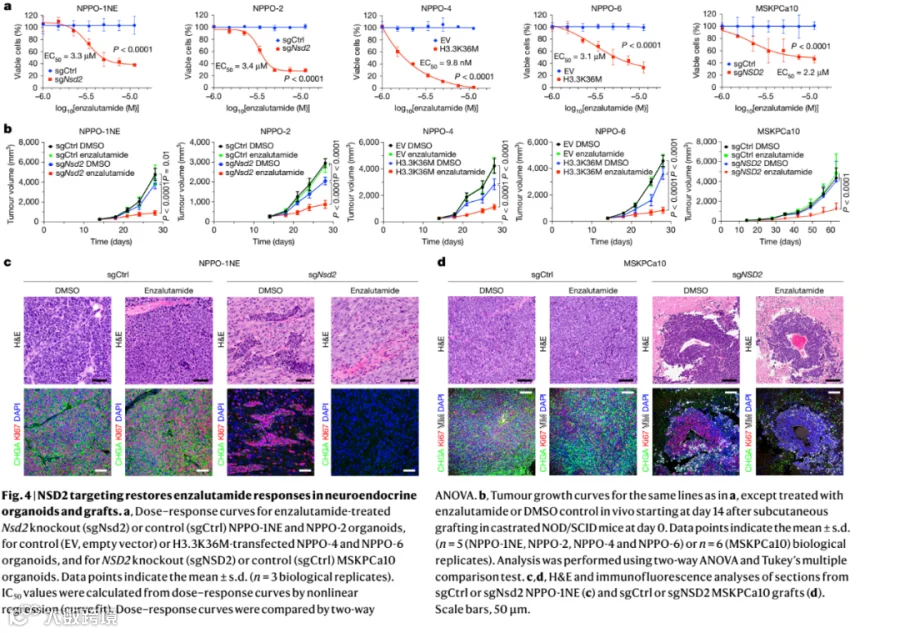
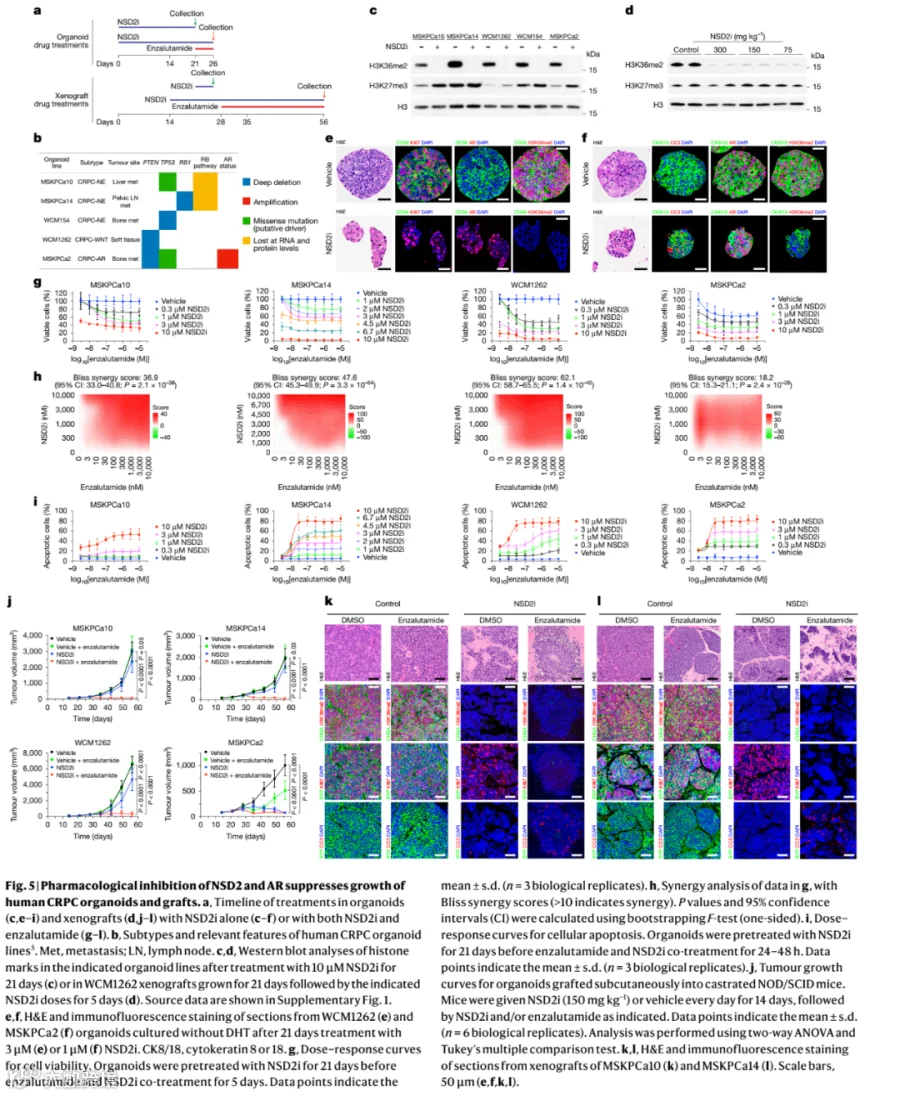
5. 小分子抑制剂(NSD2i)抑制NSD2具有协同治疗潜力
研究合成了一种新型、高选择性的NSD2小分子抑制剂(NSD2i),其体外抑制NSD2的IC50为3.8 nM,选择性超过其他测试的甲基转移酶(除NSD1外)10000倍。
NSD2i处理能降低H3K36me2水平,并在单细胞水平上诱导细胞从NE状态(簇2/3)向腺癌样状态(簇1)转变。在多种人类CRPC类器官亚型(CRPC-NE, CRPC-WNT, CRPC-AR)中,NSD2i预处理能显著增强恩杂鲁胺的疗效,并诱导协同的细胞凋亡(Bliss协同分数 > 10)
捷方凯瑞可提供前列腺癌类器官构建、前列腺癌类器官培养基和前列腺癌类器官库服务,欢迎咨询交流!





