Targeted activation of ferroptosis in colorectal cancer via LGR4 targeting overcomes acquired drug resistance
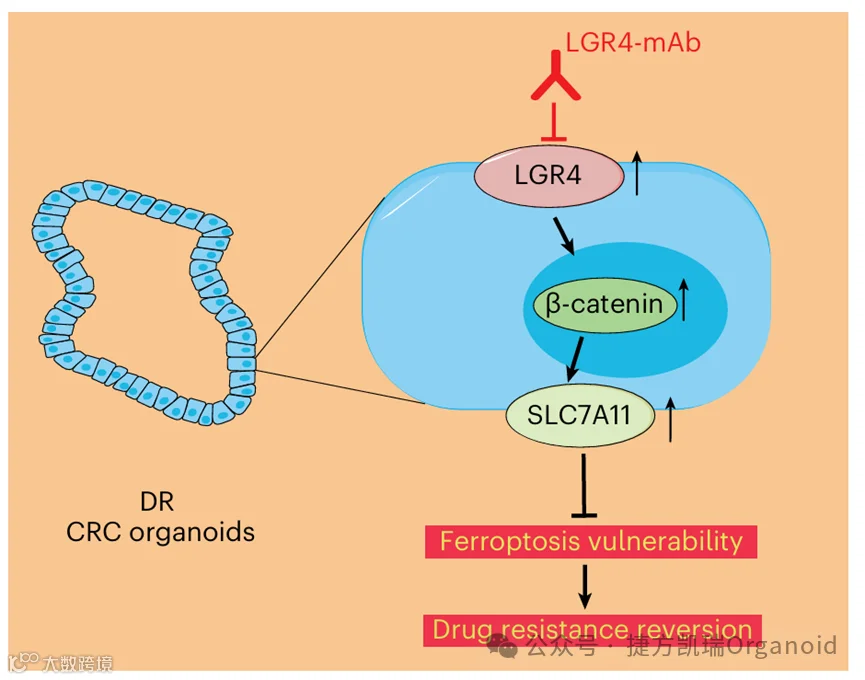
今天给大家分享由南开大学的陈佺教授发表在Nature Cancer上的一篇题为“Targeted activation of ferroptosis in colorectal cancer via LGR4 targeting overcomes acquired drug resistance”的文章。获得性耐药是癌症治疗的主要挑战,也是癌症死亡的主要原因。本研究建立了一个源自结直肠癌的类器官生物库,并通过重复低水平的化疗药物暴露来诱导获得性耐药;又设计了一种单克隆抗体(LGR4-mAb)与化疗药物联合使用时,靶向Wnt信号传导增强了铁死亡,显示了对抗难治性和复发性癌症的潜在机会。
-
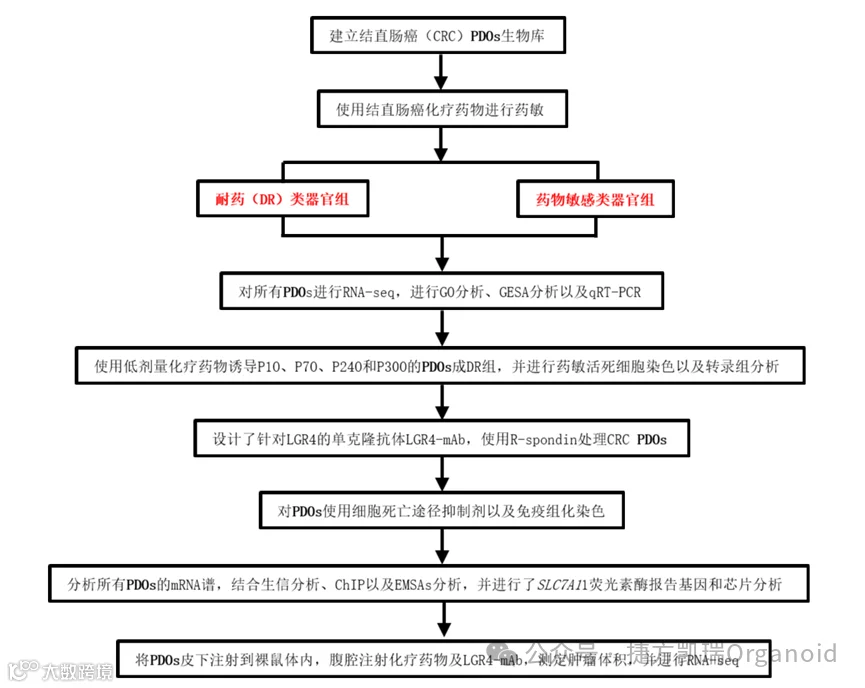
1 GR4–Wnt–β-catenin通路赋予PDOs耐药性
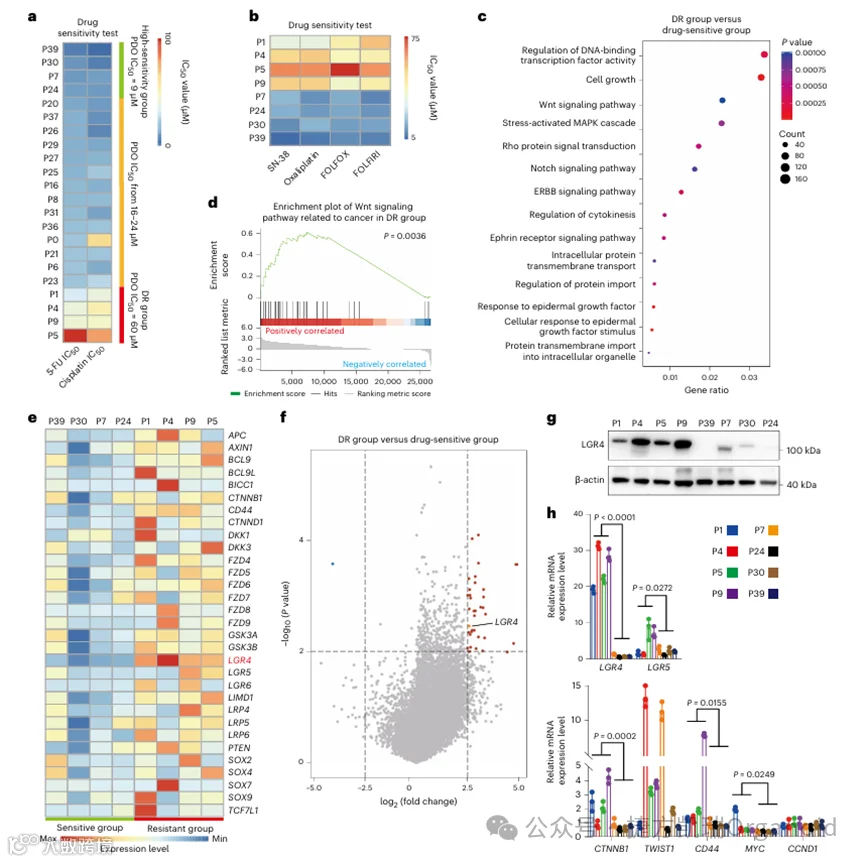
为了探索CRC耐药机制,建立了CRC PDOs生物库,包括来自40名患者的22个CRC PDOs,使用临床常用的结直肠癌化疗药物5-FU、顺铂、伊立替康(SN-38)以及FOLFOX和FOLFIRI联合施用,然后评估药物敏感性。结果显示,耐药(DR)组P1、P4、P5和P9 PDO对大多数化疗药物表现出更强的耐药性,而P7、P24、P30和P39 PDO对大多数化疗药物敏感。
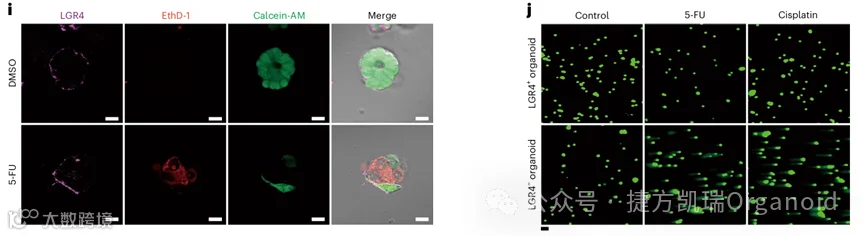
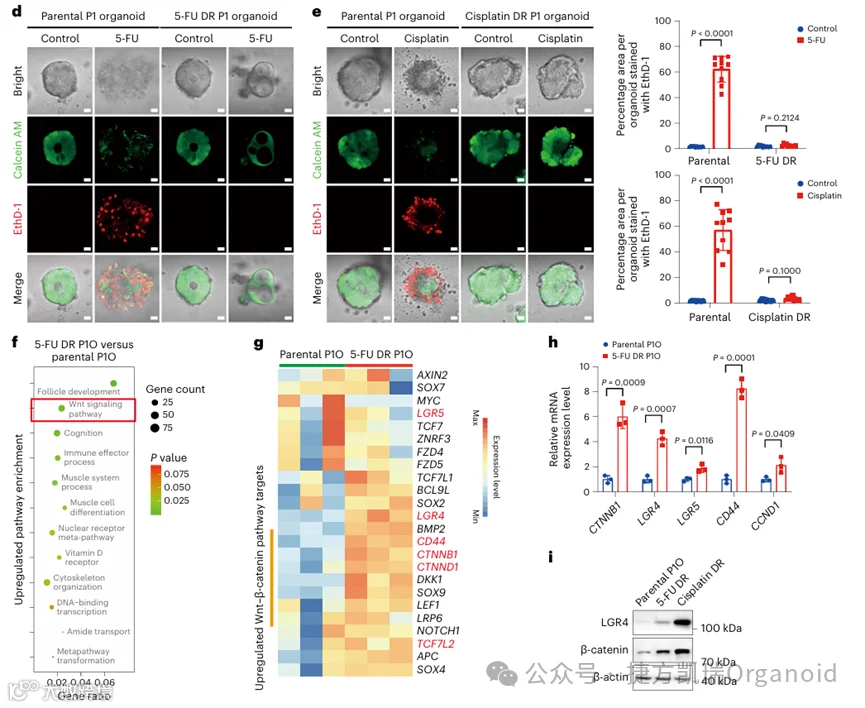
为了探索耐药机制,通过RNA测序对所有PDOs进行转录组分析,并比较DR和药物敏感组之间的信使RNA图谱,基因本体(GO)分析显示,DR组中的几种肿瘤生存途径高度富集。此外,使用Reactome的基因集进行基因集富集(GSEA)分析,得到了相似的结果,表明Wnt通路在复发组和DR组中高度上调,值得注意的是,LGR4(Wnt-β-catenin通路上游的重要分子)被发现在所有DR PDOs中显著增加。通过qRT-PCR证实了Wnt通路中基因的mRNA水平的变化;LGR4阳性细胞响应5-FU或顺铂治疗,表现出显著的DR表型。以上表明,LGR4-Wnt信号通路有助于结直肠PDOs的耐药性。
-
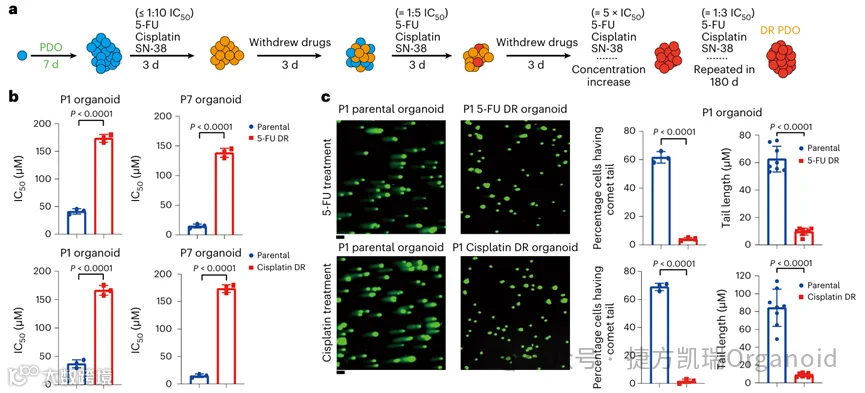
由于复发性或难治性CRC的获得性耐药在多轮化疗中不断演变,推断这种表型可以在培养的PDOs中重现。为了建立获得性耐药,首先将P1O、P7O、P24O和P30O的PDOs消化成单细胞,在基质胶中生长7天以形成单个PDOs,用低剂量的5-FU、顺铂或SN-38处理PDOs,随后剂量逐渐增加,直至达到IC50浓度的约五倍,经过这些化疗方案后,四个CRC PDOs获得了稳定的DR表型(DR P1O、DR P7O、DR P24O和DR P30O),与未经治疗的相比,IC50至少增加了四倍。根据活/死细胞染色显示,IC50浓度的药物在1周内杀死了超过50%的初始PDOs(P1O和P7O),而大多数DR PDOs在相同处理条件下仍然存活。转录组分析显示,与其亲本 PDOs相比,DR P1O中的Wnt信号通路显著上调。总的来说,LGR4和Wnt-β-catenin通路在DR PDOs中上调,导致获得性耐药。
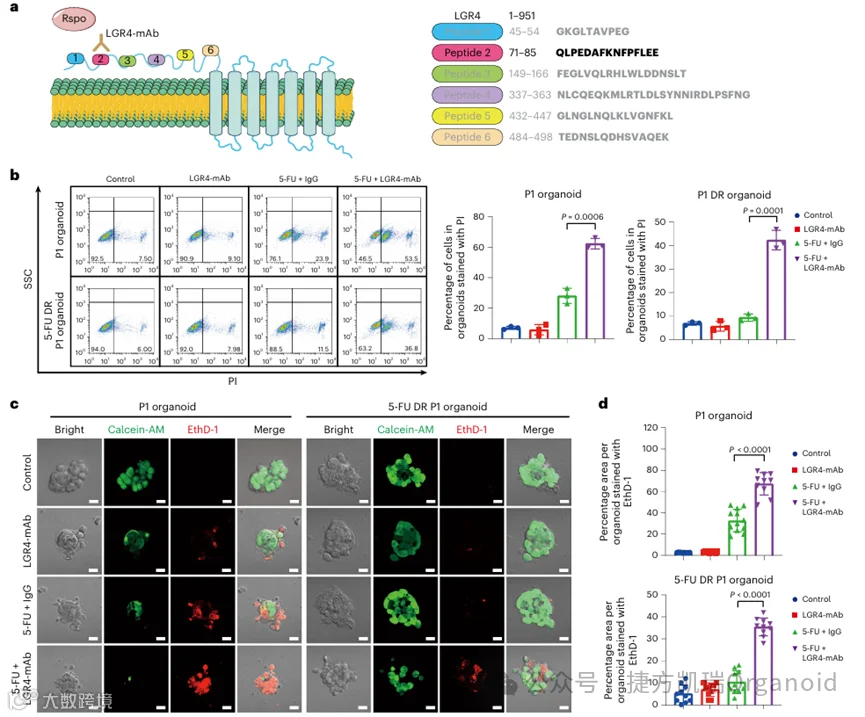
作为一种细胞表面膜蛋白,LGR4与R-spondin相互作用,激活Wnt-β-catenin信号通路,从而获得DR PDOs表型和CSC性状。因此,假设限制配体R-spondin对LGR4的可及性可能会增加结肠癌化疗药物的敏感性并克服耐药性,产生了针对LGR4的单克隆抗体(LGR4-mAb),特异性靶向LGR4的胞外结构域,抑制LGR4和R-spondin之间的结合。
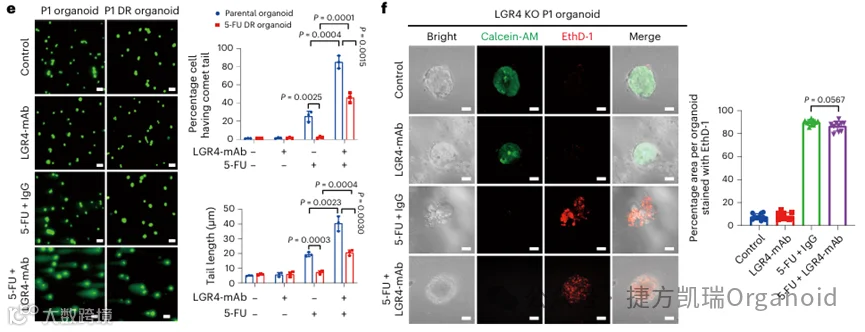
接下来,使用R-spondin处理CRC PDOs,以存在或不存在LGR4-mAb的情况下激活Wnt-β-catenin信号传导,与单独化疗药物治疗相比,添加LGR4-mAb在亲代PDOs和DR PDOs中均引起明显更多的细胞死亡;敲除LGR4使PDOs对LGR4-mAb与5-FU联合施用不敏感,尽管LGR4的敲除本身在5-FU治疗后降低了生存能力。综上所述,LGR4-mAb抑制Wnt -β-catenin通路使化疗诱导的细胞死亡变得敏感,从而克服CRC PDOs的获得性耐药。
4 LGR4抗体促进耐药PDOs铁死亡
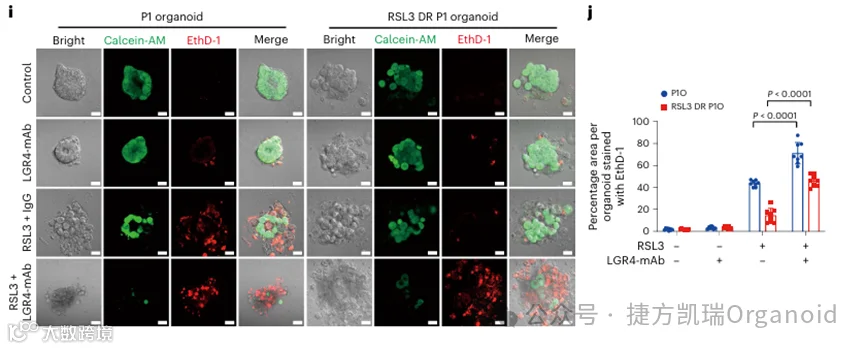
接下来,解决LGR4-mAb与化疗药物共同治疗时促进细胞死亡的潜在分子机制。为了明确细胞死亡途径,使用了特异性靶向凋亡、坏死和铁死亡途径的抑制剂,结果表明,每种抑制剂都不同程度地抑制了单独化疗药物诱导的细胞死亡,在亲本PDOs和DR PDOs中使用铁死亡抑制剂ferrostatin-1都表现出对LGR4-mAb致敏细胞死亡最显著的阻断作用。这些数据表明,铁死亡参与了LGR4-mAb和化疗联合治疗后的细胞死亡,特别是在DR PDOs中;免疫组织化学(IHC)染色显示,联合治疗后DR PDOs或亲代PDOs中4HNE水平较高,以及膜结合转铁蛋白受体,这是铁死亡的特征。此外,在LGR4-mAb和化疗药物的联合治疗下,铁下垂的分子标志物CHAC1和PTSG2的表达增加了五倍以上。这些结果表明,LGR4-mAb选择性地使CRC PDOs对铁死亡敏感,以克服获得性耐药。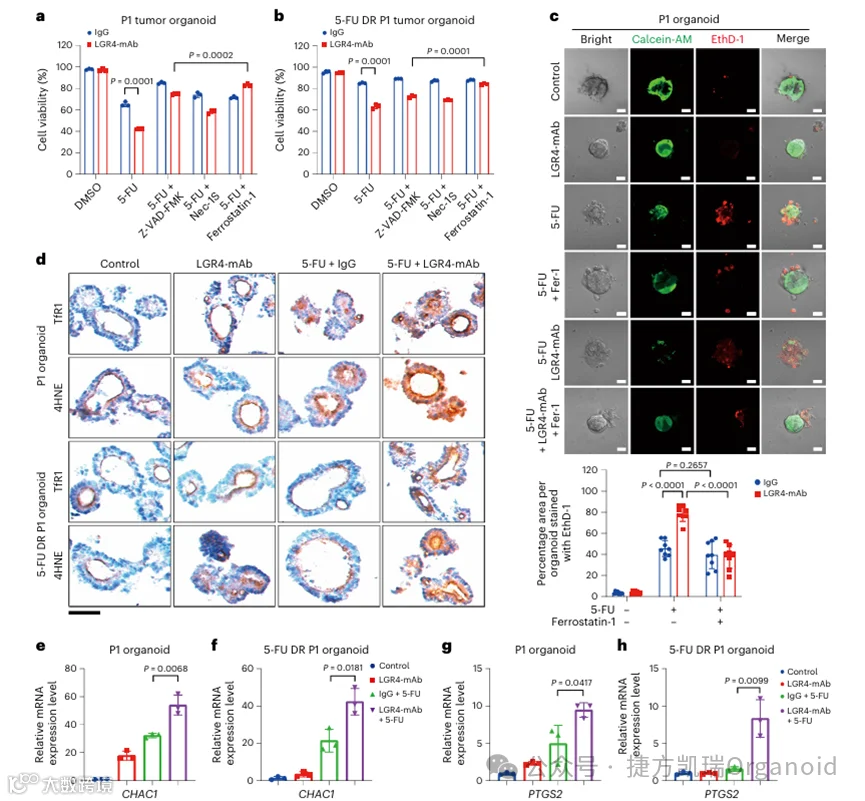
5 Wnt -β-catenin-TCF7调控SLC7A11的转录
为了更好地了解铁死亡导致获得性耐药的分子机制,以及LGR4-mAb联合化疗药物如何促进铁死亡,综合分析了DR PDOs和亲本PDOs中铁死亡相关基因的mRNA谱,与铁死亡相关的几个基因确实在DR PDOs中上调。与亲本PDOs相比,DR PDOs中 SLC7A11的表达显著增加,这与LGR4的水平呈正相关。此外,在接受或未接受5-FU治疗的DR PDOs中,LGR4-mAb显著降低了SLC7A11的表达,表明LGR4-mAb抑制了SLC7A11的转录。
接下来,使用UCSC数据库的生物信息学分析预测Wnt-3a反应元件的TCF7结合基序,通过突变分析证实了其活性,染色质免疫沉淀(ChIP)和电泳迁移率变动分析(EMSAs)进一步揭示了TCF7直接与SLC7A11的启动子结合。因此,LGR4–Wnt–β-catenin通过TCF7转录因子的启动子结合来转录调节SLC7A11基因表达。
由于LGR4通过Wnt–β-catenin途径上调SLC7A11,进一步判断LGR4-mAb是否可以抑制SLC7A11的转录,使用R-spondin、LGR4-mAb或两者处理的细胞中进行了SLC7A11荧光素酶报告基因和芯片分析,R-spondin强烈激活SLC7A11报道基因并增加TCF占有率,但添加LGR4-mAb会减弱这种作用。接着,在PDOs中进行了挽救实验,LGR4敲低P1O中SLC7A11的异位表达将RSL3诱导的铁死亡恢复至与异位SLC7A11表达的P1O相似的水平,SLC7A11的异位表达很大程度上损害了LGR4-mAb增强RSL3诱导的铁死亡的作用。综上所述,LGR4依赖Wnt信号,通过转录上调SLC7A11,促进CRC PDOs对死亡的抗性。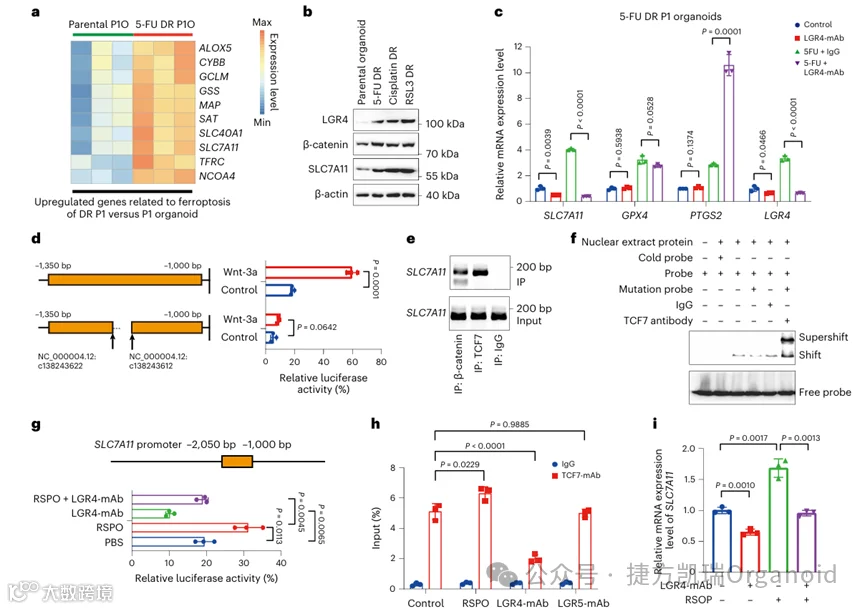
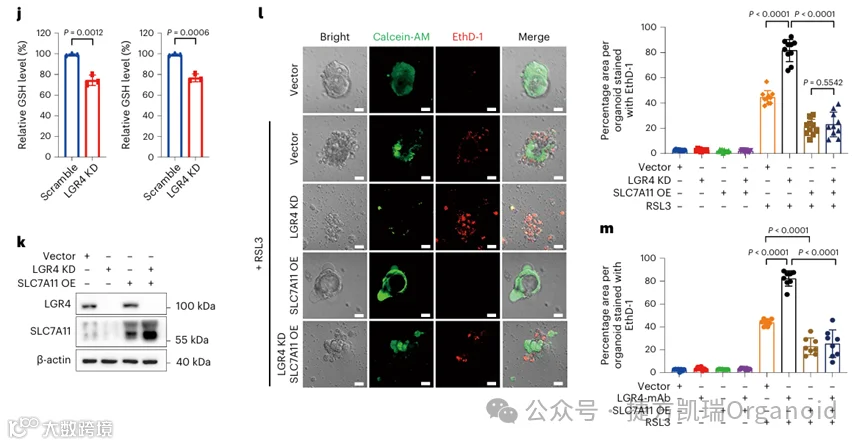 接下来,将亲本 PDOs和DR PDOs分别皮下注射到裸鼠体内,当DR PDOs形成的肿瘤体积达到50 mm3时,通过腹腔注射不同化疗药物和LGR4-mAb对小鼠进行治疗。病理分析显示,在亲本或DR PDOs中,接受LGR4-mAb和化疗联合治疗的组具有最小的肿瘤尺寸和最高的存活率。与亲本PDOs形成的肿瘤相比,DR PDOs在小鼠体内形成了更大的肿瘤,这些肿瘤对单一化疗治疗具有难治性和耐药性,联合治疗显著抑制了异种移植肿瘤的生长,而单独使用LGR4-mAb则略微减少了DR PDOs的肿瘤形成。通过PDOs生物库的化学敏感性分析表明,LGR4单克隆抗体增强的细胞死亡水平与LGR4水平密切相关。
与上述结果一致,LGR4和SLC7A11的表达水平在大多数CRC PDOs中呈正相关(>80%),对化疗药物的敏感性与LGR4和SLC7A11的表达呈反比。值得注意的是,这些PDOs在使用LGR4-mAb治疗后对化疗药物的敏感性增加,而其他抗体如临床使用的西妥昔单抗(EGFR-mAb)和市售的LGR5-mAb则没有增加。几种LGR4和SLC7A11水平较高的PDOs,如P1和P4,对化疗药物更耐药,但可被LGR4-mab致敏。当考虑这两个基因时,LGR4和SLC7A11水平均较高的结直肠癌患者的总体生存率甚至比LGR4和SLC7A11水平较低的组更差。综上所述,LGR4-Wnt通路转录调节SLC7A11的表达,并且LGR4和SLC7A11的高水平表达可以预测结直肠癌患者的阴性临床结果。值得注意的是,LGR4-mAb在体内强烈抑制LGR4-Wnt通路,降低SLC7A11水平,促进铁死亡,提高化疗药物的效率。
接下来,将亲本 PDOs和DR PDOs分别皮下注射到裸鼠体内,当DR PDOs形成的肿瘤体积达到50 mm3时,通过腹腔注射不同化疗药物和LGR4-mAb对小鼠进行治疗。病理分析显示,在亲本或DR PDOs中,接受LGR4-mAb和化疗联合治疗的组具有最小的肿瘤尺寸和最高的存活率。与亲本PDOs形成的肿瘤相比,DR PDOs在小鼠体内形成了更大的肿瘤,这些肿瘤对单一化疗治疗具有难治性和耐药性,联合治疗显著抑制了异种移植肿瘤的生长,而单独使用LGR4-mAb则略微减少了DR PDOs的肿瘤形成。通过PDOs生物库的化学敏感性分析表明,LGR4单克隆抗体增强的细胞死亡水平与LGR4水平密切相关。
与上述结果一致,LGR4和SLC7A11的表达水平在大多数CRC PDOs中呈正相关(>80%),对化疗药物的敏感性与LGR4和SLC7A11的表达呈反比。值得注意的是,这些PDOs在使用LGR4-mAb治疗后对化疗药物的敏感性增加,而其他抗体如临床使用的西妥昔单抗(EGFR-mAb)和市售的LGR5-mAb则没有增加。几种LGR4和SLC7A11水平较高的PDOs,如P1和P4,对化疗药物更耐药,但可被LGR4-mab致敏。当考虑这两个基因时,LGR4和SLC7A11水平均较高的结直肠癌患者的总体生存率甚至比LGR4和SLC7A11水平较低的组更差。综上所述,LGR4-Wnt通路转录调节SLC7A11的表达,并且LGR4和SLC7A11的高水平表达可以预测结直肠癌患者的阴性临床结果。值得注意的是,LGR4-mAb在体内强烈抑制LGR4-Wnt通路,降低SLC7A11水平,促进铁死亡,提高化疗药物的效率。
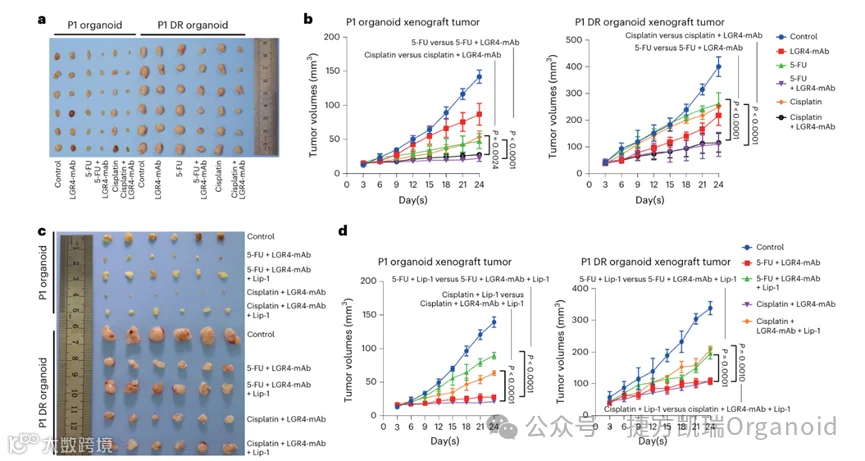
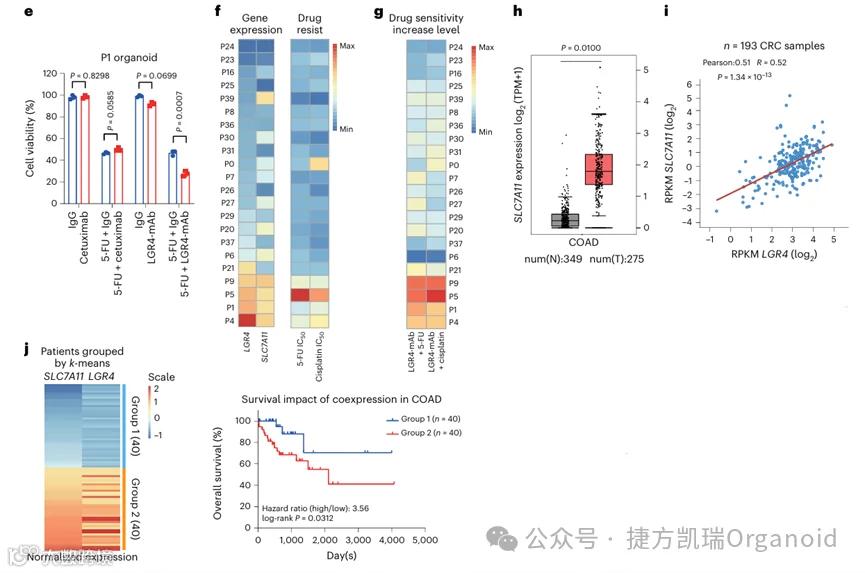
本研究设计了一种单克隆抗体LGR4-mAb,能有效抑制LGR4-Wnt信号传导,并发现LGR4-mAb能显著敏化药物诱导的铁死亡;从机制上讲,LGR4依赖性Wnt信号转导转录上调铁死亡的关键抑制剂SLC7A11,从而获得获得性耐药。因此,针对结直肠癌耐药,通过LGR4-mAb靶向LGR4来选择性激活铁死亡是一种独特而强大的方法。
Zheng, Hao et al. “Targeted activation of ferroptosis in colorectal cancer via LGR4 targeting overcomes acquired drug resistance.” Nature cancer, 10.1038/s43018-023-00715-8. 30 Jan. 2024, doi:10.1038/s43018-023-00715-8
本研究中的类器官模型培养相关试剂和实验,欢迎各位老师沟通交流,我们提供专业的类器官技术服务!

公司介绍

服务和产品:
公司地址:上海市嘉定区兴贤路1180号育成生物医药园5幢216室
Shanghai JFKR Organoid Biotechnology Co.,Ltd
 扫码添加小助手
E-mail: info@jfkrorganoid.com
公司网址:http://www.jfkrorganoid.cn/
扫码添加小助手
E-mail: info@jfkrorganoid.com
公司网址:http://www.jfkrorganoid.cn/

















 扫码添加小助手
扫码添加小助手



