

研究结果

研究背景
微卫星稳定型结直肠癌(MSS-CRC)对免疫检查点抑制剂(如抗PD-1疗法)反应较差,亟需寻找增强其疗效的方法。
丁酸盐是肠道细菌代谢产物,此前在小鼠模型中已显示其免疫促进作用,但在人类MSS-CRC中的作用机制尚不明确。
验证丁酸盐是否能增强抗PD-1疗法在MSS-CRC中的效果,并阐明其通过调控CD8+ T细胞亚群的机制。
关键实验设计与方法
模型构建:
使用MSS-CRC患者来源的类器官(PDOs)与自体肿瘤浸润淋巴细胞(TILs)共培养系统,模拟肿瘤微环境。
通过流式细胞术、单细胞RNA测序(scRNA-seq)等技术分析T细胞亚群和功能变化。
主要处理组:
对照组:TILs + 类器官。
丁酸钠(NaBu)组:TILs + 类器官 + 丁酸盐。
联合治疗组:TILs + 类器官 + 丁酸盐 + 抗PD-1抗体。
实验结果
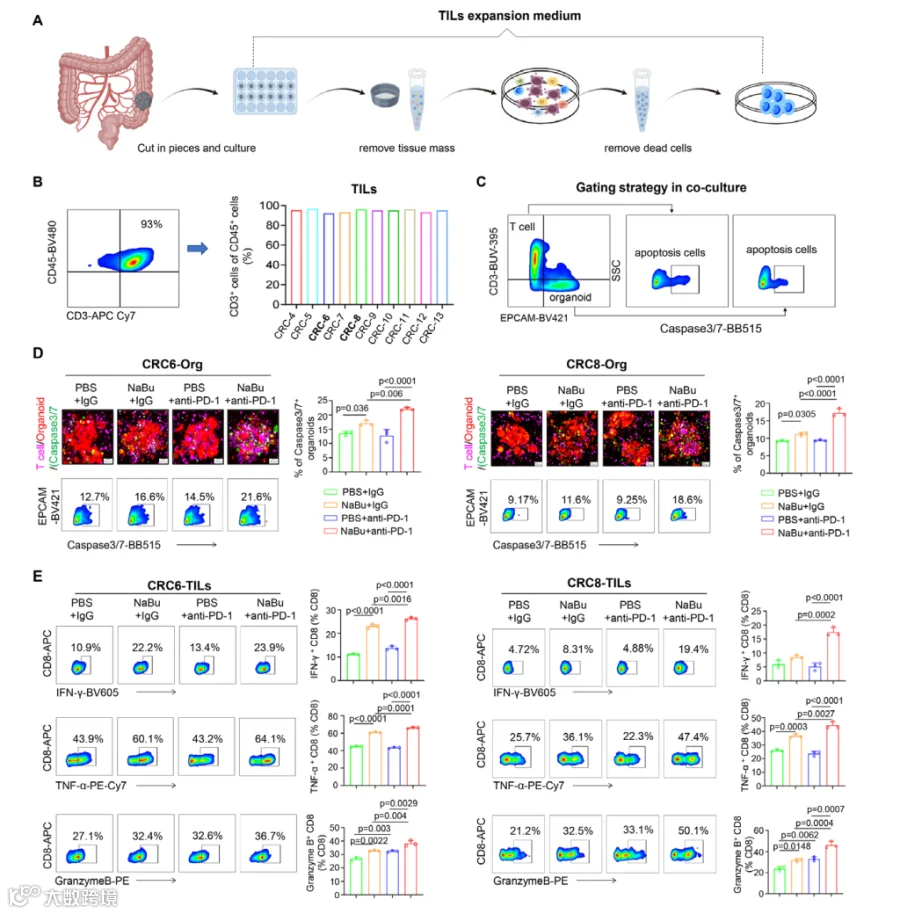
丁酸盐增强TILs的杀伤效果:
丁酸盐显著提升TILs诱导的类器官凋亡(图1D),且与抗PD-1联用后效果更显著。
丁酸盐增加了CD8+ T细胞中IFN-γ+、TNF-α+和Granzyme B+的比例(图1E),表明其激活了T细胞的细胞毒性功能。
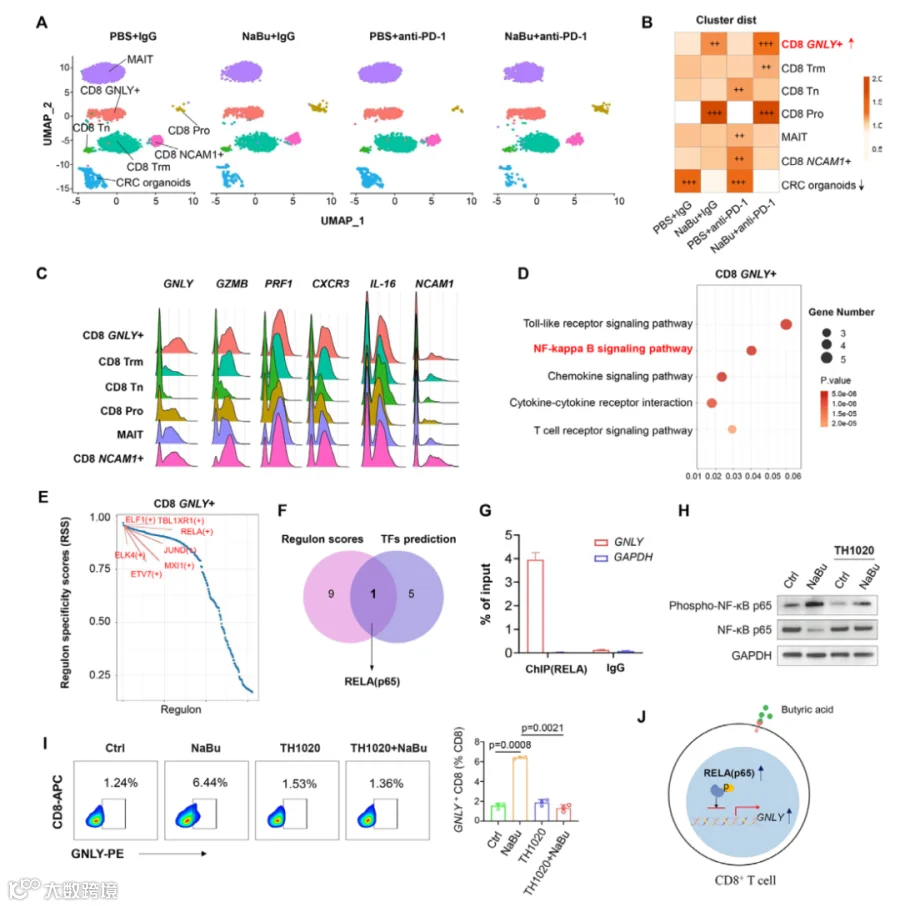
GNLY+CD8+ T细胞的关键作用:
scRNA-seq发现NaBu特异性扩增了GNLY+CD8+ T细胞亚群(图2B),该亚群高表达细胞毒性分子(GNLY、GZMB、PRF1)和趋化因子(CXCR3、IL-16)(图2C)。
联合抗PD-1后,GNLY+CD8+ T细胞比例进一步增加,提示其是丁酸盐增效的核心效应细胞。
机制解析:NF-κB通路激活:
KEGG分析显示GNLY+CD8+ T细胞中NF-κB通路富集(图2D)。
实验证实NaBu促进NF-κB(p65)磷酸化、核转位及与GNLY启动子结合(图2G-H),从而上调GNLY表达(图2I)。
使用TLR5抑制剂TH1020可阻断丁酸盐诱导的NF-κB活化和GNLY+CD8+ T细胞扩增(图2H-I),验证了NF-κB的关键作用。
研究意义与创新点
转化医学价值:
丁酸盐作为天然代谢物,安全性高,可能成为MSS-CRC免疫治疗的辅助药物,尤其适用于对抗PD-1疗法耐药的患者。
研究为“肠道菌群-代谢物-免疫治疗”联用策略提供了实验依据。
技术亮点:
患者来源类器官与自体TILs共培养系统,更贴近人类肿瘤微环境的复杂性。
结合scRNA-seq和功能实验,从单细胞水平解析了丁酸盐的靶细胞亚群。
机制突破:
首次揭示丁酸盐通过NF-κB-GNLY轴激活CD8+ T细胞,为优化联合治疗方案提供了新靶点。


 扫码添加小助手
扫码添加小助手


