


研究结果

本研究探讨了霍乱弧菌的毒力机制,通过外膜囊泡(OMVs)传递的锌金属蛋白酶HapA。与OMVs结合的HapA比其纯化形式更有效地破坏肠道上皮细胞模型中紧密连接和粘附连接的完整性,表明OMVs显著增强了HapA的致病效应。研究还详细描述了霍乱弧菌OMVs被上皮细胞摄取的过程,以及它们对关键连接蛋白(如claudin、ZO-1和β-连环蛋白)的靶向降解。这些结果凸显了OMVs相关HapA在破坏上皮屏障功能中的关键作用。此外,通过使用球状体和肠道类器官模型,实验进一步揭示了细菌致病机制,为开发靶向治疗策略提供了重要信息。
研究内容
OMVs增强HapA活性:OMVs作为载体,保护HapA免受降解,并促进其高效递送至宿主细胞。
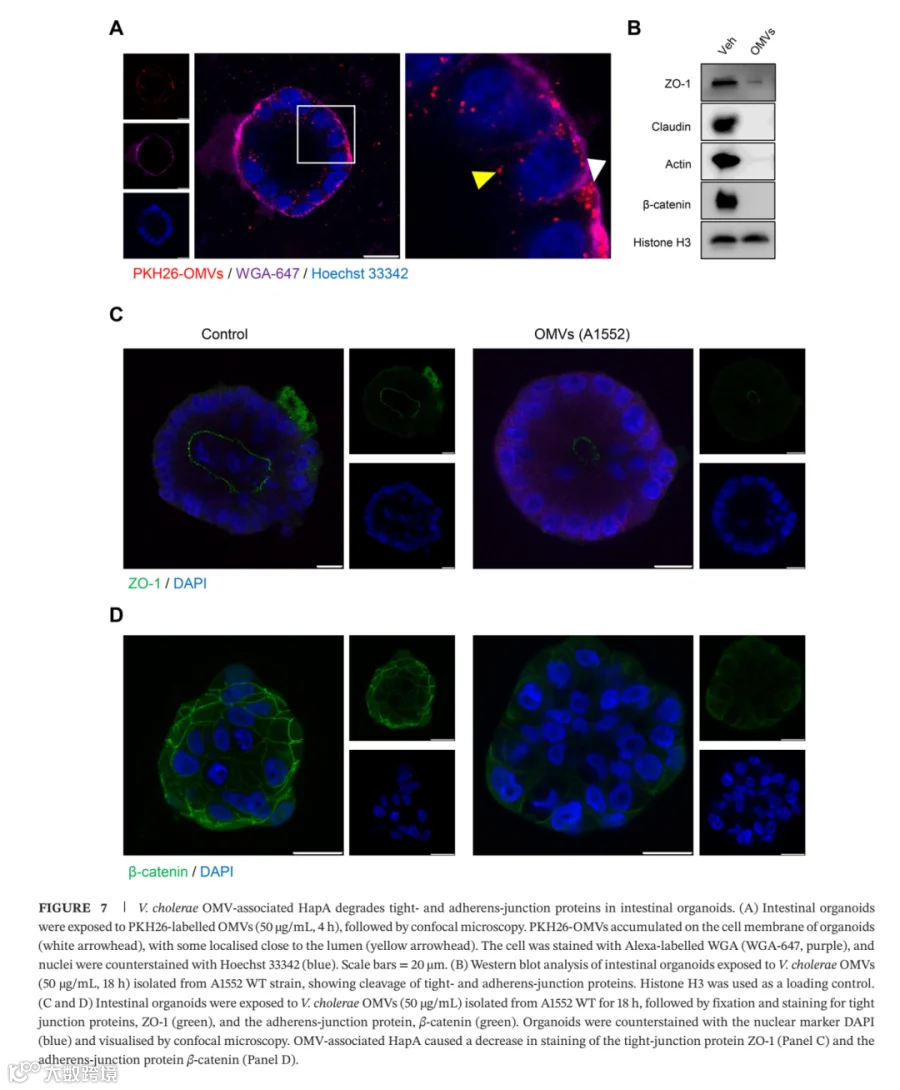
连接蛋白的靶向降解:HapA特异性降解紧密连接(如ZO-1、claudin)和粘附连接(如β-连环蛋白)的关键蛋白,破坏上皮屏障功能。
多途径内化机制:OMVs通过小窝蛋白、网格蛋白和巨胞饮作用进入宿主细胞,最终定位于溶酶体。
类器官模型的验证:在3D球状体和肠道类器官中,HapA表现出与2D模型一致的破坏作用,证实其生理相关性。


 扫码添加小助手
扫码添加小助手


