免疫细胞的精细分类一直受到各领域众多专家的关注和重视。近日,《中华预防医学杂志》发布《基于多参数流式细胞术的外周血免疫细胞亚群精细分析中国专家共识》,再次将免疫细胞精细分析推向“焦点”!
该共识综合分析了反馈意见,纳入了中国中西医结合学会检验医学专业委员会92位专家(其中大部分已使用或部分使用多参数流式细胞术进行外周血免疫细胞亚群精细分析)关于“基于多参数流式细胞术的外周血免疫细胞亚群精细分析”的文献。
多参数流式细胞术是检测免疫细胞亚群和评价免疫功能的重要技术手段。通过增加更多的参数,获取更多的细胞亚群信息,不仅可以在筛查淋巴瘤[1-3]和肿瘤前驱病变(包括癌前病变和癌前状态)[4-5],以及一些遗传性和免疫缺陷疾病的诊断[6-8]中起到一定的作用,还可以发现许多良恶性疾病的发生、发展和预后都与免疫细胞亚群有关[9-16]。在免疫治疗[17]和造血干细胞移植[18]等特殊治疗中,精细免疫细胞亚群的异常变化可能与疾病预后和并发症有关。
为规范流式细胞术外周血免疫细胞亚群的精细化检测方法和方案,进一步促进其在临床疾病诊断、治疗和健康管理中的应用,中国中西医结合协会检验医学专业委员会组织专家制定了本专家共识[19]。共15篇,不仅是基于免疫细胞精细分类的细致工作,也是免疫细胞精细分类在临床实践中广泛应用的重要基础。
共识首先指出,强烈建议在基础淋巴细胞亚群检测的基础上增加分化、发育、功能、活化等相关标志物,并根据临床需要选择不同的免疫细胞亚群组合进行精细分析,如CD25/CD127、CD28等;其次,建议进行多样性和多表型免疫细胞检测,解释免疫标记物组合的精细分类和亚群定义;第三,强烈建议使用多管8色检测方案,细化后的子组比例为上一级子组的比例。在包括TBNK绝对计数管、T细胞管、B细胞管、TCR管、Treg/Th管、DC/NK/单核管在内的多管8色系统中,基本的TBNK绝对计数需要按照国家指南进行控制,其他5管只能报告百分比进行精细分型。如果精分型报告绝对计数,则需要根据细胞亚群的特点增加细胞数量和样本量;第四,强烈建议使用参考区间或参考范围作为术语,并建议进行精细免疫细胞亚群分析,以获得健康个体的参考区间[19]。
在传统简单淋巴细胞亚群检测的基础上,增加分化、发育、功能、活化等相关标志物,根据临床应用需要,选择不同组合的免疫细胞亚群进行精细分析。
推荐强度:强烈推荐。
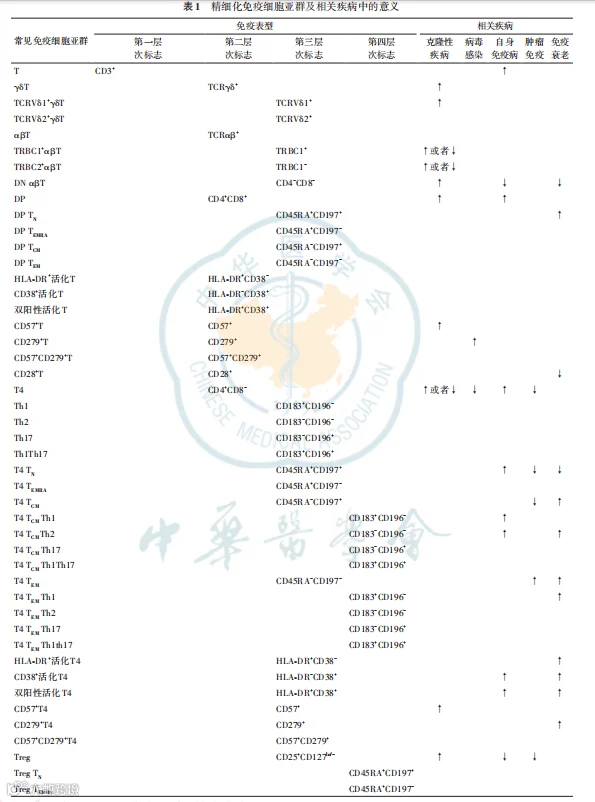
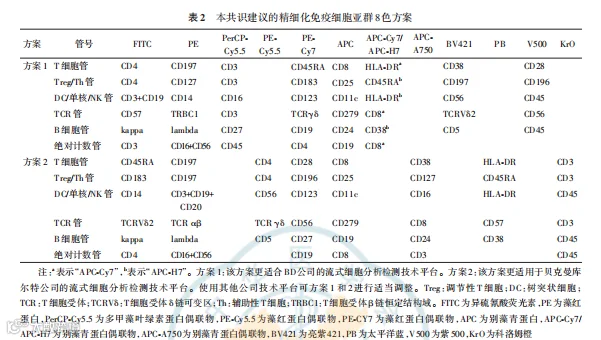
根据临床应用需要选择相应的生物标志物进行不同组合的T细胞相关检测。最低检测要求:淋巴细胞占核细胞的比例和绝对数,T细胞(包括总T细胞、CD4+T细胞、CD8+T细胞)、B细胞、NK细胞占淋巴细胞的比例和绝对数;建议增加标记提供免疫细胞亚群分析指标,如Treg细胞比率、活化T细胞比率和功能T细胞比率。抗原组合和方案见表1和表2。
推荐强度:强烈推荐。
建议采用CD3+CD4+CD25+CD127lo/-检测Treg和CD45RA/CD197,将T细胞亚群分化为TN、TCM、TEM、TEMRA。CD38/HLA-DR可用于区分单阳性或双阳性活化T细胞亚群,CD183/CD196可选择性加入,将Th亚群分为CD183+CD196-、CD183-CD196-和CD183-CD196+三个亚群。
推荐强度:强烈推荐。
根据临床应用需要选择与B细胞亚群相关的检测标志物。建议完善免疫细胞亚群的分析,包括CD27、CD24和CD38,并酌情包括kappa、lambda和CD5。推荐的抗原检测和方案见表1和表2。
推荐强度:强烈推荐。
基本的免疫细胞功能分析很少关注NK细胞、单核细胞和dc的亚群分化。精细分析免疫细胞亚群可逐步增加标记物组合,根据CD16和CD56的表达区分NK细胞亚群,使用HLA-DR+CD14+/lo和HLA-DR+CD14-分别识别谱系阴性(CD3-CD19-CD56-)细胞群的单核细胞和DC细胞群(需要注意的是,在天然免疫抑制/抑制的患者中,单核细胞和DC中HLA-DR的表达可降低);进一步用CD16和CD14对单核细胞进行分组,用CD123和CD11c对dc进行分组。
推荐强度:积极建议。
目前,MDSC研究主要用于与某些良恶性疾病相关的特异性免疫细胞亚群的研究。不建议将这些亚群包括在免疫细胞的一般基础和精细分析中。其他免疫细胞群也主要用于与疾病治疗相关的特殊免疫细胞的检测,方案根据研究和应用需要有所不同。
推荐强度:积极建议。
根据疾病特点和检测目的选择相应的组合,筛选与特殊疾病和健康管理相关的特殊免疫细胞亚群。
推荐强度:一般推荐。
由于绝对计数和精细化子群分析在操作上存在差异,建议将它们分开进行。绝对计数管只进行基本总T细胞、CD4+T细胞、CD8+T细胞、B细胞、NK细胞的比例和绝对计数。可采用单平台和双平台方法,操作分析的技术要点和质量控制详见国家指南。
推荐级别:强烈推荐。
推荐使用8色MFC管对免疫细胞亚群进行精细分析,并根据临床应用需要选择精细程度和方案。可采用多管8色及以上方案或一管超多色方法,细化子组比例为上一级子组比例。一致推荐的8色多管组合方案见表2。在使用其他MFC检测技术平台时,可以对该方案进行相应的调整和确定。
推荐级别:强烈推荐。
Diva、flowjo、kaluza等类似软件可用于数据分析。T细胞、B细胞、NK细胞、dc细胞、单核细胞、粒细胞和推荐用于分析的各种亚群的免疫表型定义和方案见表1和表2。
推荐级别:强烈推荐。
用于确定免疫细胞亚群检测结果的参考物质的术语,建议使用参考区间或参考范围代替正常值。
推荐强度:强烈推荐。
为了通过免疫功能检测达到前瞻性预警和筛查的目的,建议进行精细化的免疫细胞亚群分析,获得popRI;以popRI为参考,以相关指南为共识,解释个别检测结果,为临床诊断、治疗和健康管理提供辅助诊断信息或进一步的检测建议。
推荐强度:强烈推荐。
疾病的发展和治疗有一个规律的过程。为了预警疾病进展,发现并发症,建议建立合理的治疗和疾病恢复监测时间点,并在无并发症的患者中建立反映免疫细胞恢复的RCV。
推荐强度:积极建议。
建议将一些成熟免疫老化(如CD57)和免疫衰竭(如PD1)相关指标纳入精致免疫细胞亚群;将popRI划分为不同的年龄组,甚至创建年度变化曲线,并定期修改。
推荐强度:积极建议。
健康管理的地位越来越重要,免疫功能检测应在淋巴瘤及肿瘤前体病变的早期筛查、部分淋巴细胞克隆指标的建立等方面发挥一定的作用。建议将kappa/lambda与TRBC1、TCRV δ 1和/或TCRV δ 2逐步整合。纳入精细免疫细胞亚群检测。
推荐强度:积极建议。

从这个版本的中国专家共识可以看出,“精细化分析”和“多参数”至关重要。传统的免疫细胞检测和功能评价过于简单,仅限于检测T、B、NK细胞的比例和绝对数量,反映了免疫细胞的不完整和三维信息。通过对外周血免疫细胞亚群的精细分析,可以检测到调节性T细胞(Tregs)、树突状细胞(dc)和其他类型的免疫细胞,以及与它们的分化、发育、功能和激活状态相关的标志物,从而更准确地描述免疫细胞的分期和相关细胞功能,为临床实践提供更多可选信息。
参考文献
[1] Qiu ZY, Shen WY, Fan L, et al. Assessment of clonality in Tcell large granular lymphocytic leukemia: flow cytometric T cell receptor Vβ repertoire and T cell receptor gene rearrangement[J]. Leuk Lymphoma, 2015, 56(2):324-331. DOI: 10.3109/10428194.2014.921297.
[2] Berg H, Otteson GE, Corley H, et al. Flow cytometric evaluation of TRBC1 expression in tissue specimens and body fluids is a novel and specific method for assessment of T-cell clonality and diagnosis of Tcell neoplasms[J]. Cytometry B Clin Cytom, 2021, 100(3): 361-369. DOI: 10.1002/cyto.b.21881.
[3] Chen X, Zhao S, Liu L, et al. Flow Cytometric Pattern of TCRVδ Subtype Expression Rapidly Identifies γδT Cell Lymphoma[J]. Front Oncol, 2020, 10:844. DOI: 10.3389/ fonc.2020.00844.
[4] Galigalidou C, Zaragoza-Infante L, Iatrou A, et al. Understanding Monoclonal B Cell Lymphocytosis: An Interplay of Genetic and Microenvironmental Factors[J]. Front Oncol, 2021, 11: 769612. DOI: 10.3389/ fonc.2021.769612.
[5] de Faria-Moss M, Yamamoto M, Arrais-Rodrigues C, et al. High frequency of chronic lymphocytic leukemialike low-count monoclonal B-cell lymphocytosis in Japanese descendants living in Brazil[J]. Haematologica, 2020, 105(6):e298-e301. DOI: 10.3324/haematol.2019.230813.
[6] van der Burg M, Kalina T, Perez-Andres M, et al. The EuroFlow PID Orientation Tube for Flow Cytometric Diagnostic Screening of Primary Immunodeficiencies of the Lymphoid System[J]. Front Immunol, 2019, 10: 246. DOI: 10.3389/fimmu.2019.00246.
[7] de Haas M, Kleijer M, van Zwieten R, et al. Neutrophil Fc gamma RIIIb deficiency, nature, and clinical consequences: a study of 21 individuals from 14 families [J]. Blood, 1995, 86: 2403-2413.
[8] Lima M. Laboratory studies for paroxysmal nocturnal hemoglobinuria, with emphasis on flow cytometry[J]. Pract Lab Med, 2020, 20: e00158. DOI: 10.1016/j. plabm.2020.e00158.
[9] Bizymi N, Matthaiou AM, Matheakakis A, et al. New Perspectives on MyeloidDerived Suppressor Cells and Their Emerging Role in Haematology[J]. J Clin Med, 2022, 11(18):5326. DOI: 10.3390/jcm11185326.
[10] Xu X, Wei F, Xiao L, et al. High proportion of circulating CD8 + CD28-senescent T cells is an independent predictor of distant metastasis in nasopharyngeal canrcinoma after radiotherapy[J]. J Transl Med, 2023, 21(1): 64. DOI: 10.1186/s12967-023-03912-2.
[11] Neu SD, Dittel BN. Characterization of Definitive Regulatory B Cell Subsets by Cell Surface Phenotype,Function and Context[J]. Front Immunol, 2021, 12: 787464. DOI: 10.3389/fimmu.2021.787464.
[12] Oras A, Peet A, Giese T, et al. A study of 51 subtypes of peripheral blood immune cells in newly diagnosed young type 1 diabetes patients[J]. Clin Exp Immunol, 2019, 198(1):57-70. DOI: 10.1111/cei.13332.
[13] Rodriguez-Iturbe B, Pons H, Johnson RJ. Role of the Immune System in Hypertension[J].Physiol Rev, 2017, 97(3):1127-1164. DOI: 10.1152/physrev.00031.2016.
[14] Hardcastle SL, Brenu EW, Johnston S, et al. Characterisation of cell functions and receptors in Chronic Fatigue Syndrome/Myalgic Encephalomyelitis (CFS/ME) [J]. BMC Immunol, 2015, 16:35. DOI: 10.1186/ s12865-015-0101-4.
[15] 张晓畅, 吕跃斌, 周锦辉, 等. 中国9个长寿地区65岁及以上人群中性粒细胞与淋巴细胞比值与抑郁症状的关联研究[J].中华预防医学杂志 , 2021, 55(1): 25-30. DOI: 10.3760/cma.j.cn112150-20200812-01112.
[16] Liu W, Zhang Y, Zhu W, et al. Sinomenine Inhibits the Progression of Rheumatoid Arthritis by Regulating the Secretion of Inflammatory Cytokines and Monocyte/Macrophage Subsets[J]. Front Immunol, 2018, 9:2228. DOI: 10.3389/fimmu.2018.02228.
[17] 中国中西医结合学会检验医学专业委员会.流式细胞术在嵌合抗原受体T 细胞免疫治疗相关检验中的应用专家共识[J]. 中华检验医学杂志, 2022, 45(8): 790-801. DOI: 10.3760/cma.j.cn114452-20220218-00081.
[18] Skert C, Perucca S, Chiarini M, et al. Sequential monitoring of lymphocyte subsets and of T-and-B cell neogenesis indexes to identify time-varying immunologic profiles in relation to graft-versus-host disease and relapse after allogeneic stem cell transplantation[J]. PLoS One, 2017, 12(4):e0175337. DOI: 10.1371/journal.pone.0175337.
[19]中国中西医结合学会检验医学专业委员会. 基于多参数流式细胞术精细化分析外周血免疫细胞亚群的中国专家共识[J].中华预防医学杂志, 2023, 57(11): 1729-1747.