
西湖大学未来产业研究中心根据全球生物制药产业未来布局和我国重点研究方向,结合中国未来生物制药产业发展到2035年所面临的现状,初步提出了中国未来生物制药产业需要重点关注和大力支持的十大领域(排名不分先后)。
1 AI等信息化技术在生物医药的应用
人工智能等信息技术在生物制药领域的深度应用,被称为“人工智能+生物医药”,是指企业和研究机构将人工智能与生物制药相结合,实现生物制药领域的创新突破。
人工智能(AI)是全球发展的关键技术之一,其研究课题包括计算机视觉、自然语言处理、机器人、专家系统、推荐系统等。在技术发展不断突破、快速迭代的今天,通过不同学科、不同领域的交叉融合进行深度创新,已经成为各行业产业发展和科学研究的新范式。
生物医学是人工智能的重要跨学科研究和应用领域。
2017年,《自然》杂志报道了一个具有皮肤癌专家级诊断能力的人工智能系统[1],这是人工智能赋予生物制药领域的开创性里程碑。
2020年,DeepMind发布了人工智能算法AlphaFold 2,该算法可以根据氨基酸序列准确预测蛋白质的3D结构。其预测精度可与实验技术分析的三维结构相媲美。这一成果被认为解决了过去50年来生物学的重大挑战,在科学界引起了轰动,再次掀起了“人工智能+生物制药”的研究和产业化浪潮。
2022年,Meta基于最新的几何深度学习模型“EquiBind”开发了ESMFold,成功预测了超过6亿个蛋白质的结构,比AlphaFold 2快60倍。

图片来源:https://www.youtube.com/watch?app=desktop&v=N-eisTvUYrk
人工智能+生物制药已经应用于生物制药的多个子领域,包括新药开发、酶与蛋白质设计、医学图像分析、疾病预测、疾病预防、智能诊断、精准医疗等,并有望广泛重塑生物制药研究和产业的现状。
人工智能与生物制药的结合,可以从上游到下游应用于生物制药行业,一些应用场景已经可以为企业带来实际效益。
以新药开发为例:在研发阶段,“人工智能+生物制药”可以自动从文献中分析文本,提取与药物开发相关的关键信息,协助研发人员进行研发和产业化决策;在药物研发阶段,利用生物制药试验智能分析和临床大数据,缩短发现新的治疗靶点和药物分子的周期,降低药物研发成本;在临床验证阶段,通过人工智能对临床试验数据进行智能分析,更好地了解新药对不同患者的治疗效果。
未来,我们将看到更多人工智能应用于生物制药产业链各个环节的案例,通过人工智能的应用,进一步提升生物制药相关单位的产业竞争优势。
2 重组抗体技术
重组抗体是指利用重组DNA等分子生物学技术产生的抗体。
重组抗体的最大特点是编码其抗体蛋白的氨基酸或DNA序列是已知的。因此,在制备重组抗体时,人们可以利用重组DNA等技术,将编码重组抗体的基因序列插入到表达载体中,并将其转移到表达宿主(如哺乳动物细胞、酵母或细菌)中进行表达和纯化,从而获得特定类型的重组抗体。与多克隆抗体/杂交瘤技术生产的传统单克隆抗体不同,重组抗体具有不需要动物源生产、批量一致性高等优点,可以通过标准化的生产工艺,满足大规模抗体生产的需要,控制抗体生产质量的稳定性。
重组抗体的另一个显著优势是易于进行工程修饰。
通过分子生物学、合成生物学等方法,将重组抗体人源化,降低免疫原性;或对重组抗体的重链、轻链或部分片段区进行重排或置换,设计出具有新抗体特性的重组抗体。通过噬菌体展示等技术,人们还可以对重组抗体进行高通量抗体性能筛选,以便快速筛选出具有潜在药物功效、能够特异性靶向特定治疗靶点的重组抗体。上述特征使重组抗体能够被修改成不同的形式以用于特定的应用。
例如,特异性靶向组蛋白翻译后修饰的重组抗体不仅加速和改进了表观遗传学研究,而且有可能带来新的研究突破。
近年来,重组抗体技术不断发展,单链抗体、纳米抗体、双特异性抗体等重组抗体类型也得到了广泛的研究。许多产品也已获准上市销售。人工智能等技术的蓬勃发展也使人们能够更合理、更快速地设计出更高效的重组抗体。此外,重组抗体的制备和生产技术也在不断扩大,其中无细胞表达合成系统值得关注。无细胞表达合成系统有望在更短的时间内产生更广泛的抗体产品,因为它能够进一步实现无表达的宿主型抗体生产。由于配方调节的灵活性,无细胞合成技术也可以应用于人工智能设计但宿主表达难度高的抗体的制备和生产。
目前,基于重组抗体的药物开发也已成为生物制药领域的主流之一。未来,重组蛋白药物将在癌症、传染病、免疫、内分泌代谢、神经系统等疾病的预防和治疗中发挥巨大作用。
3 小分子抑制剂技术
小分子药物一直在医学进步中发挥着重要作用,解决了人们未满足的需求。它们也是每年批准的最大药物类型(2022年,小分子药物占FDA批准的新药的50%以上)。
未来,小分子药物有望继续在新药开发中占据重要地位。
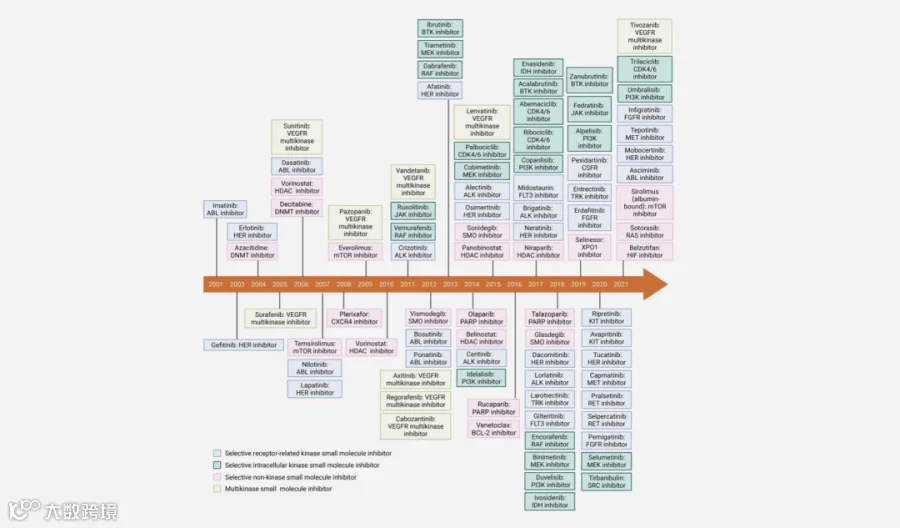
截至2022年8月5-11日,美国FDA批准用于肿瘤适应症的小分子抑制剂有88种,首次发表:2022年10月13 资料来源:https://doi.org/10.1002/mco2.181
小分子抑制剂属于小分子药物的范畴,是指一类分子量小于1000道尔顿,能够靶向蛋白质,降低蛋白质活性,或阻碍生化反应的有机化合物分子。小分子抑制剂通过直接与靶蛋白结合、与底物竞争、改变蛋白质结构或阻碍蛋白质构象变化来降低靶蛋白活性。
小分子抑制剂是目前临床常用的各种药物,包括各种蛋白质、酶、激酶、转录因子、质子泵、离子通道抑制剂等。小分子抑制剂通过快速灭活靶细胞,在精细调节细胞生命和功能方面具有显著优势,是生命科学研究中的重要工具药物。
由于其分子量小,小分子抑制剂在口服吸收、易于细胞渗透、跨越屏障(如血脑屏障)、良好的药物性能和良好的药代动力学特性方面比其他类型的药物具有优势。这些特点使得小分子抑制剂在市场和新药开发中受到广泛欢迎。近年来,得益于人工智能、计算化学、分子对接、蛋白质结构分析与预测等技术的发展,人们能够更有效地探索小分子抑制剂的新靶点,设计出合理的小分子抑制剂药物,从而加速了小分子抑制剂新药的开发。
未来,小分子抑制剂将更广泛地应用于癌症治疗和其他治疗领域,更多类型的小分子抑制剂将被引入。
4 高通量测序技术
高通量测序是指对各种生物序列(如DNA、RNA、蛋白质等)进行高通量、快速、高效、经济的测序。
在传统意义上,高通量测序通常特指高通量基因测序。国家发改委印发的《生物经济发展“十四五”规划》提出,“加快高通量基因测序技术发展,推动以单分子测序为标志的新一代测序技术创新,不断提高基因测序效率,降低测序成本。”
然而,随着近年来蛋白质等非核酸序列高通量测序技术的出现,高通量测序的含义也随之扩大。
高通量基因测序技术是基因组学等许多研究的基石技术,它的出现对生命科学和医学的发展起到了革命性的作用。例如,得益于高通量基因测序,被称为20世纪三大科学项目之一的人类基因组计划于2003年完成。
近年来,高通量基因测序技术的发展已经相对成熟,其测序对象和应用场景也变得非常多样化,如全基因组从头测序、全基因组重测序、全基因组甲基化测序、全外显子组测序、全转录组测序、RNA测序等;许多新的高通量基因测序技术层出不穷,长读段测序、单分子测序、单细胞测序、空间转录组测序等技术为生物医学研究带来了新的可能性。

随着人类基因组测序工作的完成,生命科学的研究重点可能从基因组学扩展到蛋白质组学。要更深入地了解蛋白质组的所有组成和序列信息,进一步了解生命活动和疾病发生的分子机制,关键是要有合适的高通量蛋白质测序技术作为支持。目前,高通量蛋白质测序技术虽然不如高通量基因测序技术强大。然而,非质谱高通量蛋白质测序、高分辨率蛋白质质谱、单分子蛋白质测序等新型高通量蛋白质测序技术的不断出现,也使得该技术日益成熟,带来了新的研究和产业化机遇。
中国在高通量测序领域拥有强大的研发基础和巨大的潜在市场需求,为实现该领域的弯道超车奠定了坚实的基础。
此外,高通量测序技术发展的一大特点是同时依赖生物制药硬件技术和信息软件技术的协同发展。
近年来,人工智能、生物信息学等软件算法的进步也为高通量测序技术的发展带来了新的机遇。通过更加智能化的信息技术,人们可以更高效、自动化地分析测序大数据,从而获得有意义的测序结果。
未来,高通量测序技术将在生物医学领域得到更广泛的应用,成为精准医疗等现代医学领域的重要基石;高通量蛋白质测序或将成为继高通量基因测序之后新的产业增长点。
5 药物偶联物技术
药物偶联物是指一类使用特定连接体(通常是化学链)连接具有靶向特性的配体和效应分子的药物。核心概念是靶向配体的递送和效应分子的治疗目的。
一般来说,药物偶联物的组成可以用“配体连接剂效应分子”的公式来概括。根据配体类型的不同,药物偶联物可进一步细分为:
抗体药物偶联物,肽药物偶联物,蛋白质药物偶联物,小分子药物偶联物,聚合物药物偶联物,放射性核素药物偶联物,病毒类药物偶联物,等一下。
以最近开发的具有代表性的抗体药物偶联物(antibody drug conjugates, adc)为例,以抗体作为定位配体,将adc的组成表达为“抗体连接体效应分子”。与传统药物相比,ADC具有更好的药物靶向性。
2000年,首个ADC被FDA批准用于治疗急性髓性白血病,但它存在致命毒性等缺点。
近年来,ADC技术日益先进,改良后的ADC的不良反应发生率也明显降低。随着Brentuximab vedotin(商品名Adcetris)和曲妥珠单抗emtansine(商品名Kadcyla)等新型ADC被FDA批准用于治疗霍奇金淋巴瘤和HER2阳性乳腺癌,ADC药物再次广泛进入人们的研究视野。
目前,ADC仍有巨大的发展空间。定向偶联、多价偶联、重组抗体、小分子药物等技术的进步,为ADC药物开发带来了新的可能性。基于单链抗体、纳米抗体和双特异性抗体等抗体类型的ADC药物不断涌现。
随着药物偶联技术的不断进步,药物偶联的配体、效应分子、连接体的种类选择也将日益多样化。在未来,我们将看到更多类型的药物偶联物被批准用于临床,新一代药物偶联物将继续为患者带来好消息。
6 治疗性基因编辑技术
治疗性基因编辑是指通过对基因进行靶向编辑(敲除、插入、替换、修饰等)来达到治疗效果的一种治疗方法。
治疗性基因编辑的核心技术之一是开发能够高效编辑基因的分子工具。基因编辑工具的研究已经有几十年的历史了。

2020年,法国科学家Emmanuelle Charpentier和美国科学家Jennifer Doudna被授予诺贝尔化学奖,以表彰他们基于CRISPR Cas“开发出一种基因编辑方法”,这再次点燃了基因编辑相关研究的浪潮。
CRISPR Cas基因编辑技术具有可编辑范围广、使用方便、效率高、成本低等特点,广泛应用于生命科学研究、药物开发等领域。近年来,由于该技术的日益成熟,其在治疗性基因编辑方面的直接临床研究也有所增加。
2020年3月,基于CRISPR Cas基因编辑技术的基因治疗首次直接应用于人体,治疗了一例遗传性失明的莱布尼茨先天性黑朦患者。
2022年,Vertex Pharmaceuticals和CRISPR Therapeutics开发了一种名为Excel β的治疗工具,用于遗传性血液病、地中海贫血和镰状细胞病的CRISPR Cas基因编辑疗法,已通过快速通道获得FDA批准,有望成为首个获批的CRISPR Cas基因编辑疗法。
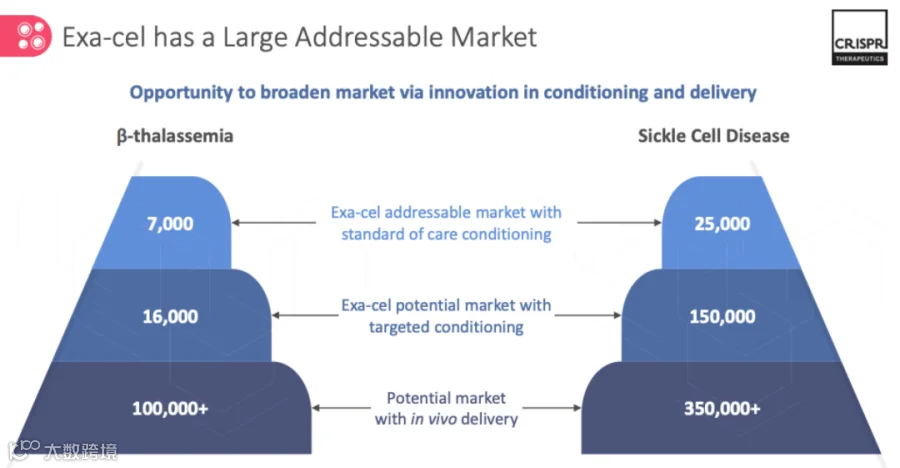
此外,许多新的CRISPR Cas系统被开发并应用于与基因编辑相关的新兴领域,如RNA编辑、单碱基编辑、先导编辑、CRISPR干扰(CRISPRi)等。
需要指出的是,虽然目前在疾病治疗领域有大量的基因编辑研究,但大部分仍处于临床前实验室研究阶段。如何进一步优化基因编辑的效率、准确性、可编辑基因序列范围,降低基因编辑脱靶效应带来的安全风险,或促进其在治疗和产业化领域的广泛应用是关键。
此外,CRISPR Cas并不是实现治疗性基因编辑的唯一技术途径,许多其他类型的基因编辑技术仍值得持续关注,如基于转座子的治疗性基因编辑技术、转录激活因子如效应核酸酶、锌指核酸酶等。
未来,我们将看到更多与治疗性基因编辑相关的新技术出现,人类将以前所未有的方式治愈一些目前没有很好的治疗方法的疾病(如基因缺乏性疾病)。
7 细胞治疗技术
细胞疗法是指将活细胞移植到患者体内以达到治疗效果的一种疗法。细胞疗法可根据所使用的治疗细胞类型进一步细分,如基于免疫细胞的细胞免疫疗法、基于干细胞的干细胞疗法等。
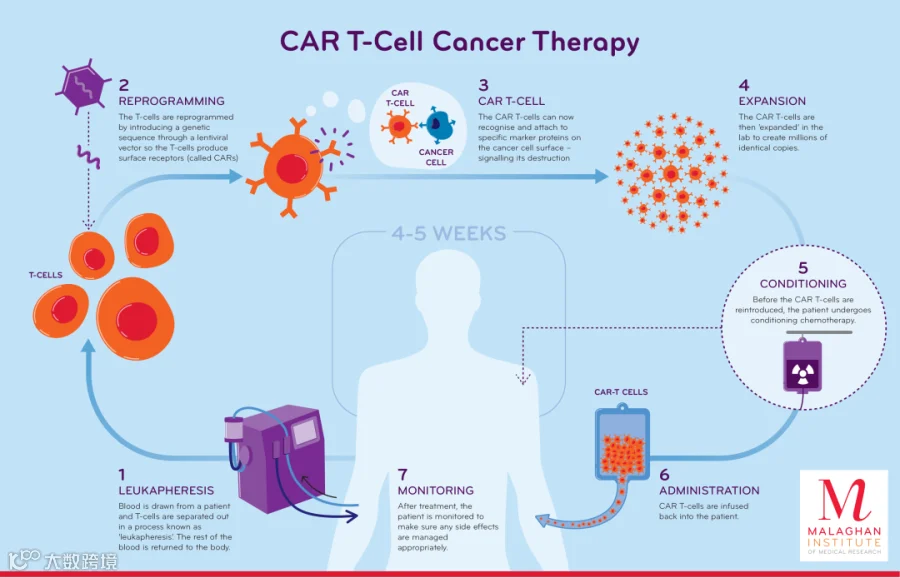
细胞免疫疗法通过将工程免疫细胞移植到体内来达到治疗效果。在细胞免疫治疗方面,CAR-T细胞(Chimeric antigen receptor T cell, CAR-T)疗法近年来取得了快速突破。其主要原理是将工程化的CAR(一种合成的跨膜受体)基因导入T细胞,从而使T细胞能够特异性杀死表达特定肿瘤特异性抗原的肿瘤细胞。
2017年,首个CAR-T疗法(由Kymriah开发)被FDA批准用于治疗急性淋巴细胞白血病。
截至2022年4月,其他5种CAR-T疗法相继获得FDA批准。然而,目前CAR-T疗法仅在血肿方面取得了良好的临床疗效,其面临的主要挑战是如何使工程免疫细胞应用于更广泛的癌症类型,特别是实体肿瘤的治疗。
针对这一点,人们也在不断开发出许多新的细胞免疫疗法,如基于非T细胞的CAR疗法(如基于NK免疫细胞的CAR-NK疗法),以及基于非CAR合成跨膜受体的细胞免疫疗法(如合成Notch受体)。
干细胞疗法是利用自然或诱导干细胞的自我更新能力和多能潜能,修复或重建病变/衰老细胞/组织的功能,从而达到治疗效果。在临床实践中,除了直接利用天然干细胞(如脐带血干细胞、间充质干细胞等)进行干细胞治疗外,诱导多能干细胞、细胞重编程等技术也值得关注。通过诱导多能干细胞和细胞重编程等技术,分化后的细胞可以在特定条件下逆转恢复到干细胞样状态(或直接转化为靶细胞类型)进行治疗。这类技术由于具有逆转细胞命运的潜力,也可能为抗衰老领域带来希望。目前抗衰老领域市场前景巨大,但尚未取得重大突破。
在未来,更多类型的细胞将被开发用于细胞治疗;基于患者的个性化和定制细胞疗法有望为更多无法治愈的疾病提供新的治疗选择。
8 新型药物递送技术
给药系统是指从空间、时间、剂量等方面综合调节药物在机体内分布的技术系统。通过加强治疗药物对靶标区域的输送,它最大限度地减少了靶标区域外的积累,改善了患者的健康。

与传统的口服片剂、胶囊、静脉注射剂、吸入制剂、透皮贴剂等传统给药系统相比,新型给药系统是指采用整体技术壁垒较高的新型给药技术(如基于脂质体、纳米颗粒、微球、外泌体、工程AAV载体、3D打印药物制剂等给药技术)来递送各类药物的系统。
新型给药系统通过调节药物的给药和释放位置,改变药物在体内的代谢行为,改善药物缓释和控制特性,穿透生理屏障(如血脑屏障),提高药物的疗效,减少毒副作用。
2018年,FDA批准推出首个使用脂质纳米颗粒作为递送载体的RNAi药物Onpattro;2021年,首个mRNA疫苗Comirnaty批准了脂质纳米颗粒作为递送载体。
总体而言,目前已经开发和上市的新型给药系统产品数量仍然相对较少。
未来,为了满足各种新药的给药需求,如基因药物、mRNA药物、多肽和蛋白质药物、细胞药物等,我们还需要更多创新的新药给药系统。
9 免疫检查点抑制剂
免疫检查点抑制剂是指一类靶向肿瘤的免疫治疗药物,其主要机制是阻断一类称为免疫检查点的蛋白质,恢复免疫系统杀伤肿瘤细胞的能力,从而起到治疗肿瘤的作用。
2018年,美国科学家詹姆斯·艾利森(James Allison)和日本科学家本庶佑(Tasuku Honjo)因对免疫检查点抑制剂的贡献而获得诺贝尔生理学或医学奖。

图片来源:twitter.com/NobelPrize/
目前可用的免疫检查点抑制剂主要是针对免疫检查点PD-1/PD-L1或CTLA-4的单克隆抗体。
2011年,FDA批准了首个免疫检查点抑制剂,靶向CTLA-4的Ipilimumab单克隆抗体,用于治疗黑色素瘤。随后,靶向PD-1/PD-L1的免疫检查点抑制剂被批准用于黑色素瘤、肺癌和结肠癌等肿瘤。
此外,目前有多种针对免疫检查点靶点的免疫检查点抑制剂正在研究中,如LAG-3、TIM-3、TIGIT、VISTA等;此外,双特异性抗体也是免疫检查点抑制剂研究和开发的重点,目前正在开发多种双特异性抗体,可以同时靶向PD-1/PD-L1和CTLA-4。
未来,随着对肿瘤免疫调节机制的研究更加深入,有望开发出更多可应用于不同肿瘤治疗的免疫检查点抑制剂。
10 脑机接口技术
在专家问卷反馈中,脑机接口技术被提及的相对较多,并且有可能对未来的生物制药产生重大影响。脑机接口(Brain Computer Interface, BCI)是指一种人机连接方式,可以直接在大脑信号与机器(最常见的是计算机、芯片或机器人肢体)之间建立通信通路。通过脑机接口技术,人们可以通过机器提取和识别大脑中神经系统编码的信息,如记忆、决策、情绪等;基于机器接收到的大脑信息,人们可以进一步调节大脑活动。

脑机接口在神经科学、神经和精神疾病的研究以及临床治疗等方面具有丰富的应用前景。例如,通过脑机接口,人们可以更好地捕捉大脑不同区域在不同时间、不同状态下产生的神经活动信号,进而研究大脑的信息编码机制。这也有望激发新的人工智能算法的发展;通过脑机接口,人们可以更好地监测生理病理状态下不同神经和精神疾病的脑信号,破译疾病发病机制,进而制定相关疾病的针对性治疗方法;人们还可以通过植入能够刺激神经的脑机接口芯片来纠正错误的神经活动或促进正常神经信号的重建,有可能治疗一些难以治疗的脑相关疾病(如癫痫、视力丧失、听力丧失、阿尔茨海默病等);脑机接口也用于恢复残疾或瘫痪患者的行动能力。残障患者可以通过无创脑机接口控制外肢,替代残障肢体的功能。
根据《中华人民共和国国民经济和社会发展“十四五”规划和2035年远景目标》,神经科学和人工智能是国家战略性科技力量,脑机接口技术(脑机集成技术)是其中的关键技术。
未来,脑机接口技术有望推动神经科学和人工智能领域的研究突破,并在神经和精神疾病的诊断、治疗和康复等临床领域实现更广泛的应用。
END



汇光生物



