如今,亚马逊市场的竞争越来越激烈,产品的利润越来越低;有些卖家朋友开发一些竞争相对较小,尚且利润较好的品类或产品。而医疗器械类(510k)的产品,由于是亚马逊的受限类商品,以及法律等规则形成的门槛;使得医疗器械类(510k)商品是比较符合要求。
然而,在亚马逊销售医疗器械(510k)相关产品时,商家需要深入了解并严格遵守美国食品药品监督管理局(FDA)的合规性要求和市场准入流程。以下将提供更多细节,帮助商家更好地理解和应对这一过程。
一、510k合规性要求
1. 明确产品分类
首先,商家需要确定所销售的医疗器械产品是否属于需要提交510k申请的范围。FDA根据风险等级将医疗器械分为三类:
-
I类(低风险):
-
牙齿保护器 -
防毒面具头带 -
储液袋 -
压差传感器 -
.......等等
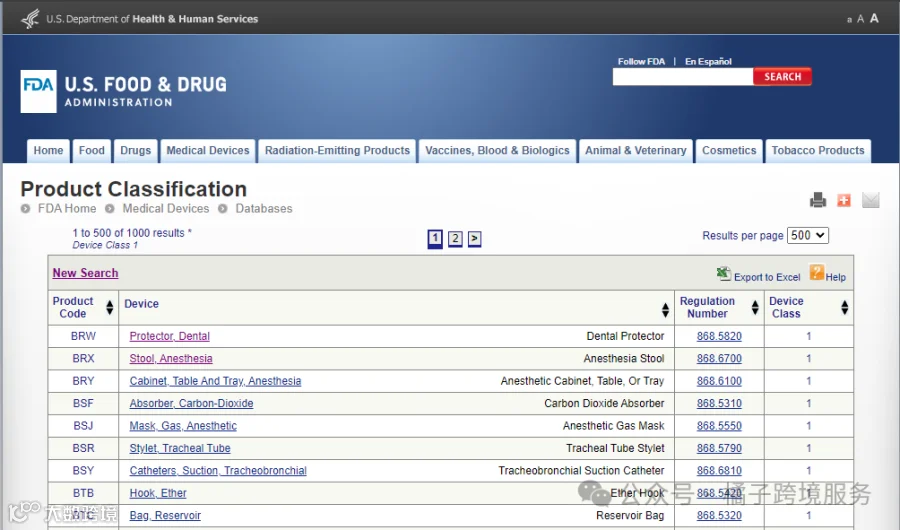
II类(中等风险):
n氦气分析仪
n红光面膜
n麻醉传导导管
.......等等
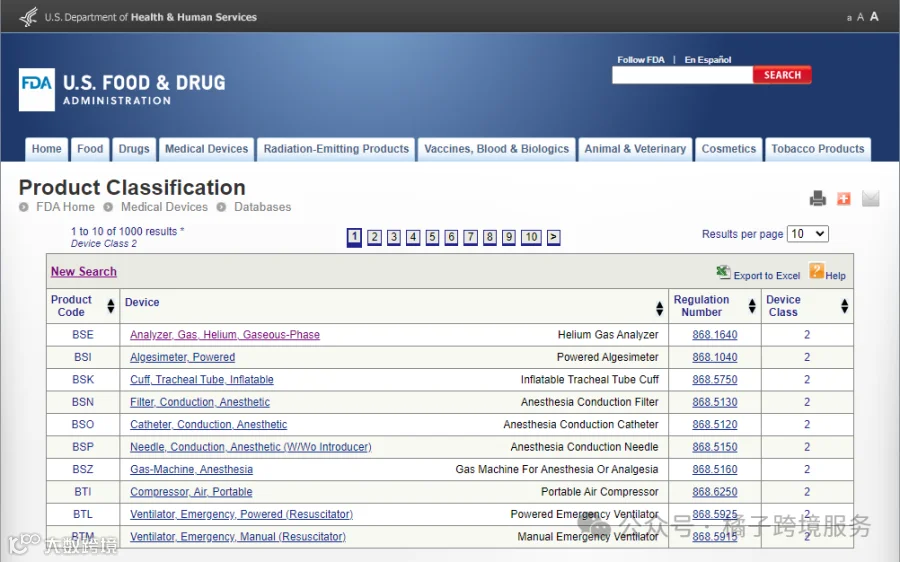
III类(高风险):
电麻醉设备
肺水监测仪
.......等等
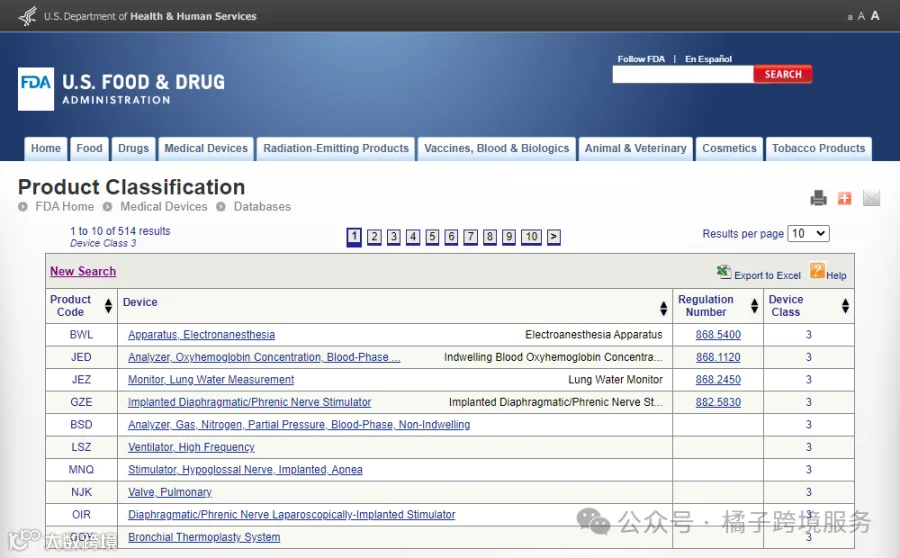
大多数II类器械和部分I类、III类器械需要提交510k申请。商家可以查阅FDA的医疗器械分类数据库,以确认产品的具体分类。
2. 准备510k申请资料
如果产品需要提交510k申请,商家需要准备详尽的申请资料。这些资料通常包括:
行政信息:如公司名称、地址、联系方式等。
设备描述:包括产品的预期用途、工作原理、结构组成等。
对比分析:证明新产品与已获FDA批准的类似产品(称为“谓词设备”)在安全性、有效性方面实质上等效。
性能数据:包括产品的测试报告、临床数据(如适用)等。
标签和使用说明:确保产品标签和使用说明书符合FDA的要求。
3. 提交510k申请
商家需通过FDA的电子提交系统(eSubmitter)提交510k申请。在提交过程中,商家需确保申请资料的准确性和完整性,以便FDA进行审查。提交后,商家将获得一个确认号码,用于跟踪申请状态。
4. 等待审查与反馈
FDA会对提交的510k申请进行审查,这一过程可能需要几个月到一年不等的时间,具体取决于产品的复杂性和FDA的工作负荷。在审查过程中,FDA可能会要求商家提供额外的信息或澄清。商家需及时响应并提供所需的信息,以加快审查进程。
5. 获得市场准入
一旦510k申请获得FDA批准,商家即可在亚马逊上销售相关产品。此时,商家需在产品页面上提供FDA颁发的510k编号作为合规性证明,并确保产品信息的准确性和完整性。
二、亚马逊平台要求
除了遵守FDA的合规性要求外,商家还需满足亚马逊平台对医疗器械产品的特定要求。这些要求可能包括:
l亚马逊关于医疗器械的相关政策:
https://sellercentral.amazon.com/help/hub/reference/G200164650?mons_sel_mkid=amzn1.mp.o.ATVPDKIKX0DER&mons_sel_mcid=amzn1.merchant.o.AR6XKOS2E7G9Y&mons_sel_persist=true&mons_redirect=stck_reroute
l产品图片:提供高质量的产品图片,展示产品的各个角度和细节。
l产品描述:清晰、准确地描述产品的特点、用途和规格等信息。
l合规性证明:在产品页面上提供FDA颁发的510k编号或其他合规性证明文件。
l库存管理:确保有足够的库存以满足消费者的需求,并及时更新库存信息。
l客户服务:提供优质的客户服务,解答消费者的疑问并处理投诉。
三、注意事项
l持续合规:即使产品已获得510k批准并在亚马逊上销售,商家仍需持续遵守FDA的监管要求,确保产品的安全性和有效性。
l产品变更:如果产品发生任何变更(如设计、材料、制造过程等),商家需及时通知FDA并更新产品信息。
l法律风险:违反FDA的合规性要求可能导致严重的法律后果,包括产品召回、罚款甚至刑事指控。因此,商家务必严格遵守相关规定。
四、总结
在亚马逊销售510k相关产品是一项复杂而严谨的任务,需要商家充分了解并遵守FDA的合规性要求和市场准入流程。通过准备详尽的申请资料、及时响应FDA的审查反馈、确保产品信息的准确性和完整性以及持续遵守监管要求,商家可以成功地将产品推向美国市场并获得消费者的认可。
如果卖家朋友有商品遇到了商品因510K下架 的相关问题,可以联系橘子进行解决。此外,如果想要了解510K相关市场等信息,也可以联系橘子进行了解。



