
研究进展|助力安全新型疫苗开发,哈兽研与生物物理所等单位合作全面解析非洲猪瘟病毒三维精细结构
2019年10月18日,中国科学院和中国农业科学院宣布,我国科学家首次解析出了正在困扰各国的非洲猪瘟病毒颗粒的精细三维结构。这项成果将对推动非洲猪瘟防控产生重要影响。
中国科学院生物物理研究所饶子和/王祥喜团队和中国农业科学院哈尔滨兽医研究所步志高团队合作在Science上发表了题为Architecture of African Swine Fever Virus and implications for viral assembly(非洲猪瘟病毒结构及装配机制)的文章。

图1:非洲猪瘟病毒整体结构(左:5层切面图;右:衣壳层整体结构)
中国农业科学院哈尔滨兽医研究所所长步志高在这项成果发布会上说,首次解析出非洲猪瘟病毒结构,为疫苗的创制提供了很好的线索。据《中国青年报》记者报道,步志高透露,中国研制的非洲猪瘟疫苗已经完成实验室研究阶段,主要的实验数据和结论已经得到,正在接受同行专家评估。

非洲猪瘟病毒整体结构(左:5层切面图;右:衣壳层整体结构)
该研究新鉴定出非洲猪瘟病毒多种结构蛋白,搭建了主要衣壳蛋白p72等原子模型,揭示了非洲猪瘟病毒多种潜在的保护性抗原和关键抗原表位信息,阐述了结构蛋白复杂的排列方式和相互作用模式,提出了非洲猪瘟病毒可能的组装机制,为揭示非洲猪瘟病毒入侵宿主细胞以及逃避和对抗宿主抗病毒免疫的机制提供了重要线索,为开发效果佳、安全性高的新型非洲猪瘟疫苗奠定了坚实基础。
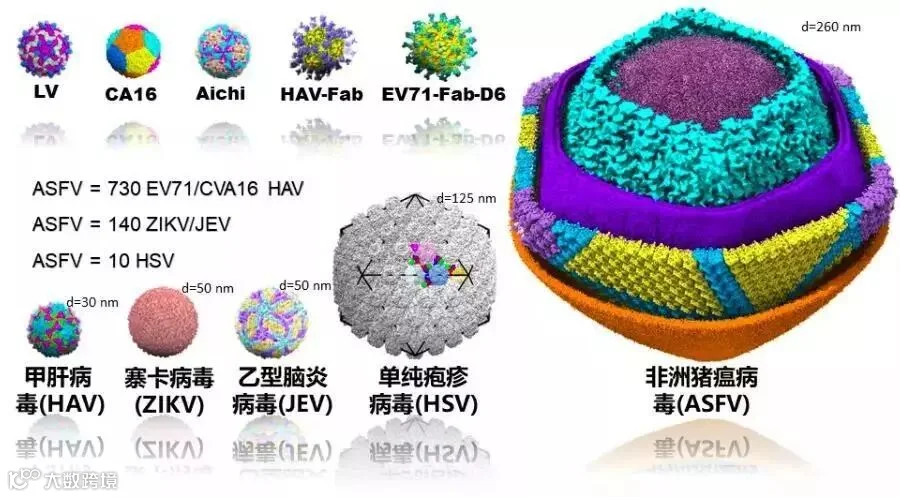
图2:非洲猪瘟全病毒与多种动物病毒对比三维结构图
该研究完整揭示非洲猪瘟病毒独有的5层(外膜、衣壳、双层内膜、核心壳层和基因组)结构特征,病毒颗粒包含3万余个蛋白分子,组装成直径约为260纳米的球形颗粒(图1和图2)。该研究新鉴定出非洲猪瘟病毒多种结构蛋白,搭建了主要衣壳蛋白p72等原子模型,揭示了非洲猪瘟病毒多种潜在的保护性抗原和关键抗原表位信息,阐述了结构蛋白复杂的排列方式和相互作用模式,提出了非洲猪瘟病毒可能的组装机制,为揭示非洲猪瘟病毒入侵宿主细胞以及逃避和对抗宿主抗病毒免疫的机制提供了重要线索,为安全高效的新型非洲猪瘟疫苗研究奠定了基础。
本研究得到中国农科院科技创新工程、国家重点研发计划、黑龙江省应用技术研究与开发计划等项目支持。
>>>以下是文章全文及翻译<<<

全文:




翻译:
摘要
非洲猪瘟病毒(ASFV)是一种巨大而复杂的DNA病毒,在没有疫苗的情况下,可引起具有高度传染性和和致死性的非洲猪瘟疫情。利用优化的图像重建策略,解析了由17280个蛋白(包括一个主蛋白(p72)和四个次要蛋白(M1249L、p17、p49和H240R)构成的高达4.1 Å的ASFV衣壳结构,这些蛋白遵循pentasymmetrons 和trisymmetrons结构。p72的原子结构决定了推测的构象表位,从而将ASFV与其他核质大DNA病毒(NCLDV)区分开来。次要衣壳蛋白在外壳下形成一个复杂的网络,通过将邻近的衣壳连接在一起来稳定衣壳。作为核心的组织者,长100 nm的M1249L蛋白沿着 trisymmetrons分子的每个边缘延伸,并与其他衣壳蛋白形成广泛的分子间网络,从而推动了衣壳骨架的形成。这些结构细节揭示了衣壳稳定性和装配的基础,为ASFV疫苗的开发开辟了新的途径。
非洲猪瘟(ASF)于1921年在肯尼亚首次发现,是猪的一种高度传染性病毒病,死亡率接近100%。在过去的十年中,ASF已遍及高加索,俄罗斯联邦和东欧的许多国家,这构成了进一步扩展的严重风险。在2019年1月至2019年9月期间,世界动物卫生组织报告已有26个国家/地区通报非洲猪瘟疫情:13个欧洲国家,10个亚洲国家,3个非洲国家。在没有疫苗或治疗方法的情况下,扑杀猪是控制疫情爆发的最有效方法,2018-2019年间有超过3000万头猪被扑杀。据估计,ASF大流行给全球养猪业造成了20亿美元的经济损失。非洲猪瘟病毒(ASFV)在环境中稳定,并在猪之间快速有效地传播。
ASFV是Asfarviridae的唯一成员,也是唯一已知的DNA虫媒病毒。尽管与其他核质大DNA病毒(NCLDV)具有类似的结构,基因组和复制特性,但ASFV的不同之处在于具有多层结构和整体二十面体形态。细胞内ASFV具有包含基因组的类核(第一层),被称为核心壳层(第二层)的厚蛋白层包围,该蛋白层由内部脂质包膜(第三层)和二十面体蛋白衣壳(第四层)包裹。当细胞外ASFV穿过质膜出芽时,它获得了外部包膜(第五层)。关于感染性病毒粒子的组成和结构,以及对诱导猪保护性免疫反应的病毒蛋白的鉴定方面的知识存在巨大空白,阻碍了疫苗的开发。
ASFV主要靶向于血液和骨髓中的单核/巨噬细胞。本文,研究人员从30-40日龄的无特定病原体(SPF)猪中分离猪骨髓(PBM)细胞,ASFV(HLJ-2018株,分离自中国ASF暴发猪场的猪脾脏样本)感染原代PBM细胞,并从细胞上清液中纯化出胞外ASFV颗粒,然后用甲醛灭活病毒粒子。纯化后的病毒粒子经冷冻电子显微镜(EM)观察。细胞外的ASFV颗粒平均直径260-300 nm,明显大于之前的观察数值(约200 nm),可能是由于电镜观察前病毒颗粒不完整或标本脱水处理所致。
与大多数NCLDVs一样,ASFV粒子的大小(直径250-500 nm)和柔性限制了其结构解析不超过10 Å。通过平均43811个粒子,我们获得了8.8 Å分辨率的ASFV二十面体重建。3D重建清晰地显示了五层的结构,其中衣壳(第四层)的最大直径为250 nm,第三层为70-Å厚的脂质双层膜,包裹着直径180 nm的核壳(第二层)。这三层遵循衣壳二十面体轮廓形态(图1A)。然而,由于二十面体导致的一些结构特征的丢失,最外层的包膜和最内层的类核呈现出较弱的密度。
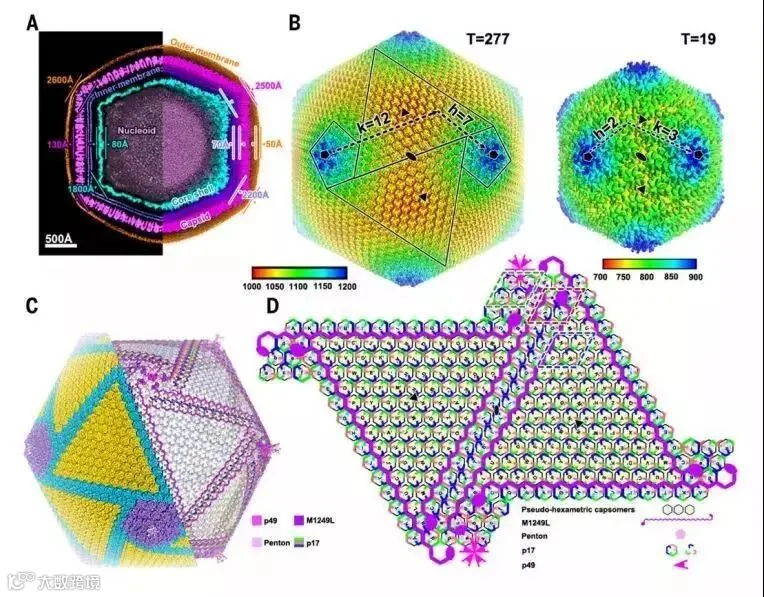
图1 ASFV病毒粒子的结构
采用基于“block-based”的重建方法结合梯度散焦校正,将衣壳重建的分辨率提高到4.8 Å (图1)。衣壳由2760个伪六聚体和12个五聚体组成,按T = 277二十面体晶格排列(h=7, k=12)(图1B)。在这个晶格中,有12个pentasymmetrons (包含30个伪六聚体和一个五聚体)和20个trisymmetrons (包含120个伪六聚体),在其他NCLDVs中也存在到类似的结构。此外,分别将核心壳重建为9 Å分辨率的180个带中央通道(直径30 Å)的6螺旋筒体和12个具有10角海星状的的五边体,产生T=19二十面体晶格(图1b)。
通过对三对称体中存在的等效拷贝进行局部平均,进一步改进了衣壳假六聚体的冷冻电镜图,以获得4.1 Å的分辨率(图2A)。多肽的主干和许多侧链被明确 (图2A),使我们能够建立ASFV主要衣壳蛋白p72的原子模型。
每个伪六聚体capsomer由3个p72分子和5个penton蛋白(不是p72蛋白)组成一个五聚体capsomer。内衣壳表面剩余的许多未被发现的密集代表了少量衣壳蛋白(图1C),可能有助于衣壳的组装和保持衣壳的稳定性。
为了确定次要衣壳蛋白的潜在特性,我们通过质谱分析了PBM细胞产生的胞外ASFV颗粒的蛋白组成,并与最近对vero细胞培养的ASFV株BA71的蛋白质组学分析进行比较,鉴定出63种病毒蛋白和25种宿主细胞蛋白,包括13个额外的病毒蛋白。次要的衣壳蛋白应该是其中之一。
结合蛋白质组学分析、ASFV颗粒中的蛋白质丰度水平以及冷冻电镜图谱与靶蛋白结构特征(包括蛋白质序列、蛋白质二级结构和蛋白质拓扑学)的相似性,鉴定了Penton蛋白(H240R)和三个次要衣壳蛋白(p17,p49和M1249L)(图1C)。每个衣壳外二十面体非对称单元包含46个伪六聚体衣壳,其中6个为pentasymmetron (a, b, c, d, e, f),40个trisymmetron(A, B, C, D, E, F, G, H, I, J, K, L, M, N, O, P, Q, R, S, T, U, V, W, X, Y, Z, A , B ,C,D , E , F , G , H , I , J , K , L , M,N ) (图1 D)。Penton和次要衣壳蛋白(p17、p49、M1249L)在外壳下形成复杂的网状结构,稳定了整个衣壳(图1、C、D)。
考虑到ASFV在细胞内和细胞外的形式都具有感染性,因此需要一种针对外膜蛋白和衣壳蛋白的抗体组合来阻止这两种类型的感染,以提供对ASFV的有效保护。p72是关键的保护性抗原之一,其单克隆抗体可以中和强毒性的ASFV。
在病毒衣壳上,p72与每个单体形成同型三聚体,每个单体采用双jelly-roll结构,构成假六聚体(也被称为p72衣壳)。在许多其他病毒衣壳蛋白(图2B)中也发现了类似的双jelly-roll折叠,包括腺病毒、噬菌体PRD1和牛痘病毒。由八个反平行β链(从B到I)组成的单一jelly-roll结构存在于多种病毒衣壳蛋白中,表明共同起源的可能性。与其他jelly-roll衣壳蛋白一样,D1E1、D2E2、F1G1和H1I1环内的四个插入形成了暴露区域(ERs)。ERs与n端碱基域一起,确定病毒类型之间的特定差异(图2、B和C)。
在空间上,p72 capsomer的冠部由ER1及其邻近的ER2形成,并且朝向衣壳的外部,这可能有助于形成构象表位(图2、B和C)。来自同一亚单位内ER3和ER4的β链构成一个四链β-片,形成p72 capsomer的头部,可能代表另一个构象表位(图2、B和C)。被ER1、ER2和ER4包围的ER3可能连接这两个构象表位。这四个ER可能构成了中和性表位,并可用于指导ASF疫苗设计(图2、B和C)。
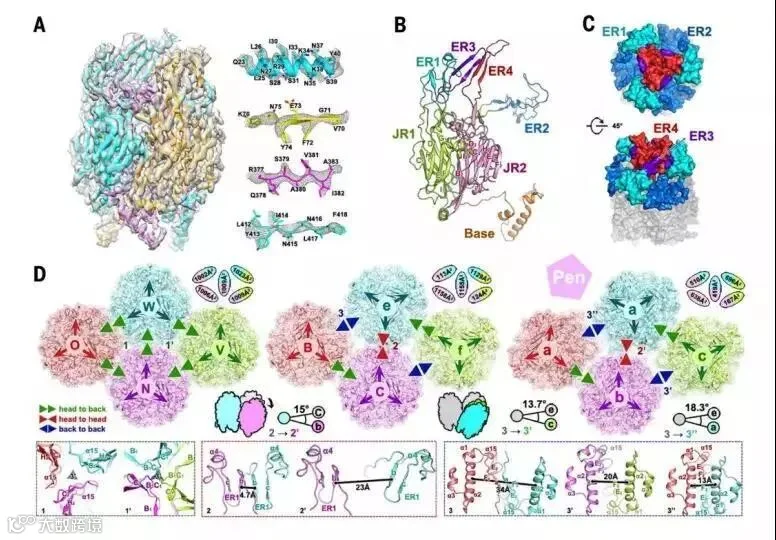
图2 p72的结构和构成
p72 capsomers除了围绕着penton来填充pentasymmetron外,还会打包形成trisymmetron和zipper(图1,C和D)。p72 capsomers采用不同的排列方式,允许三种不同的装配模式:头对背、头对头和背对背(图2D)。在三对称性中,所有P72 capsomers都是头对背排列,形成两种类型的P72 capsomers三聚体(图2D中分别标记为1和1’,其中1在拟等价三重轴上的相互作用较小,而1’在拟等价三重轴上的关联较紧密)(图2D)。在zippers和pentasymmetron中,p72 capsomer拥有所有三种接触模式,其中头对头关联以两种形式存(图2D标注为2、2’),背对背交互发生在三种不同的微环境中(图2D标注为3、3’、3’’)。zipper中的头-头相互作用直接紧密,由两个相邻的ER1形成的四股β-片形成,而由于p72 capsomer的相对旋转是由较高的曲率引起的,因此在pentasymmetron中相应的相互作用明显减少(图2D)。相比之下,与形成四螺旋的pentasymmetron相比,zipper中的背对背接触是最弱的(图2D)。总的来说,zipper中的背对背接触和所有三种模式的接触在pentasymmetron中似乎不足以促进高阶结构的组装,这表明需要少量的次要衣壳蛋白来构建触发整个衣壳组装。
由于capsomer之间接触较少,pentasymmetron中的相互作用被三种次要衣壳蛋白和penton加强(图3)。在外衣壳的五个折叠顶点处的Penton呈现出一个单一的jellyroll状和一个球形的帽(图3A),这表明penton蛋白不同于p72,但与已知的一些大型dsDNA病毒的结构观察一致(如PBCV-1、Mavirus、PRD1等)。Mavirus penton蛋白结构非常容易灵活地适用于该图谱中,其中jellyroll褶皱排列良好(图3A)。ASFV ORFs与Mavirus penton序列蛋白质BLAST比对发现了一个同源物,其序列相似性为37.7%,即H240R,这是一种未被鉴定但却是必需的病毒粒子蛋白质。H240R,长度240个残基,富含β链,预测具有单一的jellyroll卷曲和约70个氨基酸的N-末端延伸,这进一步支持了ASFV中的Penton的作用。在penton的下面,观察到微弱的灯笼状密集(~9 Å)连接penton和内膜,并与五个相邻的capsomer相关联,推测它们在顶点的组装中起作用(图3、A和C)。以往的研究报道,预测的衣壳蛋白p49 (B438L)是形成衣壳顶点所必需的,且与衣壳顶点的位置非常接近。此外,p49作为一种完整的膜蛋白,不参与病毒组装位点到质膜的颗粒运输,表明它可能位于衣壳的内壳层。根据这些观测结果,我们提出灯笼状密集是p49的五个拷贝(图3,A和C)。
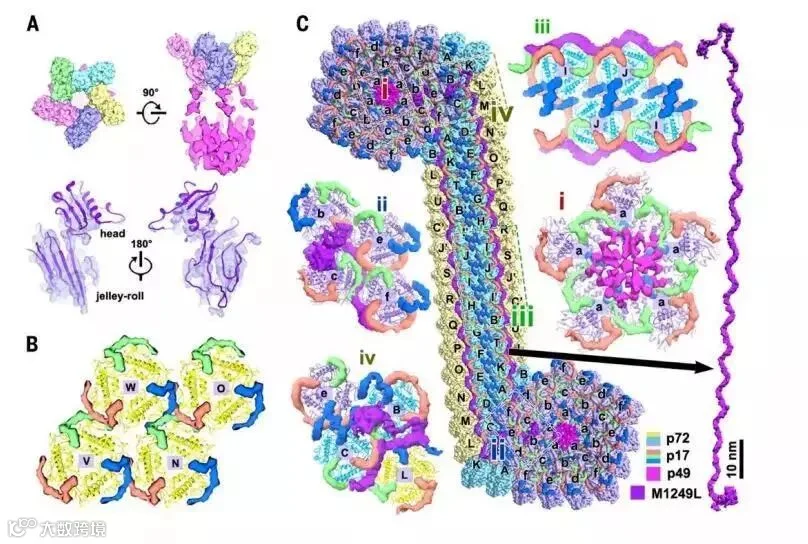
图3 次要衣壳蛋白广泛的分子间网络是衣壳稳定性的基础
内膜蛋白p17 (D117L)是衣壳和二十面体形态发生组装所必需的一种高度丰富的蛋白。我们的重建显示在p72 capsomers下面有重复的密集。由三个连续的α螺旋组成的蛇形结构与p17外域的二级结构预测吻合良好(图3B),并支持蛋白质丰度水平分析,表明密集为p17。p17与p72的碱基结构域紧密相连,三个p17拷贝将每个p72衣壳包围在内衣壳内,将p72衣壳牢牢锚定在内膜上(图3B)。有趣的是,在type 1微环境下,三个相邻的p72 capsomers的三个p17s的紧密交错介导了三个capsomers之间的相互作用(图2D和图3B)。这些连同三种capsomers在type 1微环境下的相互作用,指导由衣壳大部分组成的三对称膜中capsomers的有序包装。
然而,pentasymmetrons和zippers内的微环境更为复杂。在这里,骨架蛋白M1249L将34个capsomers连接在一起,不仅固定了一个pentasymmetron,还连接了两个相邻的pentasymmetron(图1D和图3C)。必需的长1249氨基酸的M1249L被预测为充满线圈,并显示出具有两个末端裂片(约150个残基/裂片)的纤维状结构。纤维部分长度约100 nm,有30个延伸的螺旋(~30个残基/螺旋)(图1D和图3C)。M1249L从一个五边形内的capsomer b和c(与a接触)开始,沿着zipper(capsomers c-e, d-f, B-A ..N-E, M-D and L-C)的外沿延伸,以capsomer b和c结束,与邻近的pentasymmetron上的capsomer e相互作用(图3C)。此外,M1249L广泛地与p17/p72-capsomers相互作用,形成刚性的zipper结构,其中capsomers在头对头模式(type 2)中紧密接触,生成17个双capsomers(d:B, e:C, f:D, A:E, K:F, T:G, B :H, I :I, J:J), 30个zippers构建衣壳框架。令人惊讶的是,zipper中的p17与三对称体中的p17相比采用了截然不同的构象(图3,B和C)。由两组p17对(红色和蓝色)在准等效双轴上形成的双套索结构,以及边缘的p17s(红色和绿色)和M1249L紧密交织在一起,极大地促进了capsomers沿着M1249L纤维的结合,确保zipper的正确装配(图3C)。
ASFV组装开始于病毒内膜前体的出现,其可能起源于内质网(ER),然后通过衣壳层的渐进组装进入二十面体中间体和二十面体颗粒。在病毒装配的早期,内膜是柔性的,具有各种形态,甚至是开放的结构,有各种可移动的内膜蛋白,如p17漂浮在其上。衣壳似乎是在内膜蛋白和次要衣壳蛋白的引导下组装而成,但在感染细胞中未见预组装阵列或对称体。结合以前的实验观测和我们的结构分析,这些使我们能够为进一步理解ASFV衣壳组装提出详细的假设。
首先,p49与膜结合的能力介导了五边形复合体与内膜的对接,并招募capsomers (a)形成五边形核(图4),启动装配。这与mimivirus衣壳的体内组装是一致的,从五重顶点开始,逐步完成衣壳组装。
其次,骨架单元M1249L有两个capsomer对(b-c和b-c)附着在penton core上,同时骨架单元、penton core和p17可以在内膜上移动,增加了它们形成高阶组装的机会(图4)。在p17的引导下,capsomers、骨架蛋白M1249L和p17参与zipper的形成,将相邻的penton core连接起来,逐渐形成一个多面体骨架(图4)。伴随着多面体骨架的形成,capsomers分子填充三对称体以完成衣壳组装(图4)。
在我们的模型中,骨架蛋白M1249L作为构建衣壳骨架的骨架,决定衣壳的大小。与此同时,在PRD-1、pbcv -1和Bam35中也发现了具有类似功能的纤维样蛋白,提示了类似的组装途径。
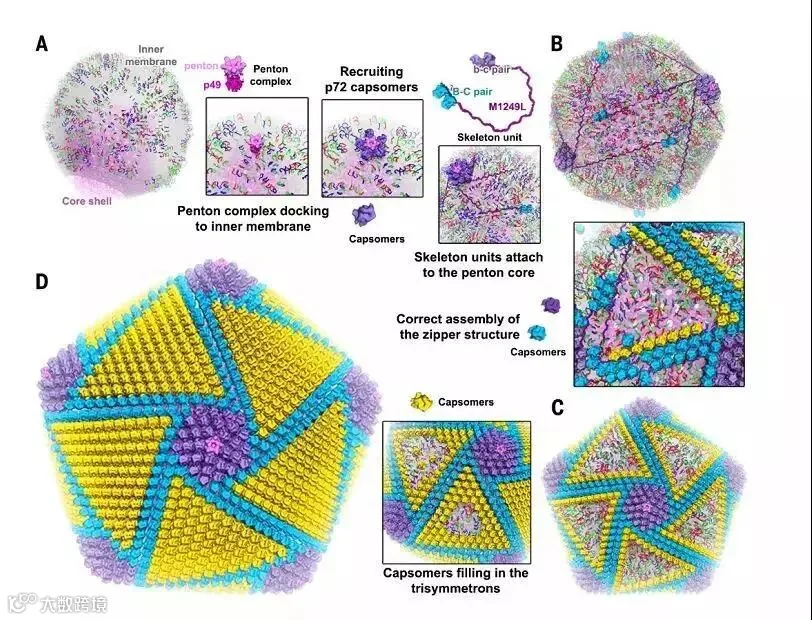
图4 ASFV衣壳的组装途径的预测
本文报道的ASFV架构具有接近原子的分辨率,这使我们能够迈出第一步,了解ASFV衣壳组装驱动因素以及其稳定性的基础。此外,其结构细节,尤其是p72原子结构,可以指导抗原决定簇的免疫原的合理设计,为安全高效的新型非洲猪瘟疫苗研究奠定了基础。
注:文章转自中国动物保健


长按上方二维码关注我们




