创伤后应激障碍(Post-traumatic stress disorder,PTSD)是一种对严重压力源的异常神经心理反应,其核心特征是恐惧记忆异常。患者会出现恐惧、焦虑、抑郁等严重的精神症状,在各种灾难后幸存者的发病率可以达到10%-30%,终生患病率高达3%-58%。目前主要治疗方法是暴露疗法和药物治疗,但两者都有局限性,寻找治疗PTSD的有效药物仍然是临床方面迫切需要的。
根据中医理论,PTSD是一种抑郁综合征,其发生与心脏和肾的缺陷有关。黄精益气养血,滋补五脏,因此它在传统中医中被用作治疗抑郁症综合征的处方。黄精多糖(PSP)是主要活性成分,但是PSP对创伤后应激障碍的影响及其机制尚不清晰。对此,安徽中医药大学朱国旗研究员团队开展相关研究,研究成果于Journal of Ethnopharmacology(医学Q2,IF:5.40)期刊上发表题目为“Polysaccharides from Polygonatum cyrtonema Hua prevent post-traumatic stress disorder behaviors in mice: Mechanisms from the perspective of synaptic injury, oxidative stress, and neuroinflammation”的研究论文。
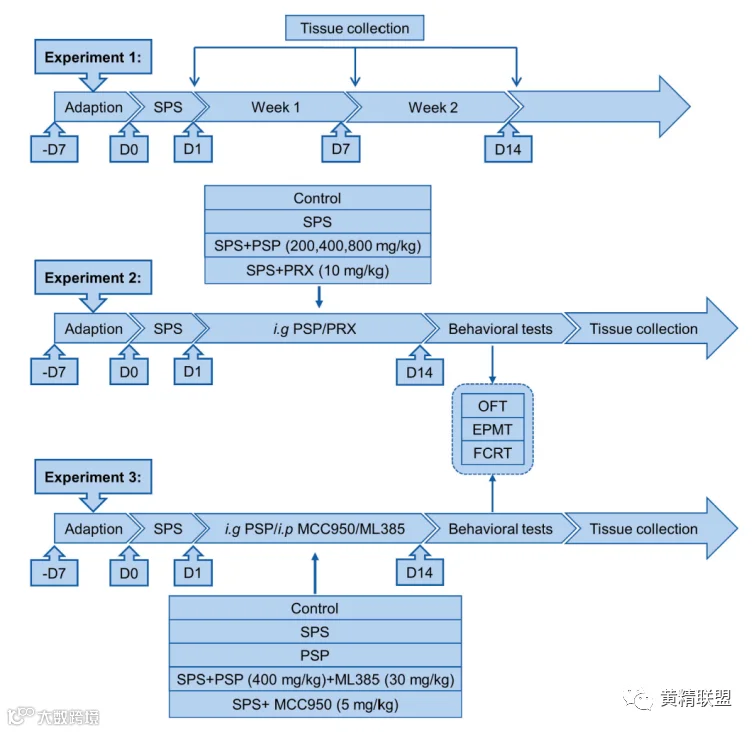
研究团队前期从多花黄精的根茎中提取制备了粗多糖:石油醚回流去除低极性成分,用水回流提取,Sevage法脱蛋白,透析后得到分子量为6kD至14 kD的PSP溶液。超高效液相色谱(UPLC)结果显示PSP主要含有六种糖类和糖醛酸。本研究中,成年雄性小鼠先通过单次连续暴露于约束、强迫游泳、麻醉和足部电击四种压力源建立单次延长应激(Single prolonged stress,SPS)模型,建模后第1、7、14天麻醉并斩首收集血清和海马组织。然后实验小鼠被分为六组:对照组、SPS组、低剂量PSP组、中剂量PSP组,高剂量PSP组(200、400和800 mg/kg)和阳性对照组(10 mg/kg 帕罗西汀)。进一步实验设立了对照组、SPS组、PSP组(最佳剂量),SPS+PSP+ML385(30 mg/kg)五组。给药后进行行为测试(露天试验: open field test,OFT;高架十字迷宫测试:Elevated plus maze test,EPMT;恐惧调节任务:fear conditioning task,FCT)(图1)。
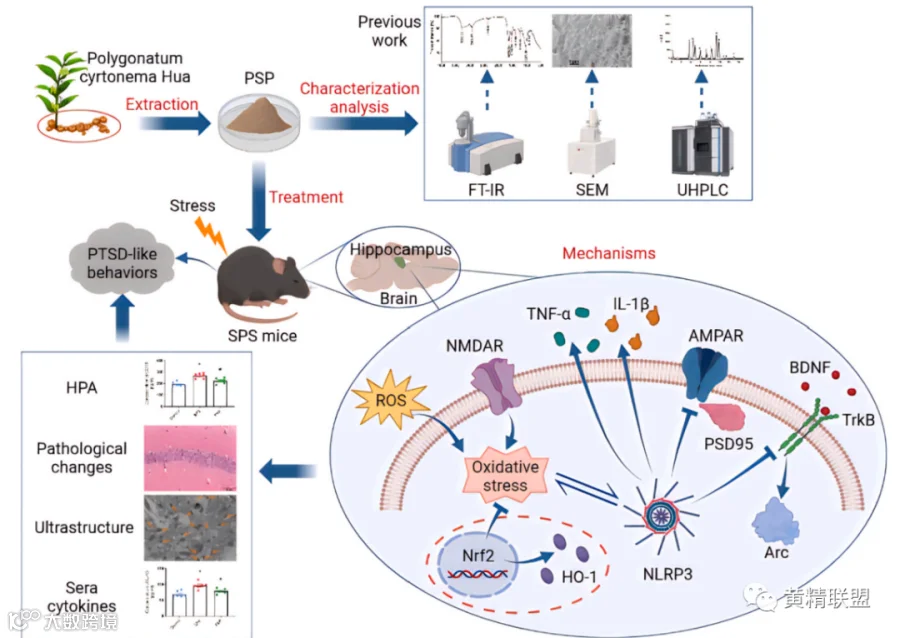
SPS模型小鼠表现出显著的PTSD样症状(高度的恐惧记忆和焦虑),而帕罗西汀(PRX)和PSP给药改善了SPS诱导的恐惧和焦虑样行为。由于中等剂量(400mg/kg)的PSP改善诱导小鼠PTSD样行为的效果最为明显,因此选择该剂量的PSP用于进一步研究(图2)。PSP抑制SPS小鼠海马区GFAP的表达(图3,图4)。TEM观察到PSP给药减弱CA1区突触数量(图5G和H)。PSP处理使小鼠海马体SOD活性和丙二醛含量降低及核因子红细胞2相关因子2(Nrf2)和血红素氧合酶1(HO-1)的表达水平明显高于对照组,这些结果表明PSP减少SPS诱导的氧化应激(图6)。PSP显著降低SPS小鼠血清中白细胞介素1(IL-1β)和肿瘤坏死因子α(TNF-α)以及海马NOD样受体蛋白3(NLRP3)和衔接蛋白凋亡相关斑点样蛋白(ASC)的表达水平表明PSP改善SPS诱导的炎症反应(图7)。上述研究表明氧化损伤、炎症反应和突触可塑性密切相关。PSP可能通过调节氧化应激和NLRP3介导的炎症影响Nrf2/HO-1信号通路,从而改善SPS诱导的突触损伤和PTSD样行为(图10)。
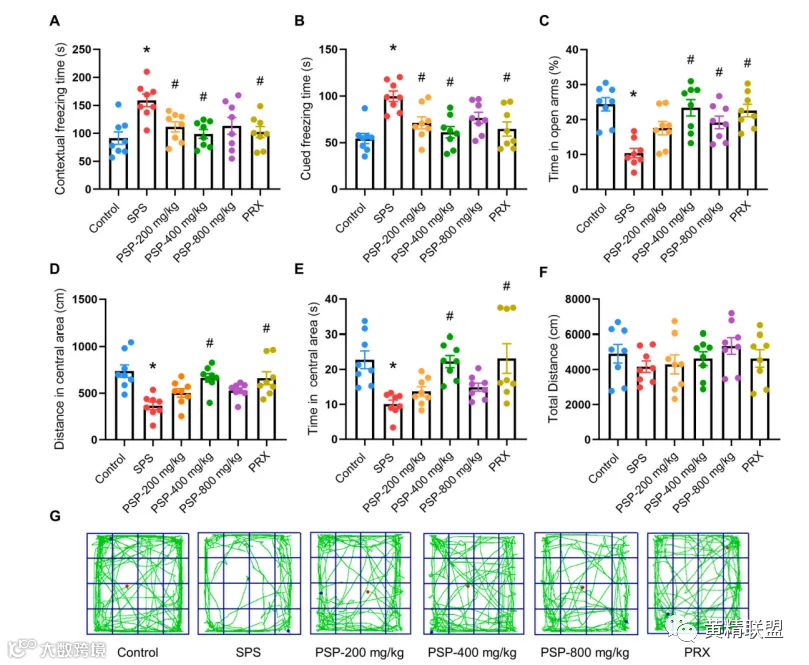
图2 PSP减轻SPS小鼠的恐惧记忆获得和焦虑样行为。(A,B)情境和提示恐惧测试中的冻结时间。(C)EPMT中探索张开双臂所用时间百分比。(D,E)OFT中在中心区域行走距离和时间。(F)OFT中覆盖的总距离。(G)描绘的运动痕迹。
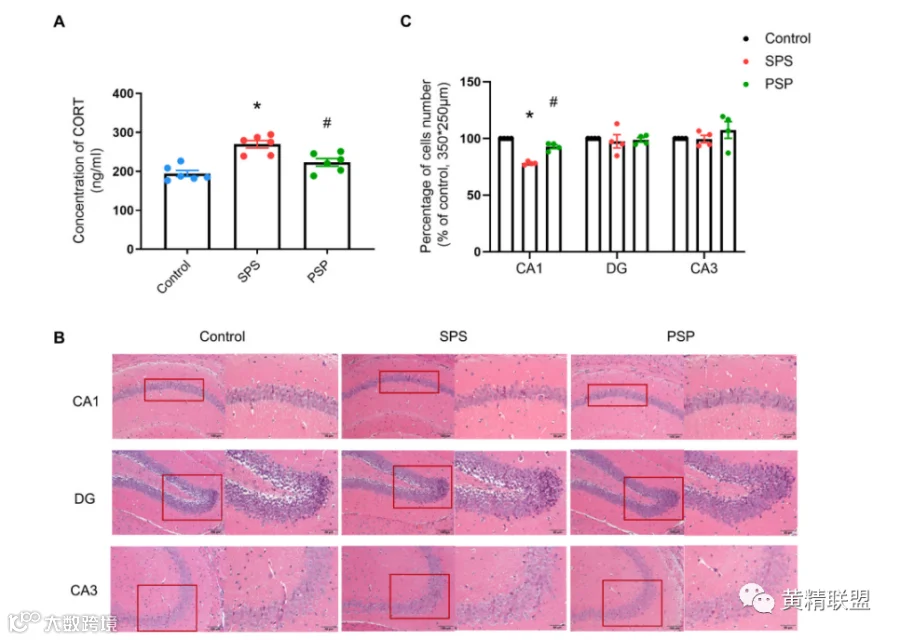
图3 PSP降低SPS小鼠肾上腺轴功能亢进,改善海马CA1区细胞损伤。(A)血清CORT水平。(B)海马CA1、DG和CA3区的HE染色。(C)CA1、DG和CA3区域中的细胞数量,由苏木精—伊红进行染色。
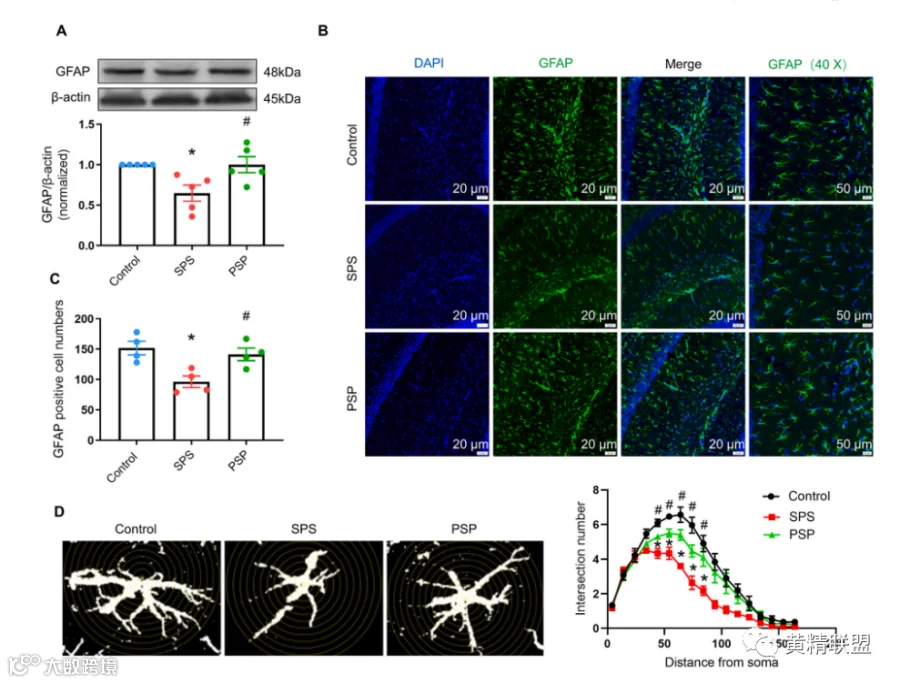
图4 PSP预防SPS诱导的星形胶质细胞异常。(A)GFAP的代表性印迹和定量数据。(B)显示CA1区GFAP表达的典型免疫荧光图像。(C)GFAP免疫荧光定量。(D)Sholl分析的代表性图像和定量数据。
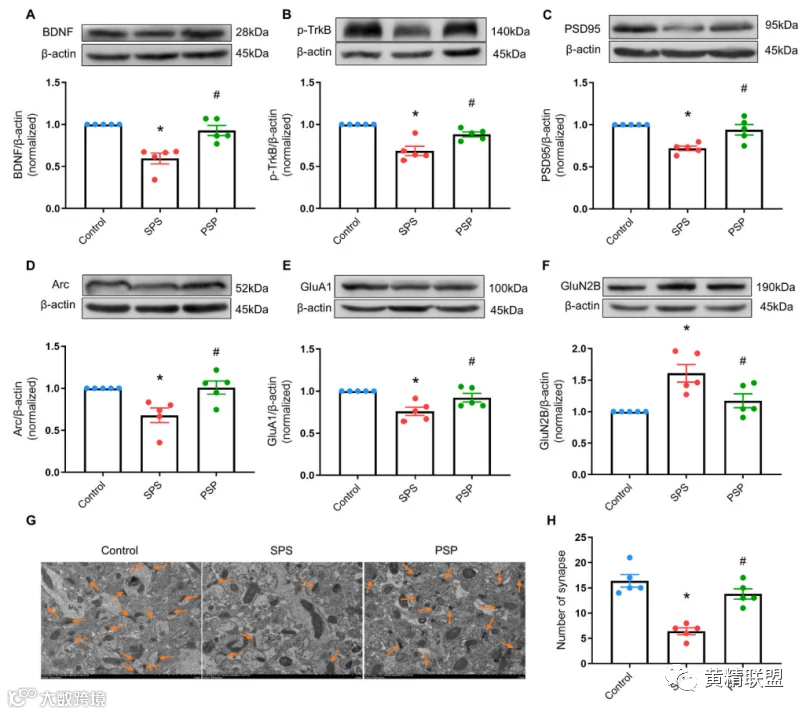
图5 PSP改善海马突触SPS小鼠的可塑性。(A-F)BDNF/β-肌动蛋白,p-TrkB/β-肌动蛋白、PSD95/β-肌动蛋白和Arc/β-肌动蛋白、GluA1/β-肌动蛋白和GluN2B/β-肌动蛋白。(G)海马CA1区突触结构的代表性图像海马体。箭头表示突触结构。(H)突触数量。
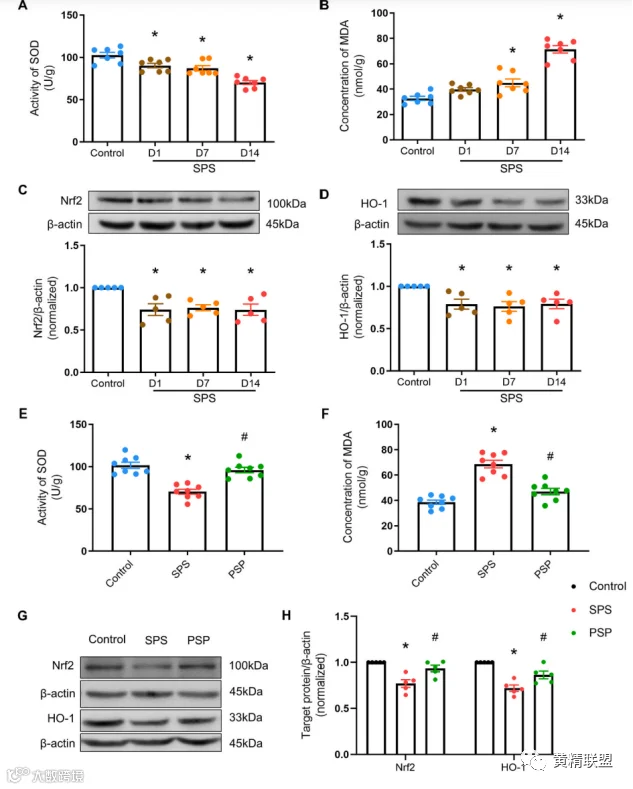
图6 PSP改善SPS诱导的氧化损伤。(A,B)实验1。(C,D)代表性印迹和Nrf2/β-肌动蛋白和HO-1/β-肌动蛋白的定量数据在实验1中。(E,F)海马水平SOD和MDA。(G,H)Nrf2/实验2的β-肌动蛋白和HO-1/β-肌动蛋白的代表性印迹和定量数据。
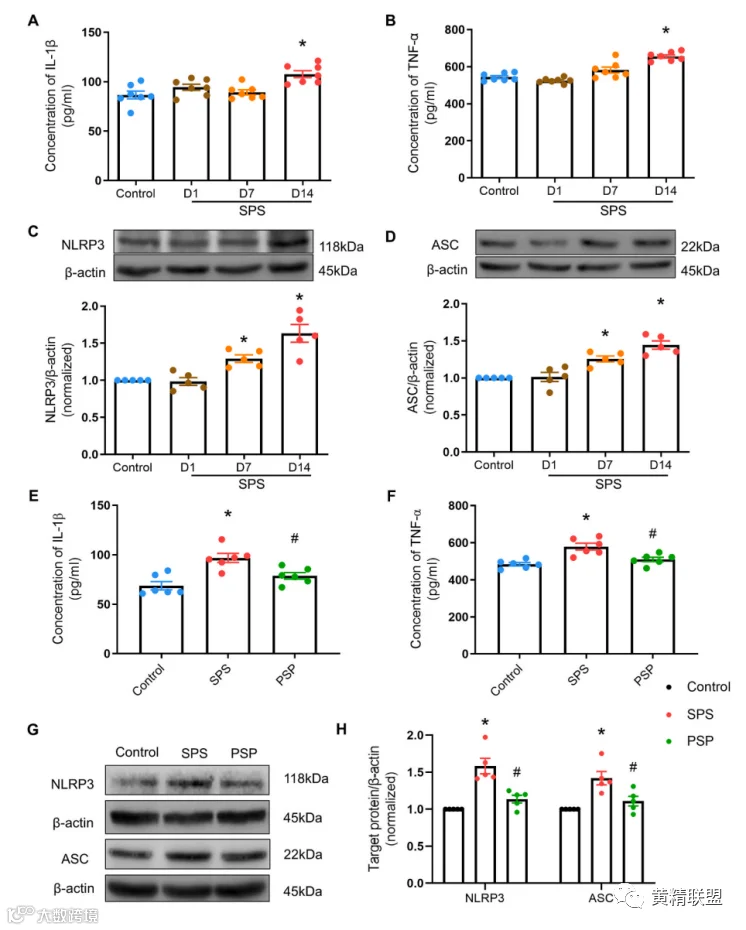
图7 PSP抑制SPS诱导的炎症响应。(A,B)实验1中血清IL-1β和TNF-α水平。(C,D)代表性印迹和定量实验1中NLRP3/β-肌动蛋白和ASC/β-肌动蛋白的数据。(E,F)来自实验2的IL-1β和TNFα的血清水平。(G,H)代表NLRP3/β-肌动蛋白和实验2的ASC/β-肌动蛋白。
安徽中医药大学朱国旗教授和杨绍杰博士为论文的通讯作者,原文链接:https://doi.org/10.1016/j.jep.2023.117165