人口老龄化正在成为一个全球性的挑战,探索抗衰老策略,开发抗衰老药物具有科学和现实意义。多糖是黄精属植物中最丰富的活性物质,据报告,黄精多糖可通过提高免疫力、抗氧化、增强端粒酶活性、改善线粒体功能等机制发挥延缓衰老的作用。关于黄精多糖抗衰老活性的研究大多是利用原多糖进行的,而对黄精多糖进行结构修饰的研究较少,选择合适的方法修饰黄精多糖的结构对有效提高其生物活性具有重要意义。发酵是一种很有前途的生物改性方法,在天然产物的结构改性中得到越来越广泛的应用,且具有反应条件温和、特异性高、环境友好等特点。本研究以滇黄精为原料,以益生菌副干酪乳杆菌为菌株,对滇黄精多糖进行发酵修饰,发酵后采用超滤法对发酵后的水解多糖进行分段。通过比较发酵前后样品在体内和体外抗衰老活性的差异,快速筛选出最佳活性多糖组分,进一步分析其理化性质,初步阐明发酵对滇黄精多糖(Polygonatum kingianum polysaccharides,PKPS)活性和结构的影响。为多糖结构的生物修饰研究提供了科学参考,也为快速筛选最佳抗衰老活性多糖提供了新思路。研究成果在国际期刊International Journal of Biological Macromolecules(Q1,IF:8.2)上发表。
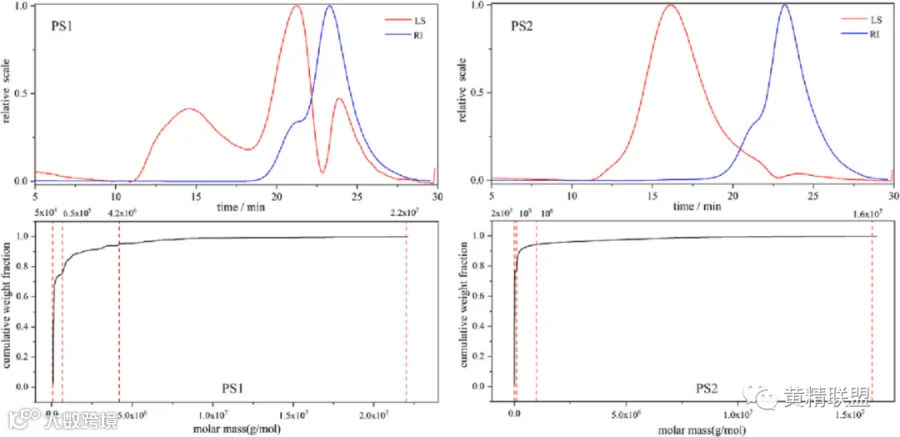
发酵对PKPS分子量(Molecular weight,Mw)具有显著降低的影响,这种变化可能是由于发酵过程中糖苷酶水解导致多糖的糖苷键断裂所致,表明发酵对多糖的水解有积极作用,从而对多糖产生影响(图1)。由于发酵后PKPS的分子量变化显著,为了理清发酵是否影响了PKPS的抗衰老活性,进一步对发酵前后多糖的活性差异进行比较。采用超滤法将发酵总多糖(PS2)分离为PS2-1 (Mw>100 kDa)和PS2-2(Mw<100 kDa)两个组分,并进行体外活性测试。通过体外抗氧化活性、降血糖降血脂作用、延缓MRC-5细胞(即人胚肺细胞,常用于疗效实验)衰老能力等指标,快速评价PKPS的抗衰老相关活性。
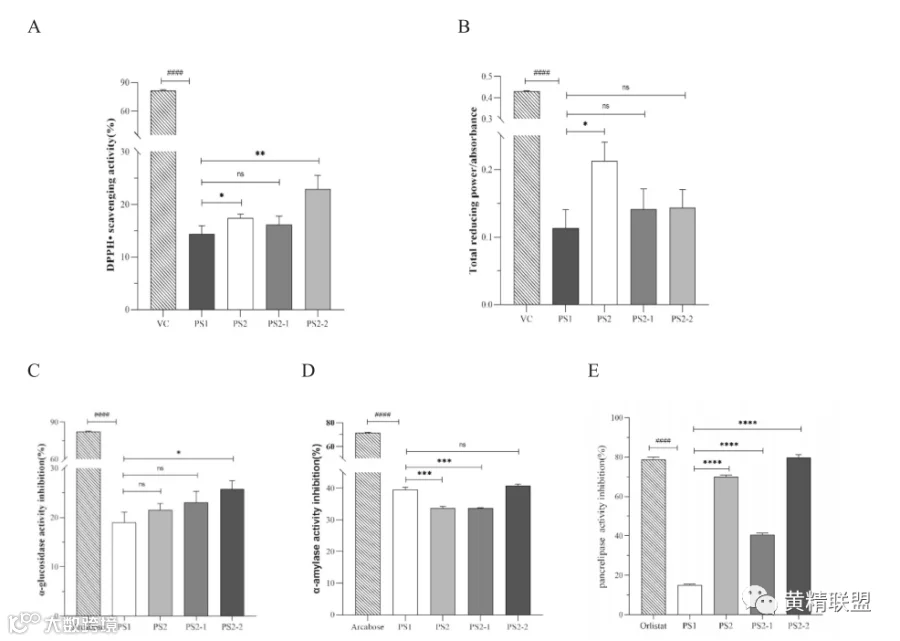
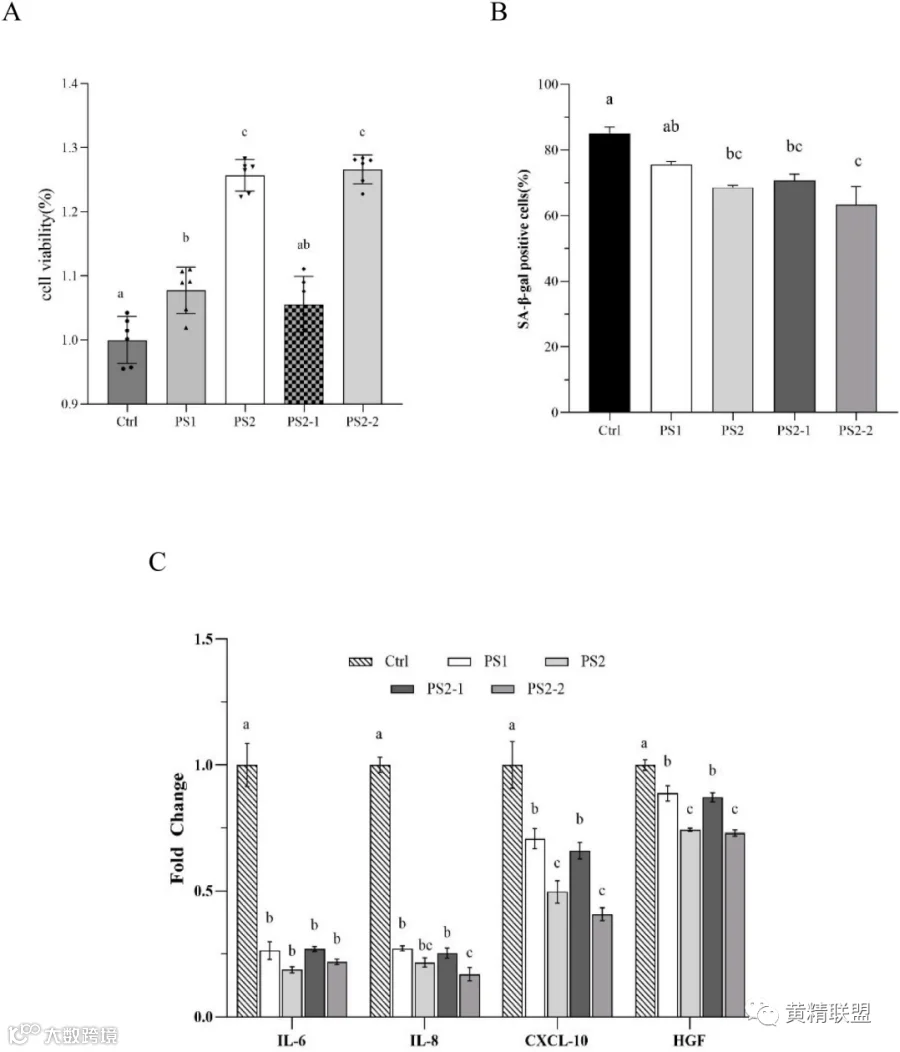
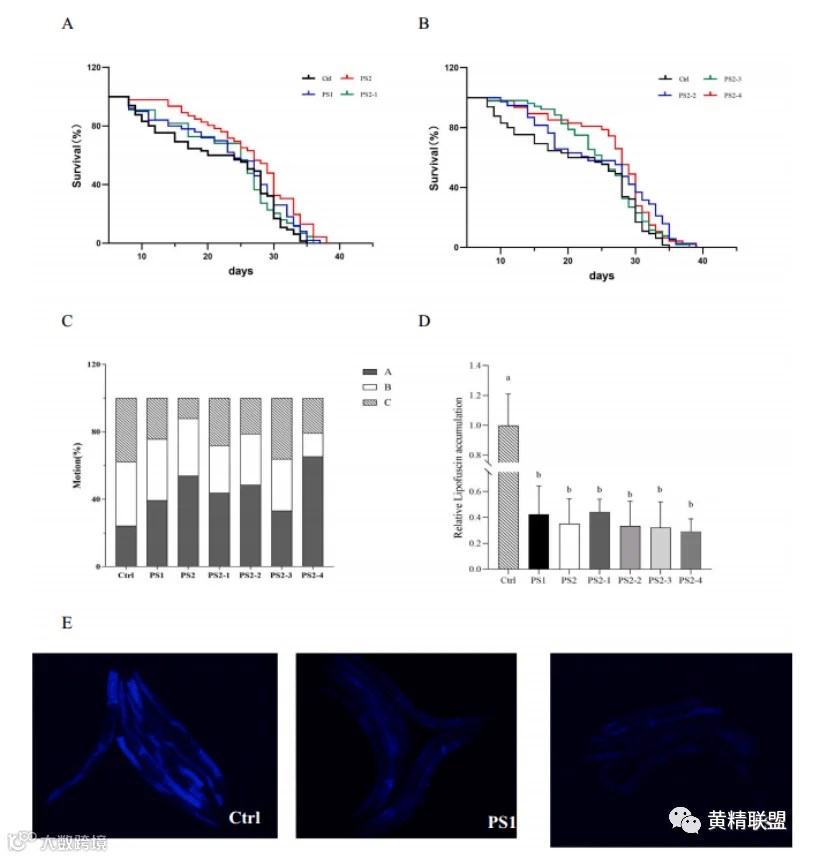
研究表明,抑制α-葡萄糖苷酶、α-淀粉酶等消化酶的活性,可减少小肠对葡萄糖的吸收,从而降低血糖,此外,有效抑制脂肪酶活性有助于控制多余脂肪的吸收,改善血脂水平。PS2对DPPH的清除能力和对Fe3+的还原能力显著提高,发酵对PKPS的抗氧化活性有增强作用(图2 A-B),且发酵后PKPS对α-葡萄糖苷酶活性的抑制作用有所增强(图2 C-D)。原始多糖PS1的脂肪酶抑制作用较低,但发酵处理后活性得到了非常显著的提高(图2 E)。另外,在延缓细胞衰老方面,发酵多糖PS2组和PS2-2组对细胞增殖能力的提高效果更好(图3 A),当β-半乳糖苷酶越强,细胞衰老程度越高,全发酵多糖组的染色细胞阳性率有所降低,其中PS2-2组效果最好(图3 B)。在多糖样品的干预下,MRC-5细胞中各因子的分泌水平明显下调,表明PKPS可延缓衰老(图3 C)。寿命是衰老最直接的指标,常进行蠕虫实验进行衡量。发酵后多糖各组分的活性均有不同程度的提高,蠕虫的寿命相对延长(图4 A-B)。在PKPS的干预下,各组蠕虫的运动能力有所提高,发酵组运动能力更高(图4 C)。图4 D-E为荧光显微镜下15天虫体内脂褐素的积累情况,荧光强度越高,脂褐素的积累越高。对照组的蠕虫荧光强度更强,表明脂褐素积累更大,衰老程度相对更高。相比之下,饲喂PKPS后,各样品组的荧光亮度均显著降低,说明PKPS可以缓解蠕虫的衰老程度。其中,从发酵多糖中分离出的最低分子分数PS2-4(10-50 kDa)具有较好的抗衰老活性。
理化性质方面,发酵后的组成也发生了明显变化。葡萄糖的摩尔比在PS2中下降,而在PS2-4中相对增加;与PS1相比,PS2-4的果糖含量显著降低(图5)。从图6的红外光谱也可看出,有吡喃糖的存在,也有α型糖苷键的特征。PS2和PS2-4的峰谱与PS1相似,均存在多糖的特征吸收峰,说明发酵过程中的生物转化反应是温和的,没有导致多糖结构的破坏。图7为多糖样品在扫描电子显微镜下500倍和5000倍放大后的形貌。发酵前后多糖样品的显微形态有显著差异。原始多糖PS1表面粗糙多孔,发酵后的多糖表面光滑,特别是PS2-4比PS2更光滑,组织更细,说明发酵过程对多糖的组织结构产生了影响。在本研究中,发酵后PKPS的分子量降低,其化学组成、单糖组成和微观形态也发生了变化,这是其抗衰老活性增强的关键原因。在后续研究中将进一步分离纯化发酵多糖片段并分析其详细结构,有助于更好地阐明结构-效应关系,阐明最佳抗衰老活性多糖的结构特征。
图1 SEC-MALS-RI测定的多糖样品(PS1、PS2)的摩尔质量分布的色谱图和累积重量分数分析。LS:激光光散射信号;RI:差示折射率信号。
图2 PKPS体外抗衰老活性 以DPPH清除率表示的自由基清除能力(A);总还原能力以Fe3+还原能力表示(B);体外降糖活性分别以α-葡萄糖苷酶抑制率和α-淀粉酶抑制率表示(C)-(D);用脂肪酶抑制率表示体外降血脂活性(E)。
图3 PKPS对MRC-5细胞衰老水平的影响 细胞增殖活力以细胞存活率为代表(A);细胞β-半乳糖苷酶活性用染色阳性细胞的比例表示(B);MRC-5复制性衰老模型中SASP因子的相对分泌水平(C)。
图4 PKPS对秀丽隐杆线虫寿命、运动能力和脂褐素积累的影响。寿命曲线(A)-(B);运动能力,评分标准(C):A:蠕虫呈灵活自由爬行状态,在板内运动频繁;B:蠕虫移动非常缓慢,有些蠕虫爬行一段距离后就不动了;C:蠕虫在盘子里是不能动的,除非轻轻触碰它的头或尾。不同处理组15天虫脂褐素积累水平用相对荧光强度表示(D);蠕虫荧光显微镜照片显示脂褐素积累(E)。
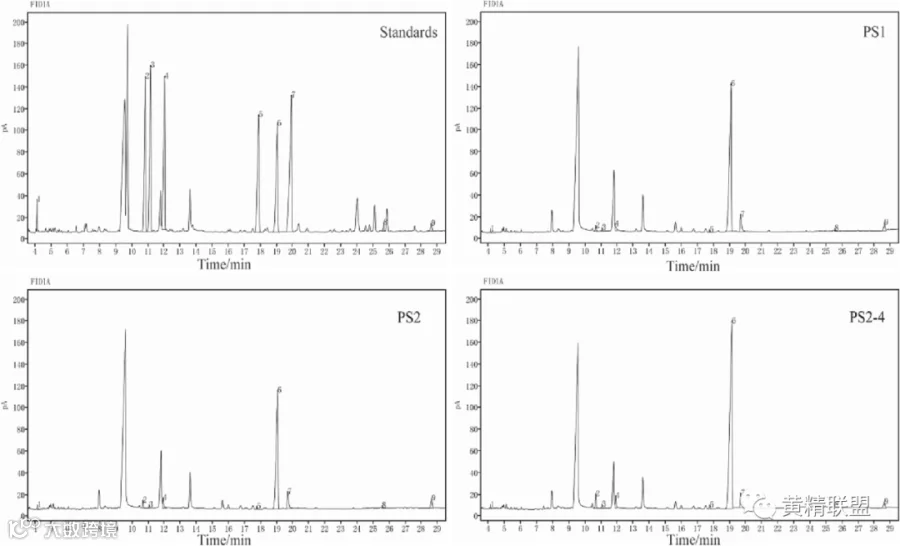
图5 GC法分析多糖样品(PS1、PS2、PS2-4)的单糖组成。图中的数字表示单糖为:1葡萄糖醛酸,2植物种子,3阿拉伯糖,4木糖,5甘露糖,6葡萄糖,7半乳糖,8半乳糖醛酸,9果糖。
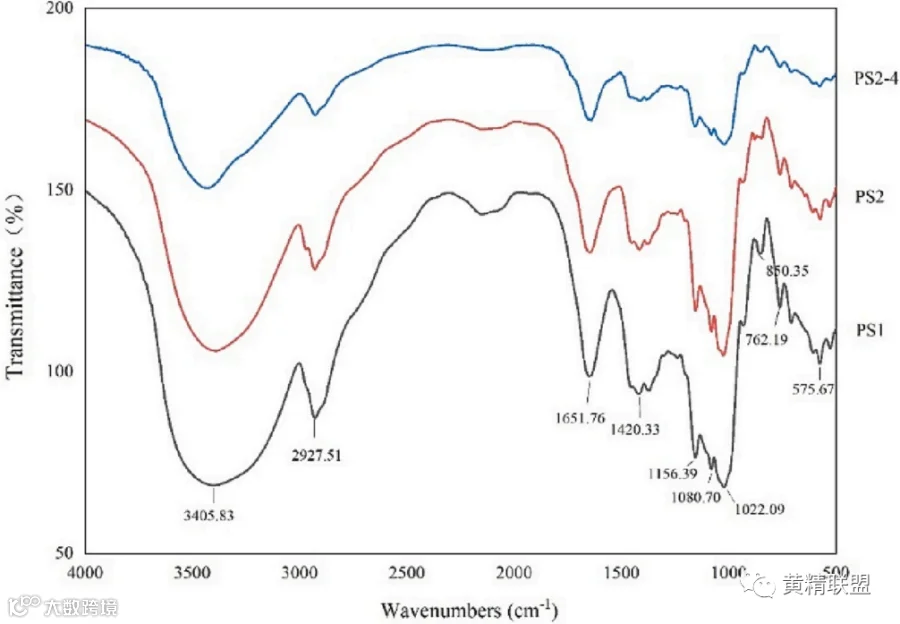
图6 多糖样品包括PS1、PS2、PS2-4的红外光谱
图7 多糖样品(PS1, PS2, PS2-4)在扫描电子显微镜下500倍(第一行)和5000倍(第二行)放大的SEM图像
华南理工大学姜建国教授为通讯作者,华南理工大学与云南中医药大学团队合作发表。
原文链接:https://doi.org/10.1016/j.ijbiomac.2023.123661
 请扫二维码关注“黄精联盟”公众号
请扫二维码关注“黄精联盟”公众号


 请扫二维码关注“黄精联盟”公众号
请扫二维码关注“黄精联盟”公众号


