溃疡性结肠炎(ulcerative colitis,UC)是一种常见的慢性炎症性肠病(inflammatory bowel disease,IBD),已经对全世界数百万人造成影响。目前的治疗通常使用5-氨基水杨酸盐、别嘌呤硫醇、类固醇和抗肿瘤坏死因子等,这些昂贵的疗法限制了UC治疗的持续性和有效性,可能还会引起高血压、糖尿病等不良反应。因此,迫切需要开发更有效和更安全的新治疗策略。
多花黄精(Polgonatum cyrtonema)在中国被用作传统的滋补食品和草药,其多种生物活性化合物广泛用于治疗疾病,比如抵抗骨质疏松、抗疲劳、降血糖、治疗脂肪肝和阿尔兹海默症等。这种潜在的健康益处与多花黄精的次生代谢产物(多糖、皂苷、黄酮类、酚类等成分)密不可分。前期研究表明,低聚果糖(fructooligosaccharides,FOS)是多花黄精主要组成成分之一,具有显著的生物活性。PFOS能够显著抑制小鼠脂多糖(lipopolysaccharide,LPS)诱导的腹膜炎中血清促炎细胞因子(TNF-α,IL-1β)和减少小鼠肺组织中炎症单核细胞的积聚。但是,PFOS是否有益于肠道炎症尚未确定。
为了研究PFOS在结肠炎保护中的潜在机制,澳门科技大学吴剑波教授的小组继续探索,其研究成果在国际期刊Biomedicine&Pharmacotherapy(Q1,IF:7.5)上发表。
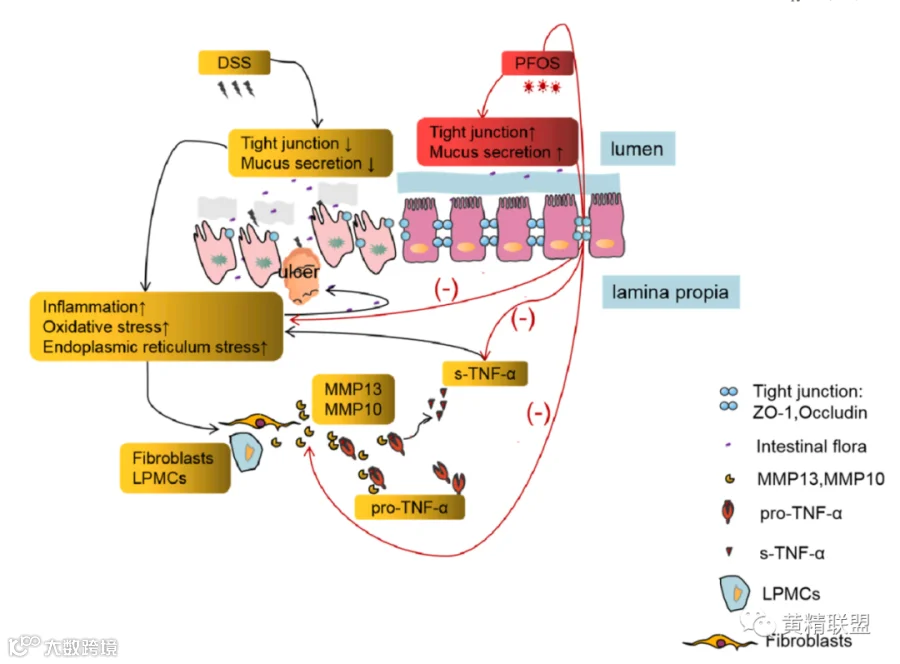
本研究首次调查PFOS在葡聚糖硫酸钠(dextran sulfate sodium,DSS)诱导的肠炎模型进展中的作用。PFOS可以调节抗炎细胞因子,并在粘膜屏障的保护下调MMP13 (matrix metalloproteases,MMPs),导致对DSS诱导的小鼠结肠炎模型的有益作用。此外还发现PFOS可以选择性地促进益生菌,包括双歧杆菌、异普氏菌和阿利斯蒂普菌。研究结果证实PFOS可能被用作患有肠道功能障碍人群的有效补充剂。
DSS诱导的结肠炎导致粘膜破坏障碍细菌抗原导致各种炎症细胞的活化,并最终导致炎症、氧化应激、内质网应激(ER,endoplasmic reticulum)和MMPs的高表达。MMP13将前TNF-α转化为可溶性TNF-α,加重了上述病理过程。PFOS早期的干预使MMP13的表达下调,改善粘膜屏障,并保护小鼠免受DSS诱导的炎症、氧化应激和内质网应激的影响。
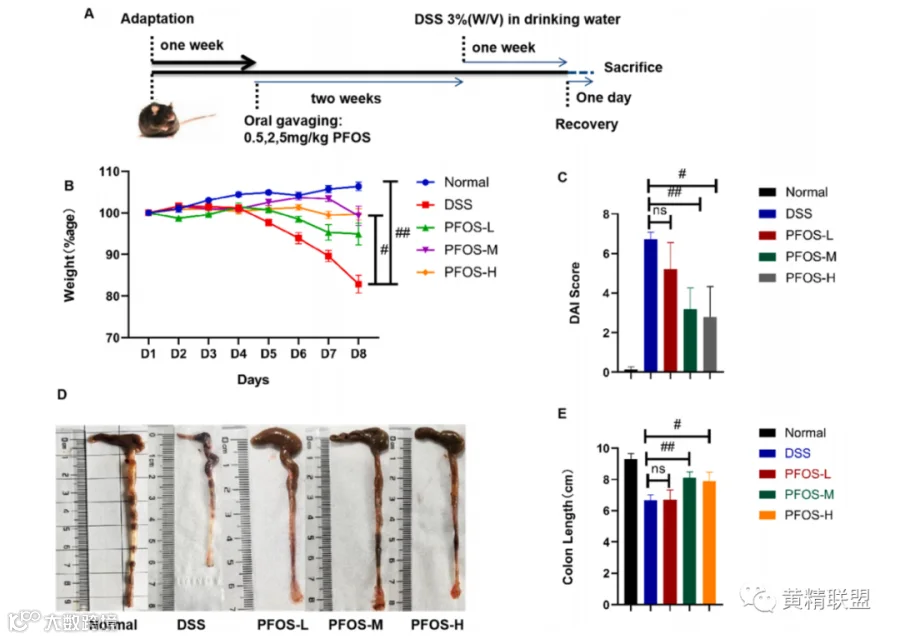
图1.结肠炎程度的实验设计和PFOS治疗。(A)四组小鼠正常饮食适应一周后,接受PFOSL 0.5 mg/kg,PFOS-M 2 mg/kg,PFOS-H 5 mg/kg 或相同体积的PBS治疗2周。3%DSS治疗从第4周开始,持续7天,然后恢复一天。 每天监测体重变化(B)。 PFOS的疾病活动指数(C)。每组DSS治疗后7天结肠外观的代表性图像(D)。小鼠的结肠长度如所示(E)。#p<0.05,##p<0.01(下同)。
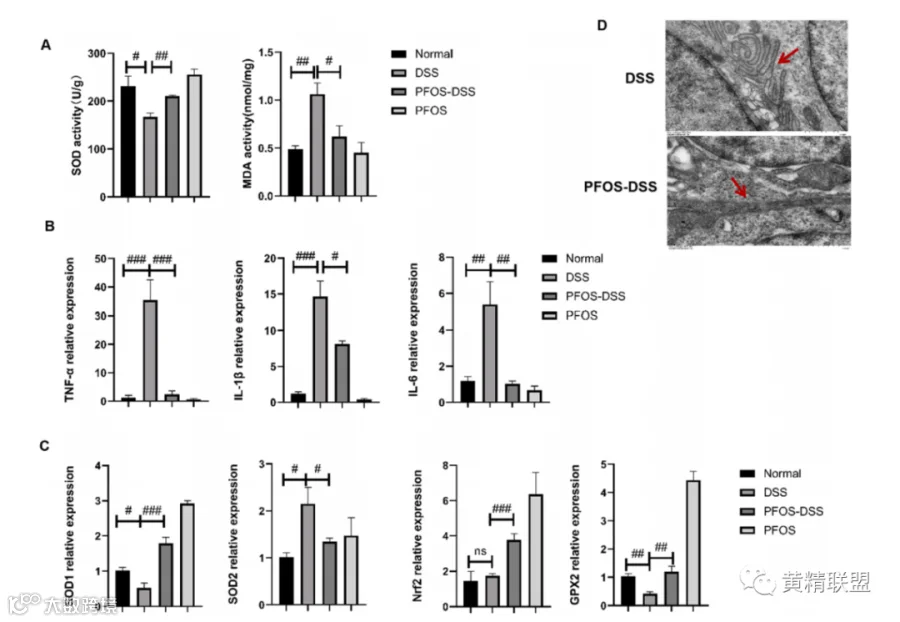
图2. PFOS保护小鼠免受DSS诱导的炎症、氧化应激和内质网应激的影响。(A) 血清SOD和MDA水平(n=5–6/组)。(B)PFOS对炎症相关基因表达的影响。(C)通过qPCR 分析PFOS改善氧化应激基因。(D)PFOS-DSS和DSS小鼠的形态TEM图像。红色箭头表示内质网,显示内质网管腔扩张,有双层膜DSS组中的结构。PFOS有力地阻止了ER扩张,显示出ER管腔连续的完整性。
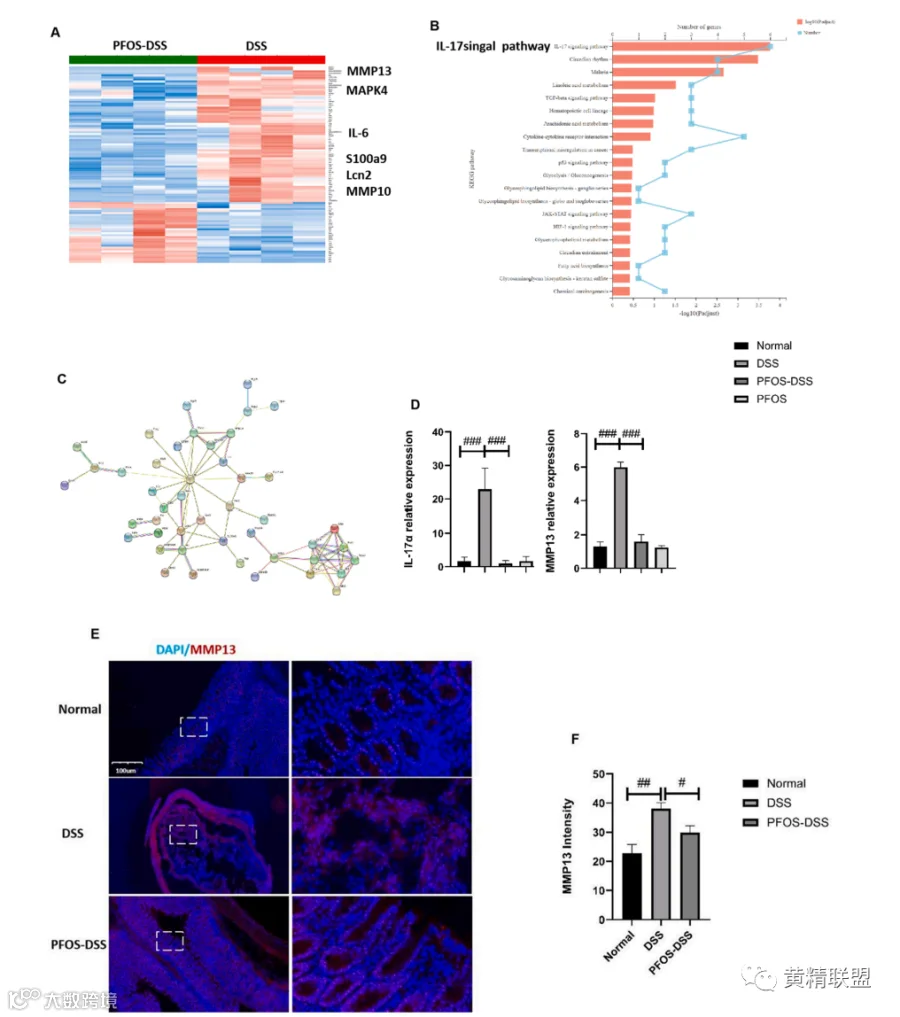
图3. PFOS改变小鼠结肠中的基因表达。(A)小鼠结肠组织差异表达基因的热图。(B) KEGG分析显示IL-17信号通路。(C) 相邻基因重复出现的搜索工具(STRING)差异基因的网络可视化。IL-17信号通路中表达的基因。边缘代表蛋白质-蛋白质关联。(D) IL-17、MMP13和MMP10的qPCR检测。(E)通过免疫荧光显微镜获得的MMP13在结肠切片中表达的代表性图像。(F)使用了图像J软件免疫荧光的半定量分析。
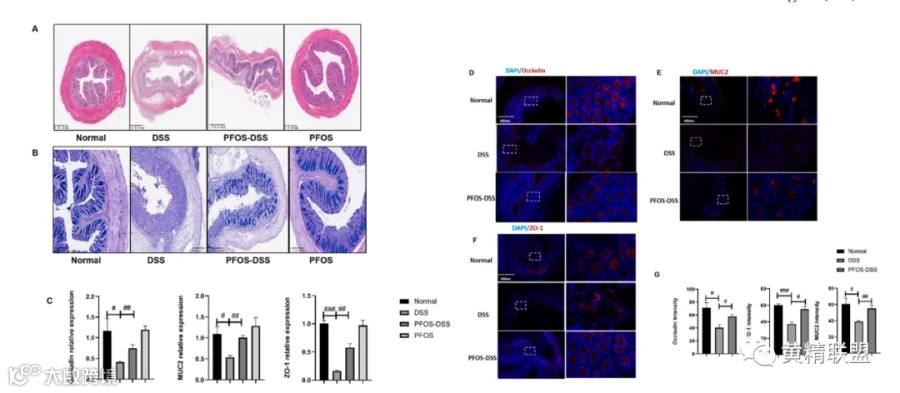
图4. PFOS降低MMP13的表达并改善粘膜屏障功能。(A) 结肠切片的H&E染色如图所示。(B) 阿尔新蓝染色切片显示结肠为杯状细胞。(C) 通过RT-qPCR检测ZO-1、MUC2和Occludin 1的表达。(D-F)代表结肠切片中ZO-1、MUC2和Occludin 1的免疫荧光染色。(G)ZO-1,MUC2和Occludin 1通过显示分布差异的图像J软件。
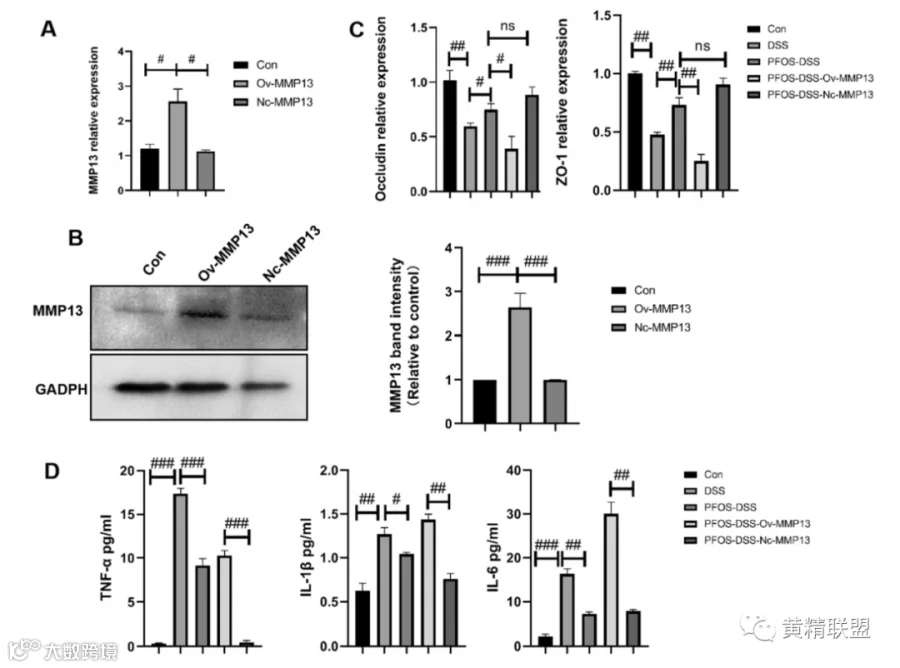
图5. MMP13的高表达减弱PFOS的抗炎和粘膜屏障保护作用。(A、B)人结肠粘膜上皮细胞系,NCM460用于模拟溃疡性结肠炎的体外模型。MMP13通过用MMP13 pCDH-CMV-MCS-EF1-GFP+Puro转染而过表达质粒。如所示,来自过表达载体的MMP13的代表性免疫印迹和定量。(C) 屏障功能障碍相关的表达通过qPCR测定包括ZO-1、Occludin在内的蛋白质。(D) 使用酶联免疫法评估炎症相关因子TNF-α、IL-6和IL-1β的水平套件。
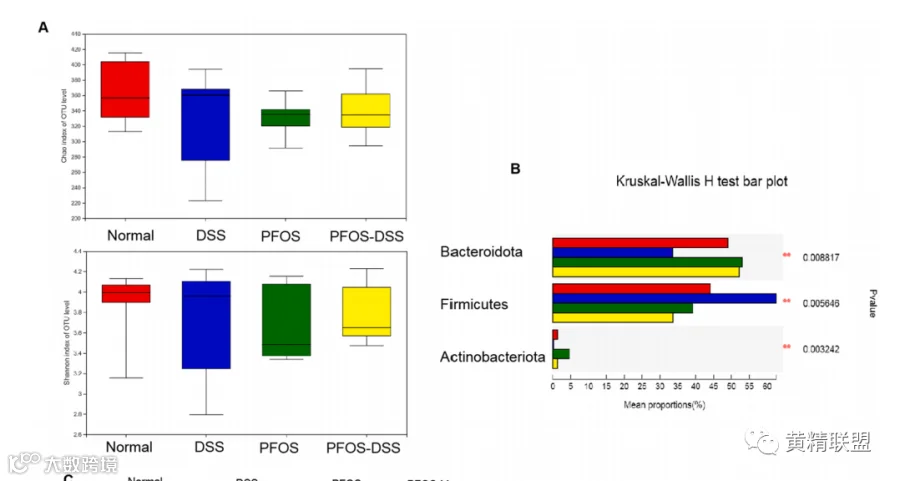
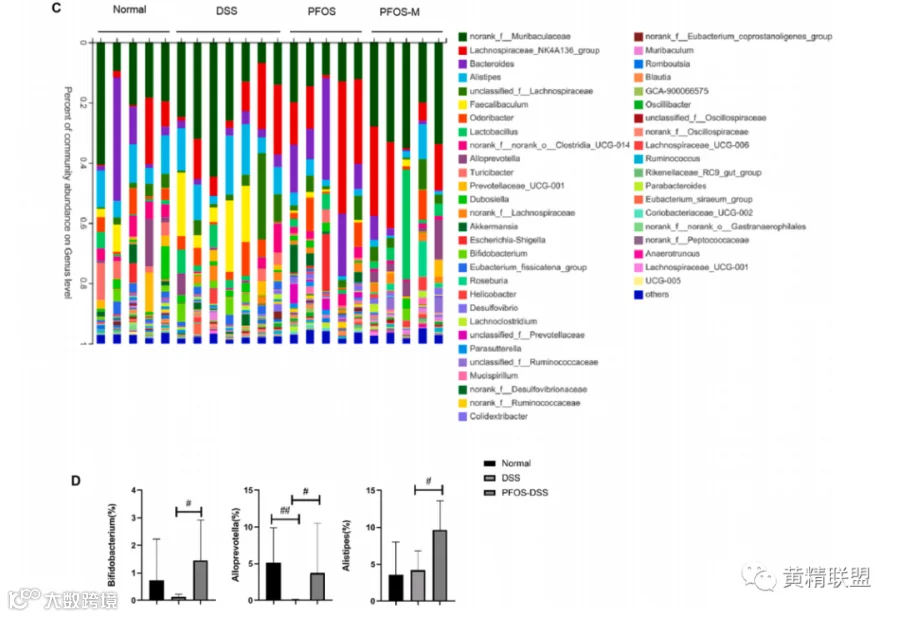
图6.在DSS诱导的结肠炎模型中,PFOS在一定程度上调节肠道微生物群失调。(A)α之间无统计学意义不同小鼠组肠道细菌丰富度(Chao1指数)和多样性(Shannon指数)的多样性分析。(B) Kruskal Wallis级别和检查门水平组间显著性检验。(C)属水平的肠道细菌组成的分类分布。(D) 三种益生菌PFOS治疗后显著增加。
澳门科技大学吴剑波教授为论文的通讯作者,原文链接:https://doi.org/10.1016/j.biopha.2023.114562
请扫二维码关注“黄精联盟”公众号
支持单位:
浙江农林大学森山大健康研究院
浙江农林大学新化黄精研究院
新化县颐朴源黄精科技有限公司
浙江农林大学磐安共富学院
编辑:周茜
审核:刘京晶