国家卫生健康委联合教育部、体育总局等多部门协同推进于2025年启动为期三年的“体重管理年”专项活动。活动旨在通过加强科学普及和宣传倡导,提高全民的体重管理意识,动员社会广泛参与,提升全民体重管理意识和技能,普及健康生活方式,推动部分人群体重异常状况的改善,加强慢性病防治。
随着人们生活水平的提高、高热量和高脂肪食物的饮食结构、身体锻炼不足和久坐不动的生活方式,导致全球肥胖的发病率不断攀升,肥胖现在已经成为世界各国所共同面临的严重公共卫生问题。众所周知,由肥胖引起的心血管疾病、2型糖尿病、高血压、冠心病以及各种癌症等疾病是它给人们带来的主要危害。然而,对于脂质代谢紊乱导致的肥胖和肝脏脂肪积累,目前仍然缺乏有效的治疗手段。因此,寻找能够有效对抗肥胖的干预措施,已经变得至关重要。
黄精(Polygonatum sibiricum rhizome, PSR)是天门冬科植物,具有药用和膳食补充品的同源性。《名医别录》曾记载:“黄精,味甘,平,无毒。主补中益气,除风湿,安五脏。久服轻身、延年、不饥”。PSR具有多种生物活性成分,如多糖、黄酮、生物碱、皂苷等,常用作抗炎、抗骨质疏松剂、免疫增强剂等。然而,关于PSR水提液(PSR water extract,PSRwe)对肥胖的影响及其潜在机制的研究还很缺乏。因此,甘肃省陇东生物资源保护利用与生态修复重点实验室的欧晓彬教授团队在《Phytomedicine》(中科院1区TOP,IF=6.7)发表了“Multiomics reveals the ameliorating effect and underlying mechanism of aqueous extracts of polygonatum sibiricum rhizome on obesity and liver fat accumulation in high-fat diet-fed mice”的研究论文。

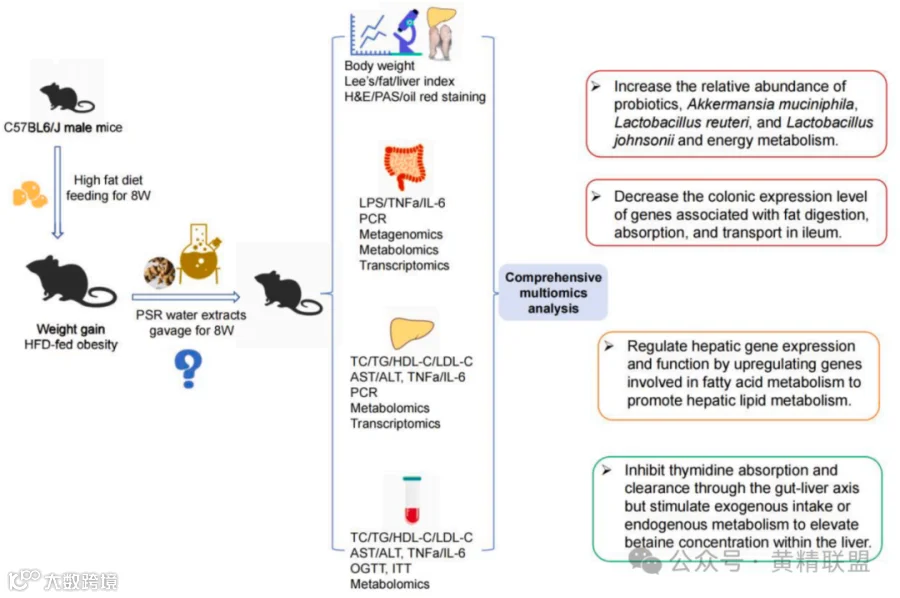
本研究通过构建高脂饲料(high-fat diet,HFD)诱导的肥胖模型,系统解析PSRwe调控代谢综合征的多维机制;评估体重动态、脂质代谢谱及肝脏脂肪变性等关键指标;整合肠道菌群宏基因组-结肠/肝脏转录组-血液/肝脏代谢组多组学数据;构建“菌群-代谢-基因”跨维度互作网络,揭示PSRwe通过肠肝轴代谢网络重编辑改善能量稳态的作用靶点,为肥胖及相关代谢性肝病的营养干预提供转化医学证据。
将PSRwe(2.5、5.0、7.5、10.0mg/kg)和奥利司他隔天灌胃给肥胖小鼠,HFD模型组和对照组同时灌胃生理盐水,剂量根据小鼠体重(body weight,BW)调整,持续6周。解剖取样进行组织形态学、生理生化分析,以及多组学联合研究(图1A)。研究发现,奥利司他治疗1周后的体重明显下降;然而,接下来的几周会出现体重反弹,并且3周后的减肥效果相对低于PSRwe组(图1B)。相反,对于PSRwe治疗的小鼠,治疗3周后观察到BW 持续下降,且没有反弹(图1B)。多组学联合分析证实PSRwe通过多靶点调控网络实现代谢稳态重塑,其持续减重效应显著优于传统药物奥利司他。形态学分析表明,PSRwe治疗可减少肝脏大小和脂肪组织积累(图1C)。此外,PSRwe治疗可以降低腹部脂肪重量、皮下脂肪量、肝脏重量和Lee 's指数(图1C)。口服葡萄糖耐量试验(OGTT)和胰岛素耐量试验(ITT)结果显示,PSRwe可降低面积下曲线(AUC),表明胰腺β细胞的血糖调节能力增强,储备功能增强(图1D)。
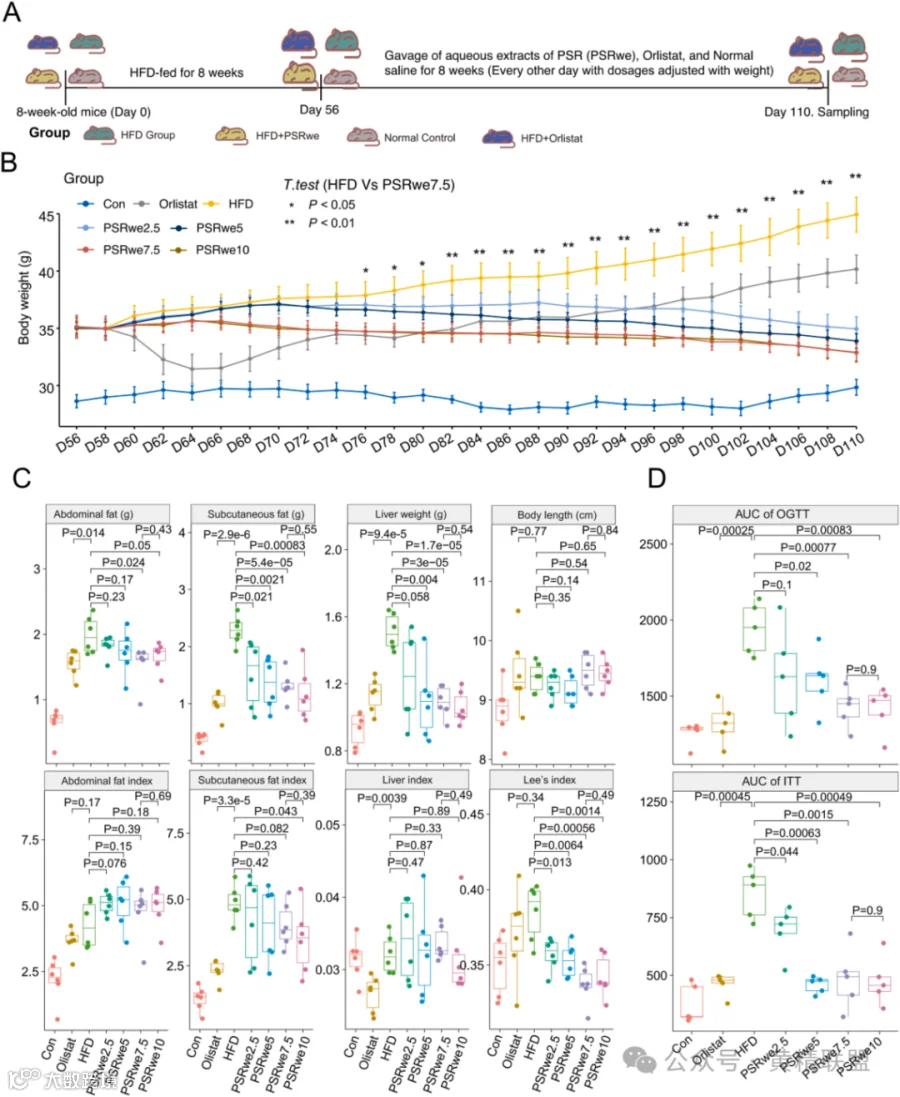
图1实验示意图、动物形态和生理指标
注:(A)动物实验过程示意图。(B)PSRwe和奥利司他治疗期间体重的变化。(C)动物形态学指标。(D)OGTT和ITT的AUC。
生化分析显示,PSRwe组的血液中脂联素(Adiponectin,ADPN)、瘦素(Leptin,LEP)、总胆固醇(Total Cholesterol,TC)、甘油三酯(Triglycerides,TG)、高密度脂蛋白胆固醇(High-Density Lipoprotein Cholesterol,HDL-C)、低密度脂蛋白胆固醇(Low-Density Lipoprotein Cholesterol,LDL-C)和游离脂肪酸(Free Fatty Acids,FFA)水平降低。相反,在PSRwe组的肝组织中,LEP、TC、TG、LDL-C和FFA水平显著降低;然而,ADPN和HDL-C水平升高(图2A)。此外,PSRwe治疗使得肥胖小鼠结肠、血液和肝脏中白细胞介素-6(Interleukin-6,IL-6)和肿瘤坏死因子-α(Tumor Necrosis Factor-alpha,TNF-α)水平降低,结肠的脂多糖(Lipopolysaccharide,LPS)水平降低,肝组织中丙氨酸氨基转移酶(Alanine Aminotransferase,ALT)和天门冬氨酸氨基转移酶(Aspartate Aminotransferase,AST)水平降低。对肝脏和脂肪组织进行染色观察,显示PSRwe处理6周后可显著降低脂质含量和脂肪细胞体积(图2B)。
综上所述,PSRwe(7.5 mg/kg)可通过改善体重增加、肝脏和脂肪组织质量、Lee's指数、与肥胖相关的血液标志物、葡萄糖代谢能力、胰岛素敏感性、脂肪含量和脂肪含量,有效减轻高脂饮食小鼠的肥胖和肝脏脂质积累,以及减少肝脏脂质沉积和脂肪细胞肥大。
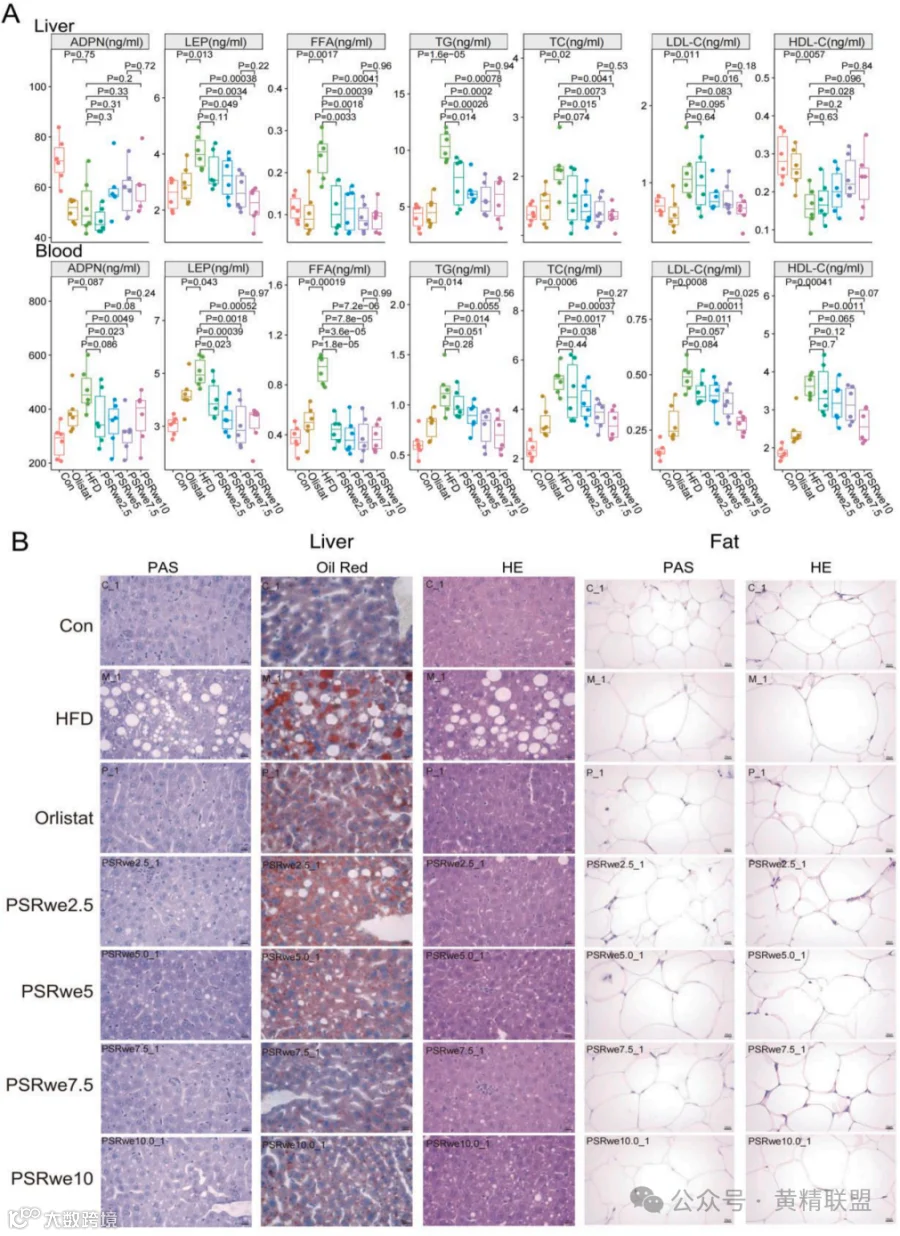
图2 生化指标及肝、腹部脂肪组织学染色
注:(A)小鼠血液和肝脏中ADPN、LEP、FFA、TG、TC、LDL-C、HDL-C水平上的差异。(B)肝脏PAS、油红O、H&E染色,腹部脂肪组织PAS、H&E染色。
通过宏基因组测序研究7.5 mg/kg PSRwe和奥利司他对肥胖小鼠肠道菌群的影响。基于属水平的Bray-Curtis距离的PCoA显示,HFD组和PSRwe组之间肠道菌群组成存在显著差异,而HFD组和奥利司他组之间无显著差异(图3A)。α多样性分析表明,与肥胖小鼠相比,PSRwe治疗后显著增加肠道菌群的多样性和丰度(图3B)。在HFD组和PSRwe组之间鉴定出10个显著不同的属。PSRwe组的嗜粘阿克曼氏菌、拟杆菌、阿利斯氏菌等细菌较HFD组富集,厚壁菌和粘毛菌的丰度显著降低(图3C)。PSRwe组与肥胖组间共发现21种差异显著的菌种,其中,嗜粘阿克曼氏菌、阿利斯氏菌、罗伊氏乳杆菌、嗜酸链球菌等显著富集;与HFD组相比,PSRwe组小鼠肠道中schaedlillum mucispirum和厚壁菌门细菌ASF500明显减少(图3D)。
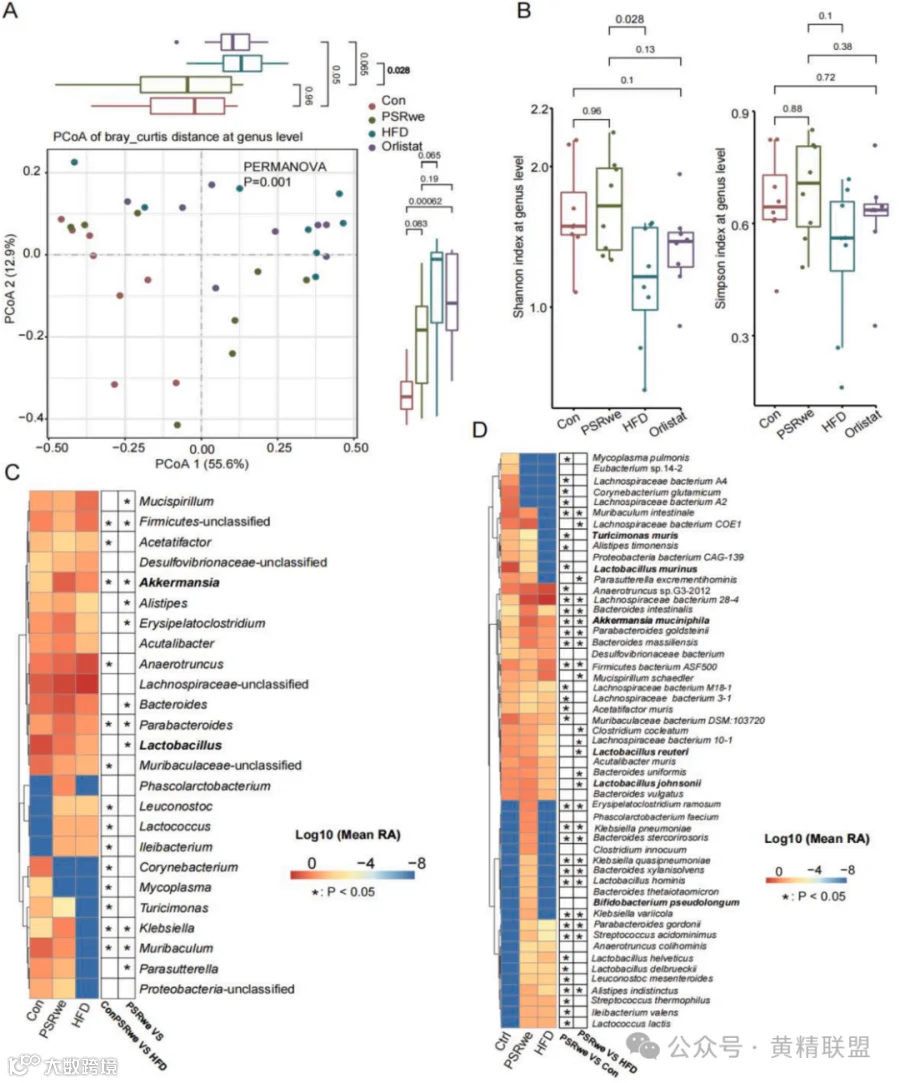
图3 肠道菌群组成的变化
注:(A)不同实验组肠道菌群的PCoA分析。(B)汉诺指数和辛普森指数的分析。(C)组间在属水平上的差异。(D)组间在种水平上的差异。
为进一步验证肠道菌群的功能变化,对PSRwe组和HFD组的结肠内容物进行代谢组学分析,共观察到165种显著不同的代谢产物(图4)。其中,PSRwe治疗小鼠的109种代谢物水平显著升高,56种代谢物水平明显降低(图4A)。PSRwe组中代谢产物水平升高主要与cAMP信号通路、氨基酸的生物合成、鞘脂代谢、ABC转运蛋白、神经活性配体-受体相互作用等多种途径相关(图4B-C),在PSRwe组中显著富集。然而,PSRwe组参与氨基和核苷酸糖代谢、胰高血糖素信号通路、半胱氨酸和蛋氨酸代谢相关的KEGG通路的代谢产物减少(图4D),则在肥胖组中显著富集。上述结果表明,PSRwe治疗改变肠道菌群的组成、功能和代谢物谱。
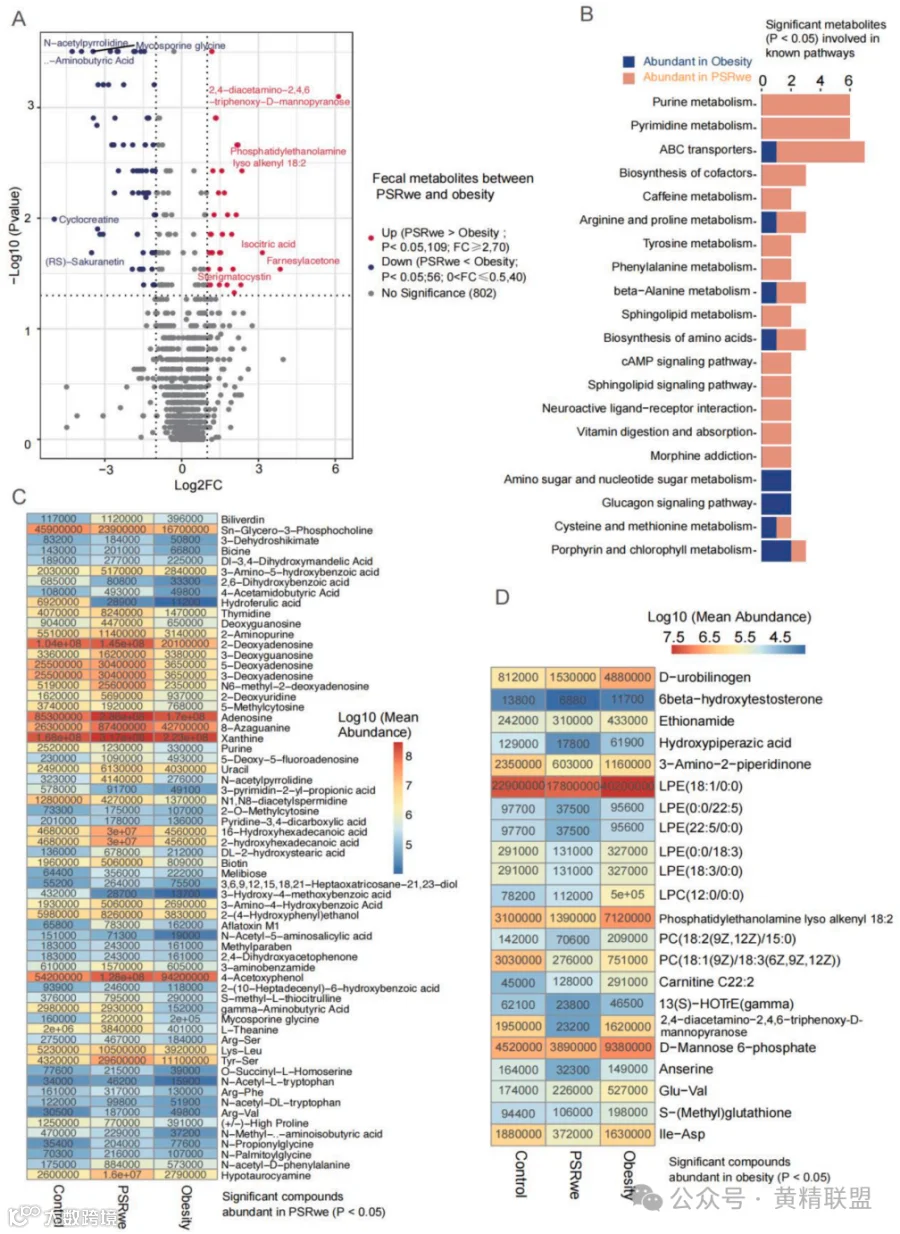
图4 结肠物代谢特征
注:(A)PSRwe组和HFD组的结肠代谢差异。(B)PSRwe组和HFD组结肠代谢物的KEGG通路。(C-D)PSRwe组和HFD组的结肠代谢物分布。
肠道菌群组成、功能和代谢物的变化可能通过肠-肝轴影响肠上皮的基因表达和肝组织的基因表达。因此,对肥胖组和PSRwe组小鼠的结肠和肝脏组织进行转录组分析。
通过转录组分析发现PSRwe组结肠组织中存在显著基因表达调控特征,共鉴定出184个上调及229个下调差异表达基因(图5A)。功能注释显示,上调基因主要富集于染色体结构维持、RNA结合功能及金属离子应激响应(镉/锌/铜离子反应)等生物学过程;而下调基因则主要参与线粒体能量代谢、泛素化降解系统及糖脂代谢调控等关键通路(图5B-C)。KEGG通路分析揭示脂质消化吸收相关通路呈现显著抑制特征,结合代谢表型证实PSRwe治疗可通过重塑肠道糖脂代谢网络,抑制脂肪吸收相关酶活性、调节碳水化合物分解代谢,有效改善肥胖小鼠的代谢紊乱。
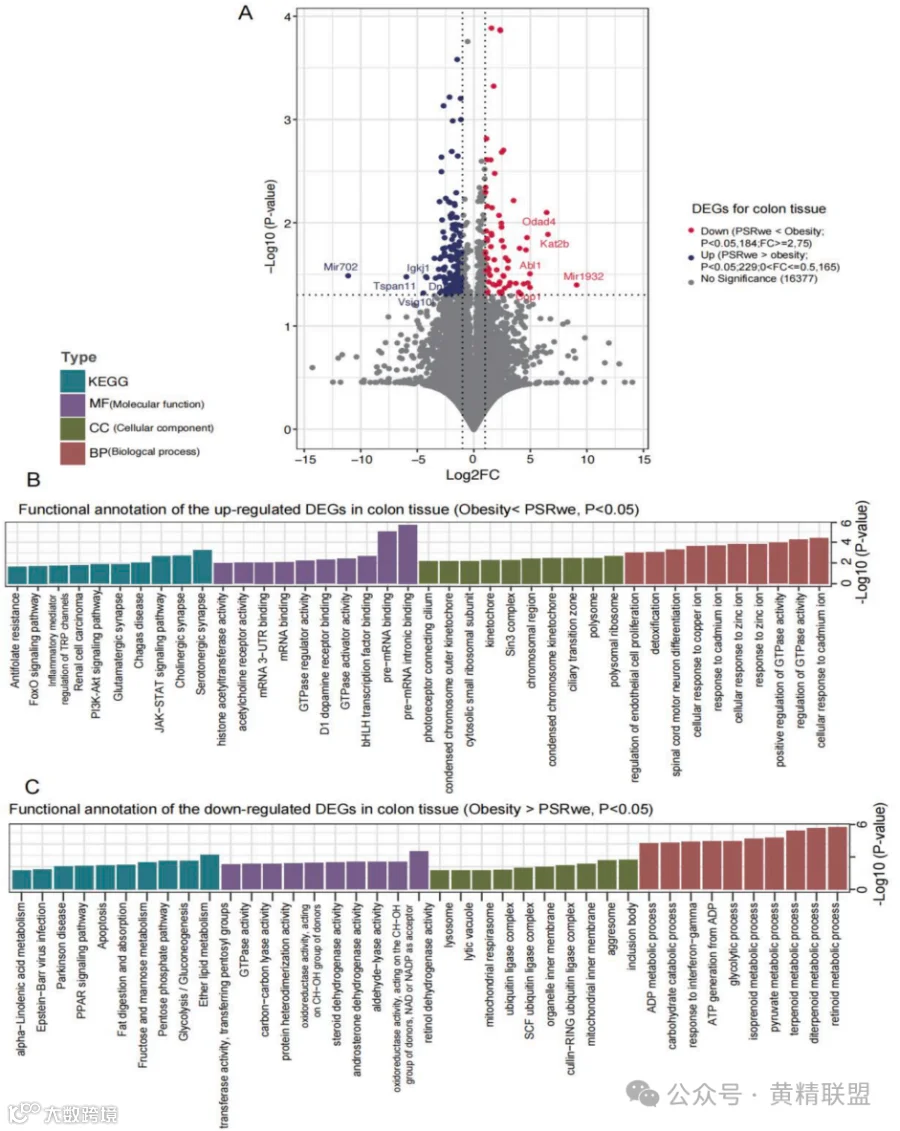
图5 PSRwe治疗和肥胖小鼠在结肠组织中的差异表达基因
注:(A)PSRwe组和HFD组的DEGs关系图。(B-C) DEGs上调和下调的GO注释和KEGG通路分析。
肝脏转录组分析揭示PSRwe治疗调控脂代谢关键通路,PCoA分析显示HFD组与PSRwe组呈现显著基因表达分型(图6A),共鉴定2791个差异基因(图6B)。功能解析表明,上调基因主要参与脂质分解代谢网络及氨基酸代谢,同步激活溶酶体降解与核糖体合成系统(图6C);下调基因则富集于固醇代谢轴及氧化还原酶系统(图6D)。通路互作网络证实PSRwe通过双重调控机制重塑肝脏代谢稳态,激活不饱和脂肪酸生物合成及脂质分解代谢,抑制固醇类物质合成及亚油酸代谢通路,从分子层面解释PSRwe改善脂质代谢紊乱的作用靶点。
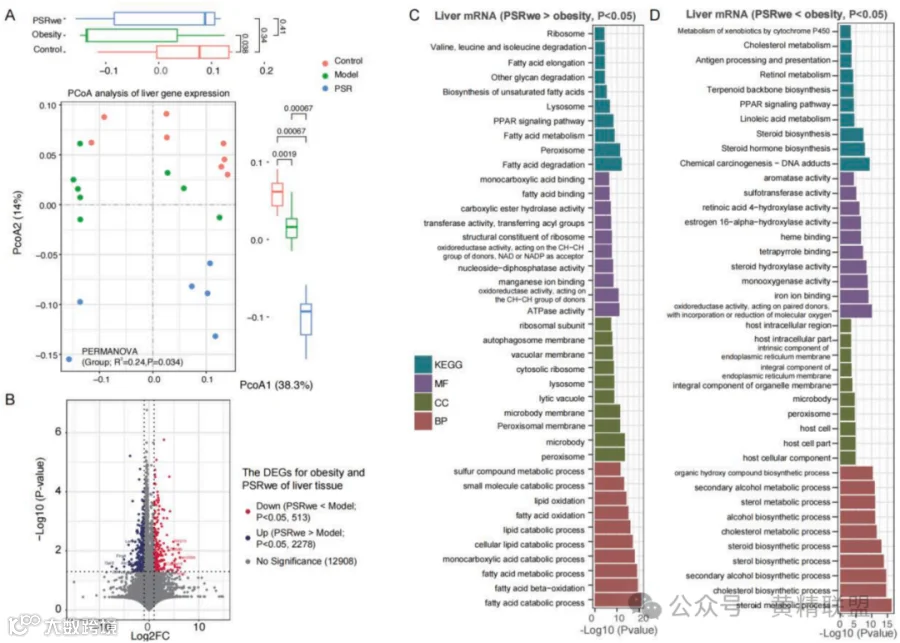
图6 PSRwe治疗与肥胖小鼠肝脏基因表达
注:(A)肝脏基因PCoA表达分析显示两组间存在显著差异。(B)肝脏基因差异分析。(C-D) PSRwe组小鼠肝脏中DEGs上调和下调的GO注释和KEGG通路分析。
通过聚合酶链式反应(PCR)验证PSRwe调控肠肝轴脂代谢的关键机制(图7),在肠道层面呈现差异化调控,结肠中Pla2g3、Abca1等脂肪吸收相关基因表达上调,而回肠中Npc1L1、Mttp等核心转运基因表达下调;肝组织中Ehhadh、Acox1等脂肪酸氧化关键酶基因及Elovl3等延长酶基因表达量上升。说明PSRwe通过肠道区域特异性抑制脂质吸收转运与肝脏脂质代谢网络激活协同发挥代谢改善作用。进一步证实PSRwe抑制肠道脂肪消化和吸收,同时增加肝脏脂质代谢。
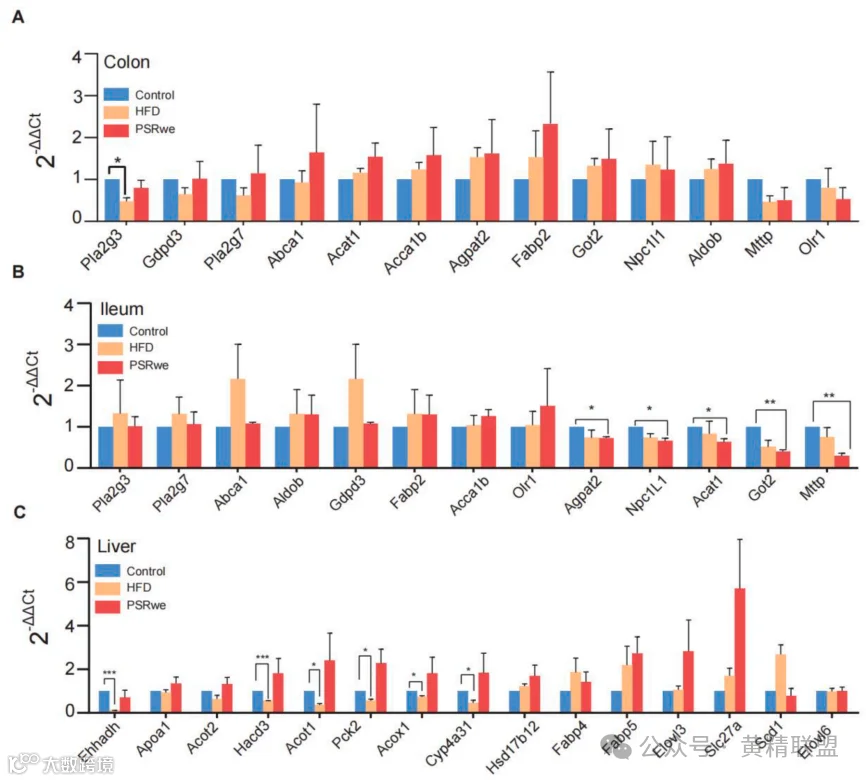
图7 肠道脂肪消化、吸收和运输的基因以及脂质氧化代谢的肝脏基因的PCR验证结果
肠道菌群-代谢物-宿主基因互作网络分析揭示PSRwe治疗的多效调控机制(图8),Spearman相关性分析显示,PSRwe组肠道菌群中富集的特征菌(Akkermansia muciniphila等)与脂肪吸收相关基因呈负相关,证实肠道菌群重塑通过抑制肠道脂质转运降低吸收效率;同时该菌群与神经信号通路基因呈现正相关,表明PSRwe治疗可通过“代谢-神经调控网络”双向作用,优化肠道脂糖代谢,激活脑肠轴信号传导。
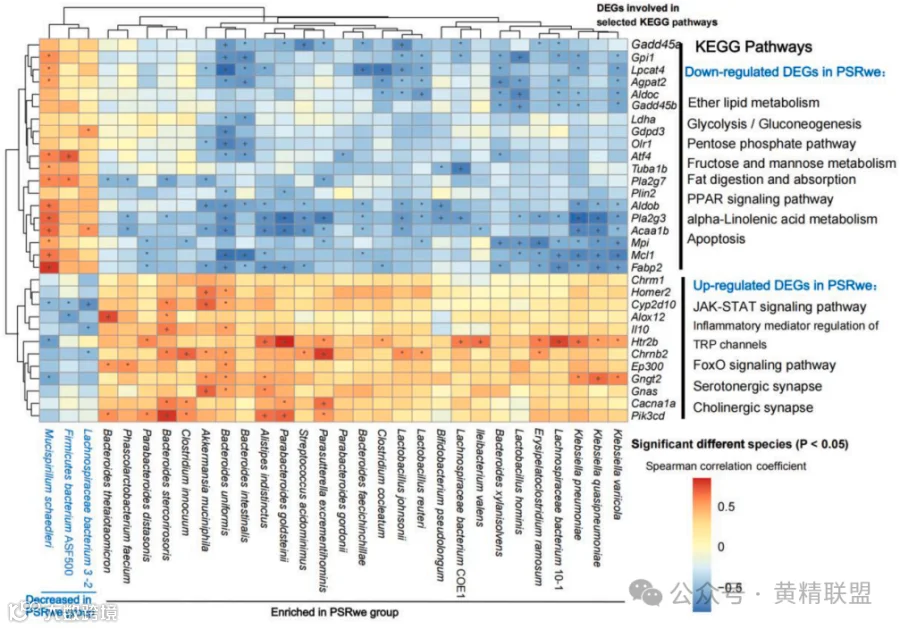
图8 不同物种与结肠DEGs的相关性分析
对肠道菌群组成与肝脏脂质代谢相关途径的肝脏基因表达之间的复杂关系也进行研究(图9),肝脏脂代谢关键基因与肥胖组特征菌群呈正相关,介导胆固醇合成及脂肪酸延伸;而PSRwe组特征菌群通过正向调控脂肪酸氧化枢纽基因及糖异生关键酶,形成“菌群-代谢基因”双向通讯网络,证实“致病菌”驱动脂质合成代谢和益生菌激活脂质-糖代谢轴,PSRwe治疗通过重构肠肝菌群生态实现代谢网络重编辑,同步阻断脂质异常蓄积与促进能量消耗。
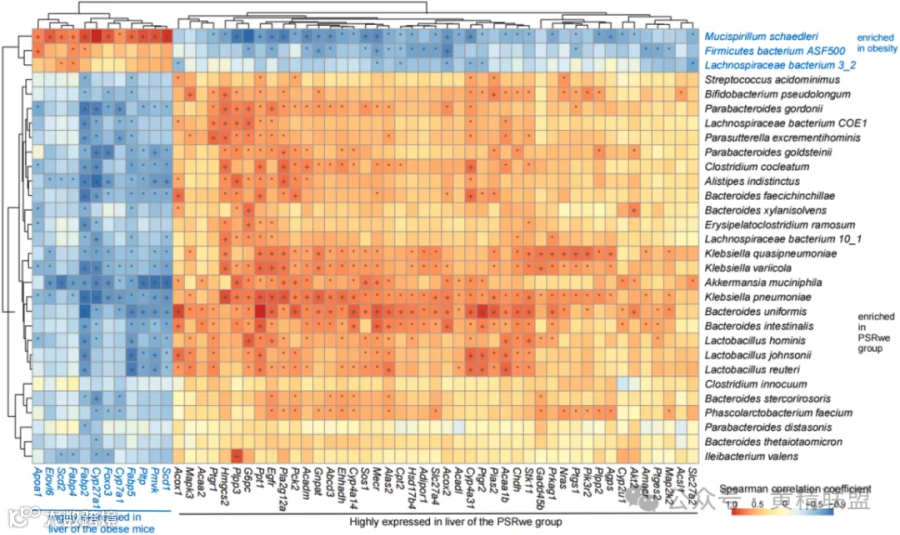
图9 不同物种与肝脏脂质代谢相关DEGs的相关性分析
肝脏代谢分析显示PSRwe治疗重塑脂代谢轴与氨基酸代谢网络,同步抑制HFD诱导的相关炎症代谢物(FFA/LPCs)并激活AMPK/FoxO能量感知通路(图10A-D)。血浆代谢组揭示系统性代谢改善,脂毒性代谢物显著下调,菌群共代谢产物上调(图11A-B)。跨组织代谢枢纽分析鉴定8个核心调控分子(如鹅胺/LPEs),其动态变化呈现器官特异性,鹅胺在肠-肝-血三联下调指示菌群胆汁酸代谢网络重编辑以及LPEs组织梯度分布反映磷脂重塑特征(图11C-D)。代谢物-菌群互作网络证实PSRwe治疗通过“菌群代谢物-宿主代谢酶”双向调控轴,同步优化肝脏脂肪代谢降解能力,增强肠道屏障功能并改善系统性能量稳态。
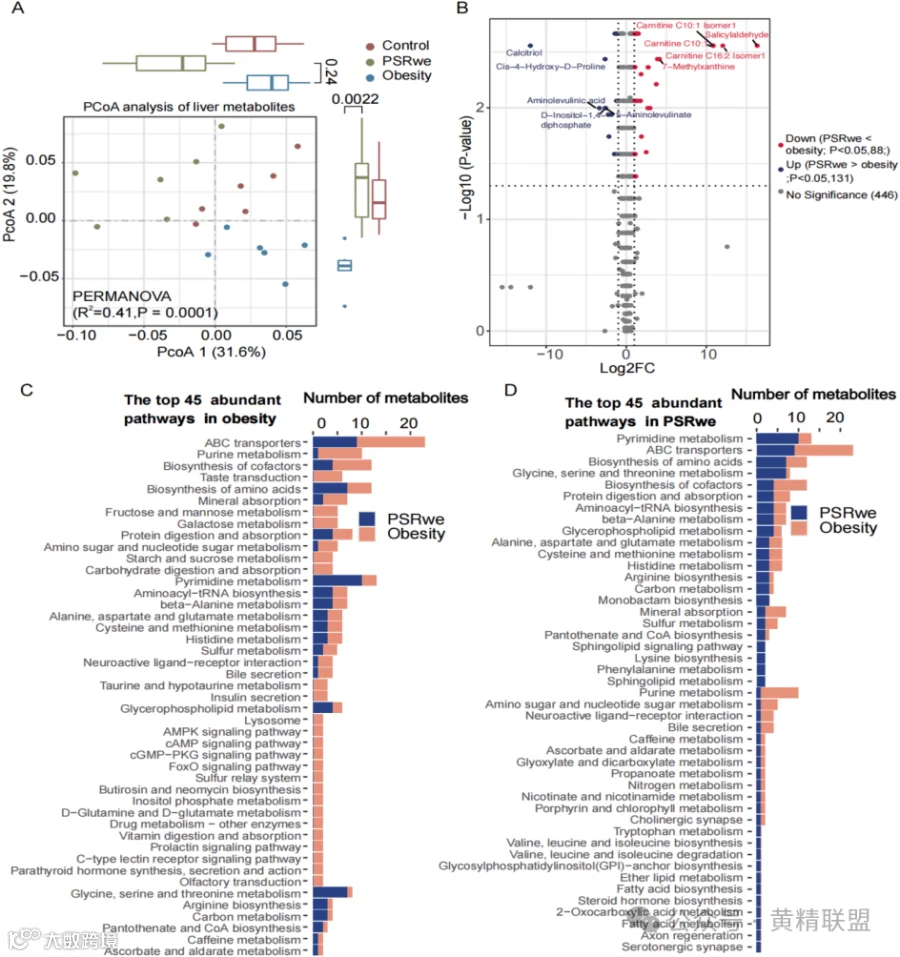
图10 肝脏代谢物分析
注:(A)肝脏代谢物PCoA分析。(B)肝脏代谢物差异分析。(C-D)肝脏中富集的显著不同代谢物的前45条途径。
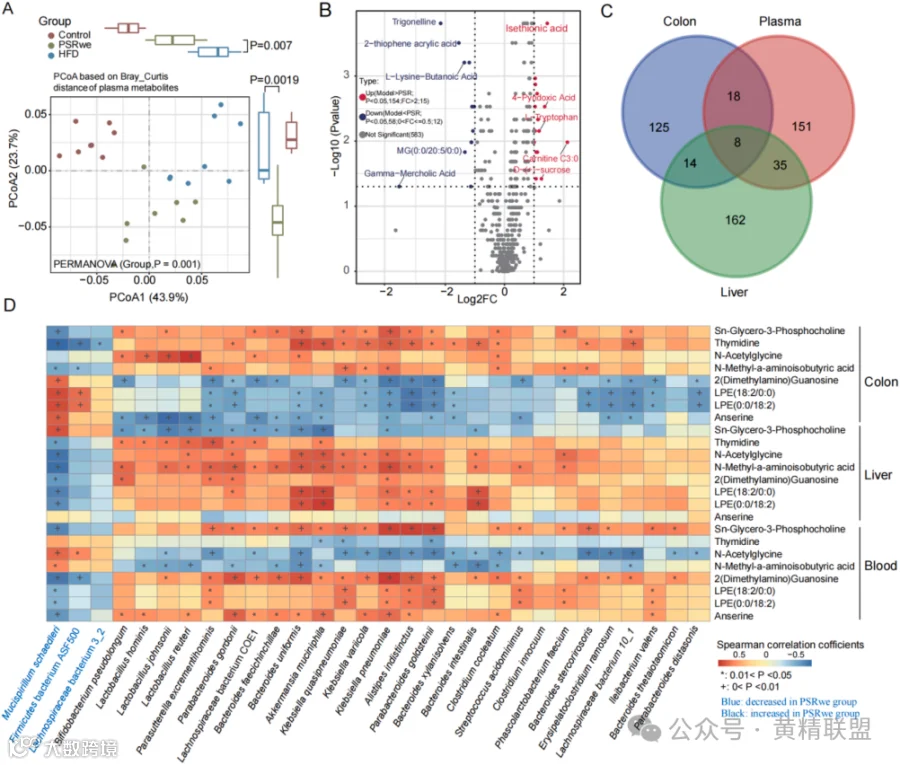
图11 血浆代谢物及结肠内容物、血浆和肝脏代谢物的相关性分析
注:(A)血浆代谢物的PCoA分析。(B)血浆代谢物的差异分析。(C)结肠内容物、血浆和肝组织中常见代谢物的维恩分析。(D)在结肠内容物、血浆和肝脏中存在差异的肠道菌群和8种常见代谢物的相关性分析。
跨组织代谢组学鉴定32个核心调控分子,其中胸腺嘧啶呈现器官特异性动态。与对照组相比,肥胖小鼠的粪便胸腺嘧啶水平显著降低,但PSRwe治疗后,粪便胸腺嘧啶水平显著升高。肝脏异常蓄积逆转,血浆水平协同调控(图12A)。为阐明PSRwe减轻食源性脂肪诱导的肥胖和肝脏脂肪沉积的潜在机制,研究PSRwe中特定成分在血浆和肝脏中的吸附,从而建立它们之间的联系和差异(图12B)。关键代谢物溯源甜菜碱作为PSRwe的特征成分,通过“肠道吸收-肝脏富集”路径,激活胆碱代谢酶Chdh,驱动肝脏甜菜碱生物合成循环(图12C)。研究证实PSRwe双重作用,抑制致肥因子胸苷的肠道吸收并增强肝脏清除以及促进抗肥胖介质甜菜碱的跨膜转运。代谢-基因互作网络揭示,十六烷二酸通过ω-氧化通路重塑脂肪酸代谢,N-丙酰甘氨酸介导肠道菌群-宿主共代谢调控,共同构成PSRwe改善脂质代谢紊乱的分子基础。上述结果表示,PSRwe可以通过抑制致肥成分胸苷的结肠吸收和增强肝脏对胸苷的清除,同时提高抗肥胖成分甜菜碱在血液和肝脏中的水平,有效缓解HFD诱导的肥胖和肝脏脂肪沉积。
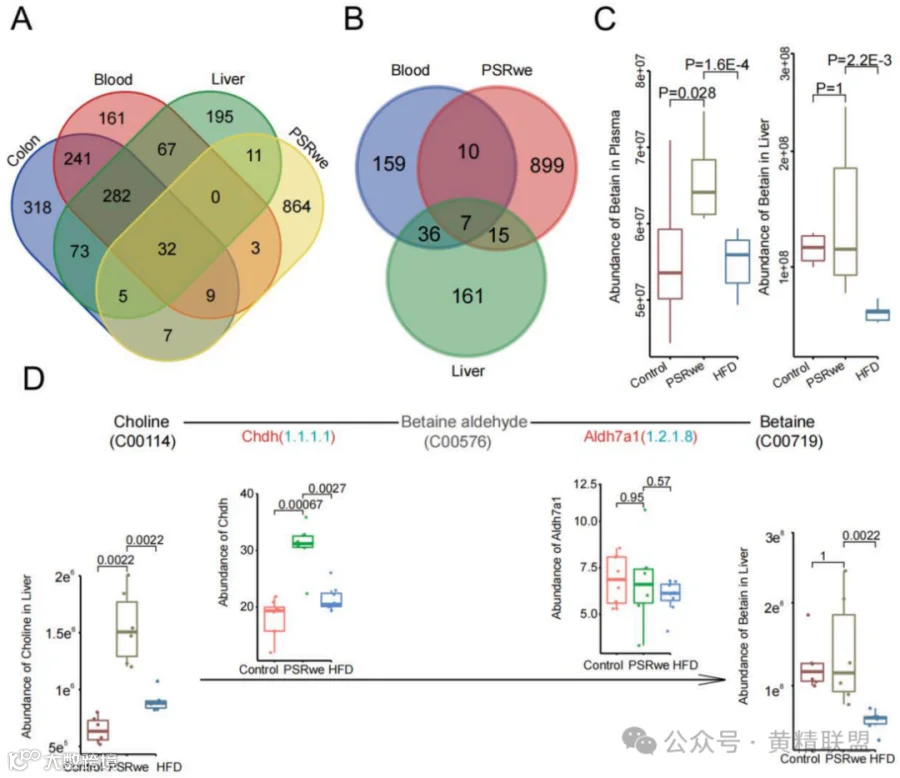
图12 多组学关联分析显示,甜菜碱可能是缓解肥胖和肝脏脂肪积累的有效成分
注:(A) PSRwe、结肠内容物、血浆和肝组织中的代谢物分析。(B)PSRwe、血浆和肝组织中的7种常见代谢物。(C)血浆和肝脏中甜菜碱的丰度。(D)胆碱在肝脏中被Chdh和Aldh7a1代谢为内源性甜菜碱途径。
本研究发现,PSRwe可以帮助我们减轻因为摄入过多高脂肪食物而带来的肥胖和肝脏脂肪堆积问题。具体来说,PSRwe能调整肠道菌群结构,让肠道里的嗜粘阿克曼氏菌、罗伊氏乳杆菌、约氏乳杆菌等这些有益菌变得更多,可以帮助我们更好地消化食物,调节身体的能量代谢,让身体可以高效地利用能量。同时,PSRwe还能降低结肠中与脂肪消化、吸收和转运有关的基因表达水平,这样一来,身体就不会容易吸收脂肪。同时,增加肝脏中和脂肪酸代谢相关的基因的表达,帮助肝脏更快地分解脂肪。此外,通过促进自身外源性吸收以及胆碱的内源性代谢,加快肝脏对致肥胸苷的清除速度,使其更快地从肠道排出去,同时提高抗肥胖甜菜碱在肝脏中的含量,可以帮助我们更好地控制体重。这些研究结果给利用黄精膳食减重降脂提供一种新思路。
甘肃省陇东生物资源保护利用与生态修复重点实验室的欧晓彬教授为该论文的第一作者兼通讯作者与兰州大学第二医院翠英生物医学研究中心王奇助理研究员为该论文的共同通讯作者。
转载请在开头注明:本文转载自公众号——黄精联盟
原文链接:https://doi.org/10.1016/j.phymed.2024.155843



