你还在为疲劳而烦恼嘛?随着日益激烈的社会竞争和越来越快的生活节奏,饮食不规律、睡眠不足、作息不规律、 精神紧张等现象普遍存在,这些现象会导致越来越多的人出现疲劳症状。

全球约20%的成年人受疲劳影响。在严重情况下,过度疲劳会引起内分泌失调、免疫力下降或器质性紊乱,对人体健康构成重大威胁。如不消除持续性疲劳,会严重影响患者的生活质量和工作效率,可能导致衰老、癌症、高血压、冠心病、多发性硬化症和帕金森病等。

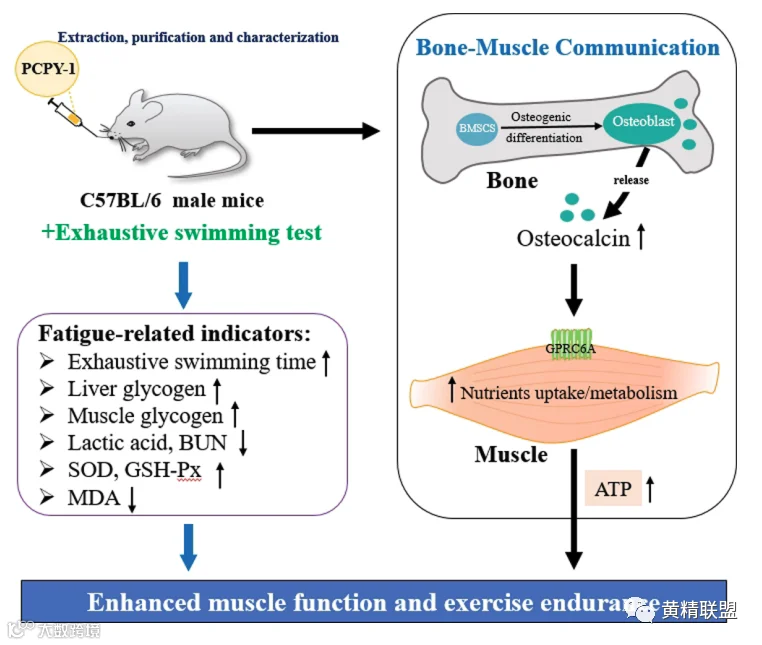
为了研究黄精多糖对骨骼和肌肉之间的生化通讯作用机制,合肥工业大学食品与生物工程学院查学强教授团队,通过解析黄精均一多糖(P. cyrtonema ,PCPY-1)结构表征,研究了其抗疲劳作用其机理。该研究通过使用游泳力竭小鼠模型和小鼠骨髓间充质干细胞/小鼠成肌细胞(BMSCs/C2C12)共培养系统,从骨钙素介导的骨骼肌通讯方面研究了PCPY-1的抗疲劳机制。研究成果在国际期刊Journal of Agricultural and Food Chemistry (Q1,IF:5.895)上发表。

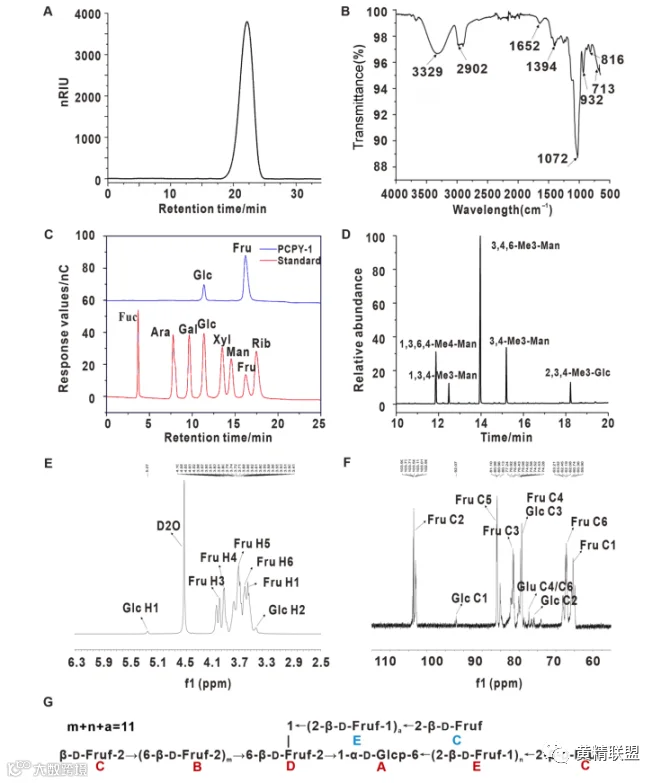
首先利用高效液相色谱(HPLC)、气相色谱质谱联用(GC-MS)、核磁共振(NMR)等手段研究了黄精多糖PCPY-1的结构特点(图1)。HPLC分析表明,PCPY-1是一种均匀的多糖组分,呈单个对称峰。PCPY-1的相对分子质量和总碳水化合物含量分别为4200 Da和84.2%(图1A),由果糖和葡萄糖以摩尔比15:1组成 (图1B、C)。通过甲基化分析和核磁共振波谱对PCPY-1的一级结构进行了表征。在甲基化的PCPY-1的水解产物中观察到五种类型的醛糖醇乙酸酯(图1D)。结合单糖组成分析、甲基化和NMR光谱(图1E、F)的结果,得到了PCPY-1的主要结构(图1G)。
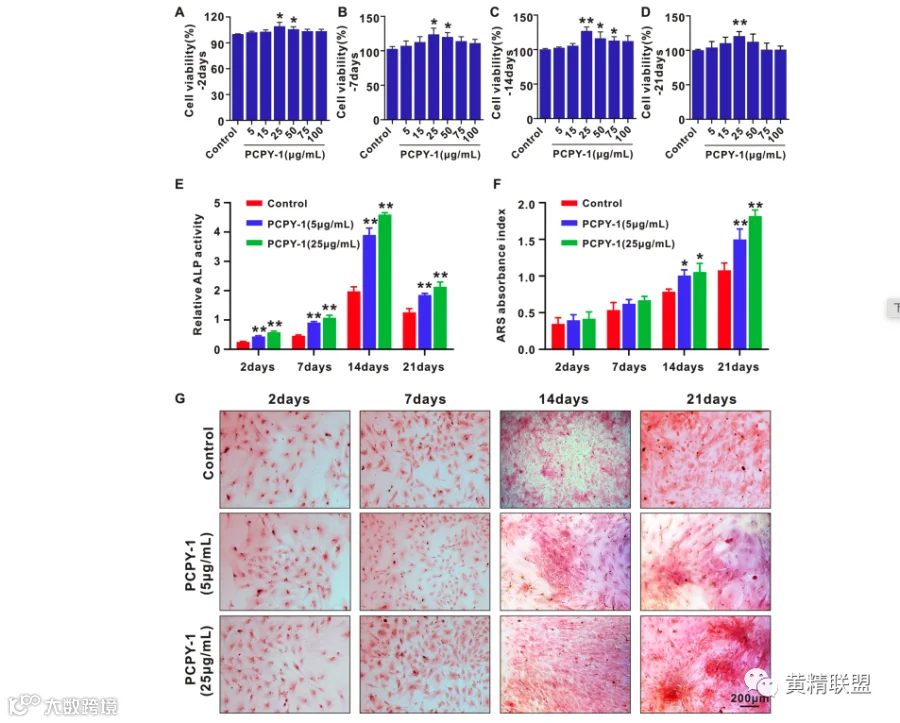
如图2所示,体外细胞实验表明PCPY-1在最高浓度100 μg/mL孵育21天对骨髓间充质干细胞没有毒性。ARS染色结果显示(图2 F、G),与对照组相比,PCPY-1(25 μg/mL)在BMSC成骨分化21天后可以明显增强矿化结节的生成。这些结果表明PCPY-1在体外促进了骨髓间充质干细胞的增殖和成骨分化。
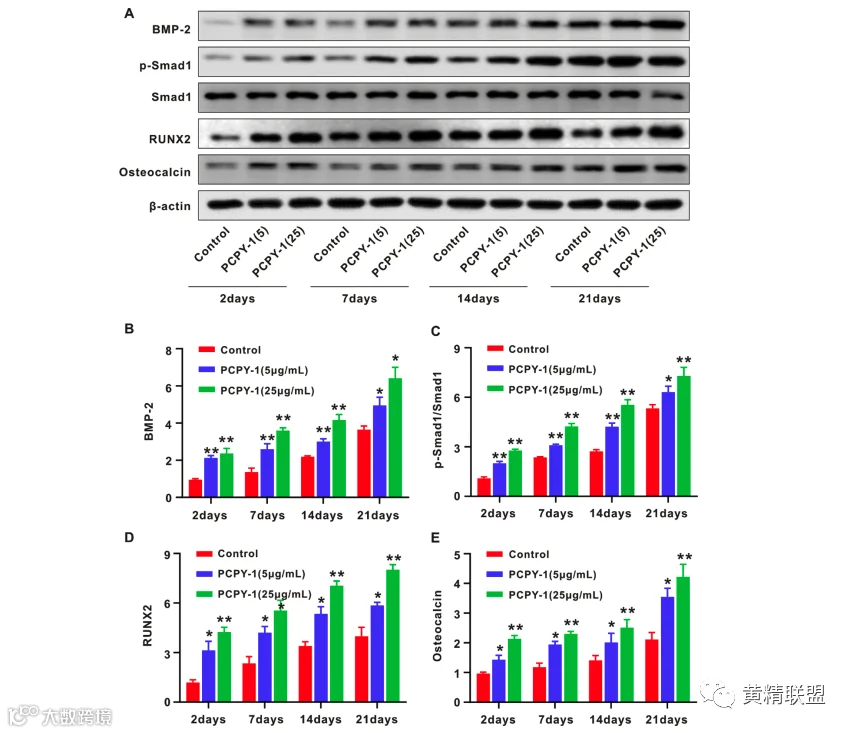
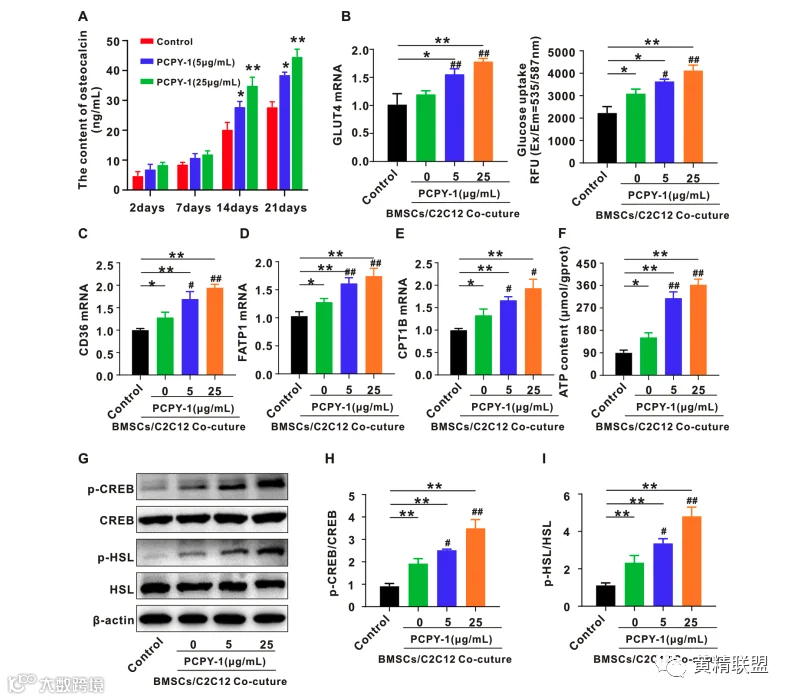
骨髓间充质干细胞的分化受到一系列信号和分子的特异性调节。BMP-2是一种众所周知的诱导生长因子,可以刺激多种干细胞的成骨分化和矿化,下游转录因子Smad1和RUNX2是至关重要的BMP-2的细胞内效应物。在分化2、7、14和21天后,与对照组相比,PCPY-1显著上调BMSC中BMP-2、p-Smad1、RUNX2和骨钙素蛋白的水平(图3A-E)。进一步推断PCPY-1可能是促进BMSCs向成骨细胞分化的有效途径。
骨骼肌是人体能量代谢的重要组织。一般来说,葡萄糖和脂肪酸是骨骼肌产生能量的主要底物来源。这些能量底物通过特定的代谢转运蛋白,如葡萄糖转运蛋白4型(GLUT4)、脂肪酸转运蛋白(FATP1)和脂肪转运蛋白(FATP1)、CD36等转运到肌肉细胞中。为了探究PCPY-1对骨钙素介导的骨骼肌通讯的影响,建立了BMSCs/C2C12细胞的共培养系统。结果表明(图4),PCPY-1可以增强骨钙素介导的BMSCs与C2C12细胞之间的通讯,从而有利于骨钙素介导的C2C12细胞的能量代谢和ATP的产生。
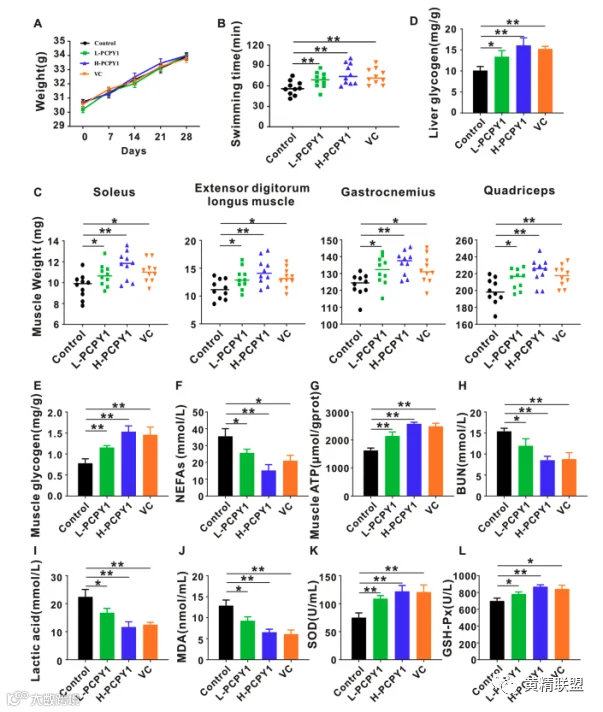
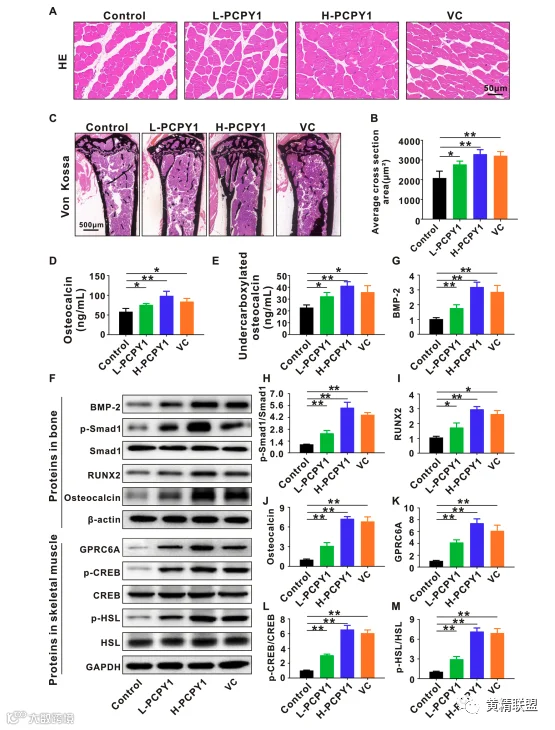
骨钙素可以调节肌肉能量代谢,从而在运动中对抗疲劳。PCPY-1可以增加骨钙素和羧化不足的骨钙素的循环水平(图6D,E),并激活GPRC6A在骨骼肌中的表达(图6F、K),从而调节葡萄糖和脂肪酸的代谢,改善骨骼肌功能和运动表现(图5和图6)。骨髓间充质干细胞是一种多能干细胞,是体内成骨细胞最重要的来源。研究进一步利用骨髓间充质干细胞探讨PCPY-1在成骨分化中的作用。研究结果表明,PCPY-1可以在体外(图2-4)和体内(图5和6)提高骨钙素水平,促进肌肉能量代谢和ATP生成,从而改善疲惫的游泳小鼠的运动表现。
以上研究表明,多花黄精均一多糖PCPY-1可以作为一种新型的抗疲劳食品有效成分进行开发。
转载请在开头注明:本文转载自公众号——黄精联盟
合肥工业大学食品与生物工程学院罗建平教授与合肥工业大学查学强教授为论文的通讯作者。

请扫二维码关注“黄精联盟”公众号
支持单位:
浙江农林大学森山大健康研究院
浙江农林大学新化黄精研究院
新化县颐朴源黄精科技有限公司
浙江农林大学磐安共富学院


