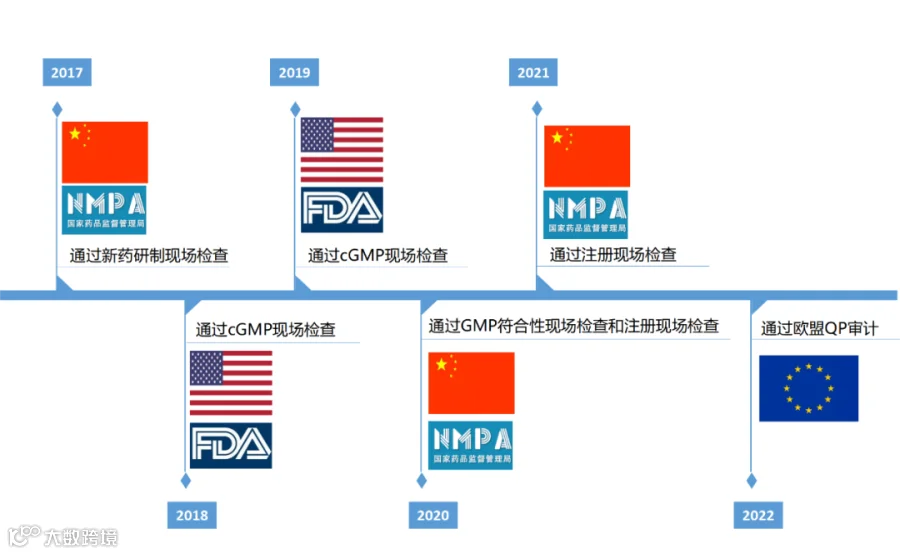
近日,广州玻思韬控释药业有限公司(以下简称“玻思韬”)与国内某知名药企合作的创新药项目顺利通过欧盟QP审计。这是玻思韬首次通过欧盟审计,这标志着玻思韬的研发生产基地和质量管理体系达到欧盟GMP标准,能够保障产品的高品质研发和生产。
此次欧盟QP审计依据欧盟GMP的行业指南执行,外籍审计官对玻思韬加速器厂区和瑞祥路厂区的生产管理体系、QA体系、产品包装、标签与检验等方面进行了全面系统的检查,整个审计历时2天。在2022年10月13日,审计官出具了QP
Declaration,标志着玻思韬已顺利地通过了本次审计,为合作开发的创新药物走向欧洲市场打下坚实基础。
玻思韬秉承“安全、有效、可控”的理念,依据US21CFR Part210&211、European Union、中国现行版GMP、ICH等国内外法规,建立一套涵盖药品研发和药品生产的符合中、美、欧标准的质量管理体系。玻思韬的研发与生产基地之前已通过中、美GMP检查。本次顺利通过欧盟QP审计是玻思韬质量体系建设的又一重要里程碑,再次证明了玻思韬已建立了一个良好药品研发与生产的管理体系,并拥有一支精通国内外药品生产管理规范的专业团队。未来玻思韬仍将严格按照建立的GMP管理体系实施产品的研发与生产,确保药品的质量与安全。