多花黄精(Polygonatum cyrtonema Hua, PCH)富含生物活性化合物,具有抗氧化、抗菌和抗炎等多种生理活性。传统上利用“九蒸九制”对其进行加工,旨在“减毒增效”。“减毒”是指减轻黄精生品的刺激性,“增效”是指提高黄精的药效。传统观点认为,每次蒸制次数的增加都会增强草药的活性,并有助于其消化吸收,但这一论断缺乏科学理论依据。目前的研究主要考察了PCH蒸制过程中多糖的结构和活性,以及其他活性成分的动态变化。但是这样的评价过程往往忽视了活性物质在人体胃肠道中经一系列消化过程被释放的动态过程。事实上,摄入富含生物活性物质的食物并不能保证被机体放大吸收。食品基质中的各组分可以协同或拮抗地相互作用,影响生物活性物质的释放,进而影响其吸收、代谢和生理功能。
在此背景下,南昌大学食品科学与资源管理国家重点实验室在《Journal of Functional Foods》(2区,IF:3.8)上发表了“Effects of nine-steam-nine-bask processing on the bioactive compounds content, bioaccessibility, and antioxidant capacity of Polygonatum cyrtonema Hua”的研究论文,采用体外消化法考察了不同蒸制次数的PCH中生物活性物质、生物可及性和抗氧化活性的变化。
研究将PCH进行不同次数的蒸制,共分为6组:0蒸0制(zero-steam-zero-bask, ZSZB),1蒸1制(one-steam-one-bask, OSOB),3蒸3制(three-steam-three-bask, TSTB),5蒸5制(five-steam-five-bask, FSFB),7蒸7制(seven-steam-seven-bask, SSSB)和9蒸9制(nine-steam-nine-bask, NSNB)。采用三步体外消化法对样品进行消化,包括口腔(oral phase)、胃(gastric phase)和肠道(small intestinal phase)阶段。
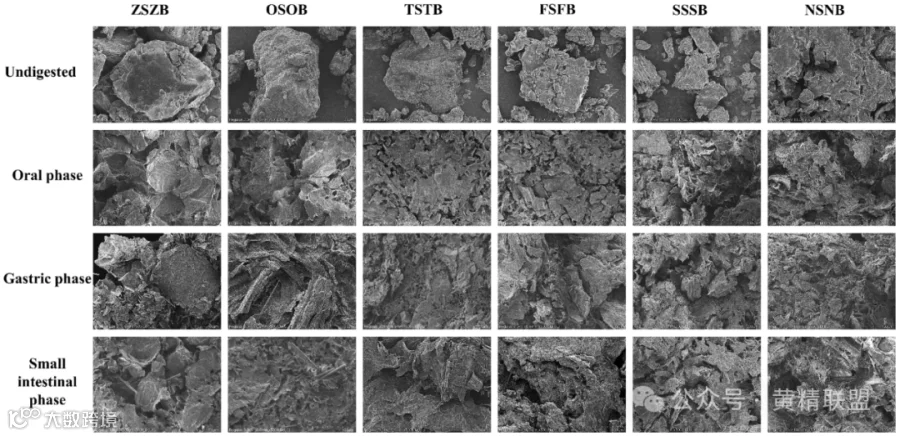
采用扫描电子显微镜(scanning electron microscopy, SEM)观察PCH消化各阶段的微观形貌,结果如图1所示。未处理的PCH粉末在500×放大倍率下呈现为大而完整的块状或片状,表面较为光滑,孔洞较少。PCH样品的表面随着蒸制循环次数的增加变得更加粗糙,褶皱、裂纹和孔洞的存在变得更加明显。在消化过程中,最初,PCH粉末具有明确的边缘和光滑的表面。在消化的口腔阶段之后,样品的表面呈现为层状或片状,充满了孔隙和空腔。经胃消化后的样品在孔径和孔隙率方面均表现出明显的上升趋势,表面呈现明显的犁沟。经肠道消化的样品表现出更高的疏松度和孔隙率,其特点是出现了分布更均匀的更细小的薄片。结果表明,蒸制处理能够破坏PCH的结构,导致PCH与消化液和酶的接触面积增加。这可能有利于活性物质的释放。
图1.不同蒸制次数的PCH体外消化前后SEM图,500×
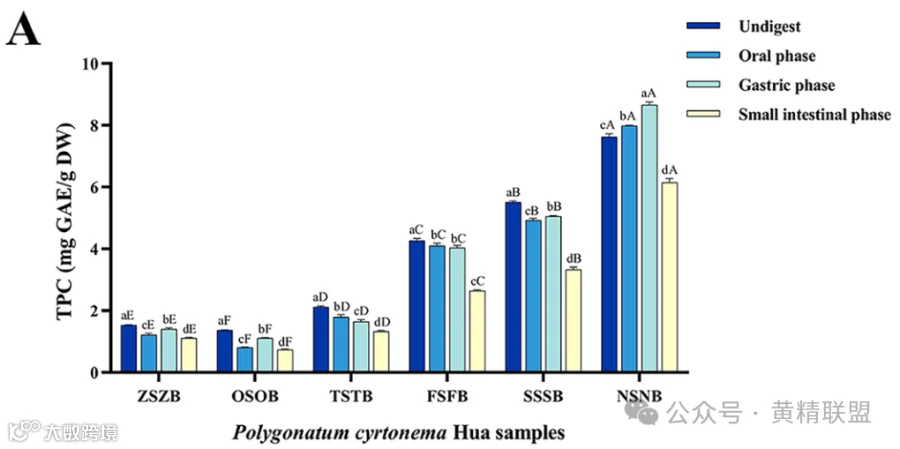
通过比较PCH样品在相同消化阶段的总酚含量(total phenol content, TPC),在每个消化阶段都观察到总体上升趋势(图2A)。TPC的增长与蒸制的频率呈正相关。
在整个模拟体外消化过程中,不同蒸制次数的PCH的TPC总体呈现先上升后下降的趋势。TPC的升高可归因于PCH细胞壁的破坏和化学键的水解,在模拟胃消化过程中通过酸和消化酶的共同作用导致多酚的释放。然而,当从酸性胃环境过渡到小肠的弱碱性环境时,TPC显著减少约30 %。
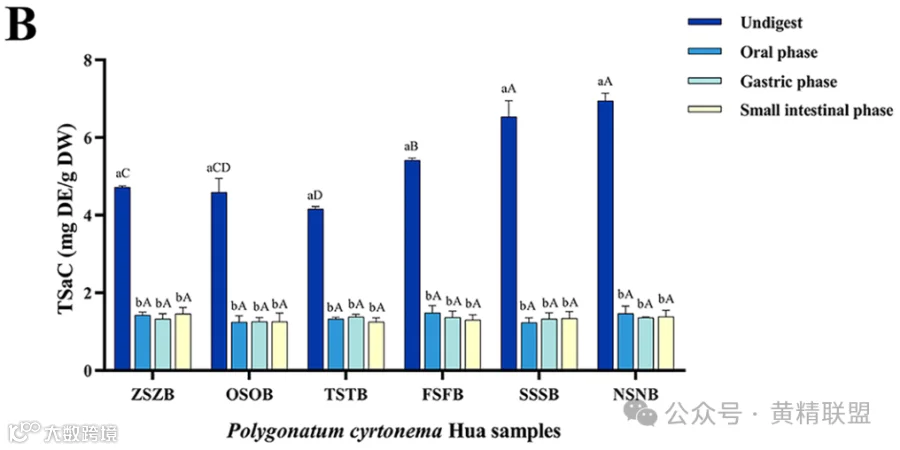
不同处理样品中总皂苷含量(total saponin content, TSaC)的变化见图2B。TSaC的变化可分为三个不同的阶段。在第一阶段,PCH在短期高温条件下主要水解产生次级糖苷和皂苷元,导致TSaC从4.724降低到4.165 mg DE / g DW。第二阶段涉及皂苷的转化过程,发生在TSaC变化率最高的第5次蒸制和第7次蒸制之间。在持续的高温条件下,皂苷除了水解外,还通过脱水和环化反应产生新的化合物。这些新形成的化合物仍然是皂苷组的一部分,导致TSaC迅速增加至6.534 mg DE / g DW。在第三阶段中,样品暴露于高温中的时间延长,皂苷反应接近完成,并产生新的、更稳定的化合物。因此,SSSB和NSNB的TSaC无显著差异。
在体外模拟消化过程中,PCH上清液中的TSaC在1.236 ~ 1.485 mg DE / g DW范围内波动,表明TSaC的消化与蒸制次数和消化阶段无关。这可能是由于部分PCH皂苷极性较低,限制了其在消化模拟液中的溶解度。
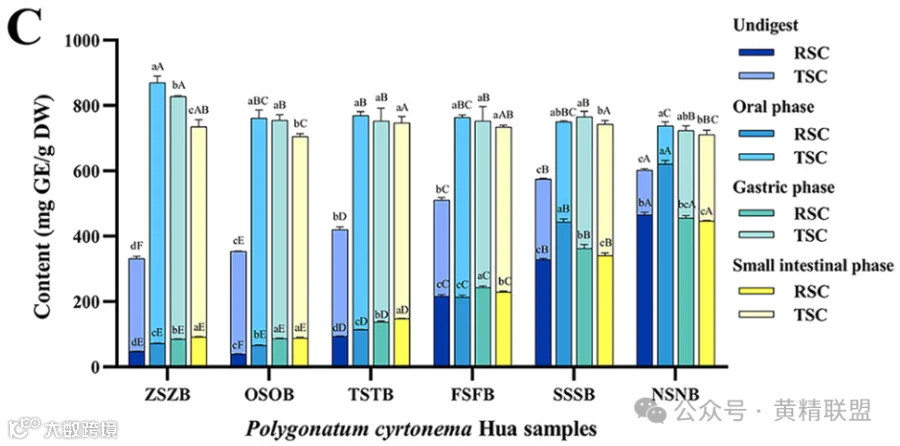
如图2C所示,随着PCH蒸制次数的增加,在未消化阶段还原糖含量(reducing sugar content, RSC)增长较快,而总糖含量(total sugar content, TSC)增长相对缓慢。所有样品的RSC和TSC在口腔阶段均高于未消化阶段,NSNB样品在口腔和未消化阶段的RSC和TSC之间的差异最小。
在消化期间,不同PCH样品的TSC没有表现出显著差异,而RSC随着处理次数的增加而成比例增加。这表明蒸制处理更有效地将PCH中的一些非还原糖转化为还原糖。
图2.不同蒸制次数的PCH在消化过程中的含量变化:A.TPC; B.TSaC; C.RSC和TSC
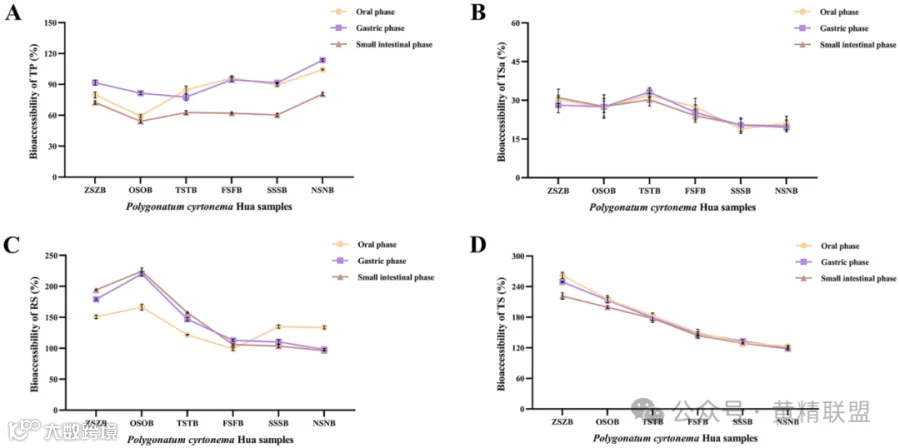
如图3A所示,总酚的生物可及性在首次蒸制处理后显著下降,分别为59.253%(口腔)、81.476%(胃)和54.183%(小肠)。随后经历了逐渐增加,最终达到104.459%(口腔),113.624%(胃)和80.691%(小肠)。NSNB样品在不同阶段表现出峰值。
模拟口腔咀嚼后,PCH中的皂苷最大有31.955%从食物基质中释放出来(图3B)。PCH总皂苷的生物可及性在加工过程中经历了轻微的下降,最终稳定在20%左右。当蒸制处理使样品中的TSaC扩增时,皂苷本身很难溶解在消化液中。这导致了总皂苷生物可及性的降低。
如图3C所示,还原糖的生物可及性在各消化阶段均呈上升趋势,由最初的蒸制后的166.447%(口腔阶段)、220.199%(胃阶段)和224.569%(小肠阶段)上升了10%以上。这种增加可归因于湿热处理改变了PCH的物理结构,从而增加了消化酶或消化液与植物材料的接触面积。尽管NSNB样品中RSC升高,但其生物可及性仅为133.518%(口腔阶段)、98.055%(胃阶段)和96.153%(小肠阶段),几乎是OSOB样品的一半。
如图3.D所示,总糖生物可及性从262.052%(口腔阶段),249.180%(胃阶段)和221.477%(小肠阶段)下降,顺序为:ZSZB > OSOB > TSTB > FSFB > SSSB > NSNB。这表明蒸制处理对PCH中总糖的生物可及性产生了不利影响。
图3.不同蒸制次数的PCH在消化过程中生物可及性的变化:A.TP; B.TSa; C.RS; D.TS
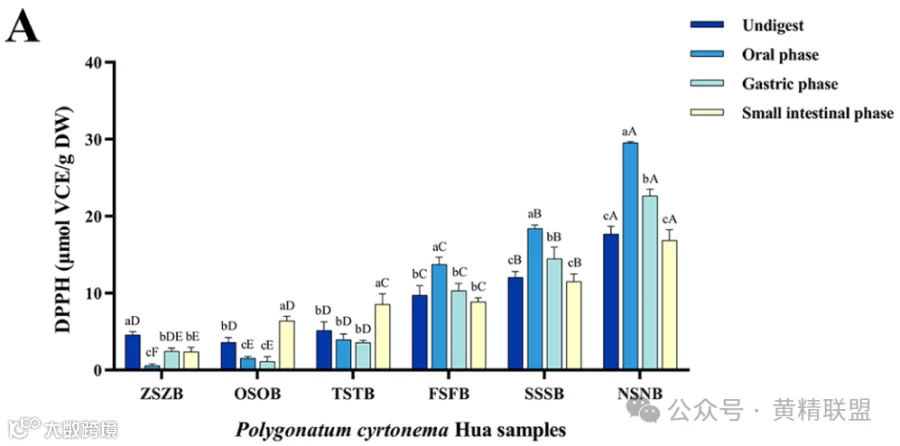
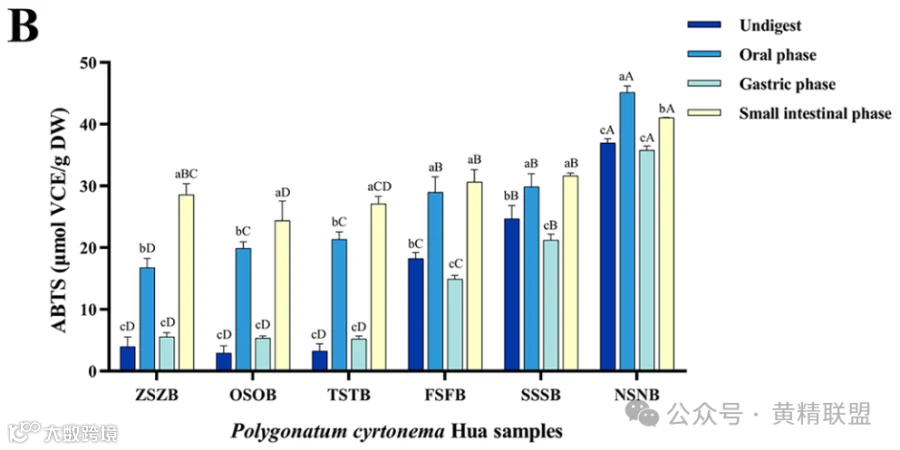
DPPH和ABTS清除能力实验中,PCH的体外抗氧化活性均表现出与蒸制周期持续时间相关的上升趋势(图4A - B)。NSNB样品在消化(即未消化期、口腔期、胃期和小肠期)的各个阶段均表现出较好的DPPH和ABTS自由基清除能力。
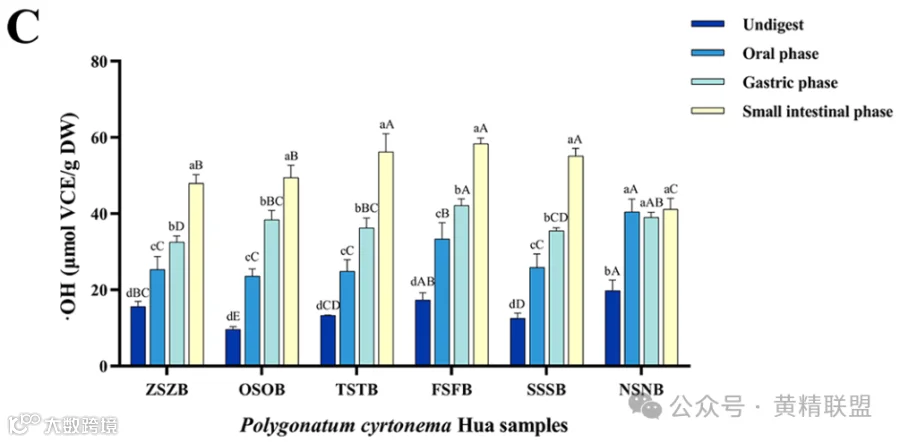
PCH在不同消化阶段的羟自由基清除能力在一定范围内波动,未消化阶段为9.659~19.837 μmol VCE / g DW,口腔阶段为23.612~ 40.471 μmol VCE / g DW,胃阶段为32.541 ~ 42.192 μmol VCE / g DW,小肠阶段为41.142~ 58.368 μmol VCE / g DW(图4C)。研究结果表明,蒸制次数对该过程没有显著影响,而消化对该过程的影响呈现一定的规律。
综上所述,蒸制过程改变了多花黄精的结构特征,促进了活性物质的消化,改善了其营养特性,对其加工和生产有着重要的意义。
图4.三种不同方法测定的不同蒸制次数的PCH抗氧化活性:A.DPPH; B.ABTS; C.·OH
原文链接https://doi.org/10.1016/j.jff.2024.106236