多花黄精在中国大部分地区(如湖南、安徽、浙江、江西、湖北)均有栽培,作为药材和食品使用有着悠久的历史,常用于炖菜、粥、药茶、药酒等功能性食品。黄精中含有多糖、皂苷和黄酮类化合物,在糖尿病的防治中具有重要作用。高异黄酮是一种罕见的类黄酮,它在连接类黄酮骨架上的B环和C环的三碳链上含有甲基或新的环组合,表现出广泛的生物学特性,例如抗氧化、抗炎、抗突变、抗菌和降血糖活性。据报道,高异黄酮类化合物可通过抑制葡萄糖转移来调节葡萄糖代谢紊乱,改善葡萄糖摄取并减轻氧化应激。目前已从黄精植物中分离出48种高异黄酮类化合物。
为了避免刺激咽喉,增强疗效,传统工艺会把黄精的根茎进行蒸制、干燥,直至根茎变黑、柔软、味甜,这一加热过程对化学成分产生很大影响,最终使其生物活性发生变化。然而,除了多糖和皂苷外,关于黄精蒸制过程中高异黄酮成分变化的研究很少。
论文“In vitro hypoglycemic and antioxidant activities of steamed Polygonatum cyrtonema Hua with various steaming degrees: Relationship with homoisoflavonoids”研究了不同蒸制程度的多花黄精根茎中高异黄酮的组成、降血糖和抗氧化活性,并分析了高异黄酮对这些活性的贡献,发表在期刊Food Biosience(中科院二区,IF:5.2)上,浙江工业大学食品学院聂晓华为论文第一作者,孟祥河教授为论文的通讯作者。

将干燥的多花黄精根茎在高压锅中在不同温度(100、110、120和130 ℃)下蒸60 min。后切成厚度约1 cm的薄片,在60℃下干燥至恒重,研磨成粒径<160 μm的粉末。根据颜色(图1),将100、110、120和130℃蒸过的根茎分别命名为浅蒸(LSR: light-steamed rhizome)、中蒸(MSR: medium-steamed rhizome)、高蒸(DSR: dark-steamed rhizome)和深蒸根茎(DDSR: deep-dark-steamed rhizome)。

图1. 不同蒸制程度的黄花根颜色(RR:生根茎;LSR:浅蒸根茎;MSR:中蒸根茎;DSR:高蒸根茎;DDSR:深蒸根茎)。
研究采用UHPLC-Orbitrap-MS/MS对不同蒸制条件下多花黄精中高异黄酮的含量的变化进行了定量分析。生根茎提取物中的总黄酮含量为 0.98 mg RE/g dw。随着蒸制程度的增加而逐渐增加。蒸制过程可以软化根茎基质,破坏细胞结构,从而释放出更多的游离黄酮类化合物。所有已鉴定的高异黄酮类化合物均在生根茎和蒸根茎中观察到,并且它们的峰值强度几乎随着蒸制程度的增加而增加。深蒸根茎提取物中九种高异黄酮的含量是生根茎提取物的5.79-11.60倍。此外,中蒸根茎提取物中 5,7,4'-三羟基-6,8-二甲基高异黄酮和 5,7-三羟基-6-甲基-8,4'-二甲氧基高异黄酮的峰强度略有降低。这些变化是高异黄酮在蒸制过程中损失、释放和降解共同作用的结果。
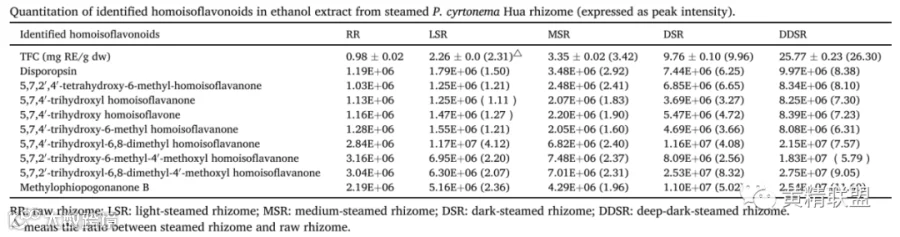
表1. 不同蒸制程度下多花黄精根茎乙醇提取物中鉴定的高异黄酮类化合物的定量(以峰强度表示)。
自由基和其他活性氧化剂在糖尿病及其并发症的发展中发挥着重要作用,该研究中,不同蒸制程度多花黄精根茎乙醇提取物的DPPH、ABTS、羟自由基清除能力和还原能力如图2所示。对自由基的抑制作用以IC50值表示,IC50值越低意味着效力越高。所有蒸制过的根茎的提取物都比生根茎的提取物表现出更强的中和受测自由基的能力,蒸制过程中多花黄精根茎提取物抗氧化活性的提高可能很大程度上是通过细胞壁释放纤维结合的抗氧化剂(尤其是酚类、类黄酮)来介导的。同时,由于在蒸制过程中一些酚类化合物的降解,热处理也会对抗氧化活性产生不利影响,最终的影响很大程度上取决于工艺条件(例如温度和时间)和植物物种性质(例如形态和营养特性)的差异。本研究中,随着蒸制程度增高其清除自由基、还原三价铁(Fe(III))的能力也随之增高。
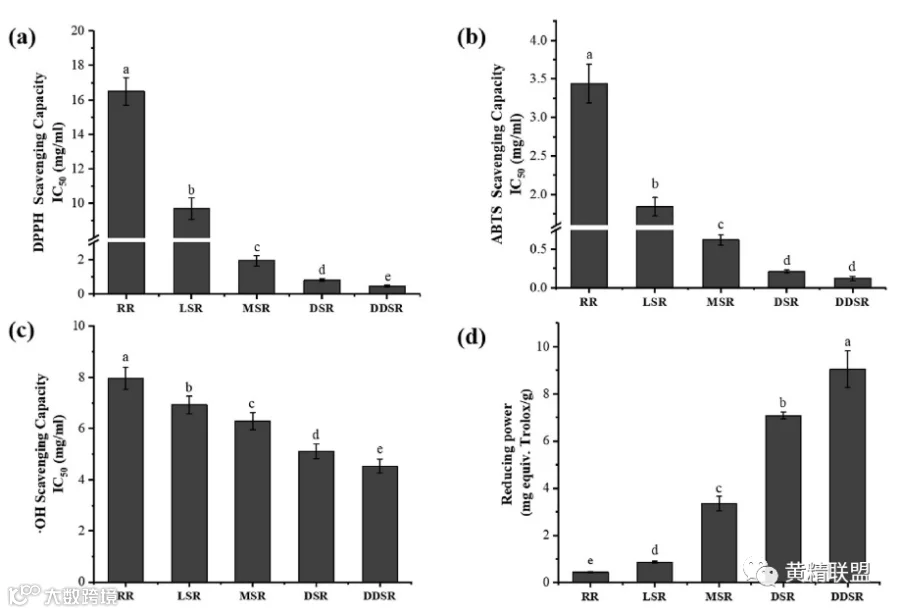
图 2. 不同蒸制程度多花黄精根茎乙醇提取物的自由基清除能力和还原能力。
α-淀粉酶和α-葡萄糖苷酶是淀粉相关的消化酶,其中前者负责淀粉水解,而后者将双糖水解成单糖,抑制这两种酶被认为是降低餐后血糖水平的有效策略。多花黄精根茎乙醇提取物对α-淀粉酶和α-葡萄糖苷酶的抑制活性如图 3所示。所有蒸过的多花黄精根茎提取物对α-淀粉酶和α-葡萄糖苷酶的抑制作用均强于生多花黄精根茎提取物。根茎的活性随着蒸制程度的增加而增强。蒸制处理后,α-淀粉酶和α-葡萄糖苷酶的IC50值分别降低26.70-83.75%和18.68-61.98%。值得注意的是,蒸过的根茎提取物对α-淀粉酶的抑制作用高于对α-葡萄糖苷酶的抑制作用。
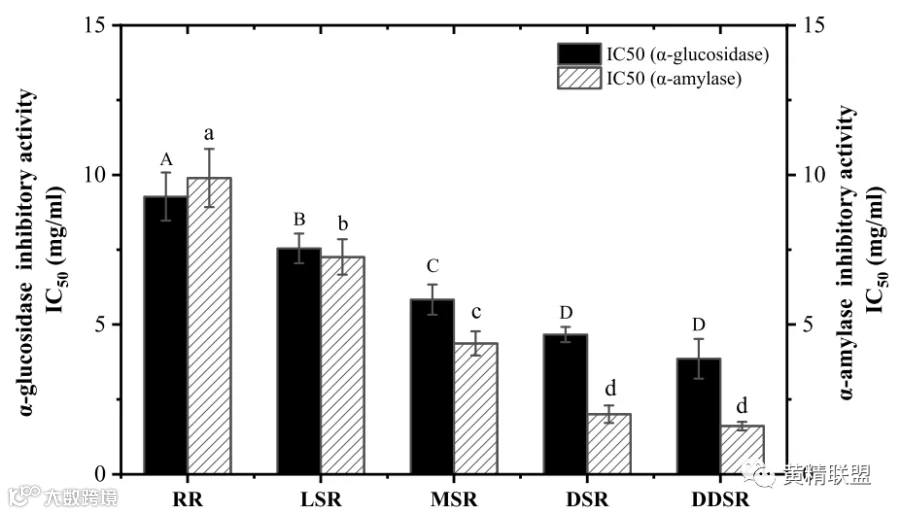
图 3. 不同蒸制程度多花黄精根茎乙醇提取物对α-淀粉酶和α-葡萄糖苷酶的抑制作用。
不同蒸制程度多花黄精根茎乙醇提取物处理的IR-HepG2细胞的细胞活力如图4所示。用MTT方法测定,用根茎提取物处理IR-HepG2细胞没有引起细胞活力的显着变化。该结果表明,这些含量的根茎提取物对细胞没有表现出毒副作用。
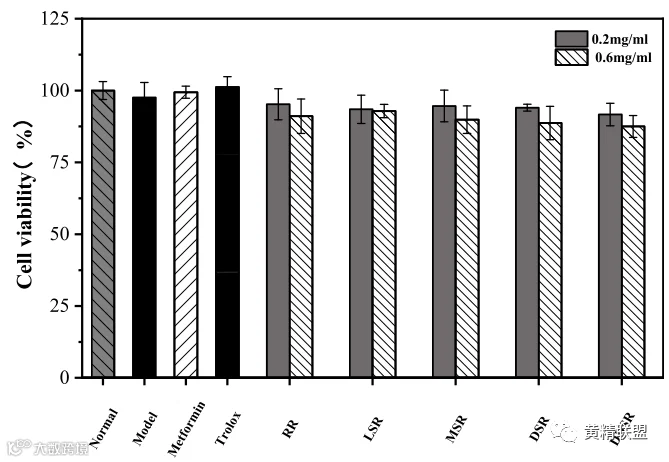
图 4. 不同蒸制程度多花黄精根茎乙醇提取物对 IR-HepG2 细胞活力的影响。
肝细胞中的胰岛素抵抗导致胰岛素信号受损和葡萄糖消耗减少,这是导致高血糖的主要原因。用高胰岛素/葡萄糖建立胰岛素抵抗(IR) HepG2细胞模型,将细胞用二甲双胍(100 μg/mL)、trolox(100 μg/mL)或根茎提取物(0.2和0.6 mg/mL)在100 μl低葡萄糖DMEM中处理24小时。将未高糖/胰岛素暴露的细胞作为正常组。将未处理的IR-HepG2细胞作为模型组。不同蒸制程度多花黄精根茎乙醇提取物处理IR-HepG2细胞的葡萄糖消耗如图5所示。模型组的葡萄糖消耗(3.60 mmol/L)较正常组(5.05 mmol/L)显着降低,表明IR-HepG2细胞模型建立成功。先前的研究证明,黄精植物中的生物活性物质(例如黄酮类化合物和皂苷)具有抗糖尿病潜力。更重要的是,所有蒸根茎提取物都比生根茎提取物表现出更强的效果,几乎显着地将葡萄糖消耗恢复到正常水平。这就说明高蒸制程度的多花黄精根茎能够有效改善外周胰岛素抵抗,促进IR细胞对葡萄糖的摄取和利用。
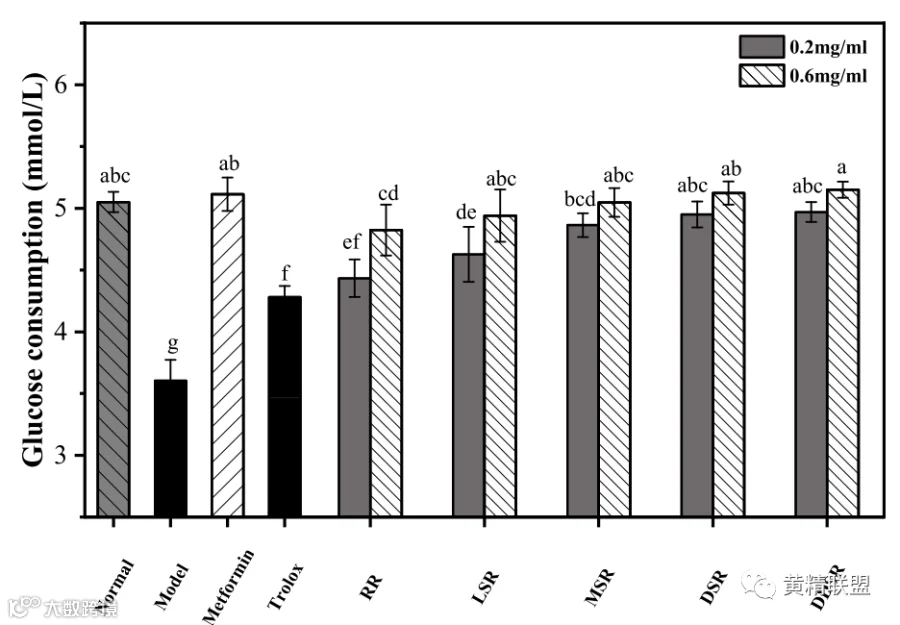
图 5. 不同蒸制程度多花黄精根茎乙醇提取物处理对IR-HepG2 细胞的葡萄糖消耗的影响。
氧化应激被认为是胰岛素抵抗的重要触发因素,并导致糖尿病的发生。因此,消除细胞内ROS可能是治疗胰岛素抵抗和糖尿病的有效方法。图6显示了经蒸熟后根茎乙醇提取物处理的IR-HepG2细胞中细胞内ROS的形成。模型组中ROS的水平比正常组高得多。在高胰岛素和高葡萄糖刺激后增加了1.23倍。与模型组相比,根茎提取物处理减少了IR-HepG2细胞中ROS的形成,其效率取决于蒸制处理的程度。特别是,0.6 mg/mL高蒸组和深蒸组的ROS水平显着恢复至Trolox处理组。很明显,蒸制过的多花黄精根茎可以发挥良好的细胞氧化损伤保护作用,从而改善线粒体功能障碍和胰岛素抵抗。在红苋菜叶和党参中也发现了蒸制处理对ROS消除的增强作用。这主要是由于热处理引起的抗氧化化合物的释放或转化。这一结果与其清除自由基的能力一致。
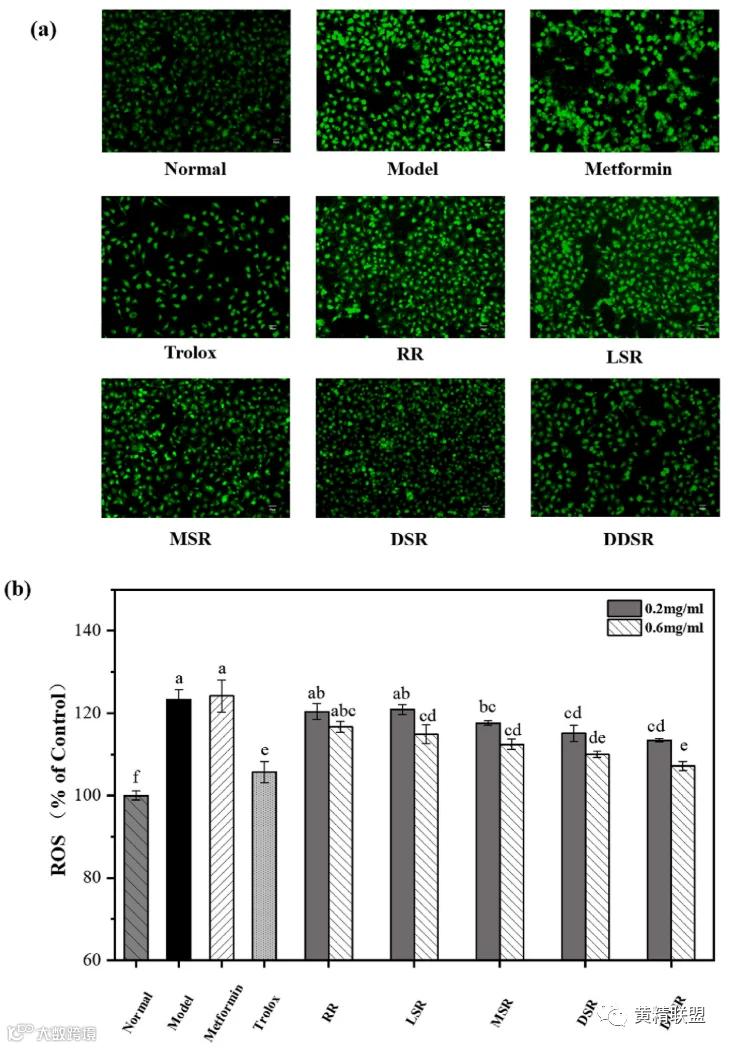
图 6. 细胞内ROS荧光染色的代表性图像(× 20放大倍数),及其荧光强度(b)。
进行多变量分析以更好地可视化和理解多花黄精根茎的蒸制程度、鉴定的高异黄酮和生物活性之间的关系。值得一提的是,IC50值越小,表明对自由基和酶活性的抑制作用越强。从图7(a)的水平聚类来看,九种同型异黄酮类化合物随着蒸化程度的增加呈现增加的趋势。而且,蒸化程度越高的根茎,其抗氧化、降血糖活性越高;尤其是经过高蒸和深蒸的根茎。从垂直聚类来看,鉴定出的同型异黄酮类化合物与IR-HepG2细胞的降低功率和葡萄糖消耗呈正相关,与其他指标呈负相关。鉴定出的高异黄酮类化合物和生物活性之间具有很强的一致性。结果表明,蒸熟程度对多花黄精根茎的高异黄酮成分和生物活性有重要影响。
主成分分析(PCA)是一种线性变换,用于突出许多不同变量的实际影响。根据总黄酮含量、鉴定的类黄酮、抗氧化活性、淀粉相关消化酶抑制活性、细胞葡萄糖消耗和活性氧生成[图7 (b) 和 (c)]进行测定。总变异来自PC1和PC2,分别占85%和7.7%。PC1中的重要变量是总黄酮含量、九种同型异黄酮和降血糖活性。 PC2中存在细胞葡萄糖消耗、DPPH自由基清除能力(IC50)和ABTS自由基清除能力(IC50)。多花黄精根茎的明显分离和区分反映了蒸制后高异黄酮成分和生物活性的显着差异。结果表明,蒸制程度和高异黄酮类化合物对这些生物活性有很大影响。
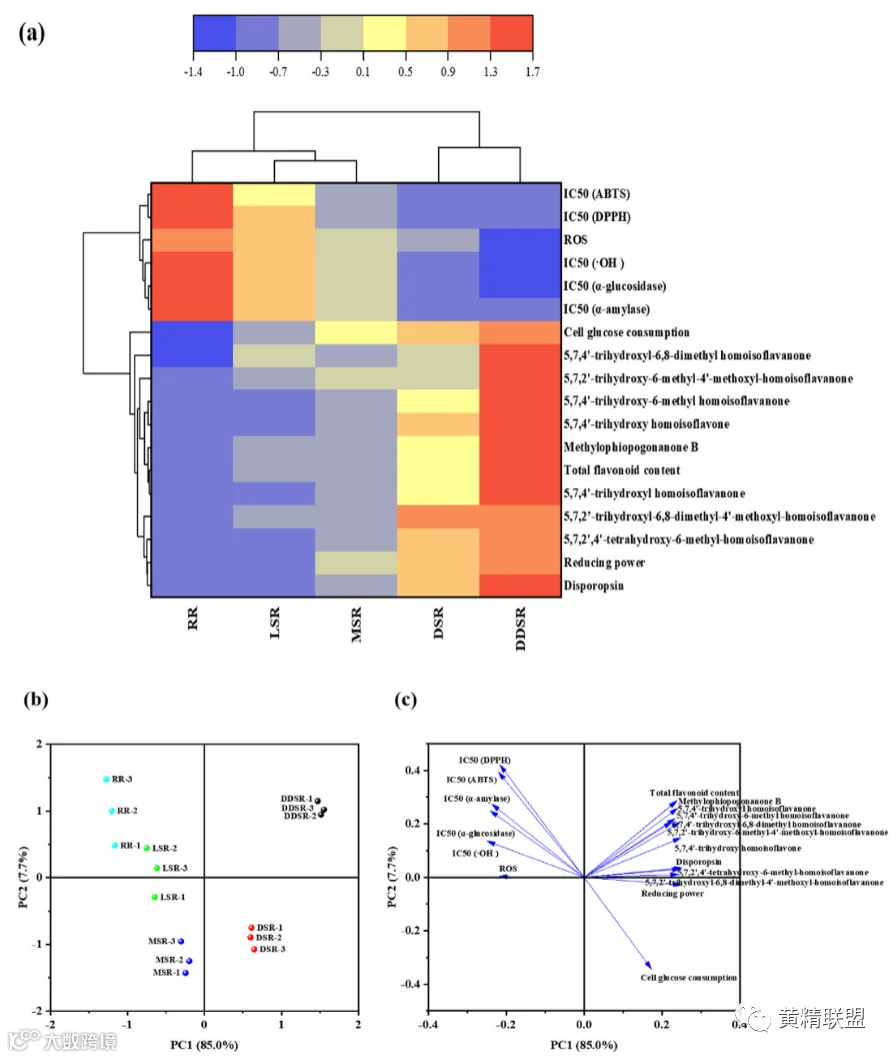
图 7. 不同蒸制程度多花黄精根茎乙醇提取物的热图和主成分分析 (PCA)。
这项研究表明,蒸制工艺显着影响了多花黄精根茎的高异黄酮成分、降血糖和抗氧化活性。这些变化很大程度上取决于蒸制程度。结果表明,蒸制过的根茎提取物比生根茎提取物具有更高的清除自由基、还原三价铁、抑制α-淀粉酶和α-葡萄糖苷酶、改善葡萄糖消耗和减轻IR-HepG2细胞氧化应激的能力,并且效率随着蒸制程度的增加而增加。在九种已鉴定的高异黄酮类化合物中,disporopsin和5,7,2',4'-四羟基-6-甲基-高异黄酮在降血糖和抗氧化活性中发挥着关键作用。深蒸过程似乎可以有效地从结合的纤维中释放高异黄酮类化合物,同时提高其生物活性。
转载请在开头注明:本文转载自公众号——黄精联盟



