在快节奏现代生活中,肠道健康问题日益突出,炎症性肠病(IBD,Inflammatory Bowel Disease)已困扰全球超1000万人。患者常遭受腹泻、便血、腹痛等症状折磨,而传统治疗药物还可能引发抗生素耐药、器官损伤等副作用,需更安全天然的解决方案。
IBD本质是肠道内的慢性失衡状态:正常情况下肠道黏膜屏障、菌群与免疫系统和谐共处,而遗传、环境等因素会打破这种平衡,导致肠道菌群紊乱(有害菌增多、有益菌减少),免疫细胞过度激活引发过度炎症反应,进而造成肠黏膜溃疡、肠道缩短变脆,甚至累及肝脾功能。核苷酸结合寡聚化结构域2(NOD2,Nucleotide-Binding Oligomerization Domain Containing2)是一种存在于免疫细胞中的模式识别受体,主要作用是识别肠道内的病原体相关分子,激活下游信号通路,启动免疫应答以清除病原体,而NOD2驱动的炎症(NOD2-Driven Inflammation)是结肠炎中“菌群紊乱→免疫异常激活→过度炎症”链条的关键环节。现有治疗手段难以根治且副作用明显,因此从天然植物中发掘“护肠因子”成为科研焦点。
拥有2000多年药用历史的黄精备受关注。研究团队已明确其多糖特性:分子量约3.7kDa,主要由β-果糖和α-葡萄糖组成,独特结构使其可被肠道菌群精准识别利用。
近期南昌大学全国重点实验室余强教授团队在《Journal of Agricultural and Food Chemistry》(1区,IF=6.2)发表封面论文“Polygonatum cyrtonema Polysaccharides Target Gut Microbiota to Suppress NOD2-Driven Inflammation and Modulate Bile Acid Metabolism in Colitis”进一步揭示了黄精多糖的“护肠”机制。

研究通过动物实验模型,采用体重监测、疾病活动指数(DAI)评分、脏器指数测定等方法,结合结肠组织形态观察,对黄精多糖(PCP,Polygonatum cyrtonema Polysaccharides)干预葡聚糖硫酸钠(DSS,Dextran Sulfate Sodium)诱导结肠炎小鼠的效果进行评估,从体重变化、肠道炎症指标、免疫器官功能等多个维度探讨PCP对结肠炎的改善作用。选取健康小鼠作为实验对象,将其随机分为六组:正常对照组(NC组)、结肠炎模型组(DSS组)、阳性药物柳氮磺胺吡啶处理对照组(SASP_DSS组),以及低(100mg/kg)、中(200mg/kg)、高(400mg/kg)剂量PCP干预组(LPCP_DSS、MPCP_DSS、HPCP_DSS组)。
结肠长度是评估肠道炎症严重程度的关键生物标志物,在该领域引起了广泛关注。在DSS干预期间,与NC组相比,DSS组的体重明显下降。施用不同剂量的PCP减轻了这种体重减轻(图1B)。相反,DSS组的疾病活动指数(DAI,Disease Activity Index)评分升高,PCP处理显著减弱了这种效果(图1C)。此外,DSS暴露导致结肠长度缩短,这种变化被PCP干预有效地逆转了(图1D)。肝脏指数和脾脏指数是小鼠免疫功能的指标,提供了评估其免疫状态的方法。DSS治疗后肝脏和脾脏指数均存在显著差异。然而,这些变化被PCP的干预有效地抵消了(图1E、F)。
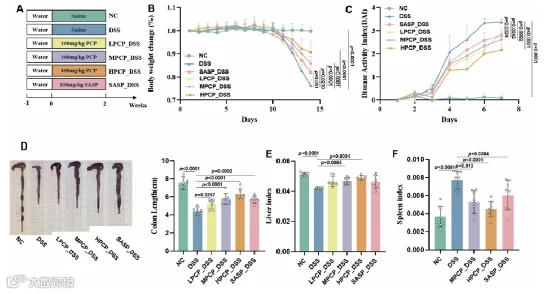
图1.PCP给药改善了小鼠的肠道屏障和炎症反应。(A)实验设计示意图。PCP对结肠炎小鼠的影响。(B)体重变化。(C)DAI分数。(D)结肠长度(cm)。(E,F)肝脏指数和脾脏指数。
为进一步研究PCP对肠道微生物群的影响,研究进行了实验2(图2A)。接受PCP治疗的小鼠和未接受PCP治疗的小鼠之间的体重变化没有显着差异(图2B)。所有治疗组小鼠结肠和肝组织的组织病理学检查显示无显著差异,表明长期摄入不同剂量的PCP不会导致小鼠组织损伤此外,HPCP干预显著增强了结肠杯状细胞的分泌(图2C、D)。
为了评估PCP对正常小鼠肠道菌群的影响,研究采用16SrRNA测序来分析实验组之间的肠道菌群差异。物种丰度曲线和α多样性指数表明,相对于NC组,PCP处理组之间没有显着差异(图2E,F)。然而,基于布雷−柯蒂斯距离(Bray−Curtis distance)揭示了NC组和PCP组之间不同的肠道微生物群组成(图2G)。
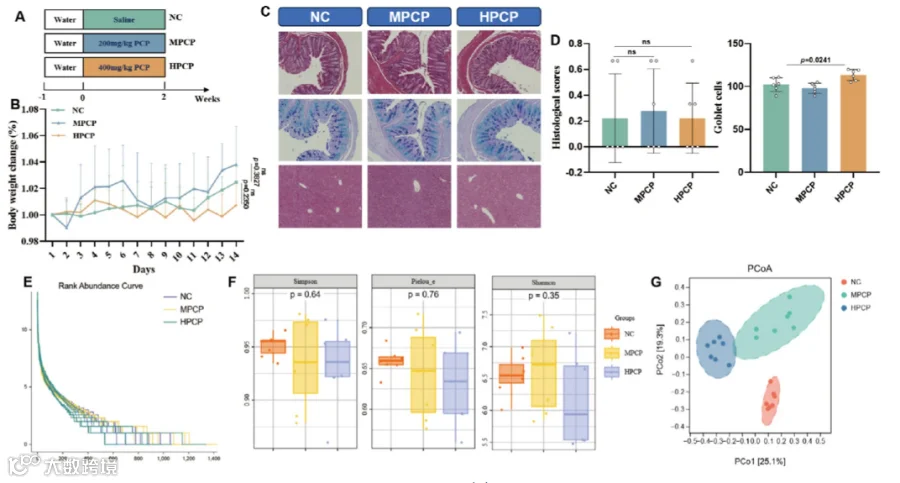
图2.五氯苯酚给药增强了健康小鼠的肠道微生物群。(A)实验设计示意图。五氯苯酚对健康小鼠的影响。(B)体重变化。(C)肝脏的苏木精-伊红染色,结肠的苏木精-伊红染色和阿尔辛蓝/过碘酸雪夫染色(比例尺:100μm)。(D)结肠的组织学评分和结肠杯状细胞数量。(E)物种丰度曲线。(F)α-多样性指数。(G)主坐标分析。
PCP修饰的肠道微生物群减轻了小鼠DSS诱导的结肠炎症状。越来越多的研究表明,粪便菌群移植(FMT,Fecal Microbiota Transplantation)是一种新兴的溃疡性结肠炎(UC,Ulcerative Colitis)治疗方法,能够通过改善肠道菌群失调来缓解肠道屏障破坏。我们之前的研究表明,不同剂量的PCP显着富集了正常小鼠肠道微生物群中的群体。鉴于这些发现,为了进一步确定PCP是否可以通过重塑肠道菌群来改善DSS诱导的结肠炎,将MPCP和HPCP治疗组以及NC组的粪便菌群移植到DSS诱导的结肠炎小鼠体内(图3A)。在DSS浓度从1.5%增加到2%的过程中,与其他组相比,DSS组在早期的体重增加表现出暂时的改善。然而,随后在后期出现了更明显的体重下降。相反,接受微生物群干预的组表现出更一致和稳定的体重轨迹(图3B)。正如预期的那样,DSS组中的小鼠患上了严重的结肠炎,结肠长度缩短,DAI评分升高证明了这一点以及肝脏和脾脏指数升高。微生物群干预组在不同程度上缓解了这些症状。此外,与肠道微生物群干预正常的小鼠相比,具有PCP修饰肠道微生物群的小鼠在结肠缩短和脾肿大方面表现出显着改善(图3C-F)。
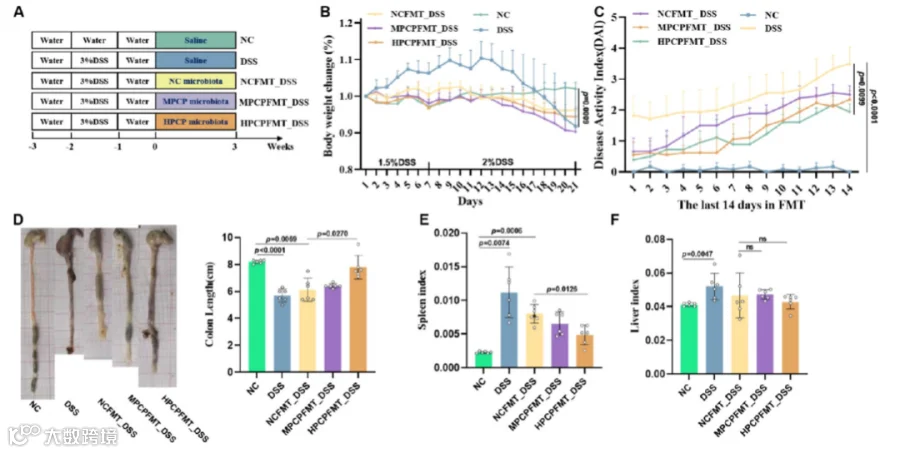
图3.用PCP治疗的小鼠的FMT改善了结肠炎。(A)实验设计示意图。PCP处理小鼠肠道菌群对结肠炎小鼠的影响。(B)体重变化。(C)DAI分数。(D)结肠长度(cm)。(E,F)肝脏指数和脾脏指数。
PCP修饰的肠道微生物群减轻了DSS诱导的结肠炎小鼠的肠道炎症并增强了肠道屏障。组织学分析显示,DSS组肠道严重损伤,杯状细胞减少,隐窝破坏,炎症细胞积聚。还观察到肝细胞损伤。相比之下,PCP修饰的肠道微生物群治疗导致大幅恢复,接近NC组。正常的肠道微生物群并未显着改善结肠炎症状(图4A)。杯状细胞分泌减少的DSS组和NCFMT_DSS组结肠病理学评分较高,但PCP修饰的肠道菌群治疗显着改善,接近NC组值(图4B)。与NCFMT_DSS组相比,MPCPFMT_DSS组和HPCPFMT_DSS组的促炎细胞因子白细胞介素–6(IL-6,Interleukin-6);白细胞介素–10(IL-10,Interleukin-10)和肿瘤坏死因子-α(TNF-α,Tumor Necrosis Factor-α)的结肠mRNA表达水平显着降低(图4C)。DSS处理下调了紧密连接蛋白mRNA表达水平闭合蛋白(Occludin);克劳丁-1蛋白(Claudin-1);闭合小环蛋白–1(ZO-1,Zonula Occludens-1)和黏蛋白2(MUC2,Mucin 2),通过PCP修饰的肠道微生物群处理恢复了该水平(图4D)。DSS组和NCFMT_DSS组的血清二胺氧化酶(DAO,Diamine Oxidase)和D-乳酸(D-LA,D-Lactic Acid)水平升高,但PCP修饰的肠道微生物群治疗后降低至接近正常水平(图4E,F)。
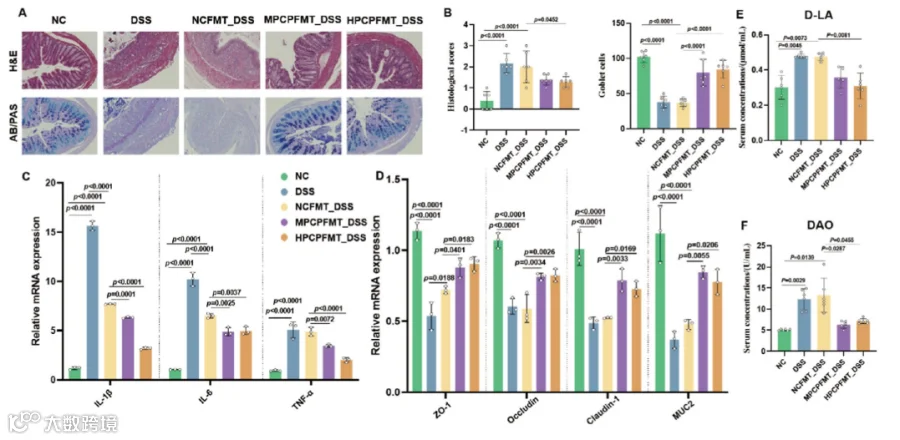
图4.PCP修饰的肠道微生物群干预改善了小鼠的肠道屏障和炎症反应。(A)结肠的H&E和AB/PAS染色(比例尺:100μm)。(B)结肠的组织学评分和结肠杯状细胞的数量。(C)IL-1β、IL-6和TNF-α的结肠mRNA表达水平。(D)ZO-1、MUC2、Occludin和Claudin-1的结肠mRNA表达水平。(E,F)血清中DAO和D-LA的相对表达。
肠道微生物代谢物是菌群与宿主互作的关键介质,对健康和疾病机制影响深远。为阐明PCP修饰的肠道菌群对结肠炎小鼠的代谢调节作用,本研究采用超高效液相色谱-电喷雾电离-四极杆飞行时间质谱(UHPLC-ESI-QTAPMS)检测肠道内容物代谢物。结果显示,正离子模式下检出1169种代谢物,以有机酸及其衍生物(32.5%)、有机异环化合物(27.7%)为主;负离子模式下检出779种,脂质类分子(37.4%)、有机酸及其衍生物(24.6%)占比最高(图5)。
PLS-DA评分图显示NCFMT_DSS组与PCPFMT_DSS组存在明显区分(图6A)。中、高剂量PCPFMT组分别有127种代谢物升高、178种下降,及132种升高、88种下降,三组共110种代谢物存在显著重叠变化(图6B,C)。KEGG分析显示PCP显著富集胆汁分泌通路(图6D)。聚类分析发现,PCP修饰菌群干预的小鼠胆汁分泌相关代谢物改变明显,白三烯C4(LTC4,Leukotriene C4)水平降低而环磷酸鸟苷(cGMP,Cyclic Guanosine Monophosphate)水平升高(图6E,F),证实PCP调节的肠道菌群通过影响胆汁酸代谢缓解结肠炎症状。
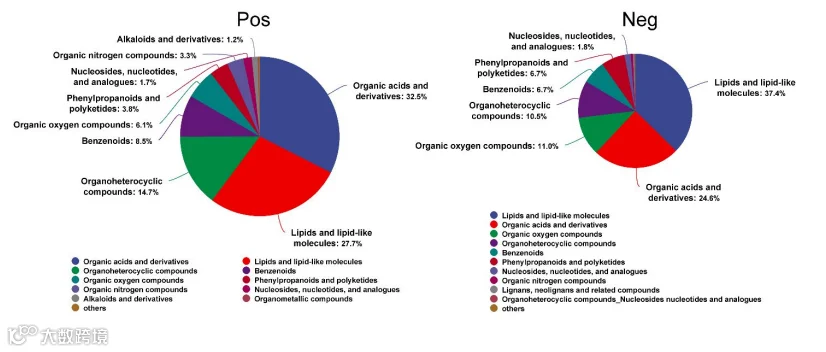
图5.采用正/负离子模式对肠道内容物中的代谢物进行鉴定。
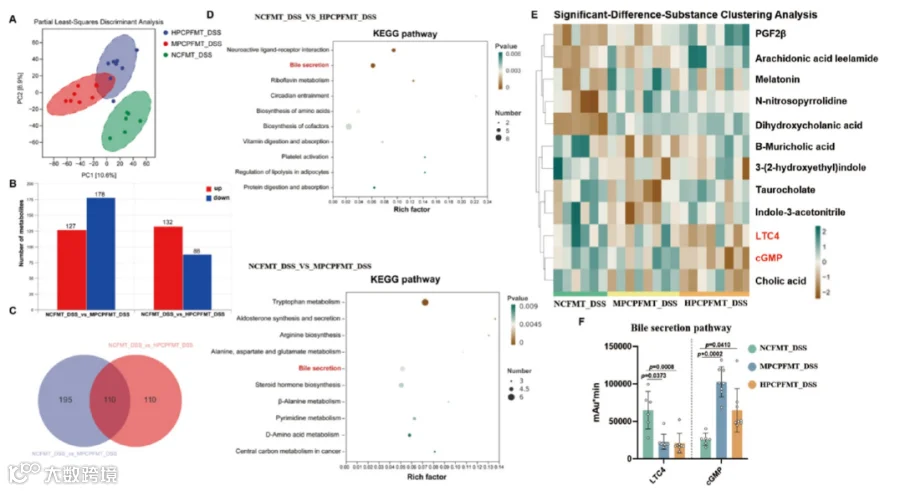
图6.PCP修饰的肠道微生物群调节DSS诱导的结肠炎小鼠的微生物代谢物。(A)主坐标分析。(乙、丙)差异物质筛选和维恩分析。(D)使用KEGG数据库对差异代谢物的代谢途径进行富集分析。(E)差异代谢物聚类分析。(F)LTC4和cGMP的相对水平。
综上所述,研究结果表明,PCP干预有效缓解了结肠炎。肠道微生物群在介导PCP的健康益处方面发挥了至关重要的作用。PCP调节的肠道菌群进一步调控NOD2自噬-炎症轴和胆汁酸代谢途径,从而促进炎症细胞因子合成的抑制和肠道屏障损伤的愈合,从而阻碍结肠炎的进展。然而,肠道菌群中对PCP有反应的特定菌株及其抗炎作用仍有待确定,这对于更深入地了解PCP的抗炎机制至关重要,并将成为未来研究的重点。尽管如此,研究提供了新的见解,极大地推动了用于结肠炎预防和治疗的创新天然药物的开发。这些数据共同强调,PCP可以发挥其益生元特性来调节肠道菌群,从而发挥抗炎作用。
南昌大学食品科学与资源挖掘全国重点实验室余强教授为本文的通讯作者。
原文链接:https://doi.org/10.1021/acs.jafc.5c04155

支持单位:
浙江农林大学森山大健康研究院
浙江农林大学新化黄精研究院
新化县颐朴源黄精科技有限公司
浙江农林大学磐安共富学院
浙江农林大学秀山共富学院
浙江农林大学苍南共富学院
编辑:王得圆
审核:刘京晶


