多花黄精(Polygonatum cyrtonema Hua),既是我国传统中药材,又是药食同源的明星作物,其根茎能缓解疲劳、改善记忆、增强免疫力,市面上以黄精为原料的保健品、药品年需求达4000吨。但近年来,根腐病在一定程度上制约黄精产业发展,患病植株叶片枯黄、根茎腐烂、生长停滞,严重拉低产量与品质。
此前,学界对黄精根腐病的致病菌、黄精自身的防御策略,以及根际微生物在病害中的作用知之甚少。而以庞志强为第一作者于2022年发表在Microbiology Spectrum(2区IF3.8)的名为“Multiomics Reveals the Effect of Root Rot on Polygonati Rhizome and Identifies Pathogens and Biocontrol Strain”的研究,通过整合代谢组、转录组、微生物组及培养实验,首次系统揭示了黄精应对根腐病的“三重防御体系”,更为病害防治提供了可落地的生防菌株。本文聚焦这篇研究的核心“结果”,探讨如何破解黄精根腐病难题。

一、黄精的根腐病与代谢物抵抗
根腐病对黄精最直观的影响,是生长受阻与鲜重锐减。研究团队在贵州省六盘水市的试验田发现,与健康植株相比,患病多花黄精的叶片和茎秆枯萎发黄,根茎出现明显腐烂,部分植株直接死亡(图1A)。定量数据显示,健康黄精根茎平均鲜重为444.27 g,而患病植株仅257.22 g,鲜重降幅超40%,且差异极显著(P<0.001),这意味着根腐病能直接切断黄精的“产量命脉”(图1C)。但令人意外的是,面对病害胁迫,黄精的代谢系统并未完全崩溃,反而启动了“定向强化”,部分药用功效成分的含量显著上升,可能合成了某些防御性物质抵抗病原菌。
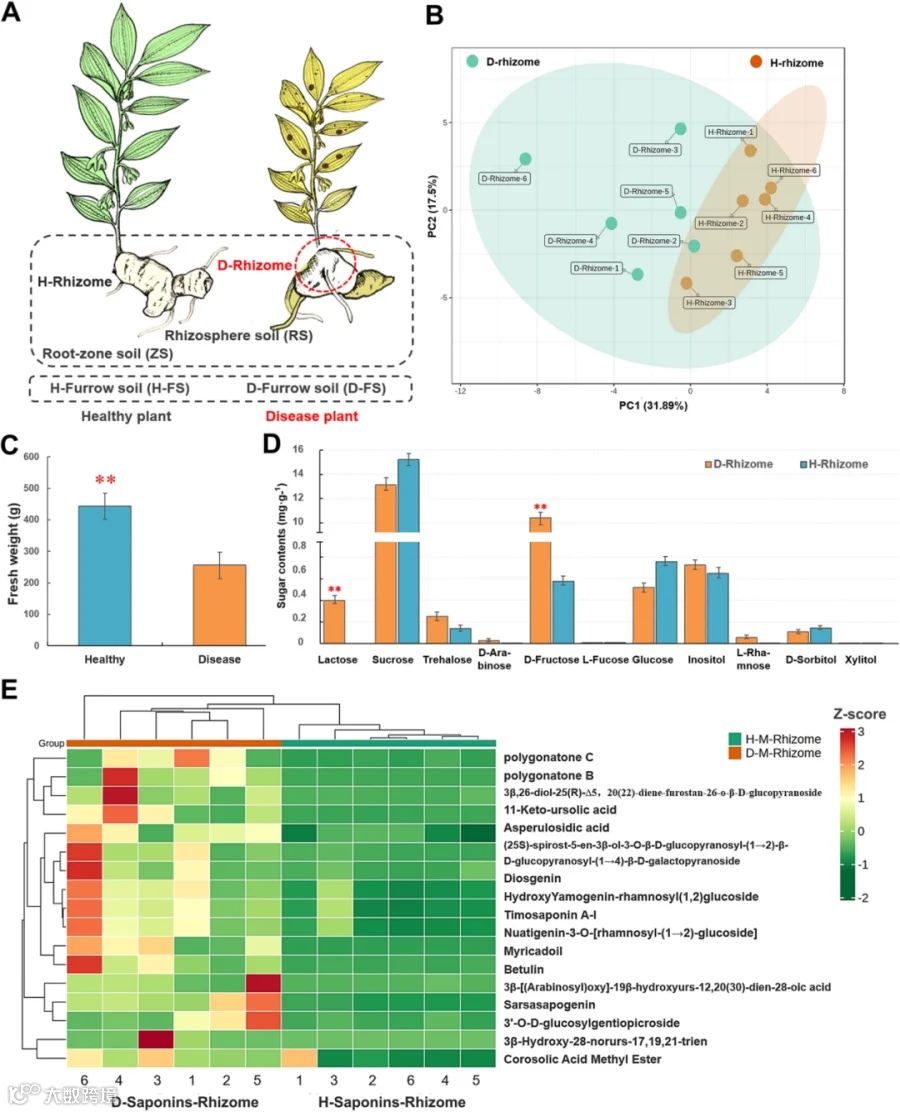
图1. 健康与患病植物根茎代谢物分析
A. 健康和患病的多花黄精及其地下土层,包括根茎土、根际土、须根土和根茎凹槽土,
H状根茎为健康根茎;D状根茎为患病根茎。
B. 健康和患病根茎的皂苷和其他代谢产物的主成分分析(PCA)。
C. 两种样品的鲜重。D. 两种样品的多糖含量。E. 根茎皂苷和其他代谢物相对含量的热图聚类。
研究团队通过靶向代谢组分析(检测13种多糖、44种皂苷及其他代谢物)发现:①糖类代谢物升高,健康黄精根茎中几乎检测不到乳糖(0 mg/g),患病后乳糖含量升至0.40 mg/g;D-果糖含量从健康植株的0.58 mg/g升至10.45 mg/g,增幅超17倍。这些糖类不仅是能量储备,更可能作为信号分子激活免疫反应;②皂苷类成分富集:作为黄精的主要药用成分,皂苷(尤其是甾体和三萜皂苷)是重要的抗菌物质。患病后,黄精根茎中的黄精碱B、C、薯蓣皂苷元、菝葜皂苷元、车叶草苷酸等皂苷含量显著上升,其中菝葜皂苷元作为典型的天然抗菌剂,其积累可能直接抑制病原菌生长;③其他防御代谢物增加:肉豆蔻酸、白桦脂醇等具有抗炎、抗菌活性的成分,在患病根茎中也出现不同程度的积累(图1B、E)。
不过,并非所有代谢物都呈上升趋势:栀子苷、齐墩果酸等成分的含量在健康与患病植株中差异不显著,这说明黄精的代谢调控具有针对性,优先强化与抗病相关的通路,而非无差别调动资源。
二、转录组解密黄精防御系统的基因
代谢变化的背后,是基因表达的精密调控。为了找到黄精抗病的分子机制,研究团队对6组健康与6组患病黄精根茎进行了转录组测序,共鉴定出28221个差异表达基因(DEGs),其中23423个基因上调、4798个基因下调,这意味着根腐病触发了黄精基因组中近3万个基因的表达重编程(图2A)。
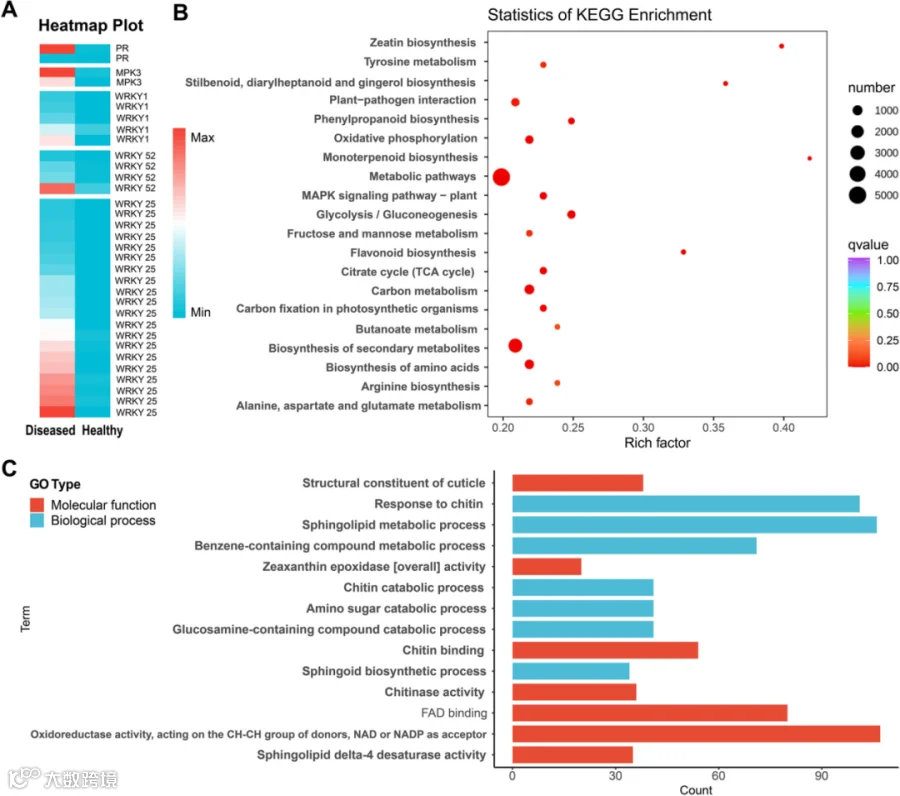
图2. 健康与患病根茎的转录组分析
A. 健康与病变根茎中防御基因的表达。
B. KEGG对DEGs的注释及通路分析。C. GO对DEGs的注释及通路分析。
通过GO(基因本体)和KEGG(京都基因与基因组百科全书)富集分析,这些DEGs的功能逐渐清晰,它们主要集中在三大防御相关通路:
①次生代谢通路:与多糖、皂苷、黄酮等防御物质合成相关的基因被大规模激活:淀粉、蔗糖、果糖、半乳糖代谢相关基因(如果糖基转移酶、β-呋喃果糖苷酶)表达上调,为乳糖、D-果糖的积累提供了酶促基础;环阿屯醇合成酶(GO:0016871)是甾体皂苷合成的关键酶,其编码基因在患病根茎中显著高表达,直接促进推动菝葜皂苷元等皂苷的合成;黄酮类物质是植物抗真菌的典型物质,GO分析显示“黄酮生物合成过程”(GO:0009812)相关基因富集显著,KEGG通路中“黄酮生物合成”(ko00941)也被高度激活。
②信号传导通路:病原菌入侵后,黄精需要快速传递信号以启动防御,而MAPK(丝裂原活化蛋白激酶)和植物激素信号通路是核心传令通路:MAPK1/2/3/6及MAPK底物MKS1的编码基因均显著上调,这些激酶能将病原菌信号从细胞膜传递到细胞核,触发下游抗病基因表达;水杨酸(SA)、乙烯(ET)是植物抗真菌的关键激素。研究发现,SA介导的系统获得性抗性通路(SAR,GO:0046224)与ET激活的信号通路(GO:0009873)相关的基因(如pathogenesis-related protein 1, PR1)表达上调,而茉莉酸(JA)合成通路基因(如JAR1、COI1)下调,这说明黄精面对根腐病,优先选择SA/ET通路。
③转录因子:转录因子是调控基因表达的“开关”。研究共鉴定出1196个差异表达转录因子(分属52个家族),其中MYB、ERF、WRKY、C2H2、NAC家族的转录因子数量最多。例如,WRKY25/29/52是植物抗真菌的经典调控因子,其在患病根茎中的高表达,可能直接调控PR1等抗病基因的开启,成为黄精防御系统的主要调控因素。
三、根腐病会破坏多花黄精根茎的微生物群落
植物的健康不仅依赖自身代谢,还与根际微生物群落密切相关,根际是病原菌入侵的第一道防线,健康的菌群结构能抑制病原菌定殖。而这篇研究首次发现,根腐病对黄精根际微生物的破坏比预期更严重。
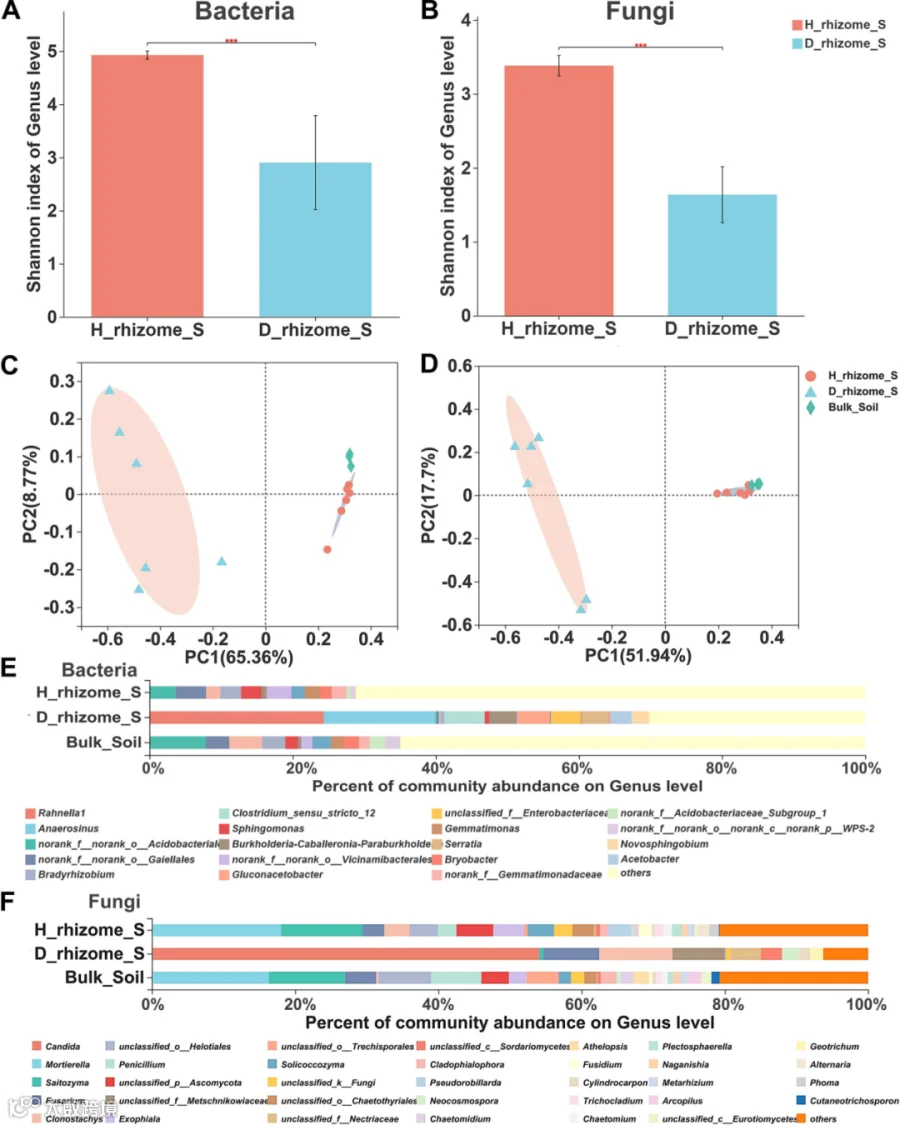
图3. 健康和患病根茎土壤的微生物群落分析
A、B. 健康与患病根茎土壤中细菌和真菌的Alpha-Shannon多样性指数。
C、D. 细菌和真菌群落的β多样性的主成分分析。
E、F. 细菌和真菌在属级别的群落结构。
研究团队采集了黄精5个微生境(根茎、根际土、须根土、根茎凹槽土、周边土)的样本,通过16S rRNA(细菌)和ITS(真菌)测序,解析了健康与患病植株的菌群差异:
①菌群多样性下降,alpha多样性分析显示,根腐病显著降低了根茎内细菌和真菌的多样性,健康根茎的细菌Shannon指数为4.93,患病后降至2.90;真菌Shannon指数从健康植株的3.98,降至患病植株的1.89(P<0.001)。多样性的降低意味着菌群稳定性下降,如同一个生态系统失去了物种制衡,更容易被病原菌入侵。
②菌群结构彻底重构,通过PCoA(主坐标分析)和ANOSIM(相似性分析),研究发现健康与患病植株的菌群结构差异极显著(P=0.003),细菌群落中,第一主成分(PC1)能解释65.35%的菌群差异;真菌群落中,PC1解释了51.94%的差异(图3C、D)。更关键的是,健康根茎的菌群与周边没有种植植物的土壤高度重叠,而患病根茎的菌群则完全偏离,这说明根腐病不仅改变了菌群结构,还打破了黄精与原生土壤菌群的平衡。
③致病菌增加,有益菌减少,在属水平上,健康与患病植株的菌群组成呈现两极分化:患病植株中,真菌中念珠菌(Candida,54.9%)、克劳氏菌(Clonostachys,10.22%)、镰刀菌(Fusarium,7.75%)显著富集;细菌中拉恩氏菌(Rahnella,24.34%)、厌氧球菌(Anaerosinus,15.61%)等潜在致病菌含量飙升;健康植株中,真菌的被孢霉(Mortierella,15.12%)、赛托酵母菌(Saitozyma,12.75%)富集(这些菌已被证实能抑制病原菌);细菌中盖勒氏菌(Gaiellales,4.22%)、维氏菌(Vicinamibacterales,3.47%)等有益菌占比更高(图3E、F)。这种致病菌增加、有益菌减少的格局,进一步加剧了黄精的病情,菌群从帮助防御的生物变成了致病的生物。
四、根际功能从“抗病屏障”转变到“致病温床”
菌群结构的变化,最终导致功能的逆转。研究团队通过BugBase表型预测发现,根腐病使黄精根际微生物的功能发生了重大转变。患病根际中潜在致病菌相关表型的比例显著上升,而健康根际几乎检测不到这类表型;生物膜能帮助病原菌抵抗植物的抗菌物质,患病根际中生物膜形成相关表型的比例更高,这意味着病原菌更难被清除。更值得注意的是,这种功能转变仅发生在根茎和根际土中,须根土和根茎凹槽土的微生物功能几乎不受影响,这说明根腐病对微生物的破坏具有微生境特异性,而根茎和根际是防控的关键部位。
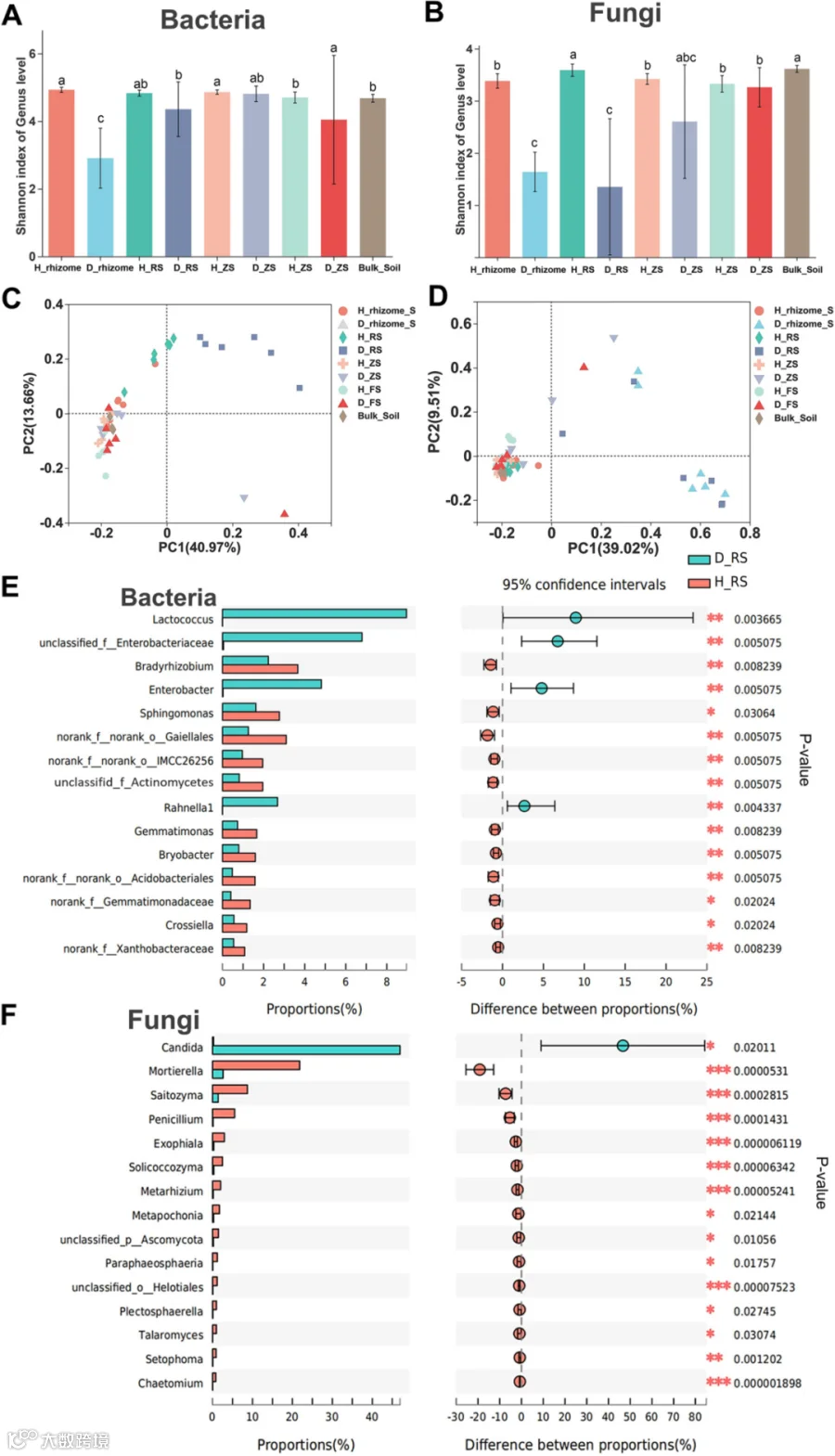
图4. 细菌和真菌群落以及所有健康和患病植物样本的差异分析。
A、B. 所有土壤样本的细菌和真菌群落的Alpha Shannon多样性指数。
C、D. 所有样本的细菌和真菌群落β多样性的PCA。
E、F. 健康和患病根际土壤细菌和真菌群落组之间的显著性检验。
五、潜在的微生物病原体与有益菌株
通过多组学分析锁定了致病菌群后,研究团队通过分离培养与致病性验证,终于找到了黄精根腐病的关键病原菌,并发现了能对抗病害的有益菌株。
①病原菌鉴定:研究从患病黄精的叶、茎、根茎、土壤中分离出59-88种真菌,通过“柯赫法则”(病原菌验证金标准)测试发现:尖孢镰刀菌(Fusarium oxysporum)和斯派塞炭疽菌(Colletotrichum spaethianum)能导致健康黄精发病,接种2周后,植株出现叶片枯黄、根茎腐烂,与田间病害症状完全一致;而念珠菌(Candida sp.)、腐皮镰刀菌(Fusarium solani)等其他真菌,均无法使健康植株发病(图5B)。这是学界首次证实,斯派塞炭疽菌能引起贵州地区多花黄精根腐病,此前该菌仅被报道能导致黄精叶斑病,此次研究更新了对黄精致病菌的认知。②找到有益菌株:在寻找病原菌的同时,研究团队从健康黄精的根茎内生菌和根际土中,分离出472株细菌,并筛选出22株潜在生防菌。其中,一株名为“紫色彩线菌(Streptomyces violascens)HJB-XTBG45”的菌株,表现出极强的抑菌能力:在体外抑菌方面,平板对峙实验显示HJB-XTBG45能显著抑制尖孢镰刀菌和斯派塞炭疽菌的生长,形成明显的抑菌圈(图5D);在体内防效方面,温室实验显示提前接种HJB-XTBG45的黄精,在感染尖孢镰刀菌后,病情指数显著降低,与未接种HJB-XTBG45的患病植株相比,其根茎腐烂程度减轻,叶片枯黄率下降超50%(图5Bd)。HJB-XTBG45能抗病的原因是什么?研究推测,该菌株可能通过合成抗生素、竞争营养或诱导黄精免疫反应,从而实现生物防治,这为黄精根腐病的绿色防控,提供了可直接应用的菌株资源。
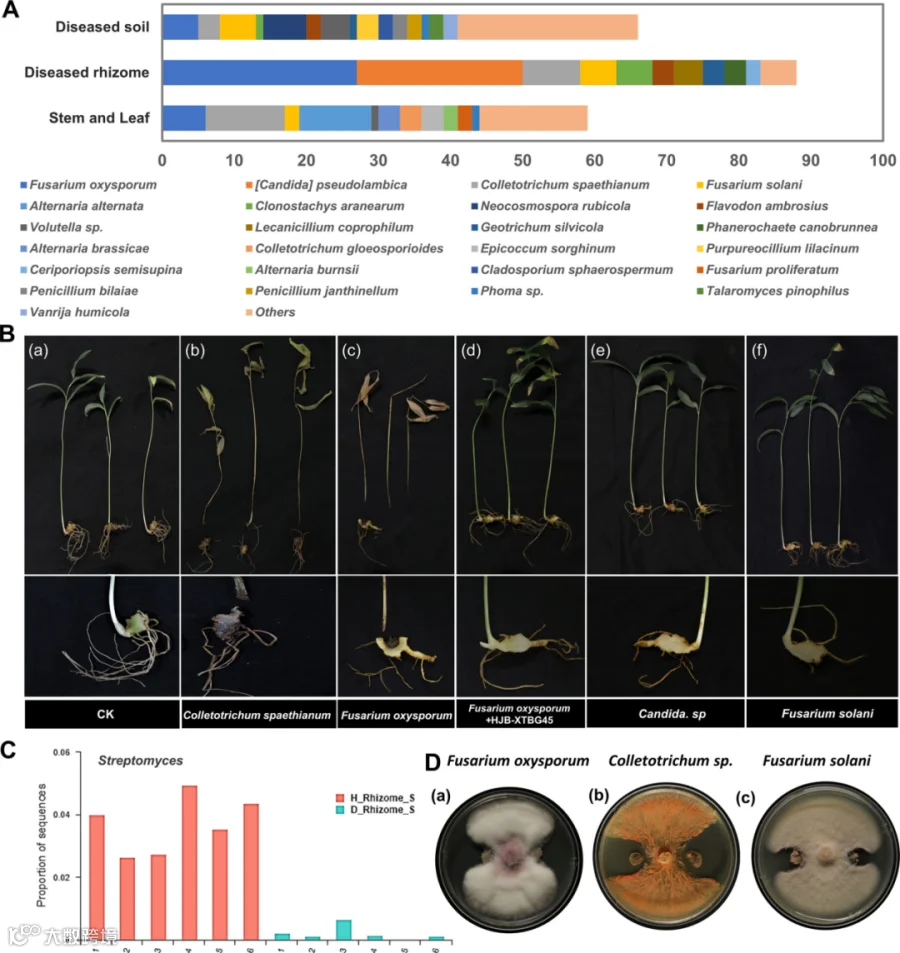
图5. 所有健康和患病根茎土壤的差异分析
A. 患病多花黄精根茎分离到的真菌群落。B. 不同病原体的接种以及HJB-XTBG45对多花黄精根茎的影响,
b和c接种菌株的植物表现出与田间相似的病害特征;a、d、e、f无疾病特征。
C. 健康与病变根茎中链霉菌的相对丰度差异。D. 紫色彩线菌XTBG45对尖孢镰刀菌的抑制作用。
结语:多组学为黄精产业保驾护航
这篇研究的价值,不仅在于揭示了多花黄精应对根腐病的代谢强化、基因调控、微生物互作三重防御体系,更在于为产业提供了切实可行的解决方案,从代谢标志物来看,乳糖、D-果糖、菝葜皂苷元等成分可作为黄精抗病性的检测指标,助力抗病品种筛选;从基因靶点来看,WRKY25/29、MAPK3/6等基因可作为分子育种的候选基因,帮助抗病品种培育;从生防资源来看,紫色彩线菌HJB-XTBG45可开发为生物菌剂,替代化学农药,实现黄精绿色种植。
对于中药材产业而言,病害防控一直是难题,而多组学技术的应用,正为破解这一难题提供新路径。未来,随着更多类似研究的开展,我们有望建立起中药材“病害预警-抗病育种-绿色防控”的完整体系,让像多花黄精这样的传统中药材,在现代化种植中实现产量与品质的“双提升”。
中国科学院西双版纳热带植物园刘贵周高级工程师为本文的通讯作者。全文链接:https://doi.org/10.1128/spectrum.02385-21
转载请在开头注明:本文转载自公众号——黄精联盟。

支持单位:
浙江农林大学森山大健康研究院
浙江农林大学新化黄精研究院
新化县颐朴源黄精科技有限公司
浙江农林大学磐安共富学院
浙江农林大学秀山共富学院
浙江农林大学苍南共富学院
编辑:周正泽
审核:刘京晶


