近期在《International Journal of Biological Macromolecules》(中科院二区,IF=8.5)上发表的 《Physicochemical characterization and protective effects of raw and nine-steamed Polygonatum cyrtonema polysaccharides on cyclophosphamide-induced immunosuppression in mice》一文中,通过构建环磷酰胺诱导的小鼠免疫抑制模型,系统评估了两种黄精多糖对免疫功能、肠道组织形态及肠道微生物群结构的调节作用,揭示了“九蒸九晒”加工通过重塑多糖结构进而增强其免疫保护效应的潜在机制,为黄精传统炮制工艺的现代科学解读及功能食品开发提供了重要依据。

本研究以未经加工的黄精多糖(PCP)和九蒸九晒黄精多糖(NPCP)为研究对象,系统比较了两者的理化特性及其在环磷酰胺(CTX)诱导免疫抑制小鼠模型中的保护作用。
结果表明,九蒸处理显著降低了多糖分子量并改变单糖组成,使其更易被肠道微生物利用。与PCP相比,NPCP在恢复免疫器官指数、提高免疫因子和免疫球蛋白水平、改善肠道组织形态以及调节肠道菌群结构和短链脂肪酸生成方面表现出更显著的保护效果。研究揭示了九蒸九晒通过重塑多糖结构、调控“肠道-免疫轴”增强黄精免疫功能的潜在机制。
一、研究思路
首先,他们通过比较两者的:总糖、尿糖含量,单糖组成,分子量大小,光谱特征(UV、FT-IR)来确定生黄精多糖和九蒸黄精多糖,本质上是不是同一种东西。
接下来测的是整体和直观指标,例如体重,脾脏、胸腺指数,血液中的免疫因子,抗体水平等变化来判断有没有起效果。并且进一步做了脾脏切片,胸腺切片,结肠切片等处理来观察免疫器官是否真的被修复了。
为什么NPCP会比PCP更强呢?
研究者提出了一个关键的假设:因为多糖本身很难被直接吸收更多是被肠道微生物利用,所以关键不在免疫系统本身,而是在肠道。
最后通过比较短链脂肪酸(SCFAs)和肠道的菌群结构得出结论:与生黄精多糖相比,九蒸黄精多糖在多个方面表现更好,在免疫保护方面更有效。
二、研究结果
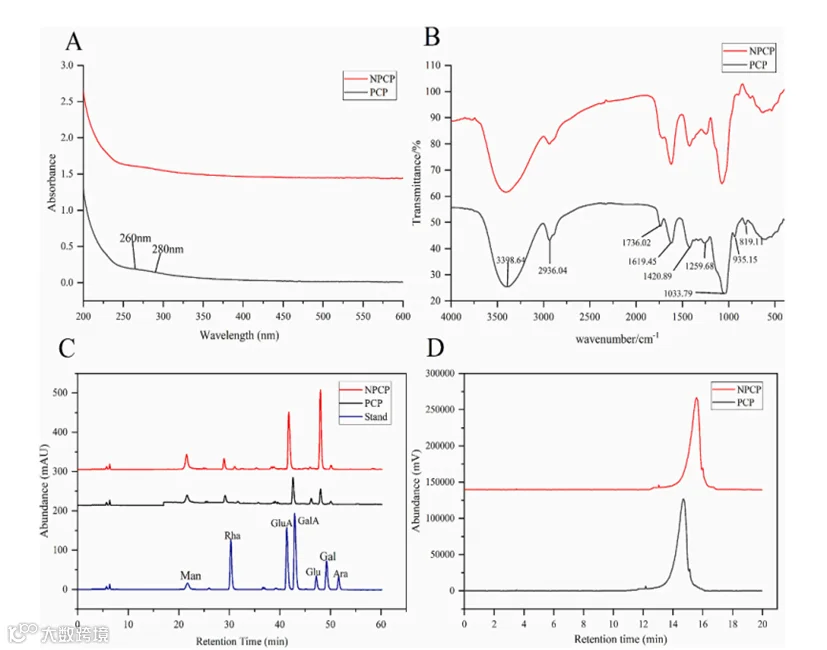
图1 PCP和NPCP的理化性质。(A)紫外光谱。(B) PCP和NPCP在400-4000cm−1范围内的FT-IR光谱。(C)单糖组成。(D) PCP和NPCP的分子量。
NPCP与PCP在UV/FT-IR上均无核酸/蛋白显著吸收(图1A),说明两种多糖样品中几乎不含核酸和蛋白杂质,说明后续实验测到的功能,主要来自“多糖本身”,不是蛋白或其他成分。
PCP和NPCP都具有典型多糖特征,但部分峰强度发生变化(图1B),说明九蒸并没有“破坏多糖”,而是改变了多糖中某些官能团比例和结构状态。
这些变化说明九蒸显著改变多糖化学特征。
PCP的甘露糖占比较高,而NPCP的半乳糖、半乳糖醛酸比例显著升高(图1C)
结果显示:不同含量和比例的单糖会影响肠道菌群和免疫调节能力,九蒸显著重塑了多糖的“原料配方”。
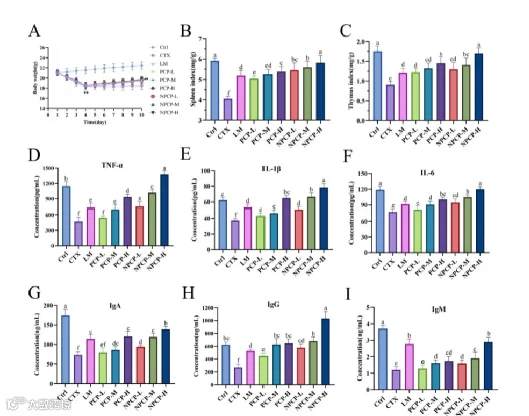
图 2 PCP和NPCP对免疫抑制小鼠的保护作用。(A)体重,(B)脾脏指数,(C)胸腺指数。(D - F)血清炎症因子分泌情况,包括TNF-α(D)、IL-1β (E)、IL-6 (F), (G - I)血清免疫球蛋白分泌情况,包括IgA (G)、IgG (H)、IgM (I),数据用平均值±SD表示(n = 8)。
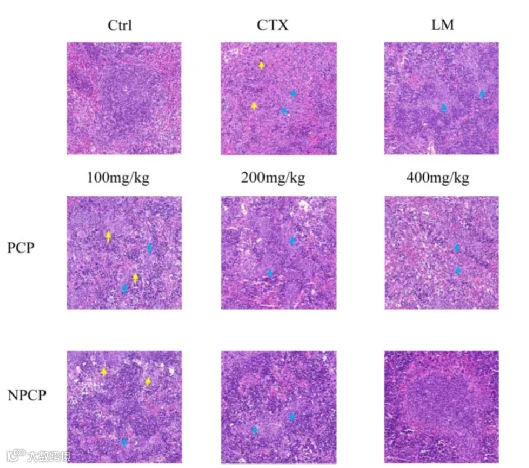
图 3 PCP和NPCP对ctx诱导小鼠脾脏组织形态的影响
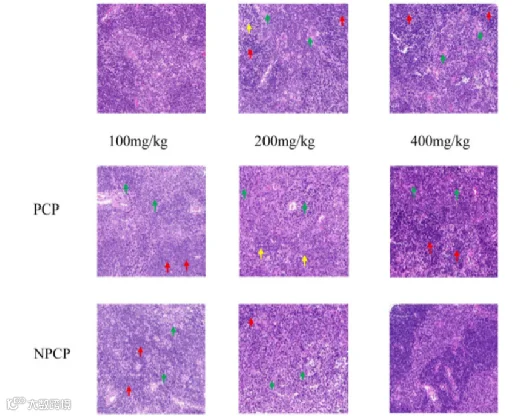
图 4 PCP和NPCP对ctx诱导小鼠胸腺组织形态的影响,100倍放大。
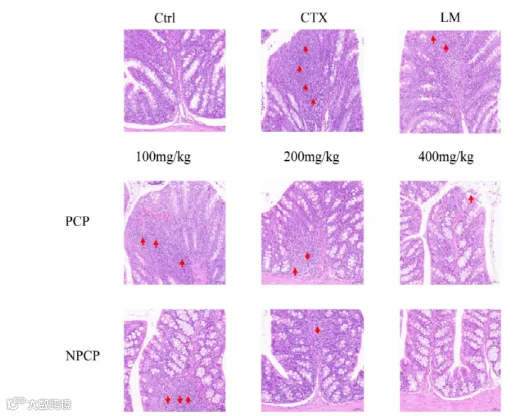
图5 PCP和NPCP对ctx诱导小鼠结肠组织学形态的影响
给小鼠注射CTX后会导致体重下降、脾/胸腺指数下降并降低TNF-α、IL-1β、IL-6、IgA/IgG/IgM这些血清炎症分子的分泌;导致胸腺皮质萎缩、淋巴细胞减少,造成杯状细胞减少与炎性细胞浸润等。
PCP与NPCP以剂量依赖方式促进恢复,且每个剂量组NPCP的恢复效果显著优于相应 PCP组(NPCP 在恢复免疫器官与提升免疫分子上更强)(图2)。
高剂量 PCP/NPCP 可部分恢复脾组织结构,NPCP恢复更明显(图3)。
NPCP的中高剂量则能让胸腺皮质变厚、淋巴细胞数回升,且对胸腺保护优于PCP(图4)。
NPCP高剂量可使结肠形态恢复接近正常,比PCP更能修复肠道黏膜损伤(图5)。
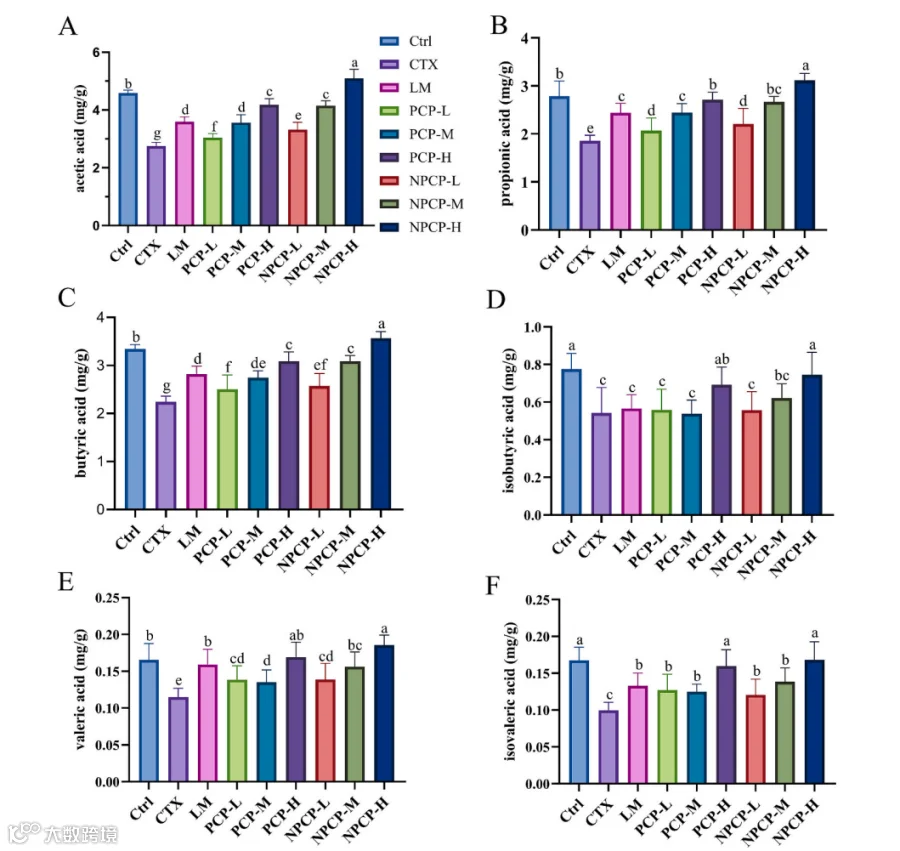
图6 PCP和NPCP对小鼠结肠SCFAs的影响。(A)乙酸,(B)丙酸,(C)丁酸,(D)异丁酸,(E)戊酸,(F)异戊酸。
给小鼠注射CTX后会降低乙酸、丙酸、丁酸及SCFAs含量;但是PCP/NPCP 会恢复这些SCFAs,且NPCP在提高乙酸、丙酸、丁酸方面显著优于PCP。这说明多糖经肠道微生物发酵产生更多有利SCFAs,有助于肠道与免疫功能恢复。
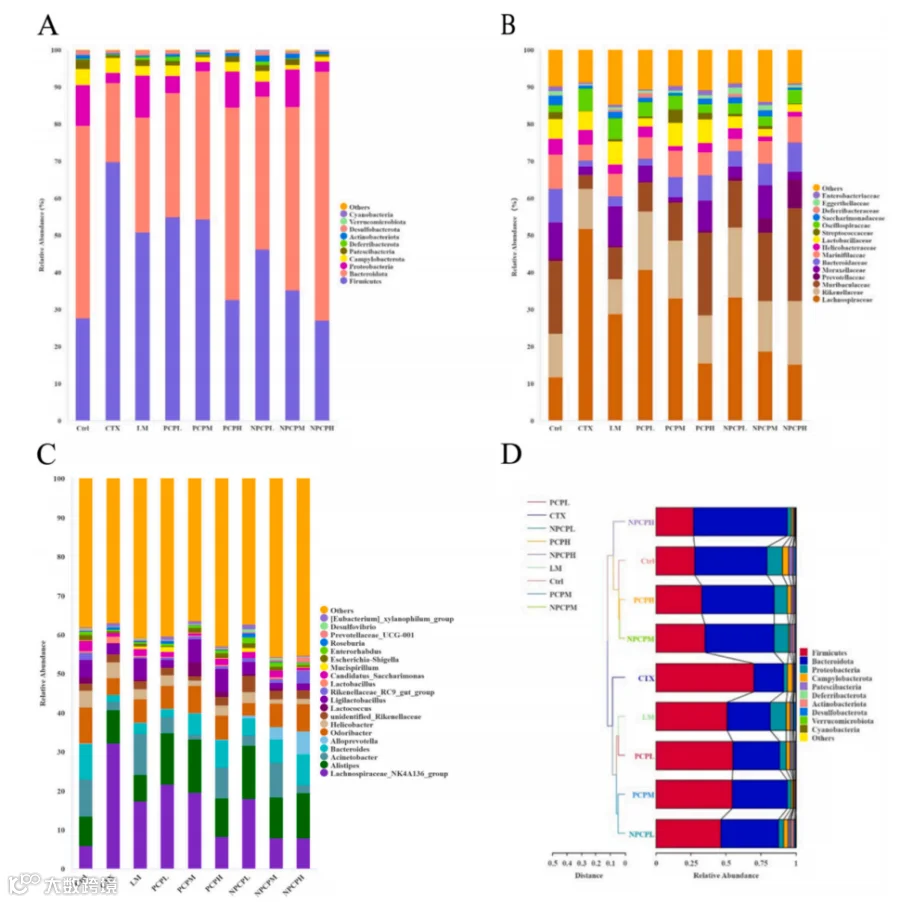
图 7 PCP和NPCP对免疫抑制小鼠肠道菌群的影响(n = 6)。(A)在门分类水平上小鼠肠道菌群的变化。(B)在家族分类水平上小鼠肠道菌群的变化。(C)属分类水平上小鼠肠道菌群的变化。(D) UPGMA聚类分析。
图7显示CTX增加厚壁菌门(Firmicutes)、降低拟杆菌门(Bacteroidetes)(F/B 比上升);PCP/NPCP可逆转该趋势,NPCP提升Bacteroidetes更明显;在科/属层面,NPCP增加Muribaculaceae、Bacteroidaceae,降低Lachnospiraceae、Oscillospiraceae(与SCFAs生成与炎症关联)。
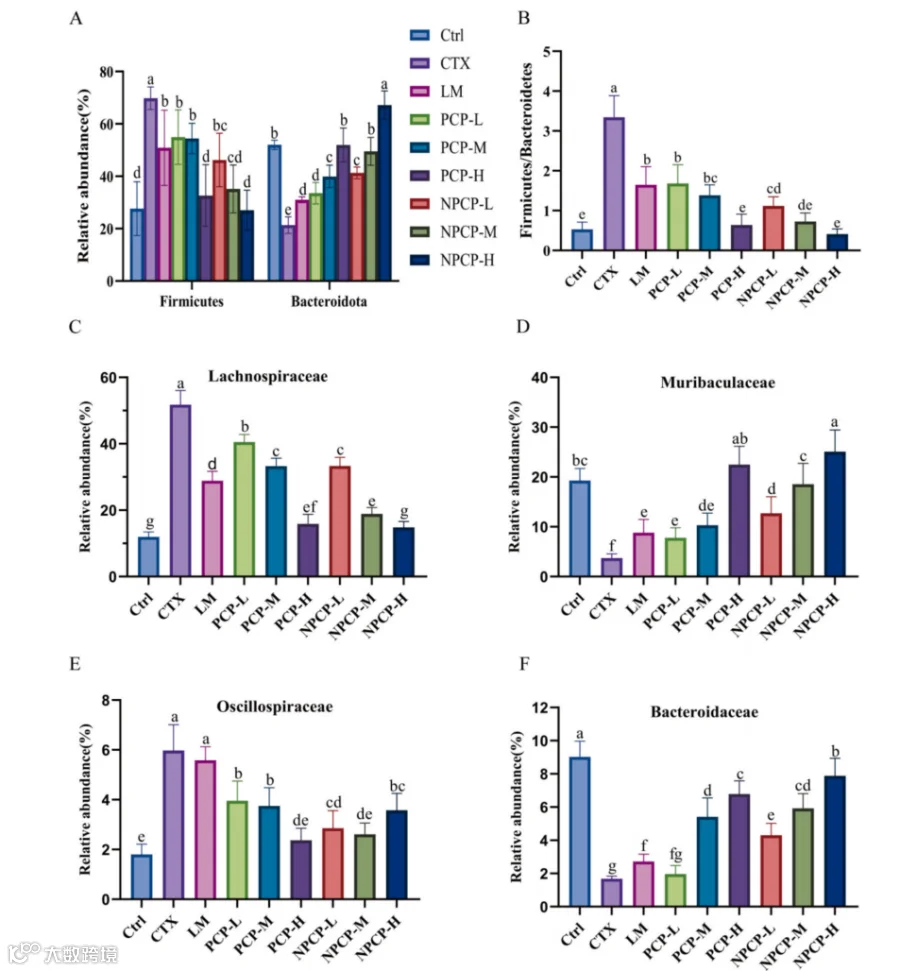
图 8 肠道菌群差异对比分析。(A)在门分类水平上,各组小鼠肠道内厚壁菌门和拟杆菌门相对丰度的比较分析。(B)各组厚壁菌门/拟杆菌门(F/B)比值比较分析。(C-F)在科水平上,各组小鼠肠道内4种肠道微生物相对丰度的比较分析。
图8定量比较显示NPCP更显著降低F/B 比,并在科级别恢复有益菌的比例(例如Muribaculaceae上升),结果表明NPCP在调节菌群方面更有优势。
三、结论
1. 九蒸九晒并非简单降刺激,而是通过重塑多糖结构提升其生物学功能。
2. 九蒸黄精多糖在免疫调节方面显著优于生黄精多糖。
3. 肠道菌群与短链脂肪酸是连接“加工-结构-免疫功能”的关键桥梁。
该研究为黄精深加工、功能食品与免疫调节产品开发提供了重要科学依据。
黑龙江省中医药科学院副院长王伟明和副研究员霍金海为本文的通讯录作者。
原文链接:https://doi.org/10.1016/j.ijbiomac.2025.141911
转载请在开头注明:本文转载自公众号——黄精联盟。

支持单位:
浙江农林大学森山大健康研究院
浙江农林大学新化黄精研究院
新化县颐朴源黄精科技有限公司
浙江农林大学磐安共富学院
浙江农林大学秀山共富学院
浙江农林大学苍南共富学院
编辑:徐珮瑄
审核:刘京晶


